Reakcje jakim ulegaja berylowce. Zastosowanie berylowców i ich związków
Reakcje berylowców z wodą
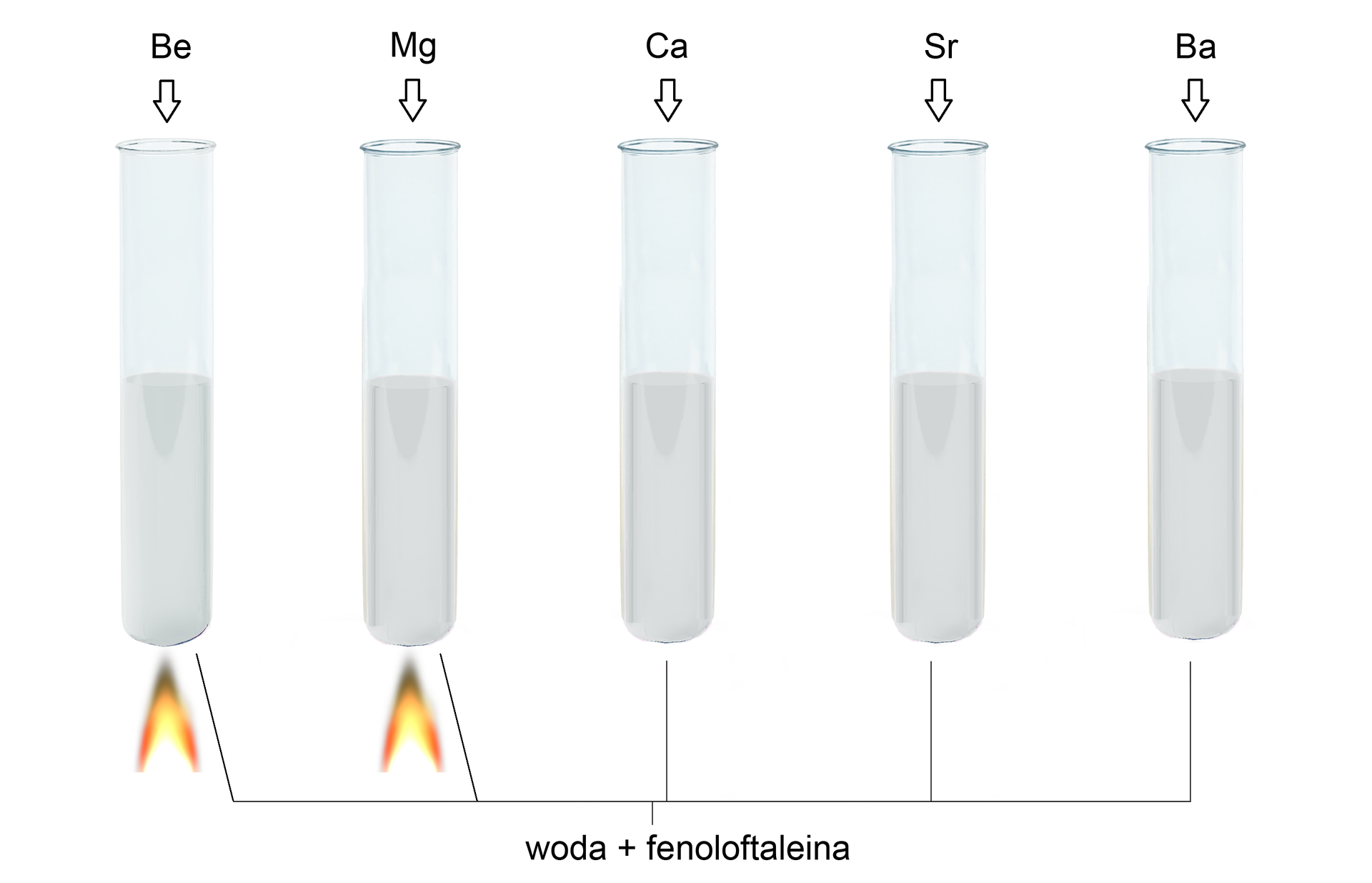
Wapń, stron i bar w sposób widoczny reagują z wodą w temperaturze pokojowej - reaktywność rośnie w dół grupy. Magnez z zimną wodą reaguje bardzo wolno, ale szybkość tej reakcji rośnie znacznie po ogrzaniu. Beryl jako jedyny z pierwiastków należących do 2 grupy układu okresowego nie reaguje z wodą zarówno na zimno, jak i po ogrzaniu. Produktami tych reakcji są odpowiednie wodorotlenki i wodór.
Powstające w reakcji z wodą wodorotlenki berylowców, począwszy od magnezu, tworzą roztwory zasadowe. Wodorotlenek magnezu jest wprawdzie bardzo słabo rozpuszczalny, a wodorotlenek wapnia słabo rozpuszczalny, niemniej ich wodne roztwory i tak przyjmują mocno zasadowy odczyn. Dzieje się tak dlatego, że wodorotlenki berylowców (z wyjątkiem wodorotlenku berylu) są mocnymi wodorotlenkami, o charakterze zasadowym, praktycznie całkowicie zdysocjowanymi w roztworze wodnym na jony.
Wodorotlenek berylu jest praktycznie nierozpuszczalny w wodzie, a charakter chemiczny tego wodorotlenku jest amfoteryczny.
Przeanalizuj poniższą symulację. Czy wiesz, jak zachowują się wybrane metale należące do berylowców, po dodaniu ich do wody oraz alkoholowego roztworu fenoloftaleiny w temperaturze 25°C? Zwróć uwagę na zmiany zachodzące w poszczególnych probówkach, a następnie rozwiąż ćwiczenia sprawdzające.
Przeanalizuj opis poniższej symulacji. Czy wiesz, jak zachowują się wybrane metale należące do berylowców, po dodaniu ich do wody oraz alkoholowego roztworu fenoloftaleiny w temperaturze 25°C? Zwróć uwagę na zmiany zachodzące w poszczególnych probówkach, a następnie rozwiąż ćwiczenia sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DFUC4ZLLZ
Beryl reaguje z wodą: Możliwe odpowiedzi: 1. w temperaturze pokojowej, tworząc wodorotlenek berylu., 2. dopiero po ogrzaniu, tworząc wodorotlenek berylu., 3. która wcześniej została ochłodzona, do odpowiedniej temperatury.
Jak zmienia się aktywność berylowców wraz ze wzrostem masy atomowej pierwiastka? Odpowiedz, posługując się przykładem reakcji berylowców z wodą.
Reakcje berylowców z tlenem
Berylowce reagują z tlenem. Magnez w reakcji z tlenem tworzy tlenek magnezu, podobnie jak wapń, bar i stront. Natomiast bar i stront mogą tworzyć nadtlenki.
Wśród tlenków berylowców tylko tlenek berylu ma właściwości amfoteryczne, a pozostałe mają charakter zasadowy. Tlenki te w reakcji z kwasami tworzą sole, np.:
Tlenek berylu, jako tlenek amfoterycznyamfoteryczny, reaguje z kwasami i zasadami, nie reaguje natomiast z wodą:
Czy znasz ogólny zapis równania reakcji chemicznej pomiędzy berylowcami a tlenem? W którym kierunku wzrasta aktywność chemiczna berylowców? Jakie są zastosowania tlenków pierwiastków II grupy układu okresowego? Przeanalizuj mapę pojęć dotyczącą tlenków berylowców i ich zastosowań, a następnie stwórz na jej podstawie własną mapę pojęć zawierającą nazwę, charakter chemiczny oraz zastosowania odpowiednich tlenków berylowców. Kolejno przejdź do wykonania ćwiczeń sprawdzających.
Czy znasz ogólny zapis równania reakcji chemicznej pomiędzy berylowcami a tlenem? W którym kierunku wzrasta aktywność chemiczna berylowców? Jakie są zastosowania tlenków pierwiastków II grupy układu okresowego? Przeanalizuj opis mapy pojęć dotyczącej tlenków berylowców i ich zastosowań, a następnie stwórz listę wypunktowanych haseł zawierających nazwę, charakter chemiczny oraz zastosowania odpowiednich tlenków berylowców. Kolejno przejdź do wykonania ćwiczeń sprawdzających.
Stwórz własną mapę pojęć
- Nazwa kategorii: Tlenki berylowców
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii: Koniec elementów należących do kategorii
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii: Koniec elementów należących do kategorii
- Nazwa kategorii:
- Nazwa kategorii:
- Nazwa kategorii: Koniec elementów należących do kategorii
- Nazwa kategorii: Koniec elementów należących do kategorii Tlenki berylowców
- Elementy należące do kategorii Tlenki berylowców
- Elementy należące do kategorii
- Elementy należące do kategorii
- Elementy należące do kategorii
Reakcje berylowców z wodorem
Berylowce tworzą także związki chemiczne z wodorem, czyli wodorki. Wodorki berylowców to zwykle białe ciała stałe. Wodorki berylu i magnezu są kowalencyjne, a wodorki wapnia, strontu i baru to wodorki typu soli. Wodorki wapnia i magnezu można otrzymać w wyniku bezpośredniej syntezy z pierwiastków w odpowiednich warunkach ciśnienia i temperatury:
Wodorek wapnia łatwo reaguje z wodą:
Reakcja ta służy do otrzymywania wodoru.
Czy wiesz, dlaczego berylowce są mniej reaktywne niż litowce? Zapoznaj się z poniższym nagraniem, a następnie rozwiąż zadania.
Dlaczego berylowce są mniej reaktywne niż litowce?
Berylowce, a więc: beryl, magnez, wapń, stront, bar i rad, są, podobnie jak litowce, metalami lekkimi. W porównaniu do metali grupy pierwszej układu okresowego pierwiastków, berylowce charakteryzują się większymi gęstościami, większą twardością oraz wyższymi temperaturami topnienia i wrzenia.
Obserwacje te wskazują jednoznacznie na to, że między atomami berylowców, w stanie stałym i ciekłym, występuje znacznie silniejsze oddziaływanie niż między atomami litowców. Wzrost siły wiązania metalicznego między atomami berylowców w stosunku do litowców można wyjaśnić odnosząc się do natury wiązania metalicznego. Chodzi bowiem o oddziaływanie elektrostatyczne między dodatnio naładowanymi rdzeniami atomowymi a zdelokalizowanymi elektronami walencyjnymi atomów, które tworzą tak zwaną chmurę elektronową. Jest więc ono tym silniejsze, im większa jest wartość ładunku rdzeni atomowych (oddziałujących z chmurą elektronową o większej gęstości) oraz im mniejsza jest odległość między oddziałującymi ładunkami, czyli im mniejszy rozmiar mają rdzenie atomowe w krysztale metalu. Analizując struktury atomów litowców i berylowców z łatwością zauważymy, że atomy berylowców posiadają w ramach swojej najbardziej zewnętrznej powłoki dwa elektrony, zwane elektronami walencyjnymi, w przeciwieństwie do atomów litowców o jednym elektronie walencyjnym. Ponadto atomy berylowców, ze względu na większy ładunek jądra w porównaniu z ładunkiem jąder atomów litowców przy takiej samej liczbie powłok elektronowych, charakteryzują się mniejszymi wymiarami ze względu na silniejsze przyciąganie elektronów walencyjnych przez jądro atomowe. Kationy berylowców są więc odpowiednio mniejsze względem kationów litowców, które leżą w tym samym okresie układu okresowego. Mniejszy promień kationów berylowców, w połączeniu z dwa razy większą gęstością elektronową chmury zdelokalizowanych elektronów walencyjnych względem kationów litowców, powoduje występowanie znacznie silniejszego wiązania metalicznego między atomami.
Mniejsze promienie atomowe berylowców względem litowców wpływają także na wartości energii jonizacji tych metali. Litowce stanowią w układzie okresowym grupę najbardziej elektrododatnich metali. Jest to związane z tym, że na ostatniej powłoce walencyjnej litowce posiadają tylko jeden elektron walencyjny, który dodatkowo jest silnie oddalony od jądra atomowego z powodu dużych rozmiarów atomów. Skutkuje to stosunkowo niewielkimi energiami jonizacji tych atomów – to znaczy, że aby wyrwać elektron walencyjny z atomu litowca, potrzebny jest niewielki nakład energetyczny. Atomy berylowców, w porównaniu do atomów litowców leżących w tym samym okresie układu okresowego, mają mniejsze rozmiary, a więc elektrony walencyjne znajdują się bliżej jądra, są silniej przez nie przyciągane, dlatego do ich wyrwania z atomu potrzeba większych nakładów energetycznych. Stąd pierwsza energia jonizacji dla atomów berylowców jest większa niż pierwsza energia jonizacji dla atomów litowców (zestawiając ze sobą pierwiastki tego samego okresu układu okresowego)
Warto także zwrócić uwagę na to, że sumaryczna energia, konieczna do odszczepienia dwóch elektronów od atomu berylowców, jest znacznie większa niż pierwsza energia jonizacji. W związku z tym, w stanie gazowym jednododatnie jony berylowców są trwalsze od jonów dwudodatnich. Zarówno znacznie większa dla jonów dwudodatnich energia sieci krystalicznej związków jonowych, jak i entalpia hydratacji stabilizują jednak jony M2+ w stanie stałym i w roztworze wodnym. To z kolei wskazuje na to, że związki chemiczne o jednododatnich kationach berylowców M+ nie są trwałe.
Opisane zależności tłumaczą mniejszą reaktywność berylowców w porównaniu z litowcami. Wszystkie litowce chętnie reagują z tlenem oraz parą wodną zawartą w powietrzu, w związku z tym przetrzymuje się je w nafcie. Wszystkie litowce gwałtownie reagują z wodą, niektóre z nich nawet w sposób wybuchowy. W przypadku berylowców podobną, lecz i tak mniejszą reaktywność względem tlenu oraz wody wykazują jedynie metale leżące w dolnej części układu okresowego. Za to beryl i magnez pasywują w obecności tlenu, pokrywając się cienką warstwą tlenków, co skutecznie zabezpiecza je przed dalszą reakcją. Z tego względu nie ma potrzeby przechowywania berylu ani magnezu pod warstwą nafty. Metale te reagują z tlenem i wodą dopiero po podgrzaniu. Wapń, stront i bar, przez swoje większe promienie atomowe, a tym samym mniejsze energie jonizacji, wchodzą w reakcje z tlenem i wodą o wiele łatwiej. Sproszkowany stront i bar mogą nawet ulec samozapłonowi w kontakcie z tlenem.
Podsumowując: berylowce, tak jak litowce, są metalami o niskich elektroujemnościach oraz o niskich wartościach energii jonizacji. To spowodowane jest dużymi rozmiarami ich atomów (w porównaniu z atomami innych pierwiastków w danym okresie układu okresowego) oraz małą liczbą elektronów walencyjnych (dla litowców: 1, dla berylowców: 2), które znajdują się daleko od jądra atomowego, a co za tym idzie – są słabo przyciągane przez jądro. Atomy berylowców są jednak nieco mniejsze od atomów litowców (leżących w tym samym okresie) i posiadają dwa elektrony walencyjne. Przekłada się to na silniejsze wiązanie metaliczne, które musi ulec zerwaniu w momencie reakcji atomów berylowców z atomami niemetali, oraz na większy sumaryczny nakład energetyczny jaki trzeba ponieść, by z atomów berylowców wyrwać dwa elektrony walencyjne i utworzyć dwudodatnie jony. Oczywiście ta energia jest odzyskiwana z rekompensatą w momencie utworzenia kryształu jonowego, gdzie powstałe kationy berylowców silnie oddziałują elektrostatycznie z anionami niemetali. Sumaryczny zysk energetyczny jest jednak mniejszy niż w przypadku reakcji z udziałem atomów litowców. Właśnie dlatego berylowce są mniej reaktywne niż litowce.
Kolditz L., Chemia nieorganiczna, Warszawa 1994, s. 33
Atkins P. W., Overton T. L., Rourke J. P., Weller M. T., Armstrong F. A., Shriver and Atkins' Inorganic Chemistry, Oxford 2010, s. 310.
Poniżej podano siedem stwierdzeń, które opisują różnice między berylowcami a litowcami (porównując pierwiastki leżące w tym samym okresie układu okresowego). Wskaż te, które wyjaśniają, dlaczego dany berylowiec jest mniej aktywny od sąsiadującego z nim w układzie okresowym litowca.
Zapoznaj się z tekstem, a następnie rozwiąż zadanie.
Beryl nie reaguje z wodą, za to lit bardzo gwałtownie. Jednym z powodów takiej różnicy w reaktywności między tymi dwoma pierwiastkami, które leżą obok siebie w układzie okresowym, jest to, że atom berylu charakteryzuje się dużo większą pierwszą energią jonizacji niż atom litu.
Wyjaśnij, dlaczego pierwsza energia jonizacji berylu jest większa od pierwszej energii jonizacji litu.
Wpływ berylowców na organizmy żywe i środowisko
Jaki wpływ na nasze zdrowie mają berylowce? Czy wszystkie pierwiastki z tej grupy są bezpieczne dla zdrowia człowieka? Zapoznaj się z grafiką interaktywną przedstawiającą wpływ berylowców na organizm ludzki, a następnie wykonaj ćwiczenia i .
Jaki wpływ na nasze zdrowie mają berylowce? Czy wszystkie pierwiastki z tej grupy są bezpieczne dla zdrowia człowieka? Zapoznaj się z opisem grafiki interaktywnej przedstawiającej wpływ berylowców na organizm ludzki, a następnie wykonaj ćwiczenia i .
Najbardziej znanym efektem wdychania berylu jest beryloza, niebezpieczna i uporczywa choroba płuc, która może również uszkadzać inne narządy, takie jak serce. W około dwadzieścia % przypadków, wynikiem tej choroby jest śmierć. Wdychanie berylu w miejscu pracy jest jej główną przyczyną. Najbardziej podatni na tę chorobę są ludzie, którzy mają osłabiony układ odpornościowy.
Zdjęcie mikroskopowe komórek. Są wybarwione na kolor różowy, ale niektóre tworzą fioletowe pasma. Pomiędzy miejscami zagęszczenia komórek są wolne przestrzenie. Indeks dolny Mikroskopijne cechy przewlekłej choroby wywołanej berylem są bardzo podobne do cech sarkoidozy. Źródło: wikipedia.org; Autor: Yale Rosen; Licencja: CC BY‑SA 2.0;
Beryl może również wywoływać reakcje alergiczne u osób nadwrażliwych na tę substancję chemiczną. Reakcje te mogą być bardzo ciężkie, czego efektem może być stan zapalny znany jako przewlekła choroba berylowa. Objawy to osłabienie, zmęczenie i problemy z oddychaniem. U niektórych osób, które cierpią na te schorzenie, rozwija się anoreksja, zasinienie dłoni i stóp, a czasami może prowadzić ona do śmierci.
Beryl może również zwiększać ryzyko rozwoju raka i uszkodzenia DNA., 2. Magnez Magnez (występujący w formie kationów M g indeks górny, dwa, plus, koniec indeksu górnego) to czwarty pod względem ilości minerałów w organizmie, który jest dostarczany między innymi z pożywieniem. Jony magnezu biorą udział w ponad sześćset reakcjach komórkowych, od tworzenia DNA po pomoc w kurczeniu się mięśni.
Zdjęcie przedstawia różne produkty i dania leżące na stole, między innymi babeczki, jogurt, pestki, ryba, jarmuż. Indeks dolny Produkty bogate w jony magnezu: babeczki z otrębami, pestki dyni, jęczmień, mąka gryczana, niskotłuszczowy jogurt waniliowy, steki halibutowe, fasola garbanzo, fasola lima, soja i szpinak. Źródło: pixabay.com; Licencja: domena publiczna;
Obecność jonów magnezu w ciele człowieka:
Niski poziom kationów magnezu wiąże się z wieloma negatywnymi skutkami zdrowotnymi, w tym z osłabieniem, depresją, wysokim ciśnieniem krwi i chorobami serca., 3. Wapń Wapń (występujący w postaci kationów C a indeks górny, dwa, plus, koniec indeksu górnego), minerał występujący w największej ilości w organizmie, znajduje się w niektórych pokarmach, a do innych jest dodawany, dostępny jest jako suplement diety i jest obecny w niektórych lekach (takich jak leki zobojętniające).
Jony wapnia:
Zdjęcie przedstawia głowę i szyję człowieka z zaznaczonymi gruczołami: skóra - kalcydiol, tarczyca - kalcytonina, przytarczyca - parathormon PTH.Indeks dolny Gruczoły uczestniczące w utrzymaniu prawidłowego poziomu wapnia. Autor: LadyofHats; Źródło: wikipedia.org; Licencja: domena publiczna;
Obecność kationów wapnia w surowicy jest bardzo ściśle regulowana i nie zmienia się ona wraz ze zmianami w dawkowaniu. Organizm wykorzystuje tkankę kostną jako rezerwuar i źródło wapnia do utrzymania jego stałego stężenia we krwi, mięśniach i płynach międzykomórkowych., 4. Stront Istotną funkcję w morskim życiu wodnym odgrywa stront, głównie w przypadku twardych koralowców, które używają go do budowy swoich egzoszkieletów.
Związki strontu, które są nierozpuszczalne w wodzie, mogą stać się w niej rozpuszczalne w wyniku reakcji chemicznych. Związki rozpuszczalne w wodzie stanowią większe zagrożenie dla zdrowia ludzi, niż związki w niej nierozpuszczalne. Dlatego też rozpuszczalne w wodzie formy strontu mogą zanieczyszczać wodę pitną. Na szczęście stężenia w wodzie pitnej są zwykle dość niskie.
Ludzie mogą być narażeni na niewielki poziom (radioaktywnego) strontu poprzez wdychanie powietrza lub pyłów, spożywanie żywności, picie wody zawierającej jego śladowe ilości lub kontakt z glebą zawierającą stront.
Produkty spożywcze, które zawierają wysokie stężenia strontu to zboża, warzywa liściaste i produkty mleczne.
Zdjęcie przedstawia dojrzałe kłosy zbóż w słońcu. Indeks dolny Pole pszenicy. Źródło: pixabay.com; Licencja: domena publiczna;
Jedynym związkiem strontu uważanym za niebezpieczny dla zdrowia ludzkiego, nawet w niewielkich ilościach, jest chromian(sześć) strontu, który powoduje raka płuc, ale ryzyko narażenia zostało znacznie zmniejszone dzięki procedurom bezpieczeństwa.
Dla dzieci przekroczenie wychwytu strontu może stanowić zagrożenie dla zdrowia, ponieważ może powodować problemy ze wzrostem kości (efekt występuje, gdy pobór strontu jest w zakresie tysięcy ppm). Sole strontu nie powodują wysypek skórnych ani innych problemów skórnych.
Radioaktywny stront (izotop indeks górny, osiemdziesiąt dziewięć, koniec indeksu górnego, S r, o czasie połowicznego rozpadu ok. pięćdziesiąt dni) stanowi znacznie większe zagrożenie dla naszego zdrowia niż stabilny stront. Wysokie stężenie radioaktywnego strontu może powodować anemię i niedobory tlenu, a nawet może prowadzić do choroby nowotworowej, w wyniku uszkodzenia materiału genetycznego w komórkach., 5. Bar Ilość baru wykrywana w żywności i wodzie zwykle nie jest wystarczająco duża, aby stanowić zagrożenie dla zdrowia. Osoby z największym ryzykiem narażenia na bar z dodatkowymi skutkami zdrowotnymi to osoby pracujące w przemyśle chemicznym związków baru. Większość zagrożeń dla zdrowia, którym mogą oni podlegać, jest spowodowanych wdychaniem powietrza zawierającego siarczan(sześć) baru lub węglan baru.
Ilustracja przedstawia prostopadłościan. Wypełniony jest pojedynczymi zielonymi kulkami oraz cząsteczkami, w których jedna żółta kulka łączy się z czterema czerwonymi kulkami. Indeks dolny Siarczan(sześć) baru - struktura molekularna kryształu. Autor: Benjah‑bmm27; Źródło: wikipedia.org; Licencja: domena publiczna;
Wiele składowisk odpadów niebezpiecznych zawiera określone ilości baru. Osoby mieszkające w ich pobliżu mogą być narażone na ich szkodliwe poziomy, które mogą być spowodowane wdychaniem pyłu, jedzeniem gleby, roślin lub picie wody zanieczyszczonej barem. Może również wystąpić kontakt ze skórą.
Skutki zdrowotne baru zależą od rozpuszczalności związków w wodzie. Związki baru, które się w niej rozpuszczają, mogą być szkodliwe dla zdrowia ludzkiego. Wychwyt bardzo dużych ilości baru, który jest rozpuszczalny w wodzie, może powodować paraliż, a w niektórych przypadkach nawet śmierć.
Małe ilości rozpuszczalnego w wodzie baru mogą powodować trudności w oddychaniu, podwyższone ciśnienie krwi, zmiany rytmu serca, podrażnienie żołądka, osłabienie mięśni, zmiany w odruchach nerwowych, obrzęk mózgu i wątroby, uszkodzenie nerek i serca., 6. Rad Rad jest naturalnie obecny w środowisku w bardzo małych ilościach. Z tego powodu zawsze jesteśmy narażeni na ten pierwiastek chemiczny i niewielkie ilości jego promieniowania, które uwalnia on do środowiska.
Poziom radu w środowisku znacznie wzrósł w wyniku działalności człowieka. Ludzie uwalniają rad do środowiska, spalając węgiel i inne paliwa. Poziom radu w wodzie pitnej może być wysoki, gdy jest on wydobywany z głębokich studni, które znajdują się w pobliżu miejsc składowania odpadów radioaktywnych.
Ekspozycja na wyższe poziomy radu może powodować skutki zdrowotne, takie jak złamania zębów, anemia i zaćma. Kiedy narażenie trwa przez długi czas, rad może nawet prowadzić do choroby nowotworowej, a ekspozycja może ostatecznie doprowadzić do śmierci. Efekty te mogą rozwijać się latami i zwykle są spowodowane przez promieniowanie gamma radu, którego fale mogą przemieszczać się w powietrzu na dość duże odległości. Dlatego kontakt z radem nie jest konieczny, aby rad powodował negatywne skutki zdrowotne.
Czy beryl ma szkodliwy wpływ na środowisko? Czy można go znaleźć w glebie, w wodzie, a może w roślinach? Zapoznaj się z grafiką interaktywną przedstawiającą informacje na temat wpływu tego pierwiastka na środowisko naturalne, a następnie wykonaj ćwiczenie .
Czy beryl ma szkodliwy wpływ na środowisko? Czy można go znaleźć w glebie, w wodzie, a może w roślinach? Zapoznaj się z opisem grafiki interaktywnej przedstawiającej informacje na temat wpływu tego pierwiastka na środowisko naturalne, a następnie wykonaj ćwiczenie .
Beryl przedostaje się do dróg wodnych w wyniku ścierania się 1. nietoksycznych, 2. zmniejszają, 3. ponadprzeciętne, 4. toksycznych, 5. skał, 6. organizmów zwierząt gospodarskich, 7. zwiększają, 8. jabłka, 9. przemysłowych ścieków, 10. powietrza, 11. przeciętne, 12. groszek ogrodowy, 13. roślin, 14. działalności człowieka i gleby. Większość produktów berylu pochodzenia ludzkiego, które dostają się do dróg wodnych, pochodzi ze zrzutów 1. nietoksycznych, 2. zmniejszają, 3. ponadprzeciętne, 4. toksycznych, 5. skał, 6. organizmów zwierząt gospodarskich, 7. zwiększają, 8. jabłka, 9. przemysłowych ścieków, 10. powietrza, 11. przeciętne, 12. groszek ogrodowy, 13. roślin, 14. działalności człowieka i pyłu berylowego z powietrza, z działalności przemysłowej osadzającej się na wodzie.
Niektóre owoce i warzywa, takie jak 1. nietoksycznych, 2. zmniejszają, 3. ponadprzeciętne, 4. toksycznych, 5. skał, 6. organizmów zwierząt gospodarskich, 7. zwiększają, 8. jabłka, 9. przemysłowych ścieków, 10. powietrza, 11. przeciętne, 12. groszek ogrodowy, 13. roślin, 14. działalności człowieka, fasola i gruszki, mogą zawierać 1. nietoksycznych, 2. zmniejszają, 3. ponadprzeciętne, 4. toksycznych, 5. skał, 6. organizmów zwierząt gospodarskich, 7. zwiększają, 8. jabłka, 9. przemysłowych ścieków, 10. powietrza, 11. przeciętne, 12. groszek ogrodowy, 13. roślin, 14. działalności człowieka poziomy berylu. Większość berylu, który dostaje się do 1. nietoksycznych, 2. zmniejszają, 3. ponadprzeciętne, 4. toksycznych, 5. skał, 6. organizmów zwierząt gospodarskich, 7. zwiększają, 8. jabłka, 9. przemysłowych ścieków, 10. powietrza, 11. przeciętne, 12. groszek ogrodowy, 13. roślin, 14. działalności człowieka z pożywieniem, jest szybko wydalana z moczem i kałem.
Sporządź mapę pojęciową, która zobrazuje zastosowania berylowców jako pierwiastków. Odszukaj niezbędne informacje w dostępnych źródłach.
Sporządź mapę pojęciową, która zobrazuje zastosowania ważniejszych związków berylowców. Odszukaj niezbędne informacje w dostępnych źródłach.