Czym dym różni się od mgły, czyli o układach koloidalnych
Czym są koloidy?
Układy koloidalne (koloidy) to mieszaniny niejednorodne, które składają się zazwyczaj z dwóch substancji – faz, z których jedna jest rozproszona w drugiej. Faza ciągła to substancja rozpraszająca, zwana też ośrodkiem dyspersyjnym. Faza rozproszona to substancja zawieszona (zdyspergowana) w ośrodku dyspersyjnym i w nim nierozpuszczalna. Średnica cząstek rozproszonych jest rzędu 10Indeks górny -7-7-10Indeks górny -9-9 m (1‑100 nm), a nawet do 10Indeks górny -6-6 m (1 µmµm). Cząstki większe niż 5 · 10Indeks górny -7-7 m (500 nm) występują w zawiesinach. W przyrodzie spotykamy różne układy koloidalne. Przykładem koloidu tłuszczu w cieczy są: masło, mleko (krople białka i tłuszczu w wodzie), majonez (przykład koloidu żółtek jajka w oleju), mgła (zawiesina kropel wody lub lodu w powietrzu). Mgła jest koloidem typu aerozolu (ciecz w gazie), podobnie jak dym (ciało stałe w gazie). Koloidami są także dymy powstające w procesie spalania oraz roztwory białek.
Podział układów koloidalnych ze względu na stan skupienia przedstawiono w tabeli poniżej.
Faza rozpraszająca | Faza rozproszona | Przykłady | Nazwa układu koloidalnego |
|---|---|---|---|
gaz | gaz | powietrze | brak |
gaz | ciecz | chmury, mgła, | aerozole ciekłe |
gaz | ciało stałe | dym, kurz | aerozole stałe |
ciecz | gaz | piana mydlana | piana |
ciecz | ciecz | mleko, lakier do paznokci, | emulsja |
ciecz | ciało stałe | kolidalne srebro w wodzie | zol |
ciało stałe | gaz | styropian, pumeks | piany stałe |
ciało stałe | ciecz | opal | emulsja stała |
ciało stałe | ciało stałe | szkło rubinowe | zol |
Wilgotne powietrze i obniżenie temperatury sprzyjają powstawaniu mgły. Gorące powietrze ma większą zdolność ,,przechowywania’’ pary wodnej. Wraz ze wzrostem temperatury, wchodzące w skład powietrza cząsteczki gazów poruszają się coraz szybciej i coraz bardziej odsuwają od siebie, tym samym pozostawiają więcej miejsca na molekuły . Gdy powietrze zaczyna się ochładzać, cząsteczki ścieśniają się i w pewnym momencie (poniżej tzw. punktu rosy) dla pary wodnej zaczyna w nich ,,brakować’’ miejsca. Wtedy właśnie część wody musi się skroplić i w efekcie powstają zawieszone w powietrzu kropelki średnicy poniżej 0,05 mm. W główce szpilki zmieściłoby się ich około tysiąca.
Cechy układów koloidalnych
Jedną z najbardziej charakterystycznych cech układów koloidalnych są tzw. ruchy Brownaruchy Browna. Pierwsze nieregularne ruchy i zderzenia małych cząstek pyłków kwiatowych „zawieszonych” w gazach i cieczach zaobserwował w 1827 r. pod mikroskopem optycznym szkocki biolog, Robert Brown. Był przekonany, że drobinki materii poruszają się dzięki „własnej woli”. Wyjaśnienie i opracowanie teoretyczne (matematyczne) ruchów Browna zawdzięczamy Albertowi Einsteinowi oraz polskiemu fizykowi Marianowi Smoluchowskiemu.
Efekt TyndallaEfekt Tyndalla to zjawisko fizyczne opisane w 1859 r. przez irlandzkiego badacza Johna Tyndalla, towarzyszące przepuszczaniu światła przez układ koloidalny. Promienie światła ulegają rozproszeniu na cząstkach fazy rozproszonej, które mają rozmiary mniejsze od długości fali świetlnej. W wyniku uginania się promieni na cząstkach fazy rozproszonej, światło staje się widoczne w postaci tzw. stożka Tyndalla.

Występowanie efektu Tyndalla jest wykorzystywane do oznaczania mas cząsteczkowych substancji rozpuszczonych w roztworach koloidalnych oraz do wyznaczania stężeń tych roztworów. Można także wyznaczać kierunki poruszania się cząstek, które poddają się bezładnym ruchom Browna.
Dlaczego mgłamgła, której fazę rozproszoną stanowią kuliste cząstki cieczy, a fazą rozpraszającą jest gaz lub mieszanina gazowa, nie jest przezroczysta?

Wiązka światła przechodząca przez krople wody ulega rozproszeniu, odbija się i przechodzi przez nie, zmieniając przy tym kierunek. Czasem zachowuje się tak, jakby odbiła się od powierzchni lustra. Dlatego wjeżdżając w mgłę z włączonymi światłami wydaje nam się, że mgła jest źródłem światła. Takie zjawisko ogranicza widoczność.
Czym jest dym?
DymDym jest układem koloidalnym, w którym fazą rozpraszającą jest gaz, a fazą rozproszoną są cząstki substancji stałych, utworzone przez zestalenie się par, sublimację lub reakcję chemiczną. Dymy powstają z przedostających się do atmosfery stałych produktów podczas spalania paliw, np. z kotłowni, pojazdów lub pochodzących z działalności przemysłowej.

Stosowanie na polu walki trujących i duszących dymów znane było już w starożytności. Uzyskiwano je zwykle ze spalania smoły, tłuszczu, siarki czy arszeniku. Według kroniki Długosza, zasłonę dymną zastosowali chociażby Tatarzy w bitwie pod Legnicą. Dymy wytwarzane celowo do walki zbrojnej to tzw. dymy bojowe. Dymy i zanieczyszczenia, których głównym źródłem są spaliny samochodowe, cząstki sadzy, popiołu, przemysł ciężki i gospodarstwa domowe (systemy grzewcze), w połączeniu z bezwietrzną pogodą i dużą wilgotnością powietrza – mgłą – tworzą smog. Ze względu na sposób tworzenia, miejsce powstawania oraz skład chemiczny, wyróżnia się smog londyński (występujący głównie w miesiącach zimowych) i smog typu Los Angeles (spotykany głównie w miesiącach letnich).
Czy w laboratorium można stworzyć mgłę?
Zapoznaj się z instrukcją doświadczenia oraz przedstawionymi obserwacjami, a następnie zapisz wnioski.
Doświadczenie należy przeprowadzić pod dygestorium ze sprawnym wyciągiem. Osoba wykonująca doświadczenie (nauczyciel) musi mieć okulary ochronne, fartuch i rękawiczki ochronne. Nie wolno wdychać oparów.

Zapoznaj się z filmem, a następnie spróbuj własnymi słowami odpowiedzieć na pytanie: czym różni się dym od mgły?

Film dostępny pod adresem /preview/resource/R5cp8gXJhDvef
Film nawiązujący do treści materiału - dotyczy rozróżnienia dymu od mgły.
Fazę dyspersyjną w przypadku mgły stanowi powietrze, a fazę zdyspergowaną stałe cząstki pozostałości po procesach spalania niewielkie krople wody.
W przypadku dymu fazą rozproszoną są stałe cząstki pozostałości po procesach spalania niewielkie krople wody, a fazą rozpraszającą jest powietrze woda.
Mgła powstaje w wyniku kondensacji pary wodnej spalania materiałów palnych. Mgła oraz dym jako przykłady układów koloidalnych zawiesin rozpraszają światło.
Emulsje
Emulsje są to układy złożone z niemieszających się cieczy, przy czym jedna z nich jest rozproszona w drugiej w postaci drobnych kropelek. Woda jest zazwyczaj jedną fazą (warstwą), natomiast drugą stanowi ciecz niemieszająca się z nią, nazywana fazą olejową. Ze względu na rozdrobnienie, emulsja wygląda pozornie na jednorodną, a jej strukturę niejednorodną można (ze względu na wymiary fazy rozproszonej) obserwować dopiero pod mikroskopem. Emulsje są jednym z rodzajów koloidów.
Budowę emulsji można scharakteryzować przez wzajemny układ faz i ich objętościowe stosunki. Ze względu na wzajemny układ faz wyróżnia się dwa rodzaje emulsji typu olej w wodzie (gdzie woda stanowi substancję rozpraszającą, w której zawieszone są kropelki oleju) i typu woda w oleju (gdzie substancją rozpraszającą jest olej, w którym zawieszone są kropelki wody).
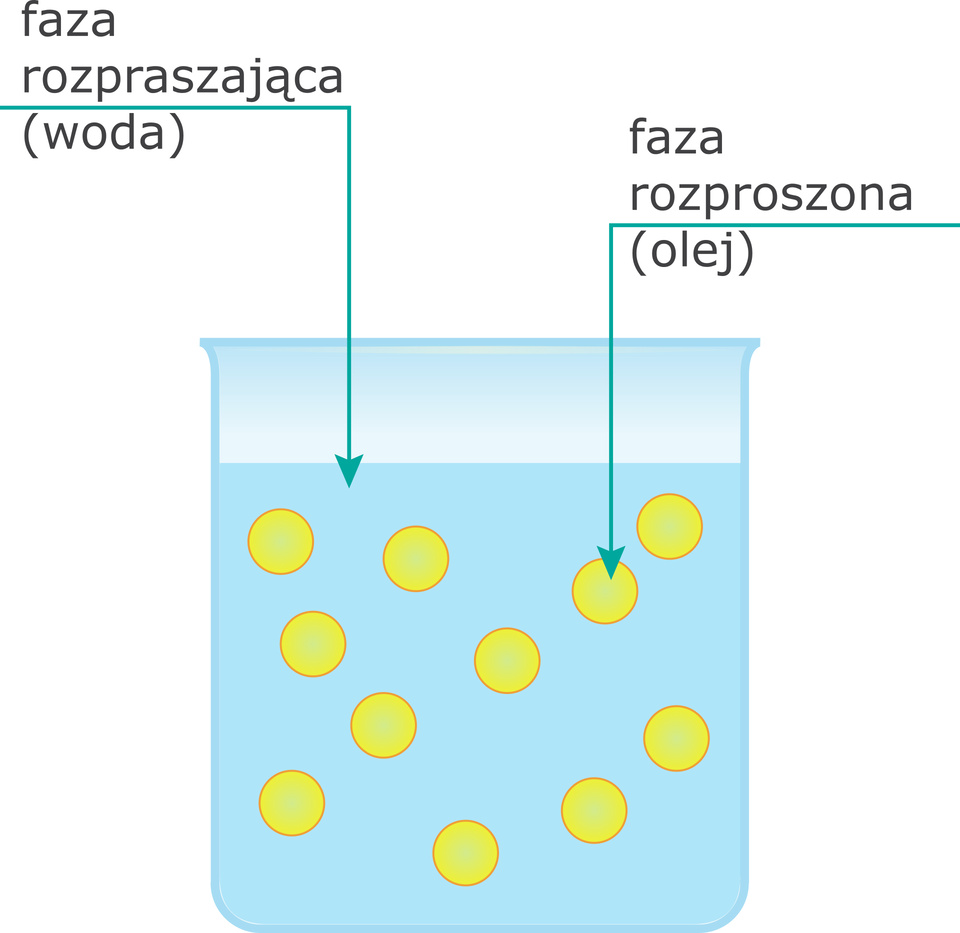
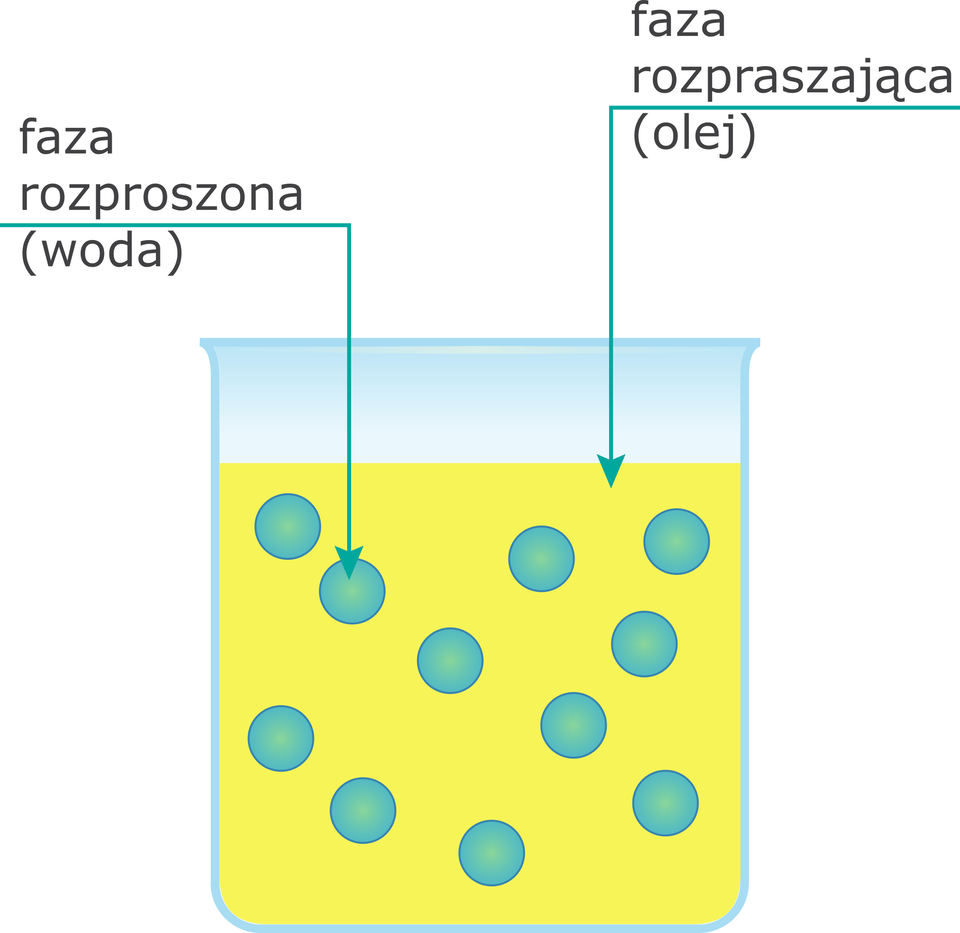
Wyróżnia się też emulsje wielofazowe, które charakteryzują się tym, że nie można dokładnie określić, która faza jest fazą rozproszoną, a która rozpraszającą, ponieważ każda z nich zawiera w sobie kropelki innej fazy.
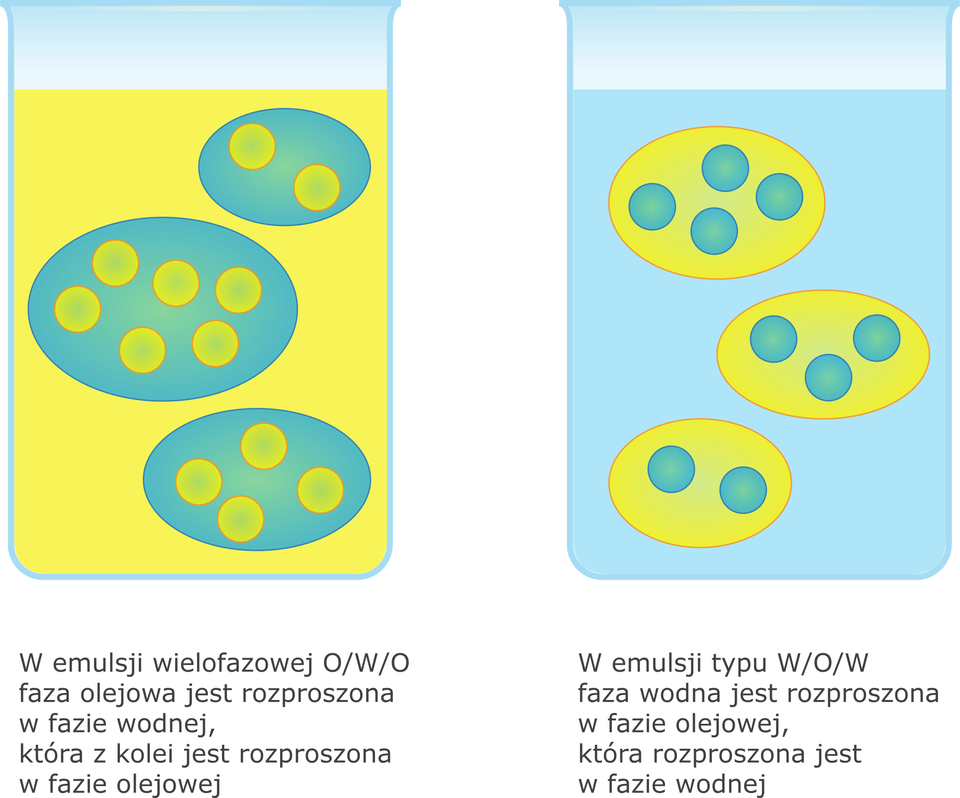
Emulsja może być trwała wskutek obecności emulgatorów. Emulgator zwykle lepiej rozpuszcza się w jednej z dwóch faz.
Emulgatory są związkami powierzchniowo czynnymi, o właściwościach hydrofobowo‑hydrofilowych, tworzącymi warstwę molekularną na powierzchni kropelek rozproszonej cieczy. Ich przykładami są mydła, detergenty, estry alkoholi wielowodorotlenowych oraz takie substancje naturalne, jak żelatyna, agar‑agar, lanolina, lecytyna, guma arabska.
Cechą charakterystyczną wszystkich emulgatorów jest ich budowa – składają się z części hydrofilowej (głowa) i hydrofobowej (ogon). Dodatek emulgatora do mieszaniny oleju z wodą powoduje ułożenie/orientację hydrofobowych ogonów na powierzchni kropelek oleju, a hydrofilowych głów w kierunku wody. Część hydrofilowa emulgatora zawsze jest „zanurzona” w wodzie – bez względu na to, czy stanowi ona fazę rozproszoną, czy rozpraszającą. Na granicy olej‑woda tworzy się w ten sposób warstwa, która zapobiega łączeniu się kropelek oleju w większe ugrupowania. Tak emulgator utrwala emulsję.

Film dostępny pod adresem /preview/resource/RuzqOyxfpc50A
Cechą charakterystyczną wszystkich emulgatorów jest ich budowa – składają się z części hydrofilowej (głowa) i hydrofobowej (ogon). Dodatek emulgatora do mieszaniny oleju z wodą powoduje ułożenie/orientację hydrofobowych ogonów na powierzchni kropelek oleju, a hydrofilowych głów w kierunku wody. Część hydrofilowa emulgatora zawsze jest „zanurzona” w wodzie – bez względu na to, czy stanowi ona fazę rozproszoną, czy rozpraszającą. Na granicy olej‑woda tworzy się w ten sposób warstwa, która zapobiega łączeniu się kropelek oleju w większe ugrupowania. Tak emulgator utrwala emulsję.
Animacja pokazuje mechanizm wpływu emulgatora na proces tworzenia się emulsji. Zaprezentowano na poziomie molekularnym w jaki sposób zachowują się dwie niemieszające się ciecze bez dodatku emulgatora oraz po dodaniu emulgatora.
Sposoby przygotowania emulsji – sosu musztardowego oraz kremu kosmetycznego

Film dostępny pod adresem /preview/resource/RXOBdJASPHeRQ
Sposoby przygotowania emulsji – sosu musztardowego oraz kremu kosmetycznego
Film przedstawia domowe metody sporządzania dwóch emulsji: sosu musztardowego oraz kremu kosmetycznego. W filmie wymienione zostały wszystkie potrzebne składniki oraz instrukcja wykonania poszczególnych czynności.
Lecytyna to emulgator, który znalazł szerokie zastosowanie w przemyśle spożywczym i kosmetycznym. Głównym jej źródłem są oleje roślinne. Czysta lecytyna stabilizuje emulsje typu , natomiast nieoczyszczona, zawierająca inne substancje towarzyszące, może utrwalać emulsje typu . Lecytyny są fosfolipidami, czyli tłuszczami, które oprócz reszt kwasów tłuszczowych zawierają w cząsteczce reszty kwasu fosforowego.

Skład kwasów tłuszczowych w lecytynie zależy od surowca, z jakiego została uzyskana.
Emulsje znalazły powszechne zastosowanie w przemyśle kosmetycznym. Umożliwiają dotarcie szerokiej gamy składników w nich zawartych w głąb skóry, a także do wnętrza włosów.
Każda emulsja kosmetyczna składa się z bazy tłuszczowo‑woskowej, emulgatorów, surowców dodatkowych oraz wody. Składniki emulsji dobiera się w zależności od przeznaczenia i sposobu działania preparatu kosmetycznego, a także od typu emulsji, jaki chcemy uzyskać. Typowymi emulsjami są kremy, balsamy i mleczka.
Konsystencja lub gęstość emulsji zależą od zawartości fazy rozproszonej, rodzaju emulgatora, lepkości fazy rozpraszającej i obecności w tej fazie substancji wpływających na konsystencję kosmetyku.
Typ emulsji | Zawartość fazy rozproszonej | Zastosowanie |
|---|---|---|
|
| kremy nawilżające, podkładowe, balsamy do ciała, maseczki, dezodoranty, niektóre odżywki do włosów |
|
| kremy, kremy na noc, lekkie kremy pod oczy, mleczka, niektóre odżywki do włosów |
|
| kremy tłuste, na noc, pod oczy, kremy uniwersalne, ochronne, mleczka do demakijażu |
Krem kosmetyczny
Najprostszy krem składa się z tłuszczu, wody i emulgatora. Często zawiera więcej niż jeden emulgator, ponieważ zapewnia to lepszą stabilność i daje pewność, że nie będzie się rozwarstwiał. Emulgatory są jednocześnie hydrofobowe i hydrofilowe. Służą zdrowiu i zdrowemu wyglądowi. Dla przykładu wymienić można lecytynę, lanolinę czy cholesterol.

Film dostępny pod adresem /preview/resource/R1cYpCCKTeUk4
Film przedstawia informacje dotyczące kremów. Omawia jakie typy emulsji wykorzystywane są do ich produkcji, jakie jest ich działanie na skórę oraz omawia ich dodatkowe właściwości.
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Biała emulsja pochodzenia naturalnego.
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Substancje utrwalające emulsję.
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Fragment budowy emulgatora oddziałujący z fazą wodną.
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Wiele z tych produktów ma postać emulsji.
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Faza nielubiąca wody – faza...
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Popularna w kuchni emulsja, dodatek do sałatek i przekąsek.
1. kosmetyki, 2. lecytyna, 3. hydrofilowy, 4. emulgatory, 5. majonez, 6. mleko, 7. olejowa
Zastosowania emulsji
Piany
Piany to układy koloidalne, które powstają na skutek dyspersji gazu w fazie ciekłej lub stałej. Fazę zdyspergowaną stanowi w nich gaz, natomiast ośrodkiem rozpraszającym może być ciecz lub ciało stałe. Ich trwałość uzależniona jest od lepkości ośrodka rozpraszającego – im większa lepkość, tym trwalsze są piany. Ze względu na kształty fazy rozproszonej wyróżnia się:
piany kulkowe, w których pęcherzyki gazu nie oddziałują na siebie;
piany wielościenne (poliedryczne), gdzie pęcherzyki gazu oddzielone są od siebie związkami powierzchniowo czynnymi.
Przykładem piany, powstałej na skutek dyspersji gazu w ciele stałym, jest szkło piankowe. Jest to materiał stosowany w budownictwie do izolacji termicznych oraz akustycznych, otrzymywany w wyniku dodania do roztopionego szkła domieszek pianotwórczych. Naturalnym odpowiednikiem szkła piankowego jest pumeks, powstały na skutek szybkiego zastygania lawy wulkanicznej wraz z pęcherzykami gazu. Podobnie jak emulsje, piany również mają wiele ciekawych zastosowań. Wykorzystywane są m.in. w pożarnictwie (w gaśnicach pianowych), w przemyśle spożywczym (bita śmietana), w metalurgii (wzbogacanie rud metodą flotacji). Piany mogą ulec zniszczeniu na skutek wysokiego ciśnienia lub promieniowania.
Notatnik
media={R17TY7A3VUjRk}


