Sporządzanie roztworu o znanym stężeniu procentowym
Jak w praktyce laboratoryjnej można przygotować roztworu o stężeniu . Ile gramów soli kuchennej (chlorku sodu, ) i ile wody należy użyć?

Film dostępny pod adresem /preview/resource/R1Ou2wONlUdHr
Film nawiązujący do treści materiału dotyczącej sporządzania roztworów o określonym stężeniu procentowym.
Obliczenia ułatwiające rozcieńczanie roztworów
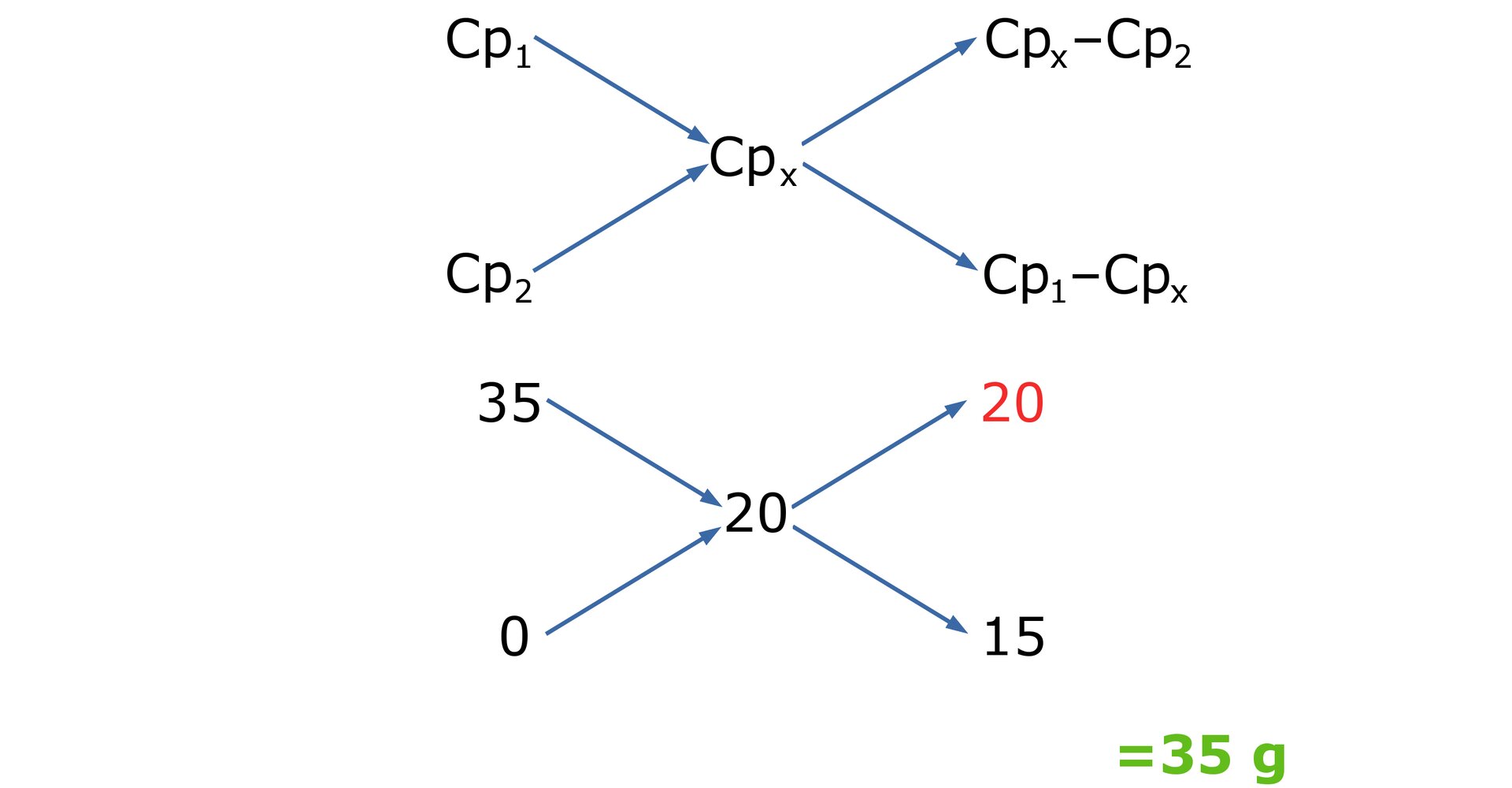
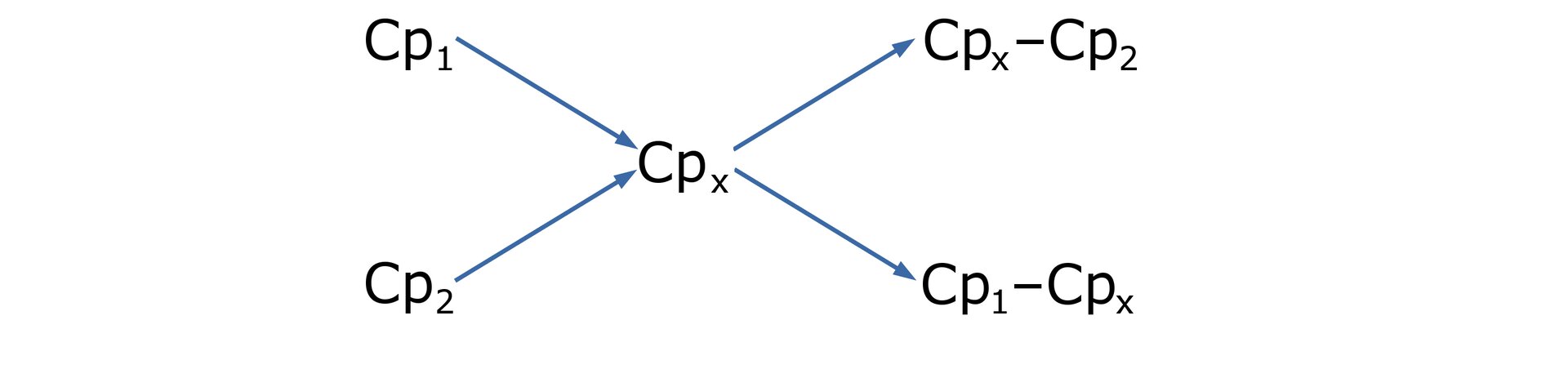
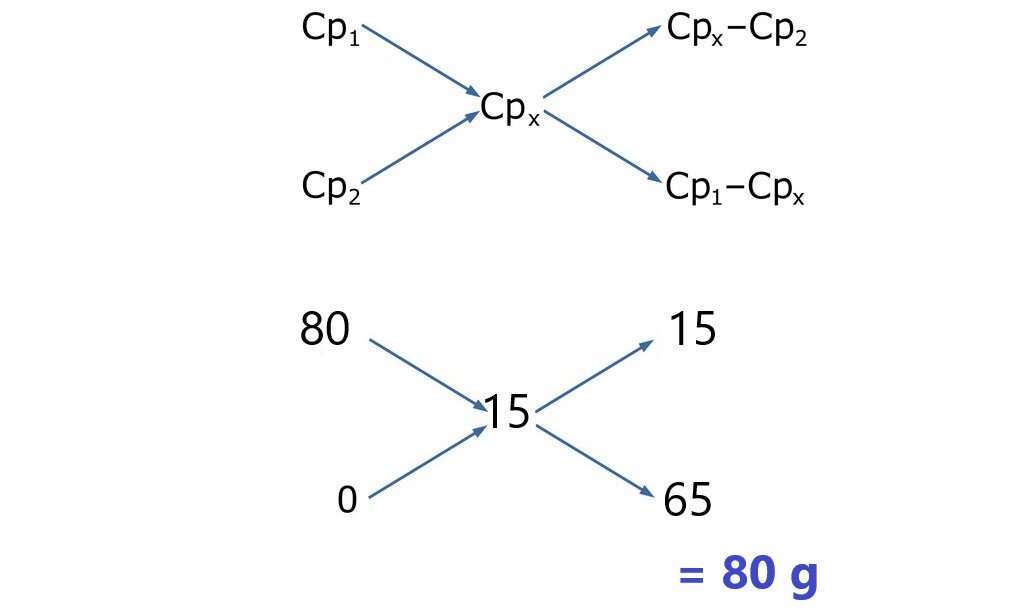
Obliczenia dotyczące mieszania lub rozcieńczania roztworów można wykonać stosując tzw. metodę krzyżową. Jeśli rozcieńczymy roztwór czystym rozpuszczalnikiem albo zmieszany dwa roztwory tej samej substancji o różnych stężeniach to otrzymamy nowy roztwór.
Opisz sposób przygotowania roztworu kwasu solnego, mając do dyspozycji butelkę kwasu solnego, którego stężenie procentowe wynosi . Na etykiecie butelki widnieją również informacje takie jak: , .
W jakim stosunku masowym należy zmieszać roztwór z roztworem tej samej substancji, aby otrzymać roztwór ?
Oblicz, ile wody należy dodać do , aby uzyskać stężenie ? Przyjmij, że gęstość wody wynosi w temperaturze .
Zaznacz poprawną odpowiedź.
Do zlewki dodano wody, a następnie wsypano azotan() kobaltu() aż do nasycenia roztworu. Co należy zrobić, aby stężenie procentowe zmniejszyło się?
Co nalezy zrobić, aby z wodnego roztworu chlorku sodu o stężeniu uzyskać roztwór o wyższym stężeniu?
Wyobraź sobie, że pracujesz w laboratorium syntezy organicznej. Realizujesz projekt, który zakłada otrzymanie pewnego związku organicznego o ciekawych właściwościach spektroskopowych. Jednym z etapów syntezy jest oczyszczanie produktu organicznego i wykonanie ekstrakcji. Procedura ekstrakcji zakłada przemycie fazy organicznej przy pomocy roztworu kwasu octowego (etanowego) o stężeniu .
W jaki sposób przygotujesz (około ) roztworu o stężeniu , jeżeli w laboratorium znajduje się wyłącznie kwas octowy o stężeniu ? Na etykiecie butelki ze stężonym kwasem widnieją również, takie informacje jak: , .
Zapoznaj się z filmem edukacyjnym i spróbuj rozwiązać ten problem. W trakcie oglądania filmu zastanów się, dlaczego w życiu codziennym znajomość stężenia procentowego roztworu jest tak bardzo ważna. Następnie rozwiąż ćwiczenia sprawdzające.
Eksperymentuj
Czy wiesz, jak sporządzić roztwór o określonym stężeniu procentowym? Przeprowadź eksperyment w laboratorium chemicznym. Pamiętaj o wyzerowaniu masy zlewki przed przystąpieniem do sporządzania roztworów.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5D9C1MZ6
Wirtualne laboratorium „Sporządzanie roztworów o określonym stężeniu procentowym”. Temperatura powietrza w laboratorium wynosi dwudziestu stopni Celsjusza.
Na stole laboratoryjnym znajduje się cylinder miarowy, czyli wysokie, wąskie naczynie z miarką do stu mililitrów, służące do odmierzania roztworów. Przezroczysta butelka wypełniona do połowy wodą. Na stole znajduje się także pusta zlewka szklana dwieście mililitrów – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych oraz waga elektroniczna z cyfrowym wyświetlaczem z funkcją tarowania – urządzenie elektryczne służące do wyznaczania mas substancji. Daną substancję umieszcza się na srebrnej tacy umieszczonej na urządzeniu. Masa ważonej substancji wyświetlana jest na wyświetlaczu. Waga pokazuje wagę w jednostce gram. Nad stołem laboratoryjnym wiszą dwie półki na których ustawione są pojemniki z substancjami chemicznymi. Na każdym z pojemników widnieje etykieta z nazwą związku chemicznego oraz środkami ostrożności. Dodatkowo na etykietach podana jest wartość rozpuszczalności danego związku w temperaturze dwadzieścia stopni Celsjusza podanych w gramach na sto gramów wody. Podana jest również masa molowa danego związku chemicznego. Na górnej półce ustawionych jest sześć pojemników w których występuje inna substancja: chlorek kobaltu () (rozpuszczalność: grama na sto gramów wody, masa molowa: grama na mol), azotan () kobaltu () (rozpuszczalność: grama na sto gramów wody, masa molowa: grama na mol), siarczan () miedzi () (rozpuszczalność: gramów na sto gramów wody, masa molowa: 1 grama na mol), chromian () potasu ( gramów na sto gramów wody, masa molowa: grama na mol), dichromian () potasu (rozpuszczalność: grama na sto gramów wody, masa molowa: grama na mol), manganian () potasu (rozpuszczalność gramów na sto gramów wody, masa molowa: grama na mol), chlorek sodu (rozpuszczalność: grama na sto gramów wody, masa molowa: grama na mol) i chlorek niklu () (rozpuszczalność: grama na sto gramów wody, masa molowa: grama na mol). Dodatkowo na półce leży szklana bagietka służąca do mieszania roztworów. Na dolnej półce ustawione są cztery pojemniki, w których są następujące substancje: chlorek kobaltu () – woda (rozpuszczalność: grama na sto gramów wody, masa molowa: 3 grama na mol), chlorek żelaza () – woda (rozpuszczalność: gramy na sto gramów wody, masa molowa: grama na mol), siarczan () żelaza () – woda (rozpuszczalność: gramów na sto gramów wody, masa molowa: gramów na mol) oraz siarczan () magnezu () – woda (rozpuszczalność: gramów na sto gramów wody, masa molowa: grama na mol). Na dolnej półce stoją w szklanym, przezroczystym okrągłodennym pudełku łyżki laboratoryjne służące do naważania.
Przed przystąpieniem do czynności naważania należy wyzerować zlewkę na wadzę. Wówczas ekran wagi pokazuje nam zero gramów i po umieszczeniu w niej wody i związku chemicznego wskaże nam właściwą masę roztworu. Do cylindra miarowego wlewamy odpowiednią ilość wody i przelewamy to do zlewki umieszczonej na wadze. Dodajemy odpowiedniej ilości danego związku chemicznego wykorzystując w tym celu łyżeczkę. Umieszczamy związek w zlewce. Masa na wadze zwiększa się o ilość dosypanego związku. Ściągamy zlewkę z wagi i wykorzystując szklaną bagietkę mieszamy zawartość. Obserwujemy rozpuszczenie związku albo powstanie osadu.
Chcąc uzyskać stężenie procent związku chlorku kobaltu () o rozpuszczalności grama na sto gramów wody i masie molowej grama na mol należy zmieszać mililitrów wody i grama związku. W zlewce obserwujemy całkowite rozpuszczenie się związku. W przypadku dodania zbyt dużej ilości związku przekraczającej możliwości rozpuszczalności obserwuje się wytrącenie osadu. W tym przypadku rozpuszczalność związku wynosi grama na sto gramów wody. Wymieszając gramów z mililitrami wody, otrzymamy roztwór o stężeniu . W zlewce zaobserwujemy wówczas osad.
Chcąc uzyskać stężenie dziesięć procent związku chromianu () potasu o rozpuszczalności grama na sto gramów wody i masie molowej grama na mol należy zmieszać mililitrów wody z gramami związku. W zlewce obserwujemy całkowite rozpuszczenie się związku. W przypadku dodania zbyt dużej ilości związku przekraczającej możliwości rozpuszczalności obserwuje się wytrącenie osadu.