Konstruowanie ogniw
Konstruowanie ogniw
Przed rozpoczęciem eksperymentu zapoznaj się z kartami charakterystyk używanych w doświadczeniu odczynników. Pamiętaj o zachowaniu ostrożności, zastosowaniu środków ochrony osobistej (rękawiczki, fartuch, okulary ochronne) oraz o zachowaniu zasad bezpieczeństwa.
Eksperyment 1
Na podstawie zgromadzonego sprzętu oraz materiału badawczego wykonaj doświadczenie w laboratorium chemicznym, w którym skonstruujesz ogniwo. Zaproponuj problem/problemy badawcze oraz hipotezę/hipotezy. Następnie rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje wyniki, a następnie sformułuj wnioski.
Eksperyment 2
Na podstawie zgromadzonego sprzętu oraz materiału badawczego wykonaj doświadczenie w laboratorium chemicznym, w którym skonstruujesz ogniwo. Zaproponuj problem/problemy badawcze oraz hipotezę/hipotezy. Następnie rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje wyniki, a następnie sformułuj wnioski.
Zapoznaj się uważnie z filmem samouczkiem, w którym poznasz zasady konstruowania ogniw galwanicznych, następnie wykonaj poniższe ćwiczenia.
Film dostępny pod adresem /preview/resource/RUwKVK0hDtppp
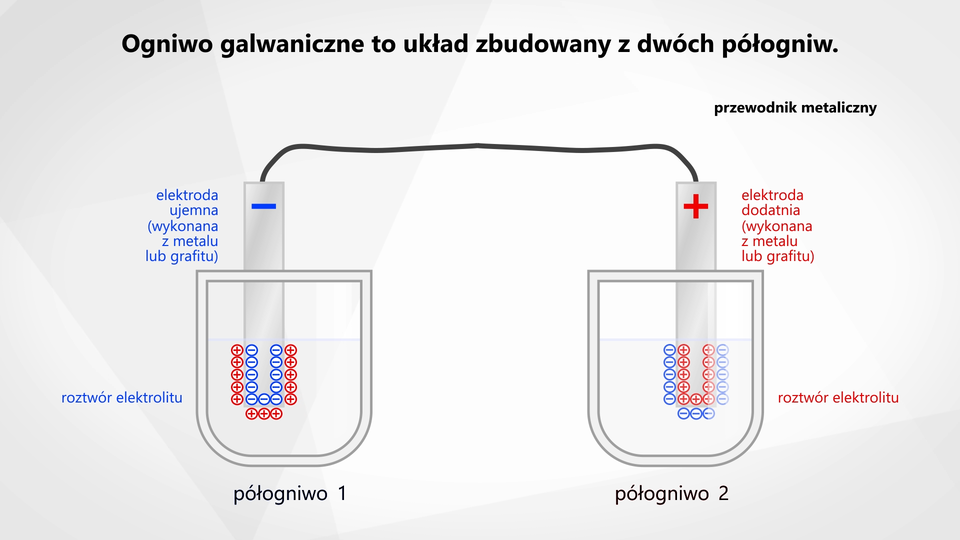
Film nawiązujący do treści materiału - dotyczy konstruowania ogniw galwanicznych. Wyjaśnia pojęcie ogniwa i półogniwa.
Uczeń miał za zadanie skonstruowanie ogniwa cynkowo–ołowiowego. Korzystając z szeregu elektrochemicznego metali, wykonaj poniższe punkty:
Ustal, który z metali będzie pełnił funkcję anody, a który funkcję katody.
Zapisz równania procesów zachodzących w półogniwach.
Zapisz sumaryczne równanie reakcji chemicznej zachodzącej w analizowanym ogniwie.
Zapisz schemat ogniwa cynkowo‑ołowiowego zgodnie z konwencją sztokholmską.