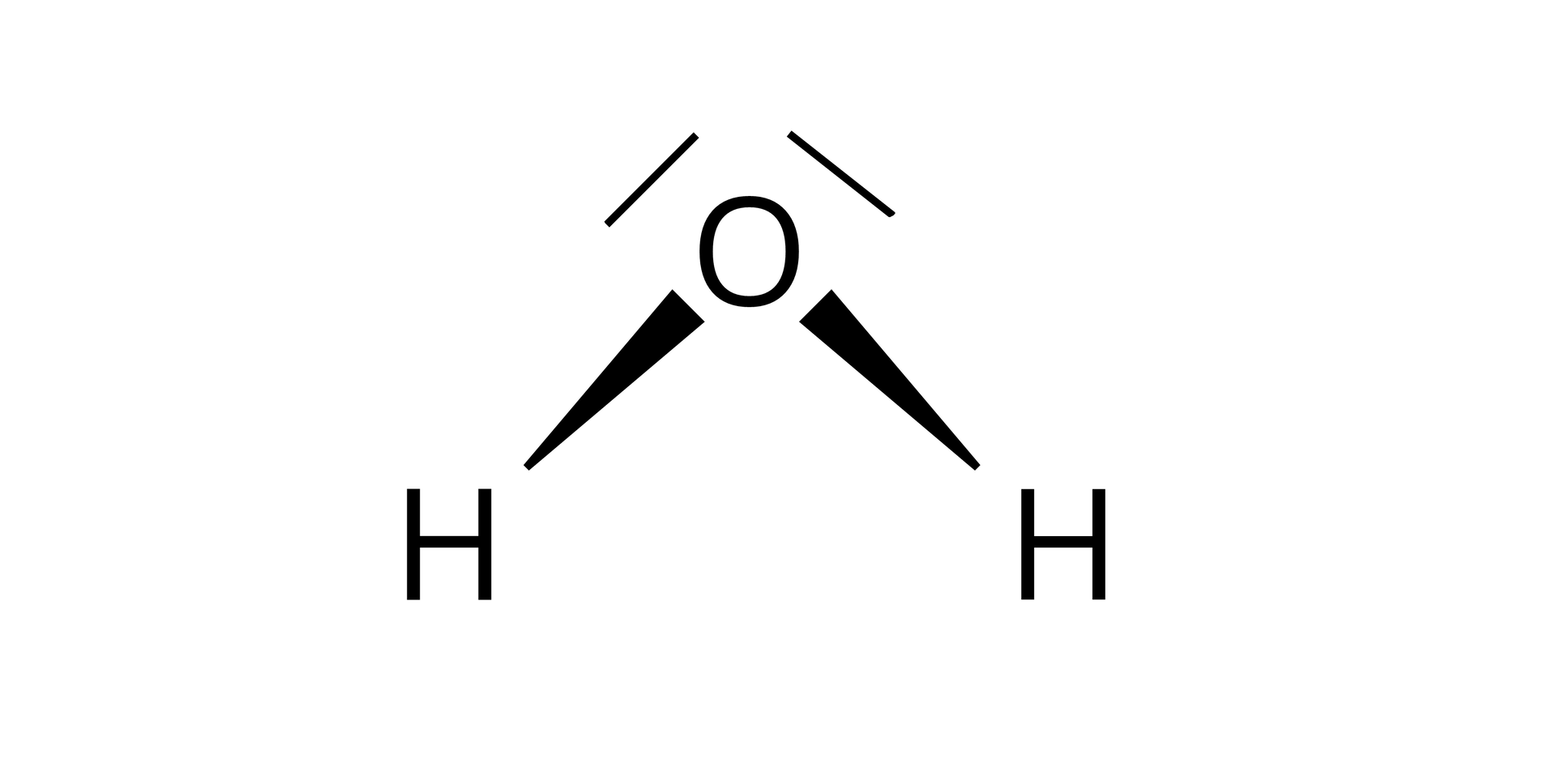
Jak graficznie przedstawić wiązania chemiczne?
Rodzaje wiązań chemicznych
- Nazwa kategorii: Rodzaje wiązań chemicznych
- Nazwa kategorii: Wiązanie jonowe
- Nazwa kategorii: Wiązanie metaliczne
- Nazwa kategorii: Wiązania kowalencyjne
- Nazwa kategorii: Wiązanie kowalencyjne niespolaryzowane
- Nazwa kategorii: Wiązanie kowalencyjne spolaryzowane
- Nazwa kategorii: Wiązanie koordynacyjne Koniec elementów należących do kategorii Wiązania kowalencyjne
- Elementy należące do kategorii Rodzaje wiązań chemicznych
- Elementy należące do kategorii Wiązania
kowalencyjne
Wiązanie jonowe
Wiązanie jonoweWiązanie jonowe jest oddziaływaniem elektrostatycznym pomiędzy jonami pierwiastków, które tworzą związek. Zwyczajowo (dla uproszczenia) przedstawia się wzory sumaryczne związków jonowych, np. soli, podając tylko skład pierwiastkowy związku. Wzór chlorku sodu czy bromku potasu zupełnie nie oddaje charakteru połączenia między atomami. Aby pokazać charakter jonowy tego związku, stosuje się następujący zapis:
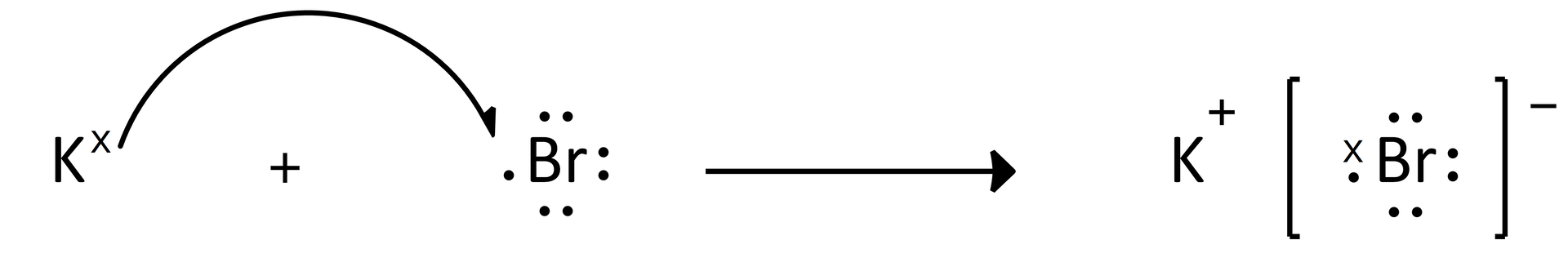
W procesie tworzenia się wiązania jonowego, pierwszym etapem jest powstawanie jonów. W przypadku reakcji potasu i bromu, zachodzi proces powstawania kationu i anionu :
Zapoznaj się z danymi zawartymi w poniższym układzie okresowym i odpowiedz na pytanie – jak zmieniają się rozmiary atomów sodu i fluoru?
Zapoznaj się z opisem ilustracji. Odpowiedz na pytanie – jak zmieniają się rozmiary atomów sodu i fluoru?
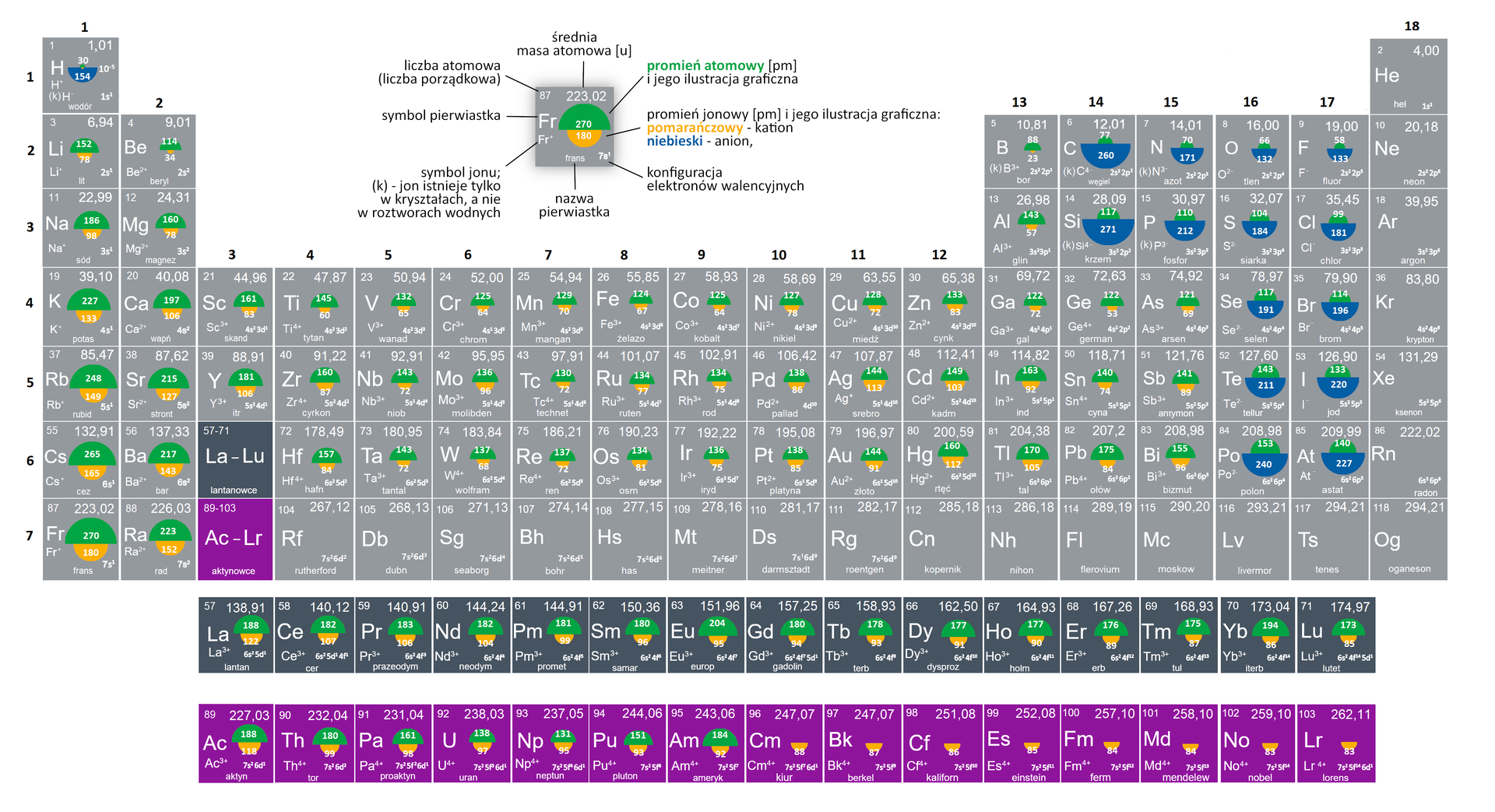
Zastanów się i odpowiedz, dlaczego tak się dzieje?
Wiązania kowalencyjne niespolaryzowane
Wiązanie kowalencyjneWiązanie kowalencyjne niespolaryzowane powstaje w wyniku tworzenia się pomiędzy atomami wspólnych par elektronowych, które najczęściej przedstawia kreska pomiędzy atomami.
Jeżeli w związku tworzą się wiązania wielokrotne, to zaznaczamy je równoległymi kreskami leżącymi pomiędzy atomami, które tworzą to wiązanie.
Wiązania kowalencyjne spolaryzowane
W przypadku, gdy atomy tworzące wiązanie kowalencyjne różnią się elektroujemnościąelektroujemnością, następuje polaryzacja wiązania i mówimy, że jest to wiązanie kowalencyjne spolaryzowane.
Przyjęto, że wiązanie kowalencyjne spolaryzowane tworzy się pomiędzy atomami, dla których różnica elektroujemności jest następująca:
Istnieją wyjątki, tj. wodorek sodu i inne wodorki metali aktywnych, dla których pomimo występującej różnicy elektroujemności niższej niż występuje wiązanie jonowe.
Polaryzację wiązania kowalencyjnego spolaryzowanego przedstawiamy albo za pomocą pogrubionej kreski, albo zaznaczając ładunki cząstkowe przy atomach.
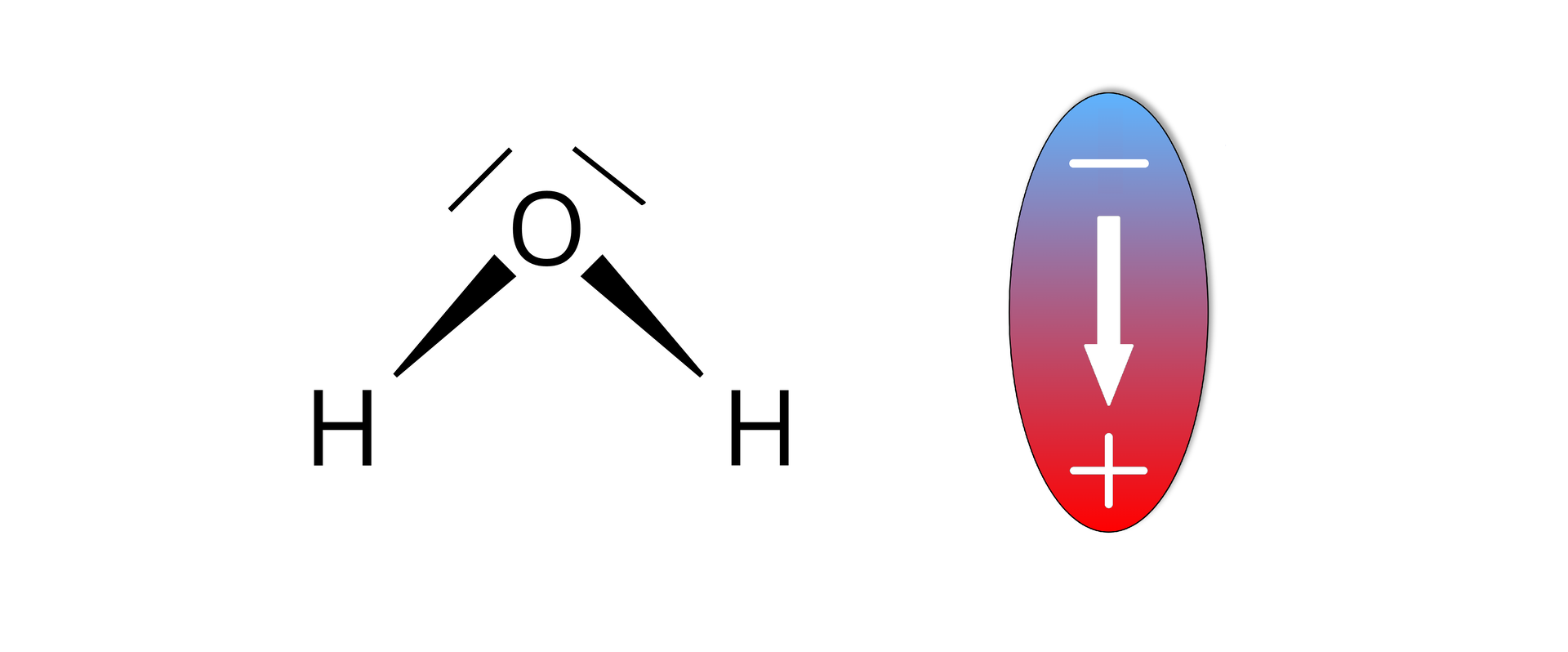
DipolDipol elektryczny i elektryczny moment dipolowy
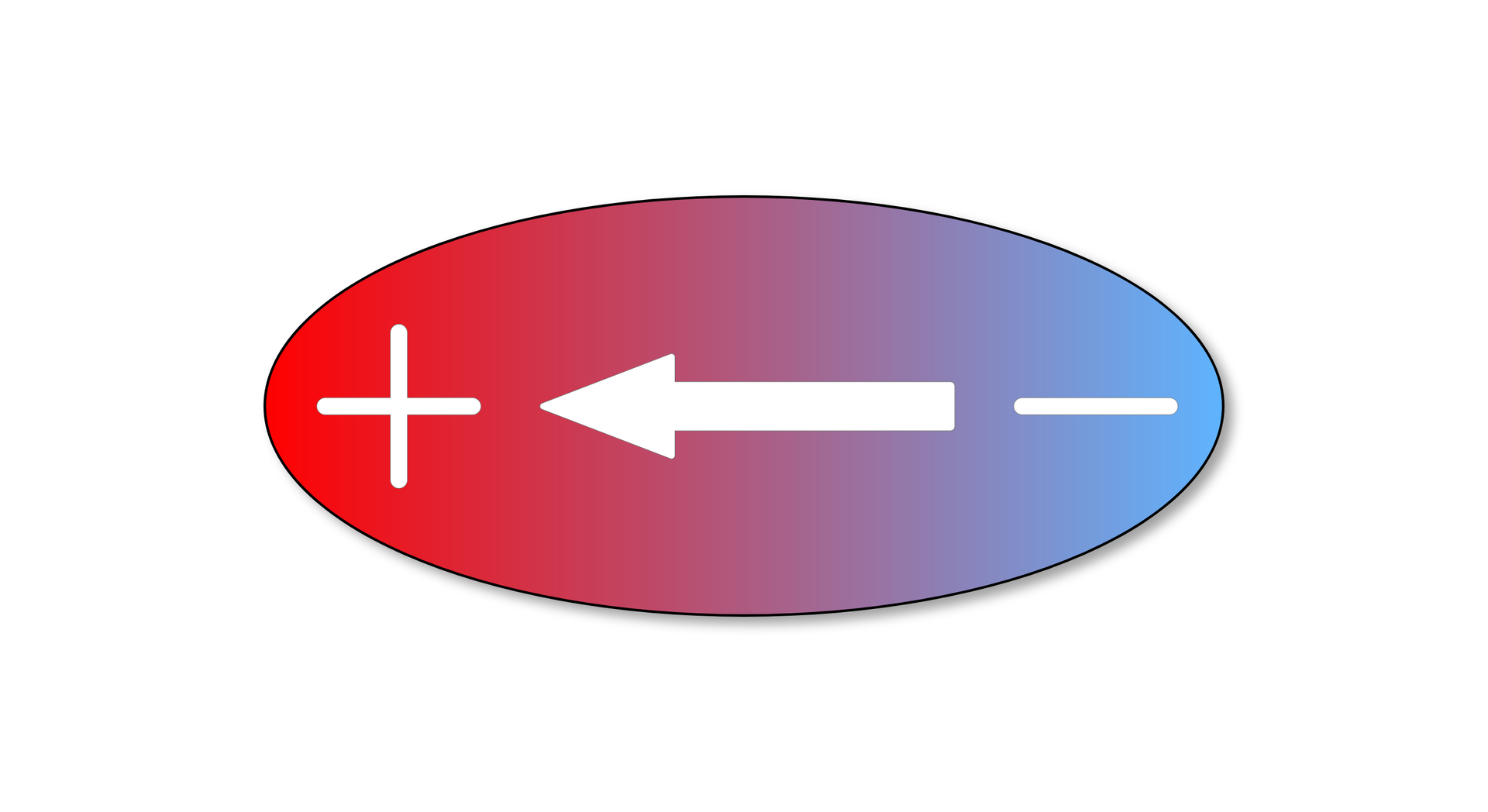
Cząsteczka spolaryzowana (posiadająca bieguny dodatni i ujemny) z fizycznego punktu widzenia jest dipolem. Do wielkości, które charakteryzują dipol, należy moment dipolowy (wielkość wektorowa).
Wiązanie koordynacyjne
Wiązanie koordynacyjne jest rodzajem wiązania kowalencyjnego. Tworzy je para elektronowa, pochodząca od jednego atomu tworzącego wiązanie – donora, przesunięta w kierunku drugiego atomu – akceptora. Wiązanie to zaznacza się strzałką skierowaną w stronę akceptora, np. w jonie amonowym – czy w cząsteczce kwasu azotowego() – .
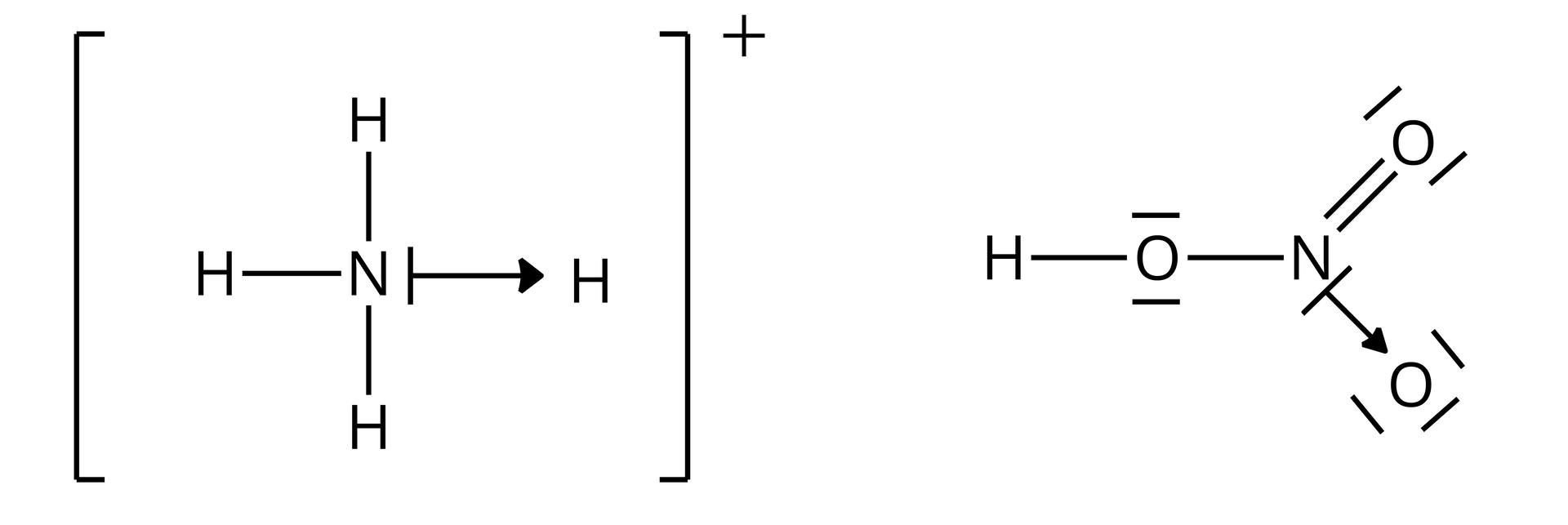
Jak wiesz, atomy w związkach chemicznych są ze sobą połączone różnego rodzaju wiązaniami. Czy wiesz, w jaki sposób można je graficznie przedstawić? Zapoznaj się z poniższą animacją i wykonaj ćwiczenia.
Film dostępny pod adresem /preview/resource/Rz0WQigC8pHAK
Film nawiązujący do treści materiału - przedstawia rodzaje wiązań chemicznych.
Rodzaje wzorów elektronowych
W celu przedstawienia wiązania chemicznego, można zastosować wzory elektronowe, zwane też wzorami Lewisa. Są to wzory strukturalne z zaznaczonym rozmieszczeniem par elektronowych wiążących (elektrony wspólne) i niewiążących (wolne pary elektronowe). Wyróżnić można trzy rodzaje wzorów elektronowych:
kropkowekropkowe (wszystkie elektrony przedstawione są za pomocą kropek);
kreskowekreskowe (każda para elektronów przedstawiona jest za pomocą kreski);
kreskowo–kropkowekreskowo–kropkowe (wiążąca para elektronowa przedstawiona jest kreską, a wolna para elektronowa zaznaczona jest jako dwie kropki).
Wiązanie koordynacyjne jest rodzajem wiązania kowalencyjnego. Tworzy je para elektronowa pochodząca od jednego atomu tworzącego wiązanie – donora, przesunięta w kierunku drugiego atomu – akceptora. Wiązanie to można zaznaczyć we wzorach kreskowych i kreskowo–kropkowych strzałką skierowaną w stronę akceptora.
Tworzenie wzoru elektronowego cząsteczki fluorowodoru
Podczas powstawania cząsteczek z atomów, w wyniku nakładania się orbitali atomowych z niesparowanymi elektronami, uzyskujemy wiążącą parę elektronową, która tworzy orbital cząsteczkowy ze sparowaną parą elektronową. Możliwe jest też utworzenie wiązania, które stanowi para elektronowa tylko jednego z atomów (wiązanie donorowo–akceptorowe). Z kolei wolne pary elektronowe cząsteczka przejmuje w tej samej postaci, w jakiej znajdowały się na atomach. Zasady tworzenia wzoru elektronowego można przedstawić, korzystając z klatkowego zapisu konfiguracji elektronowej atomów, które biorą udział w tworzeniu cząsteczki – np. fluorowodoru (HF).

Atom wodoru posiada jeden niesparowany elektron, ale do uzyskania trwałej walencyjnej konfiguracji elektronowej potrzebuje jeszcze jednego. Podobnie jest w przypadku atomu fluoru, który także potrzebuje jednego elektronu, aby uzyskać trwałą, walencyjną konfiguracją elektronową. Atom fluoru posiada siedem elektronów walencyjnych, w tym trzy pary elektronowe i jeden niesparowany elektron. Miedzy atomami wodoru i fluoru następuje uwspólnienie niesparowanych elektronów i utworzenie tym samym wiążącej pary elektronowej.
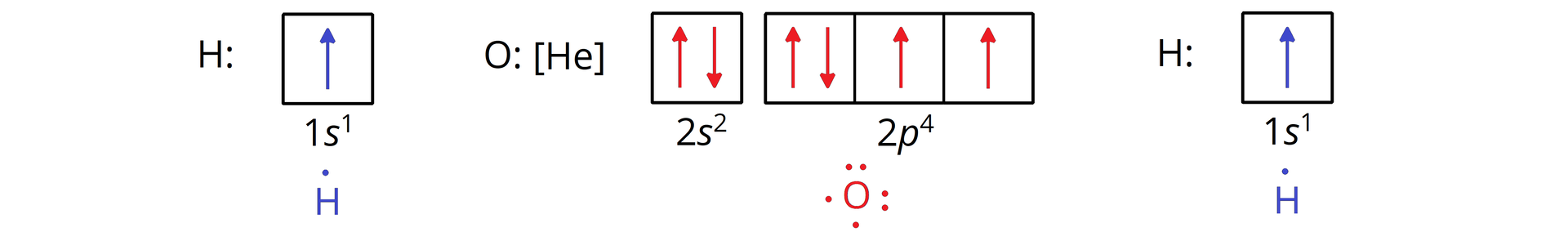
Tworzenie wzoru elektronowego cząsteczki wody
Atom tlenu posiada sześć elektronów walencyjnych, więc do uzyskania trwałej walencyjnej konfiguracji elektronowej brakuje mu dwóch elektronów. Potrzebne elektrony uzyskuje od dwóch atomów wodoru, z którymi uwspólnia swoje dwa elektrony.
Tworzenie wzoru elektronowego jonu hydroniowego
Jeżeli do cząsteczki wody przyłączy się proton, to otrzymany zostanie jon hydroniowy (). W cząsteczce wody oba atomy wodoru i atom tlenu posiadają trwałą walencyjną konfigurację elektronową. Na atomie tlenu znajdują się dwie wolne pary elektronowe, z których jedna zostanie wykorzystana na utworzenie wiązania donorowo‑akceptorowego.
Tworzenie wzoru elektronowego cząsteczki kwasu siarkowego()
Kwas siarkowy() () składa się z dwóch atomów wodoru, jednego atomu siarki i czterech atomów tlenu.

Atomy wodoru posiadają po jednym niesparowanym elektronie, więc brakuje im jednego elektronu do uzyskania trwałej walencyjnej konfiguracji elektronowej. Potrzebny elektron uzyskają od atomów tlenu, które posiadają po cztery elektrony sparowane i dwa niesparowane. Każdy z atomów tlenu przeznaczy swój jeden elektron niesparowany na wiązanie z atomem wodoru. Drugi niesparowany elektron atomów tlenu weźmie udział w tworzeniu wiążącej pary elektronowej z atomem siarki, której do uzyskania trwałej walencyjnej konfiguracji elektronowej brakuje dwóch elektronów. W ten sposób zarówno atomy wodoru, tlenu, jak i atom siarki uzyskują trwałe, walencyjne konfiguracje elektronowe. W celu przyłączenia dwóch kolejnych atomów tlenu, atom siarki przeznacza swoje dwie wolne pary elektronowe na utworzenie wiązania donorowo‑akceptorowego (atom tlenu, chcąc przyjąć parę elektronową, musi przenieść niesparowany elektron na inny orbital, na którym znajduje się elektron, dzięki czemu pozostawia jeden wolny).
Zapoznaj się z filmem pt. „Tworzenie wzorów jonów złożonych”, a następnie rozwiąż poniższe ćwiczenia.

Film dostępny pod adresem /preview/resource/RuNgQs78C37er
Film nawiązujący do treści materiału dotyczącej tworzenia wzorów jonów złożonych.
Napisz wzór elektronowy kropkowo‑kreskowy:
anionu wodorosiarczanowego() ();
anionu diwodoroortofosforanowego() ();
anionu ortofosforanowego() ().
Wskaż prawidłowy wzór elektronowy kreskowy anionu węglanowego, .
Narysuj wzór elektronowy kreskowy anionu azotanowego() .