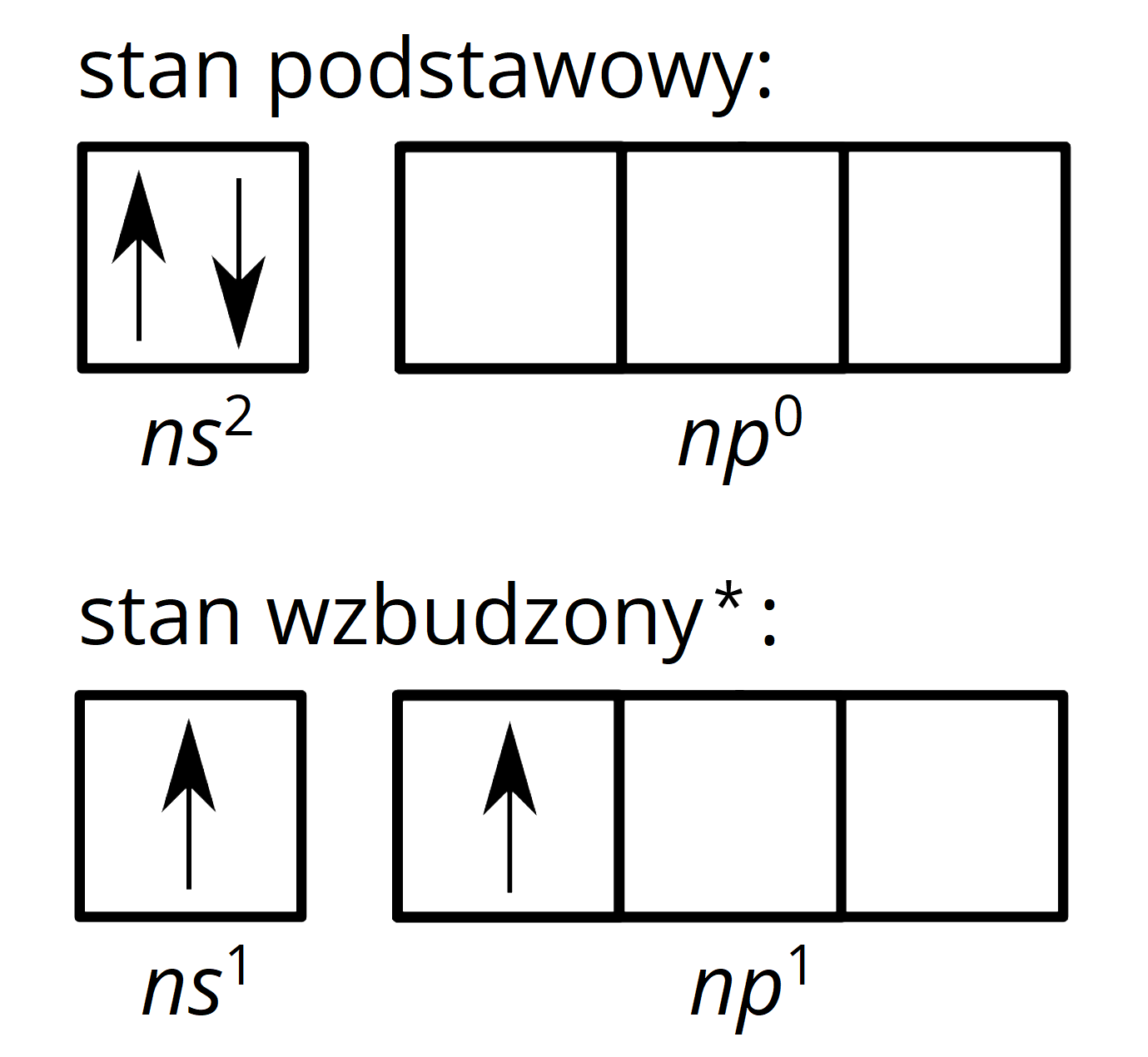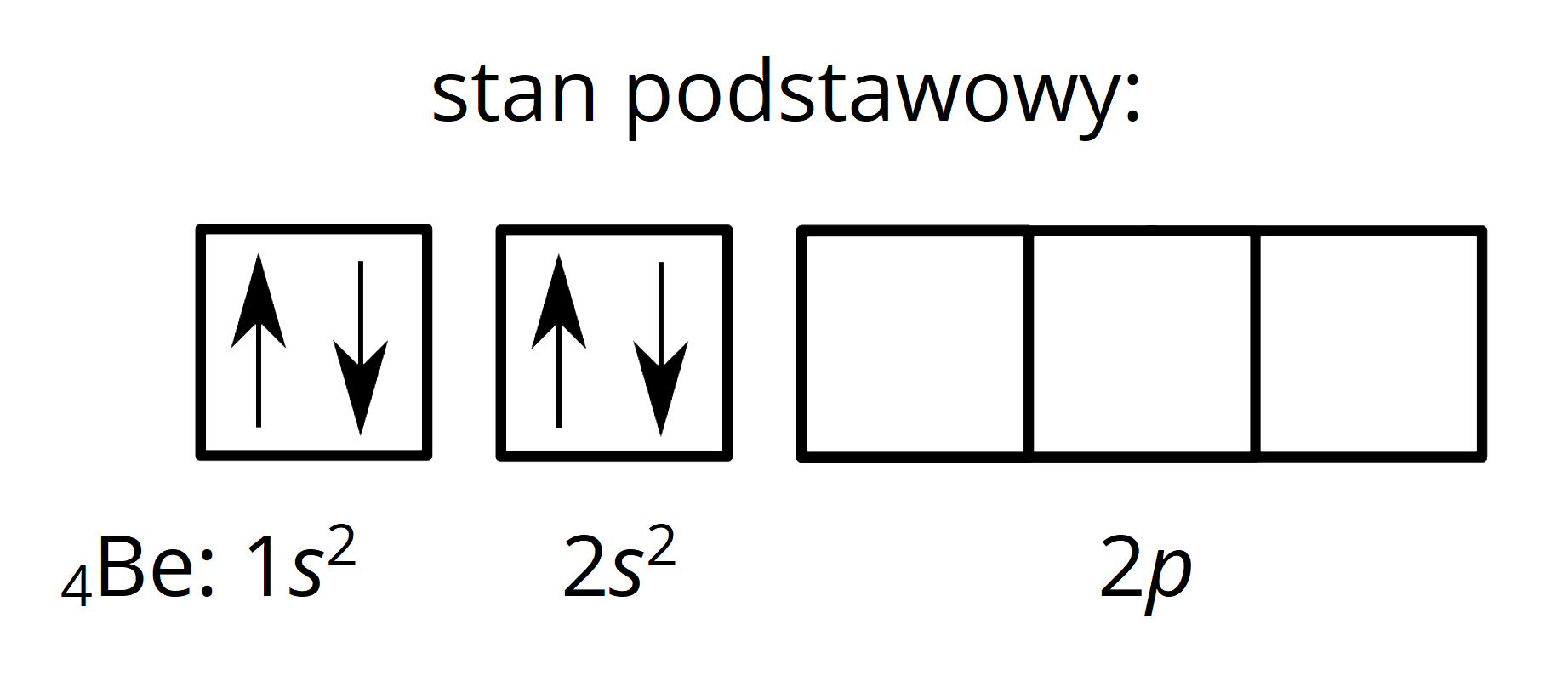Jak powstają orbitale o hybrydyzacji sp?
Kiedy powstają orbitale typu ?
Pierwszy aspekt, który należy ująć przy omawianiu zjawiska hybrydyzacjihybrydyzacji typu , to rodzaj oraz ilość orbitaliorbitali atomowych. Orbitale „mieszają się” i tworzą nowe, tzw. orbitale zhybrydyzowaneorbitale zhybrydyzowane. Jak podają źródła, w hybrydyzacji typu dochodzi do wymieszania jednego orbitalu typu oraz jednego orbitalu typu , w wyniku czego powstają dwa zhybrydyzowane orbitale typu .
Jaka powinna być konfiguracja elektronowa atomu w stanie podstawowymstanie podstawowym i stanie wzbudzonymstanie wzbudzonym, aby orbitale wymieszały się w zaprezentowany powyżej sposób?
Zapoznaj się z animacją pt. „Jak powstają orbitale o hybrydyzacji ?”, Czy potrafisz podać przykład cząsteczki o takim typie hybrydyzacji?

Film dostępny pod adresem /preview/resource/R8CRfG4p7FaSL
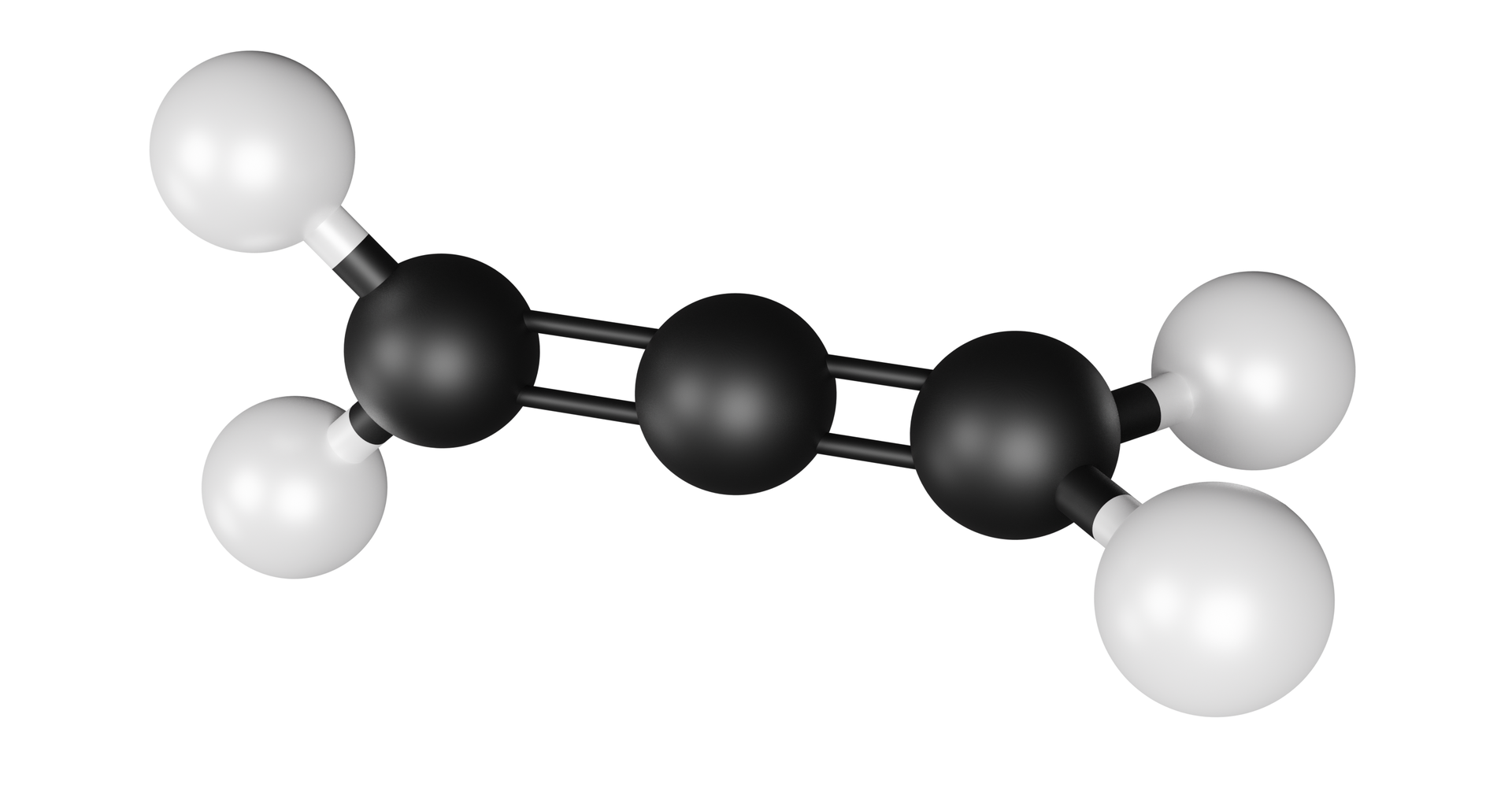
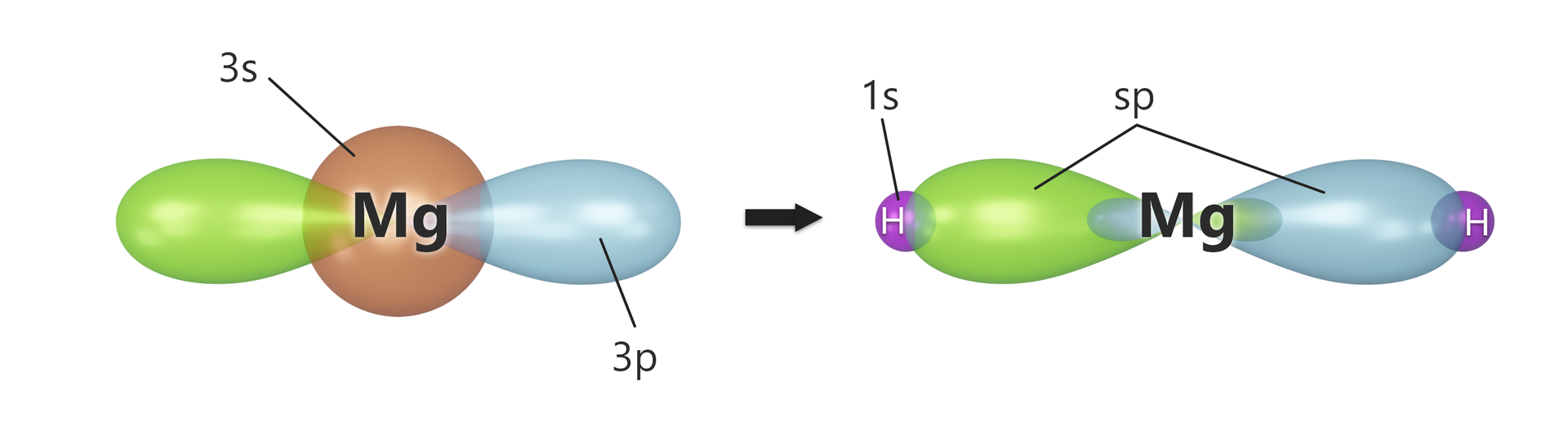
Animacja wyjaśnia powstawanie orbitali o hybrydyzacji na przykładzie wodorku berylu.
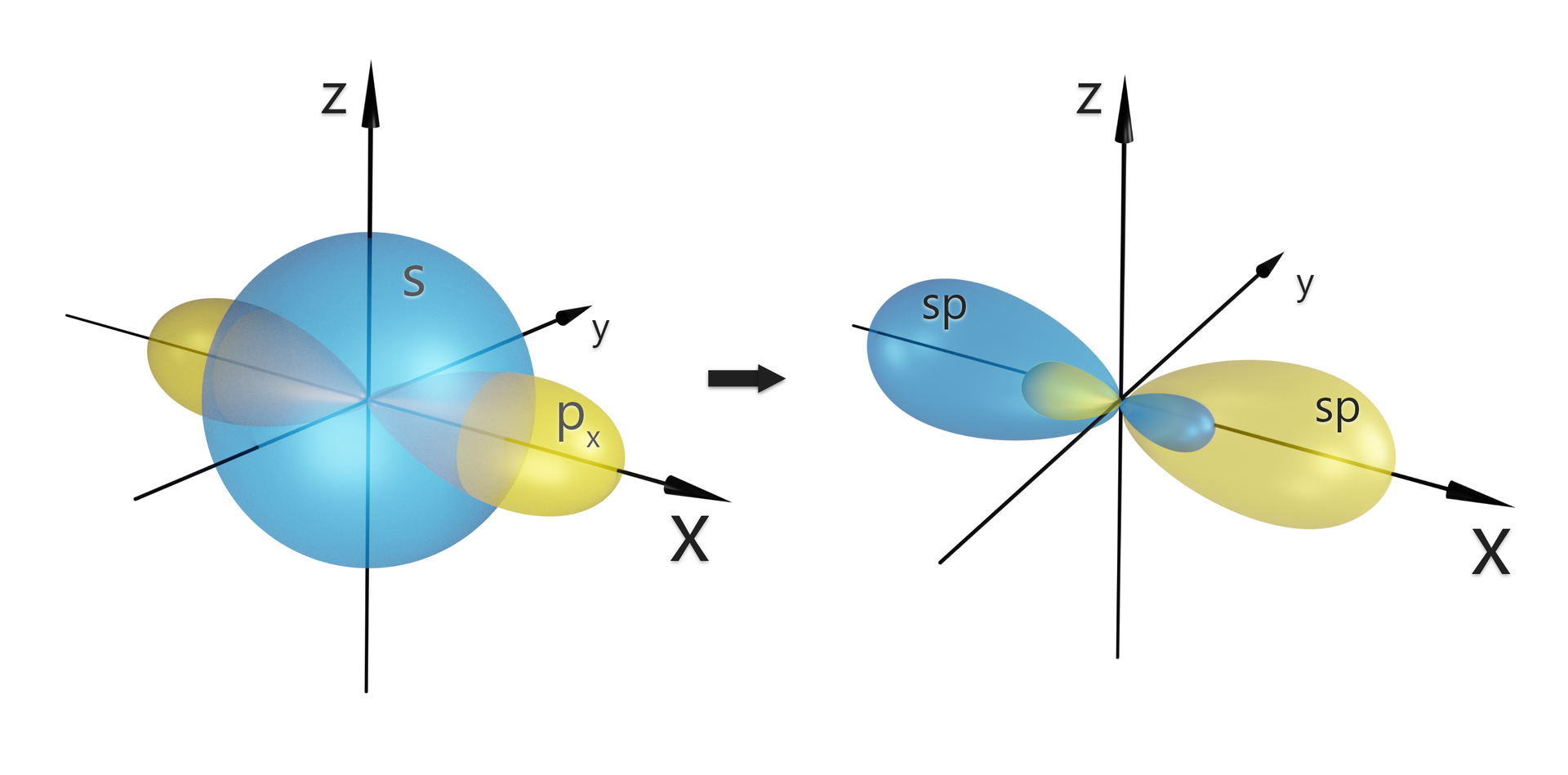
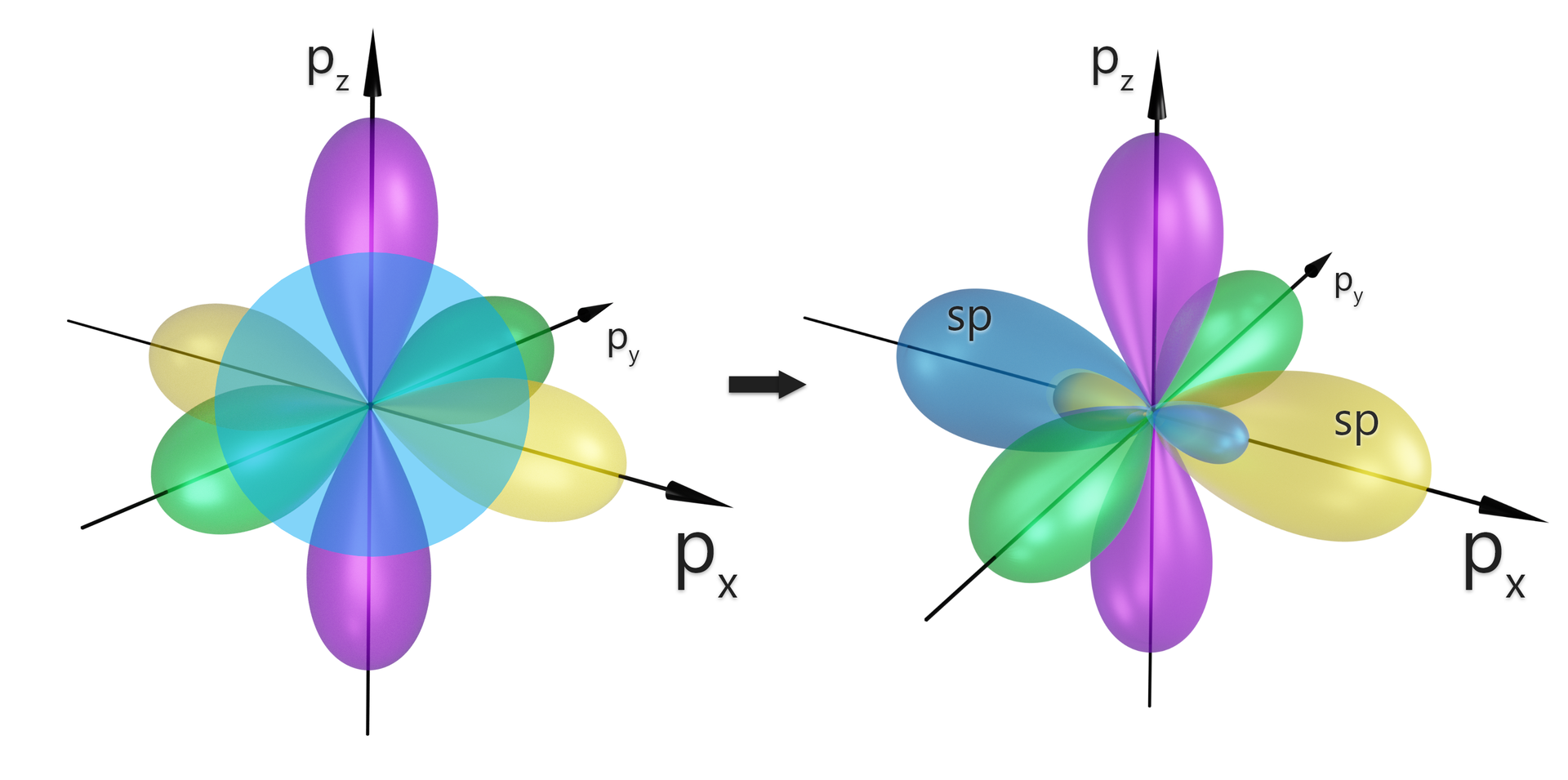
Jak ukazano na rysunkach, hybrydyzacji ulegają orbital oraz orbital , zawierające elektrony w stanie wzbudzonym. Dwa orbitale typu ( i ) pozostają niezhybrydyzowane.
Hybrydyzacja... i co dalej?
Orbitale, które znajdują się w stanie wzbudzonym, ulegają hybrydyzacji, tworząc dwa orbitale zhybrydyzowane (hybrydy) typu . Powstałe dwa orbitale typu , o jednakowym kształcie i energii, zorientowane są względem siebie pod kątem , a ich budowę określa się jako liniową (dygonalnądygonalną). Takie ułożenie orbitali względem siebie jest wynikiem dążenia do zminimalizowania elektrostatycznego odpychaniaelektrostatycznego odpychania chmur elektronowych.
Orbitale typu w różnych cząsteczkach
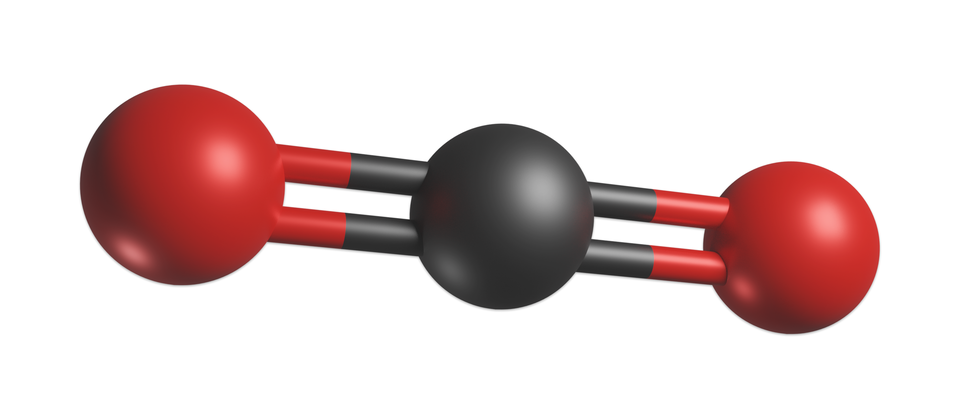
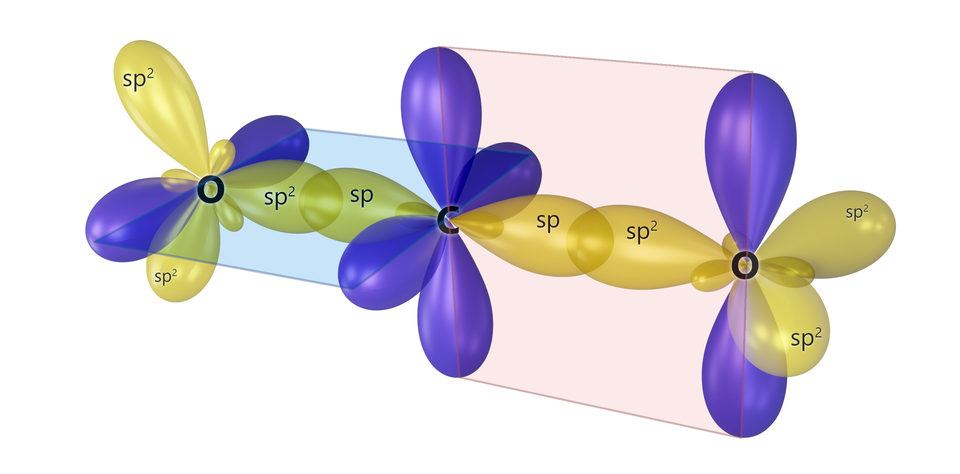
Prawidłowy kształt cząsteczki tlenku węgla(), uwzględniający efekt hybrydyzacji, przedstawiony jest poniżej.
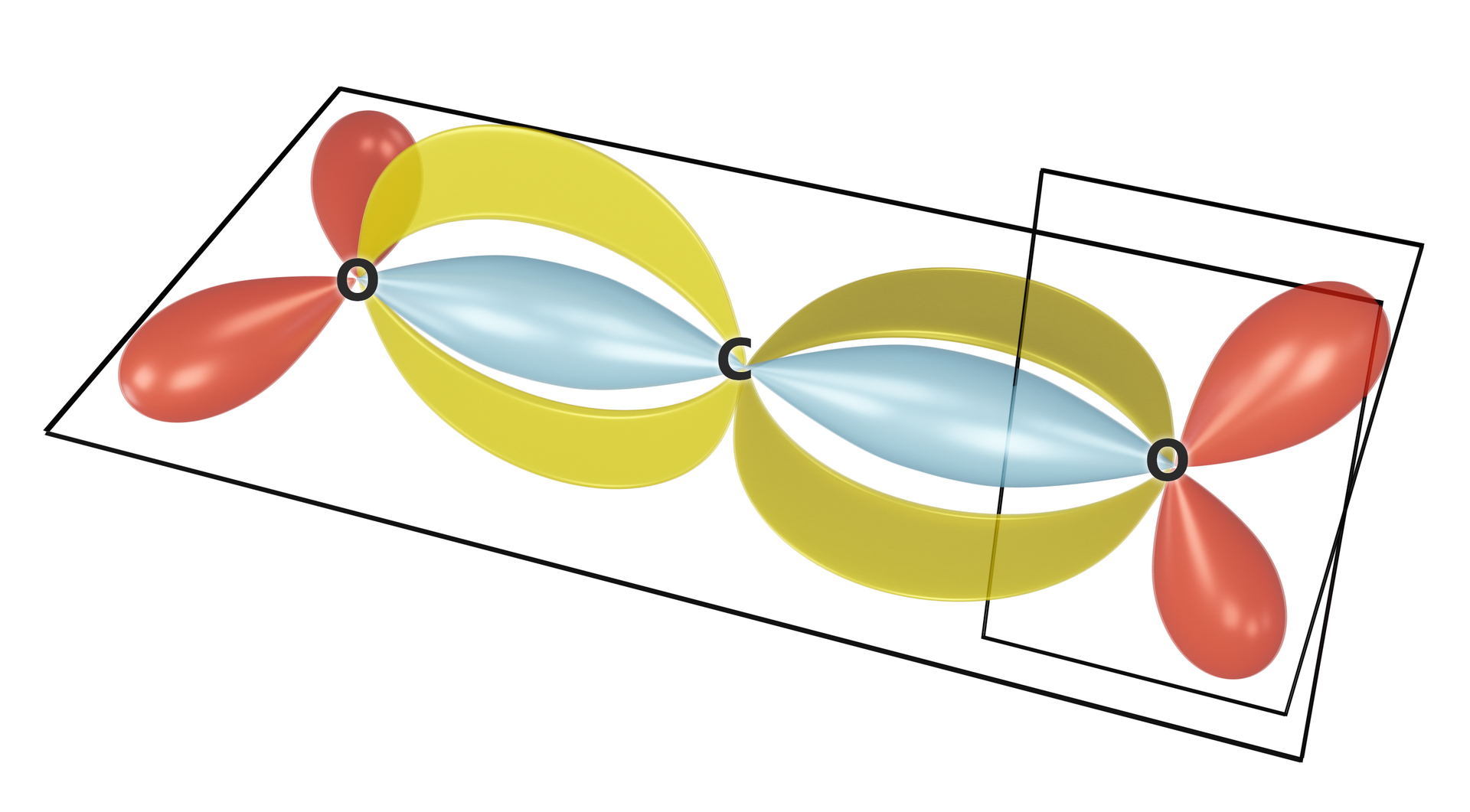
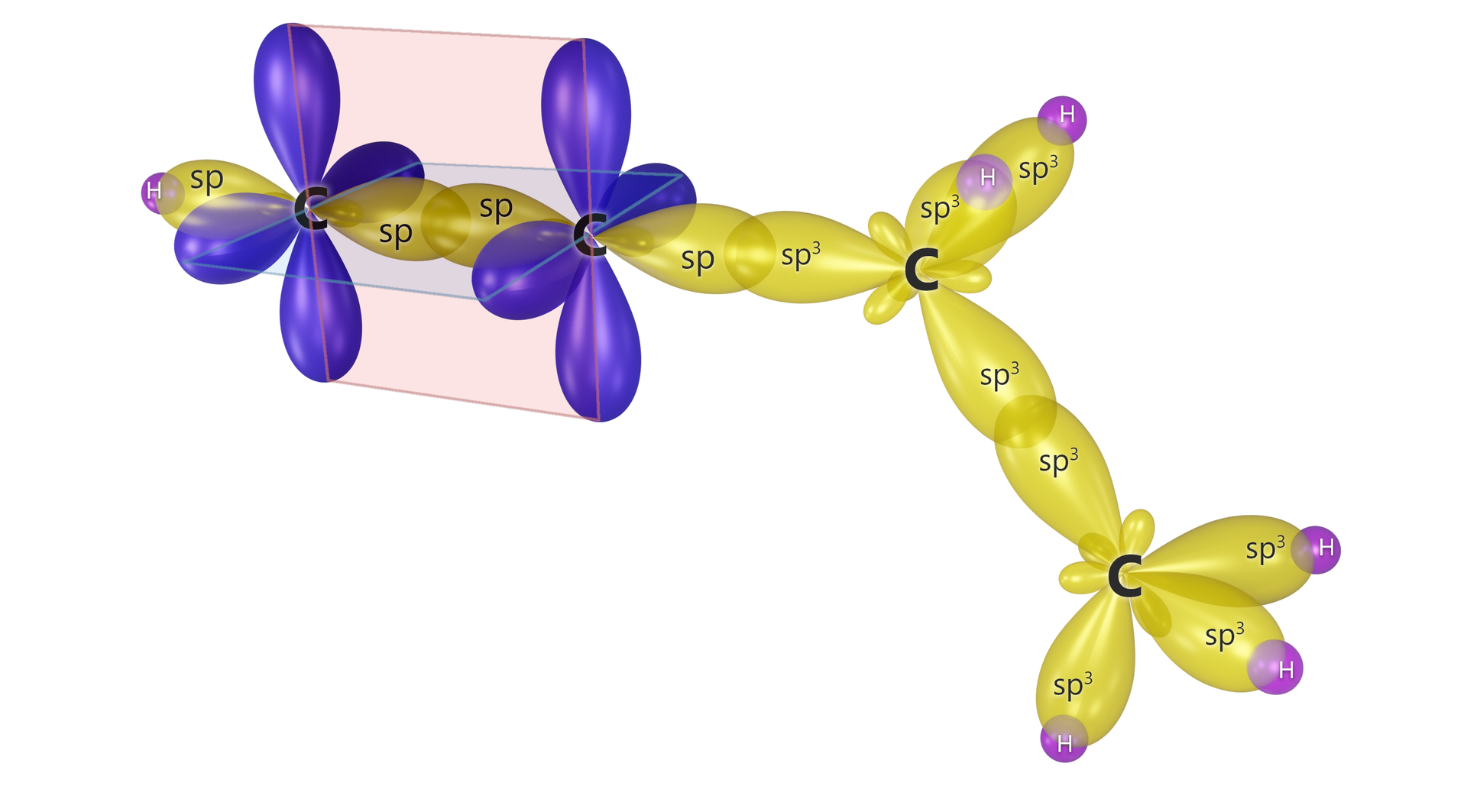
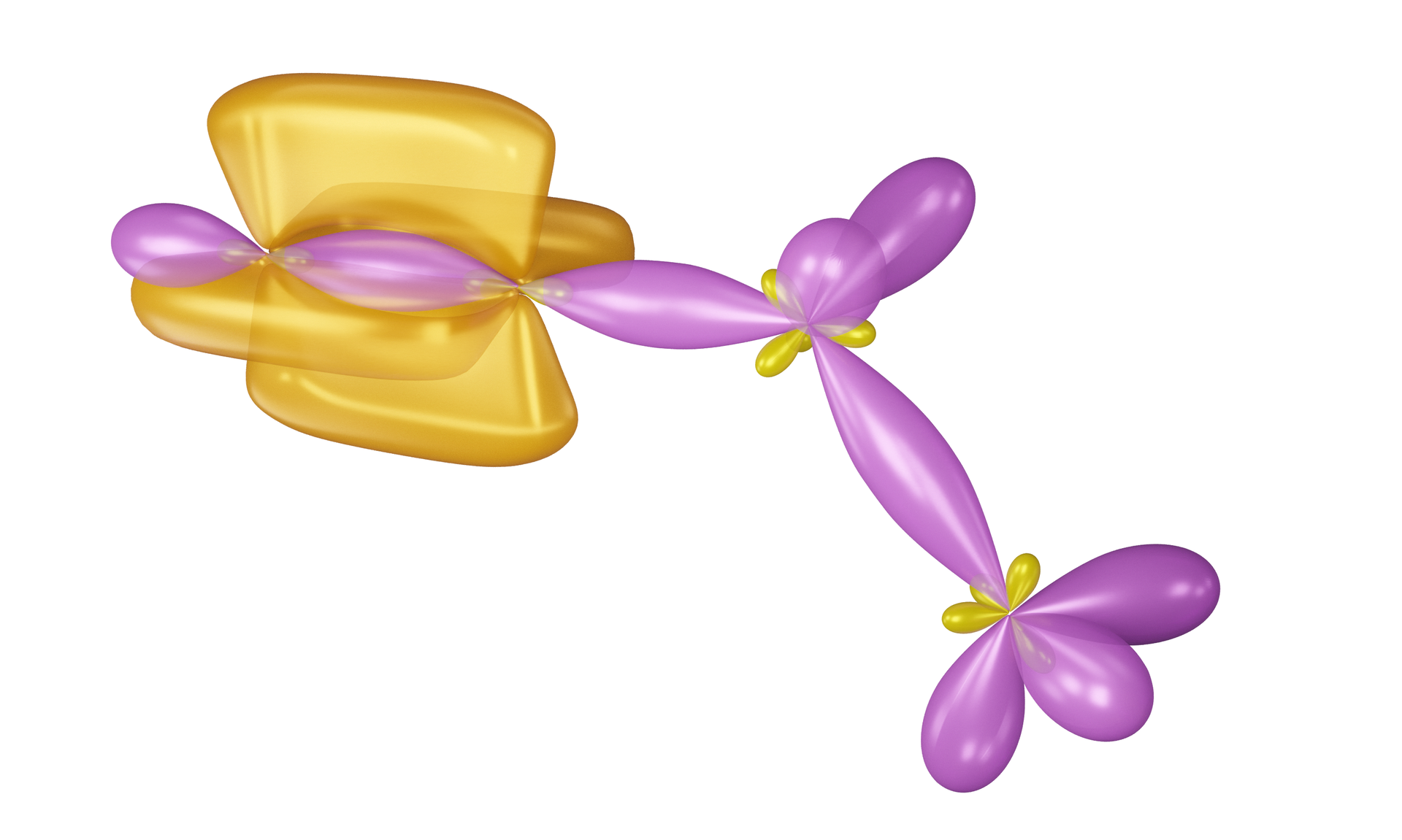
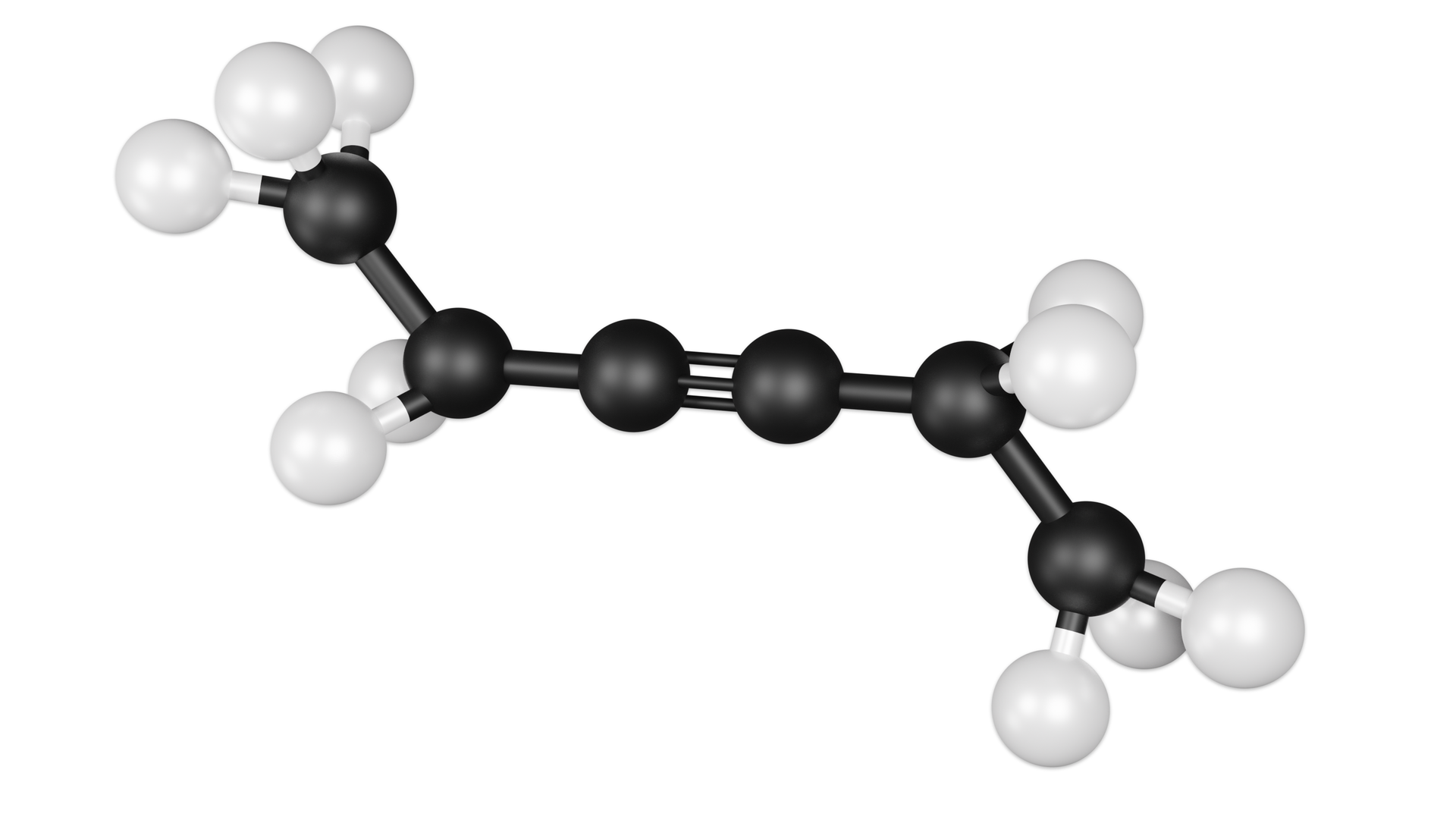
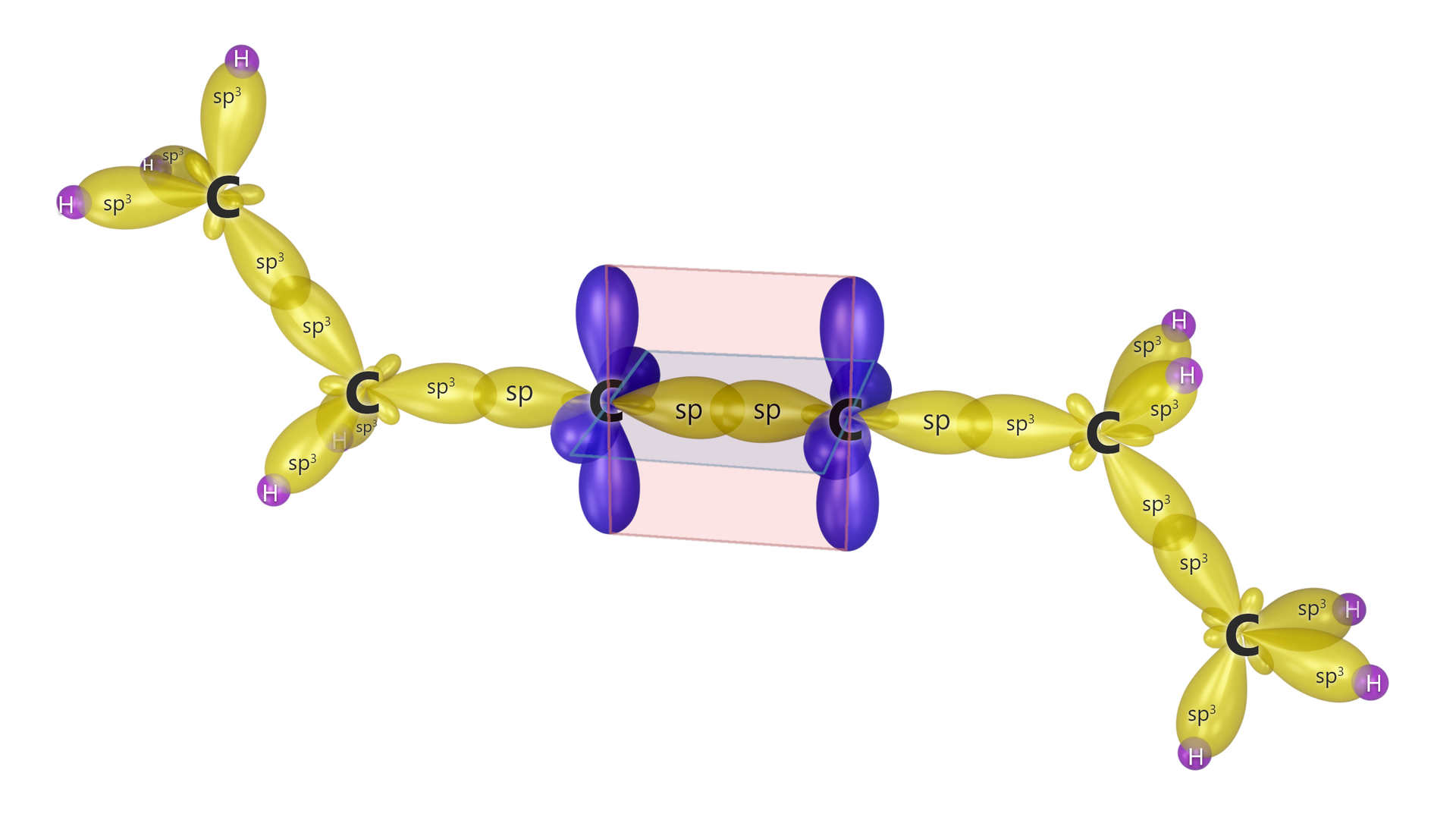
Powstawanie wiązań kowalencyjnych, za pomocą hybrydyzacji typu , można wyjaśnić nie tylko w cząsteczce , ale także w wielu typach cząsteczek nieorganicznych oraz organicznych. Orbitale mają związek z właściwościami i strukturą wiązania potrójnego (spotykanego m.in. w związkach węgla) oraz budową allenówallenów (galeria mediów poniżej).
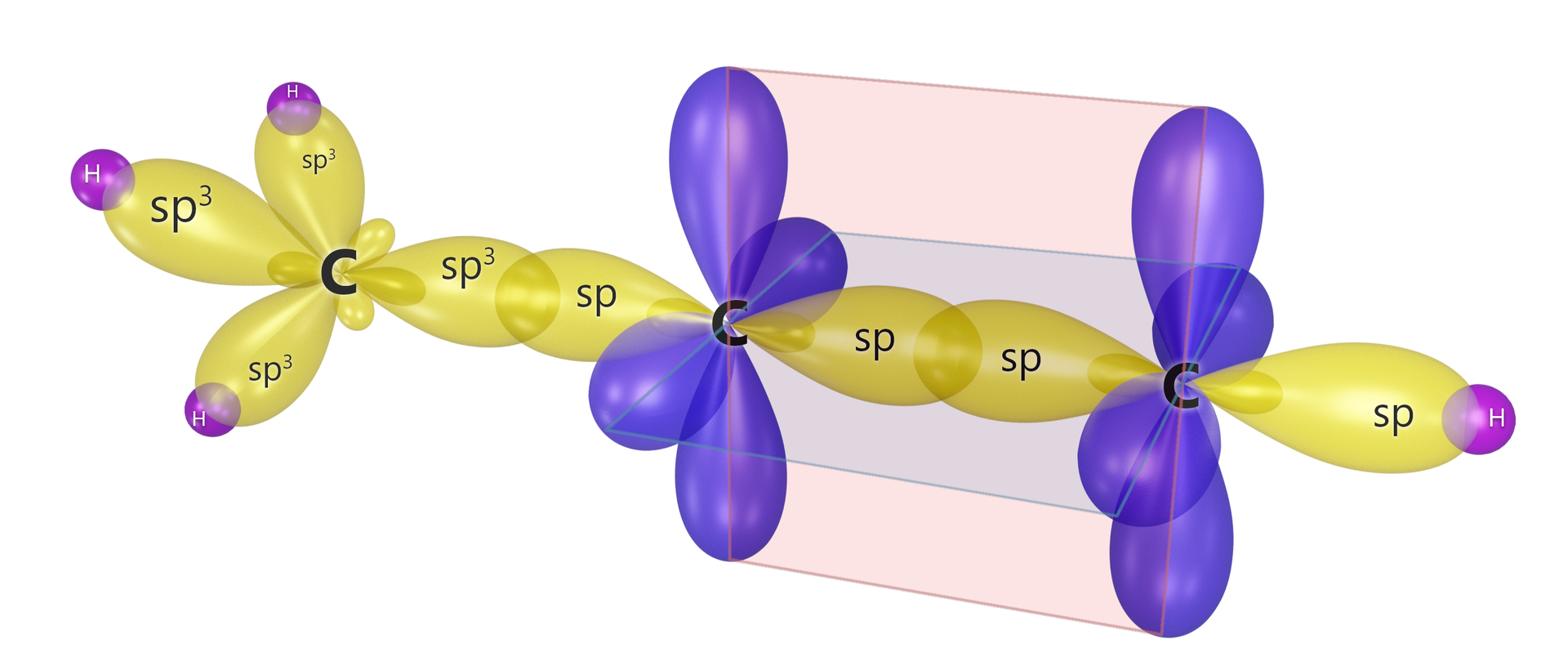
Modele cząsteczek wybranych związków węgla z wodorem - efekty hybrydyzacji
Jak wynika z powyższych modeli, kąt między wiązaniami w układach oraz jest równy . Dzieje się tak, ponieważ orbitale leżą w jednej linii.
Inne przykłady
Przykłady związków nieorganicznych, w których atom centralnyatom centralny związku przyjmuje hybrydyzację , to np. , . W cząsteczkach tych, podobnie jak w związkach organicznych, wyraźnie zaznacza się liniowość wiązań.
Konfiguracja elektronowa powłoki walenycyjnej atomu magnezu ma postać . Elektron z powłoki zostaje wzbudzony, czego efektem jest zajęcie pustego orbitalu . Rozkład elektronów w stanie wzbudzonym na powłoce walencyjnej przyjmuje postać . Orbitale oraz ulegają hybrydyzacji, tworząc dwa orbitale typu . Orbitale te zwracają się do siebie czołowo i tworzą wiązania z orbitalami dwóch atomów wodoru przez nakładanie typu -. Sytuację tę przedstawiono na poniższym rysunku.
Podsumowując
Powstawanie orbitali zhybrydyzowanych typu pomaga wyjaśnić, dlaczego cząsteczki mają budowę liniową. Ten typ hybrydyzacji występuje w przypadku:
atomów posiadających tylko dwa elektrony walencyjne (np. druga grupa w układzie okresowym) – dwa orbitale typu pozostają puste i nie ulegają hybrydyzacji (np. atom berylu w );
gdy występuje wiązanie potrójne, do utworzenia wiązania potrójnego wymagane jest łącznie sześć elektronów (dwa elektrony do utworzenia wiązania i cztery elektrony do utworzenia dwóch wiązań ) – wiązanie powstaje z nałożenia zhybrydyzowanych orbitali atomów (np. atomy węgla w acetylenie, ; atomy azotu w cząsteczce ), natomiast połowicznie obsadzone orbitale obu atomów nakładają się bocznie, w wyniku czego powstają dwa wiązania ;
gdy występują dwa podwójne wiązania przy jednym atomie (np. propadien), atom centralny tworzy dwa wiązania podwójne (dwa wiązania i dwa wiązania ), a do utworzenia jednego wiązania podwójnego potrzeba łącznie czterech elektronów (dwa do utworzenia wiązania i dwa do utworzenia wiązania : wiązanie powstaje z nałożenia zhybrydyzowanych orbitali Indeks górny 22 i , natomiast połowicznie obsadzone orbitale dwóch atomów węgla nakładają się bocznie, w wyniku czego powstają dwa wiązania ; kąt między wiązaniami utworzonymi przez trzy atomy węgla wynosi .
Jaka jest geometria orbitali zhybrydyzowanych typu ?
Czy atom berylu w stanie podstawowym zawiera niesparowane elektrony? Odpowiedź uzasadnij odpowiednim zapisem konfiguracji elektronowej atomu berylu.
Dlaczego w atomie berylu elektron z orbitalu zostaje przeniesiony na orbital ?