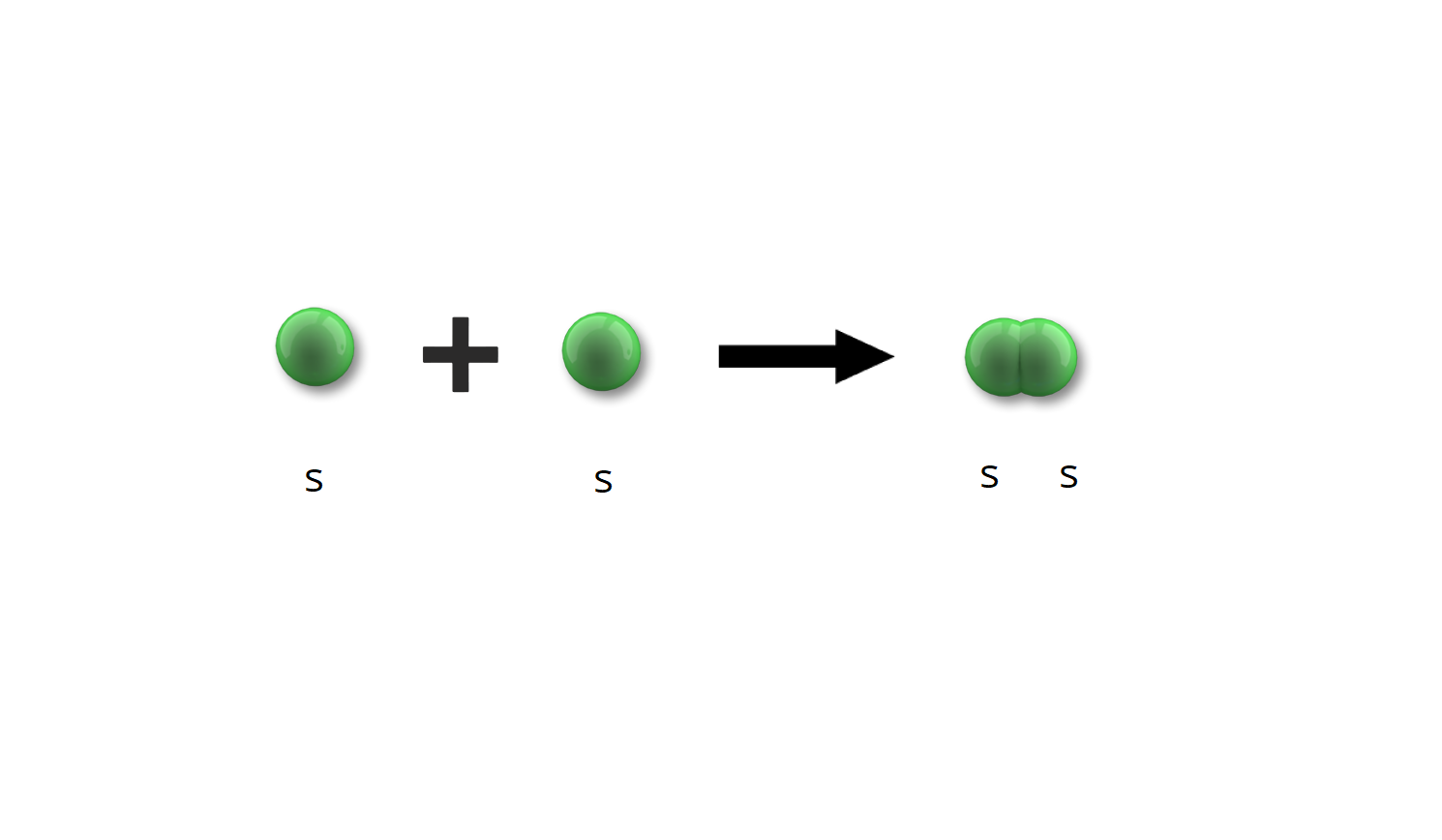Jak powstają wiązania typu sigma?
Orbitale molekularne
Powstawanie wiązań pomiędzy atomami można wyjaśnić zgodnie z zasadami mechaniki kwantowej. Teoria kwantowa oparta na obliczeniach matematycznych zakłada, że wiązanie kowalencyjne powstaje w wyniku nakładania się orbitali atomowychorbitali atomowych. Powstający charakterystyczny rozkład gęstości elektronowej – orbital molekularny – określany jest jako wiązanie (czyt. sigma) lub wiązanie (czyt. pi), w zależności od sposobu nakładania się orbitali.
W atomie mogą występować orbitale , , , . Zgodnie z kwantową teorią wiązań chemicznych, orbital molekularny (cząsteczkowy) powstaje w wyniku zbliżenia i nałożenia się orbitali atomowych, które posiadają podobną energię i jednakową symetrię względem osi łączącej dwa jądra atomowe.
Czy orbitale, powstałe z nakładania się dwóch orbitali typu , będą takie same jak z dwóch orbitali typu ?
Zastanów się, jak powstaje np. cząsteczka wodoru.
Cząsteczka wodoru () powstaje poprzez nałożenie się chmur elektronowych dwóch atomów wodoru. Elektron w atomie wodoru znajduje się na orbitalu . W wyniku zbliżania się do siebie obu chmur następuje ich nakładanie i zlanie w jedną chmurę, która obejmuje oba atomy. W taki sposób powstaje orbital molekularny obsadzony dwoma elektronami.
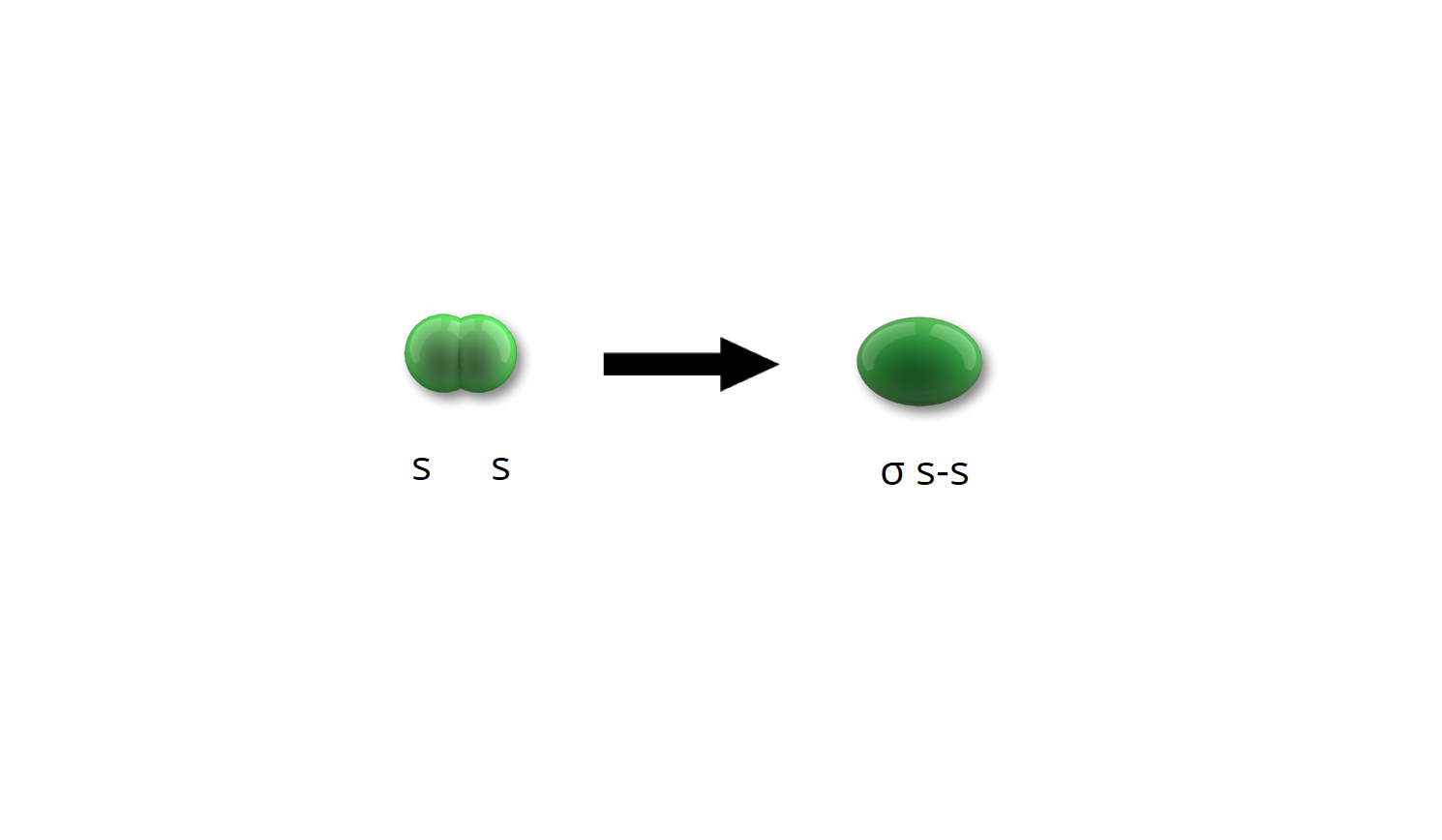
A co w przypadku, gdy niesparowane elektrony (zdolne do tworzenia wiązań) znajdują się wyłącznie na orbitalach typu ?
Z taką sytuacją mamy do czynienia w przypadku cząsteczki fluoru. Cząsteczka fluoru () powstaje poprzez nałożenie się chmur elektronowych dwóch atomów fluoru. Niesparowany elektron, zdolny do utworzenia wiązania pojedynczego, znajduje się w atomie fluoru na orbitalu . W wyniku zbliżania się do siebie obu chmur, następuje ich nakładanie. Powstaje jedna chmura elektronowa i tworzy się orbital molekularny obsadzony dwoma elektronami i o kształcie innym niż orbital .
Jaki będzie kształt orbitalu molekularnego, gdy chmury elektronowe będą pochodzić od orbitali o różnych kształtach?
Rozpatrzmy zatem powstawanie wiązania typu w kwasie fluorowodorowym (). Elektron w atomie fluoru znajduje się na orbitalu , a elektron w atomie wodoru – na orbitalu . Cząsteczka powstaje poprzez nałożenie się chmur elektronowych dwóch atomów (fluoru i wodoru). W wyniku zbliżania się do siebie obu chmur, następuje ich nakładanie. Tworzy się jedna chmura obejmująca oba atomy. W taki sposób powstaje orbital molekularny , obsadzony dwoma elektronami.
Warto zauważyć, że wiązania sigma tworzone są nie tylko przez orbitale atomowe, ale też przez orbitale zhybrydyzwoane, np. , czy , co ma miejsce chociażby w przypadku związków organicznych.
Cząsteczki, które posiadają wiązania , mają możliwość obrotu atomów wokół tego wiązania, co można zaobserwować np. w cząsteczce etanu. Jak powstają wiązania typu w tej cząsteczce?
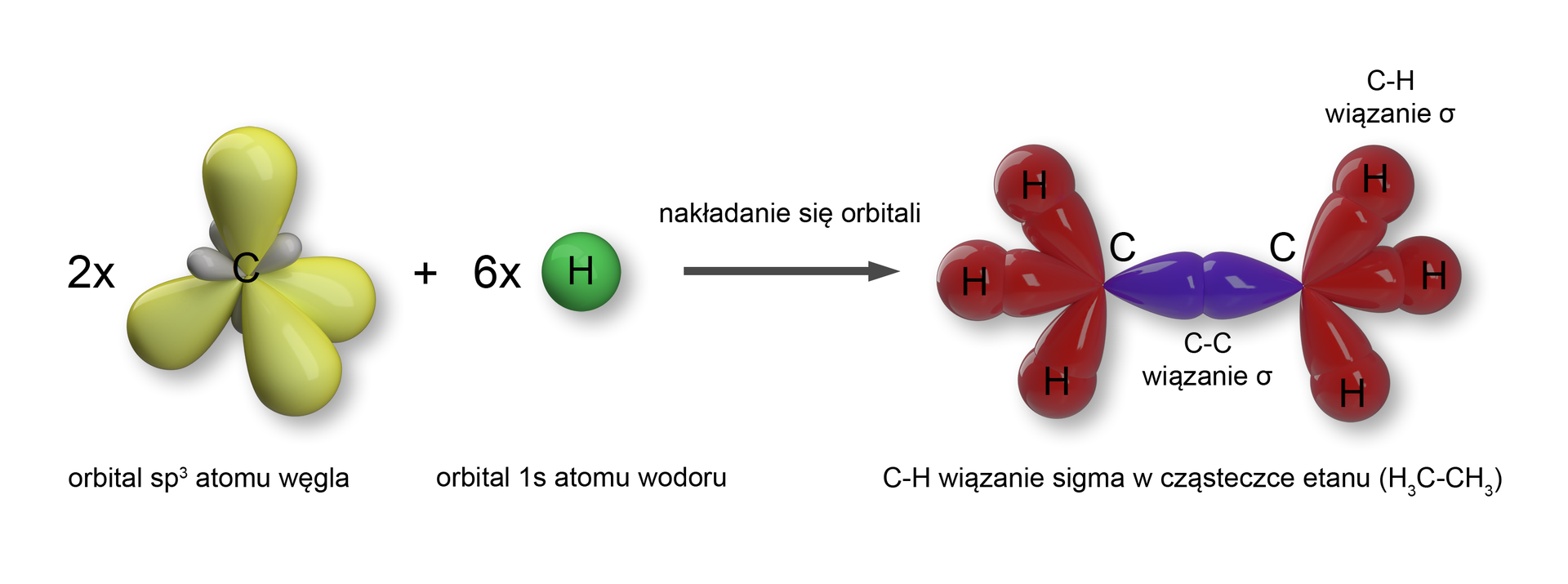
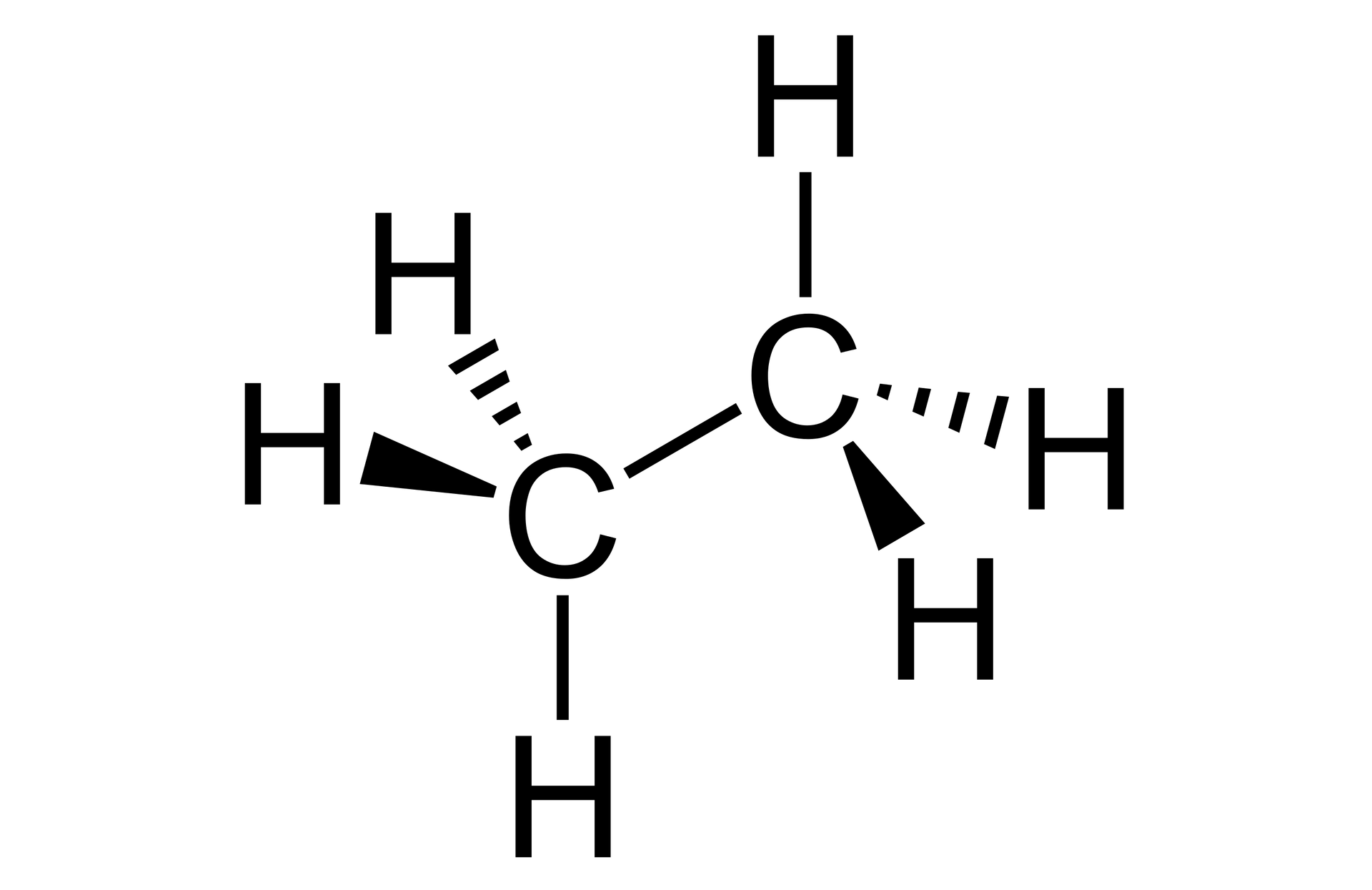
Wiązanie pojedyncze węgiel–węgiel w etanie powstaje poprzez nakładanie się pary orbitali zhybrydyzowanychorbitali zhybrydyzowanych atomów węgla. W ten sposób otrzymujemy pojedyncze wiązanie typu . Wiązanie to ma długość . Z kolei wiązania , pomiędzy atomem węgla a atomem wodoru, powstają przez nakładanie się orbitalu typu atomu węgla z orbitalem typu wodoru.
Ile wiązań sigma występuje w cząsteczce etanu?
Wiązanie a wiązanie typu
Wiązania chemiczne można podzielić, biorąc pod uwagę liczbę elektronów, które łączą atomy. Wyróżniamy zatem:
wiązania pojedyncze – utworzone przez dwa elektrony – które są wiązaniami typu ;
wiązania wielokrotne (podwójne i potrójne) – utworzone przez więcej niż dwa elektrony – w których zawsze jedno z wiązań jest typu , a pozostałe (jedno lub dwa wiązania) to wiązania typu . Istotna różnica pomiędzy wiązaniem typu oraz wiązaniem typu to siła, z jaką wiążą się ze sobą atomy. Orbitale molekularne typu tworzą wiązania silniejsze od wiązań typu . Warto dodać, że wiązania typu powstają poprzez boczne nakładanie się orbitali atomowych, ale o tym dokładniej w innej części e‑podręcznika.
krotność wiązania pomiędzy atomami węglami | typ hybrydyzacji atomu węgla | rodzaj wiązań pomiędzy atomami węgla |
|---|---|---|
wiązanie pojedyncze, np. w cząsteczce etanu 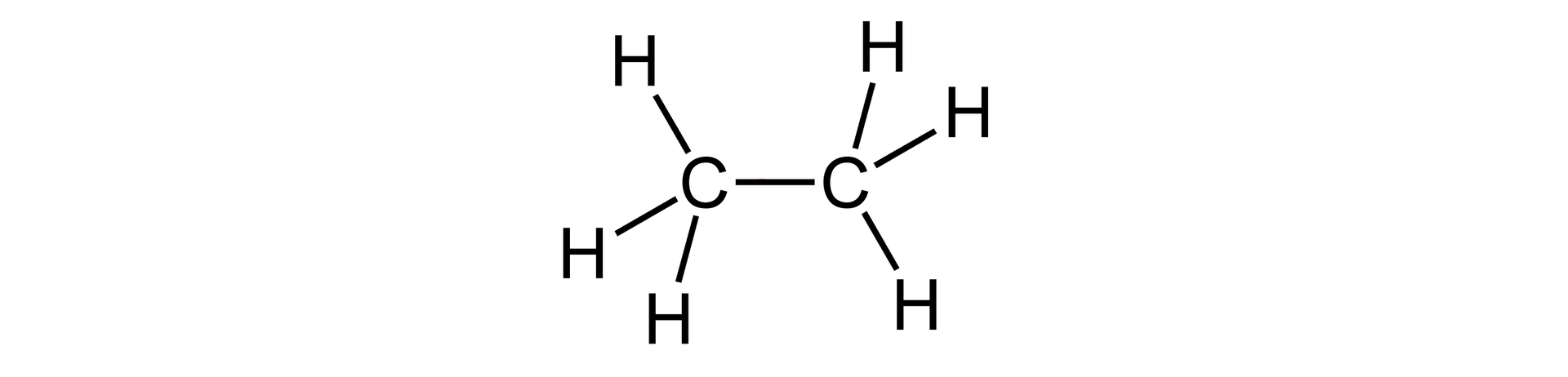 Wzór strukturalny etanu Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | 1 wiązanie | |
wiązanie podwójne, np. w cząsteczce etenu 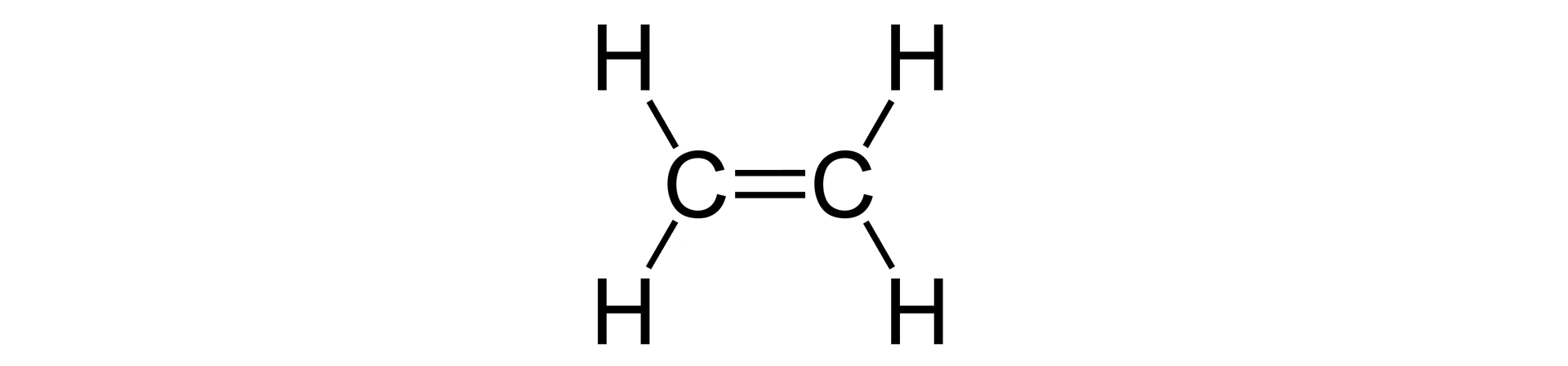 Wzór strukturalny etenu Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | 1 wiązanie | |
wiązanie potrójne, np. w cząsteczce etynu  Wzór strukturalny etynu Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | 1 wiązanie |
Podsumowanie
Czy już wiesz, jak powstają wiązania sigma? Zapoznaj się z poniższą animacją, a następnie odpowiedz na pytania zamieszczone poniżej.

Film dostępny pod adresem /preview/resource/RT9He7xE9h68I
Animacja dotyczy powstawania wiązania typu sigma.
Nałożenie się jakich orbitali prowadzi do powstania wiązania w cząsteczce ?