Badanie właściwości chemicznych aminokwasów
Właściwości chemiczne aminokwasów
Ze względu na obecność w cząsteczce grupy funkcyjnej o właściwościach kwasowych () oraz zasadowych (), aminokwasy reagują zarówno z zasadami, jak i kwasami, czyli mają charakter amfoteryczny. Oznacza to, że w roztworach wodnych (w zakresie pH od 4 do 9), zgodnie z teorią Bronsteda‑Lowry'ego, mogą zachowywać się jak kwas (donor protonu) bądź zasada (akceptor protonu). Aby potwierdzić to stwierdzenie, należy zapisać odpowiednie równania reakcji aminokwasów.
Ze względu na obecność w cząsteczce grupy karboksylowej, która zachowuje swoje właściwości, aminokwasy:
reagują z zasadami, tworząc odpowiednie sole, np.:
R1cQX06SX97mr  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.

Do reakcji należy użyć rozcieńczonego roztworu wodorotlenku, aby zmiana pH nie zachodziła zbyt gwałtownie.
reagują z alkoholami, tworząc estry, np.:
R1YLKrIrXZr1u  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.

Należy pamiętać, że reakcja estryfikacji wymaga obecności mocnego kwasu oraz ogrzania.
Ze względu na obecność w cząsteczce grupy aminowej, która zachowuje swoje właściwości, aminokwasy:
reagują z kwasami, tworząc odpowiednie sole, np. w reakcji z kwasem chlorowodorowym:
R17n4M7eHmuKq  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.

Do reakcji należy użyć rozcieńczonego roztworu kwasu, aby zmiana pH nie zachodziła zbyt gwałtownie. Należy pamiętać też, że w przypadku amonokwasów, posiadających w swojej strukturze pierścień aromatyczny, użycie kwasu azotowego(V) spowoduje nitrowanie pierścienia (reakcja ksantoproteinowa).
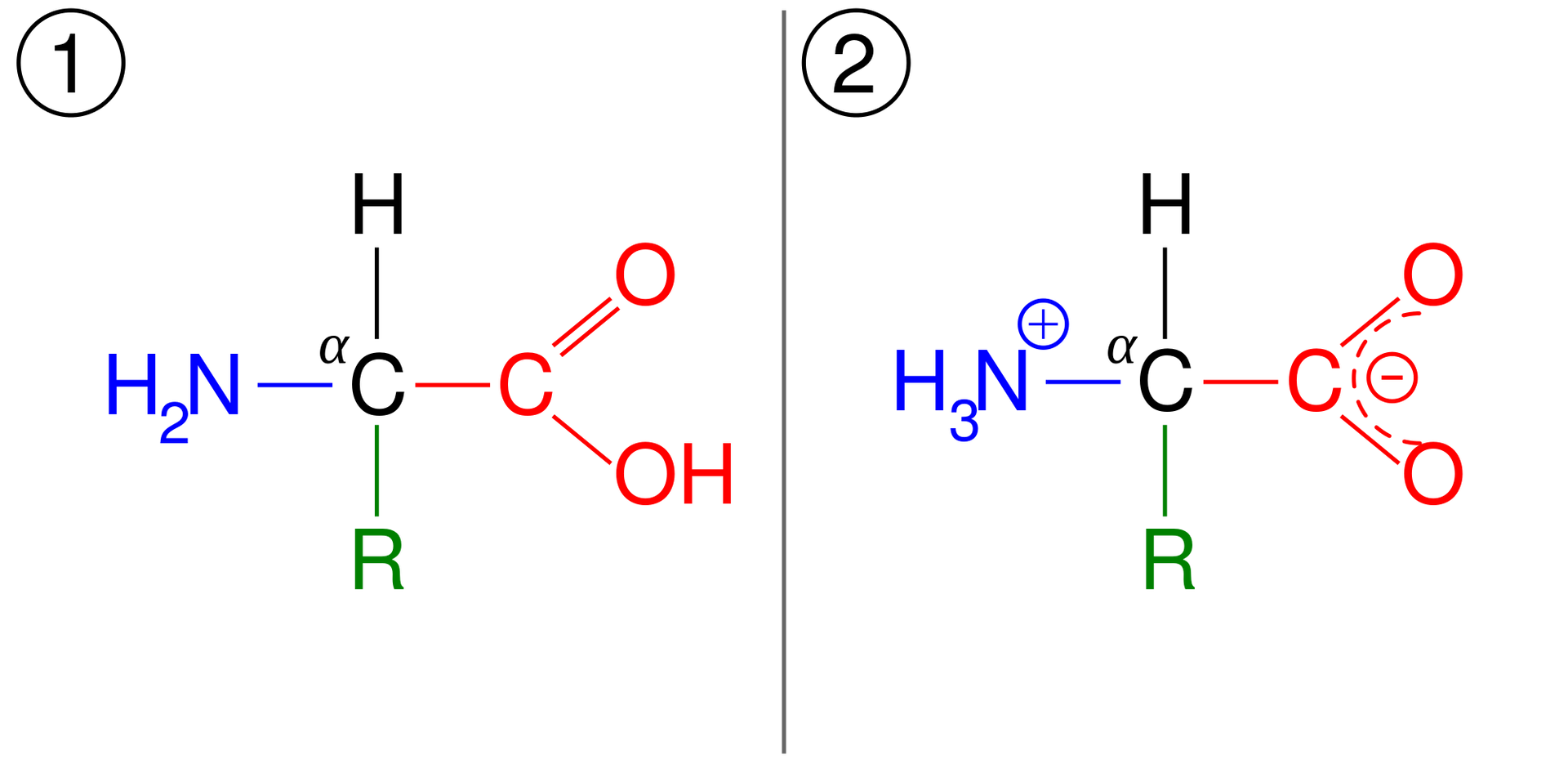
W wodnym roztworze aminokwasu, zawierającego w cząsteczce jedną grupę karboksylową i jedną grupę aminową, ustala się stan równowagi, w którym występują trzy formy jonowe:
pH roztworu | Forma, w jakiej występuje aminokwas |
|---|---|
| |
Punkt izoelektryczny |
|
|
Wartość pH roztworu, w którym istnieje dokładna równowaga między formą kationową i anionową (stężenie kationowej i anionowej formy jest minimalne i równe sobie) a stężeniem jonu obojnaczego, nazywamy punktem izoelektrycznym (). Zmiana roztworu (alkalizacja lub zakwaszenie roztworu) wywołuje przesunięcie równowagi w stronę anionu lub w stronę kationu .
Obejrzyj poniższą ilustrację interaktywną, prezentującą schemat doświadczenia potwierdzającego właściwości amfoteryczne alaniny, a następnie rozwiąż towarzyszące jej ćwiczenia.
Zapoznaj się z poniższą ilustracją interaktywną, która przedstawia propozycję doświadczenia pozwalającego na potwierdzenie charakteru amfoterycznego alaniny, a następnie rozwiąż ćwiczenia.
Zapoznaj się z opisem ilustracji interaktywnej, która przedstawia propozycję doświadczenia pozwalającego na potwierdzenie charakteru amfoterycznego alaniny, a następnie rozwiąż ćwiczenia.
Zapisz równania reakcji chemicznych potwierdzających amfoteryczność waliny.
Następnie przeprowadź doświadczenie laboratoryjne, polegające na zbadaniu właściwości kwasowo‑zasadowych glicyny i alaniny.
Przeprowadź eksperyment w laboratorium chemicznym. Zbadaj właściwości kwasowo‑zasadowe glicyny oraz alaniny. W pierwszej kolejności zbadaj pH wodnych roztworów badanych aminokwasów za pomocą uniwersalnego papierka wskaźnikowego, następnie wykonaj reakcję z kwasem chlorowodorowym (z dodatkiem oranżu metylowego) oraz wodorotlenkiem sodu (z dodatkiem fenoloftaleiny). Możesz również wykonać próbę kontrolną ( + oranż metylowy, + fenoloftaleina) w celu porównania ewentualnych zmian. Rozwiąż problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D3C3TAQZX
Przeprowadzono eksperyment w laboratorium chemicznym. Zbadano właściwości kwasowo‑zasadowe glicyny oraz alaniny. W pierwszej kolejności zbadano pH wodnych roztworów badanych aminokwasów za pomocą uniwersalnego papierka wskaźnikowego, następnie wykonano reakcję z kwasem chlorowodorowym (z dodatkiem oranżu metylowego) oraz wodorotlenkiem sodu (z dodatkiem fenoloftaleiny). Wykonano również próbę kontrolną ( + oranż metylowy, + fenoloftaleina) w celach porównania ewentualnych zmian. Zapoznaj się z opisem doświadczenia, a następnie wykonaj ćwiczenie.
Analiza eksperymentu: Badanie właściwości kwasowo‑zasadowych aminokwasów.
Problem badawczy: Czy aminokwasy posiadają charakter amfoteryczny?
Hipoteza: Aminokwasy posiadają charakter amfoteryczny.
Odczynniki chemiczne:
wodny roztwór glicyny;
wodny roztwór alaniny;
kwas chlorowodorowy;
wodny roztwór wodorotlenku sodu;
alkoholowy roztwór fenoloftaleiny;
wodny roztwór oranżu metylowego.
Sprzęt laboratoryjny:
probówki w statywie – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
pipety – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
pręcik szklany – służy do mieszania cieczy;
uniwersalne papierki wskaźnikowe – kawałek bibuły najczęściej w kształcie paska, nasączony roztworem substancji chemicznej będącej indykatorem i wysuszony.
Przebieg eksperymentu:
Do pierwszej probówki dodaj wodny roztwór glicyny, do czwartej wodny roztwór alaniny i zbadaj ich pH za pomocą uniwersalnych papierków wskaźnikowych.
Do drugiej, piątej i siódmej probówki dodaj kwas chlorowodorowy i kilka kropel wodnego roztworu oranżu metylowego.
Do trzeciej, szóstej i ósmej probówki dodaj wodny roztwór wodorotlenku sodu i kilka kropel alkoholowego roztworu fenoloftaleiny.
Do drugiej i trzeciej probówki dodaj wodny roztwór glicyny.
Do piątej i szóstej probówki dodaj wodny roztwór alaniny.
Obserwacje:
Papierek wskaźnikowy w obu przypadkach barwi się na żółto. W reakcji z kwasem chlorowodorowym, zarówno w przypadku glicyny, jak i alaniny, czerwony roztwór zmienia zabarwienie na żółte. Natomiast w reakcji z następuje odbarwienie malinowego roztworu.
Wyniki:
Odczyn wodnych roztworów badanych aminokwasów jest obojętny. Aminokwasy te reagują zarówno z kwasami, jak i zasadami.
Wnioski:
Badane aminokwasy posiadają charakter amfoteryczny, reagują zarówno z kwasami jak i wodorotlenkami. Hipoteza została potwierdzona.
