Izotopy i średnia masa atomowa
Co określa liczba atomowa?
Popatrz na fragment układu okresowego dotyczącego wodoru. Jakie informacje możesz z niego odczytać?
Zapoznaj się z opisem fragmentu układu okresowego dotyczącego wodoru. Dowiedz się, jakie informacje można z niego odczytać.
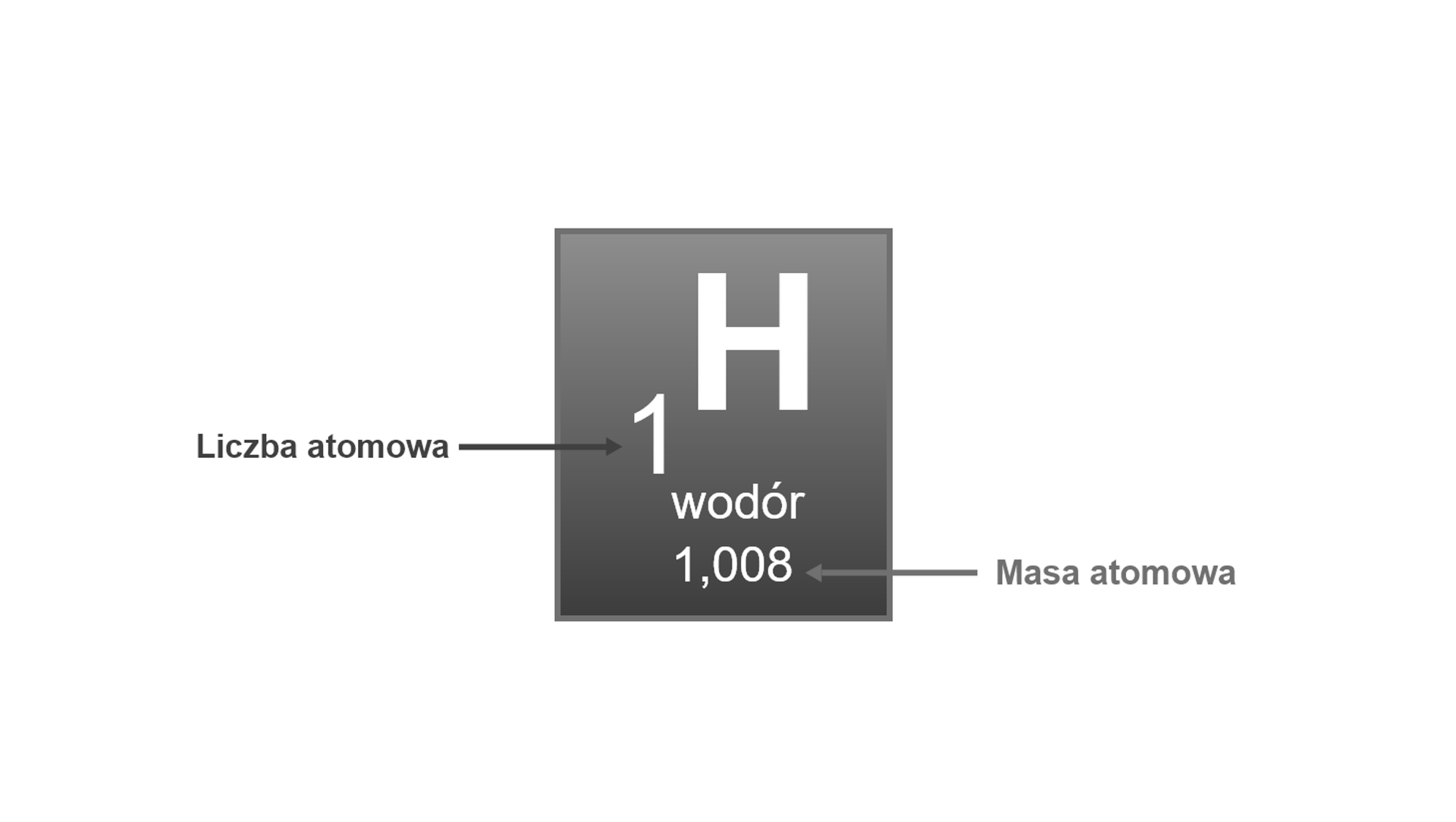
Liczba atomowa danego pierwiastka informuje nas o:
miejscu danego pierwiastka w układzie okresowym;
ilości protonów w jądrze;
ilości elektronów w chmurze elektronowej atomu pierwiastka.
Pamiętaj jednak, że z układu okresowego nie odczytasz, ile neutronów ma dany atom, ponieważ o przynależności atomu do danego pierwiastka decyduje liczba protonów w jądrze atomowym (liczba atomowa). W definicji pierwiastka nie ma określonej liczby neutronów, dlatego też atomy danego pierwiastka mogą różnić się liczbą neutronów w jądrze.
Liczba masowa jest sumą nukleonów, czyli sumą protonów i neutronów w jądrze atomu.
Masa atomowa (względna) wyrażana jest w jednostce zwanej unitem. Unit () równoważny jest masy atomu węgla . Wartość odpowiada .
Czy wszystkie atomy wodoru są tak samo zbudowane?
W przypadku wodoru występują trzy rodzaje atomów; atomów wodoru posiada w jądrze tylko – ich liczba masowa wynosi . Za pomocą symboli zapisujemy ten atom jako , czasami dla atomów tej odmiany wodoru stosuje się nazwę prot. Natomiast atomów wodoru ma w jądrze i – ich liczba masowa wynosi . Atomy te nazywa się „ciężkim wodorem” lub deuterem. Mają one nawet swój symbol chemiczny , ale stosuje się też zapis lub wodór–. Śladowe ilości atomów wodoru mają w jądrze i – ich liczba masowa wynosi . Atomy te nazywa się trytem, a ich symbol chemiczny to lub stosuje się zapis , wodór–. Na ilustracji poniżej przedstawiono rodzaje atomu wodoru.

Atomy, które mają taką samą liczbę protonów w jądrze, ale różną liczbę neutronów, nazywamy izotopami. Nazwa ta pochodzi z greckiego (izo „taki sam”, topos „miejsce”), ponieważ atomy izotopów zajmują to samo miejsce w układzie okresowym.
Izotop | |||
|---|---|---|---|
Nazwa | Prot | Deuter | Tryt |
Symbol |
Jakimi właściwościami różnią się izotopy danego pierwiastka?
Izotopy tego samego pierwiastka mają zbliżone własności fizyczne. Jednak im większa jest różnica mas atomowych izotopów (co ma miejsce np. w przypadku wodoru), tym większe mogą być różnice ich własności fizycznych. Izotopy nie różnią się właściwościami chemicznymi.
Należy pamiętać, że aby badać zmiany stanów skupienia czy gęstości, musi występować pewien zbiór atomów czy też izotopów. Niemożliwe jest badanie właściwości dla pojedynczego nuklidu.
Izotopy danego pierwiastka mogą się różnić:
temperaturą wrzenia;
temperaturą topenienia;
temperaturą sublimacji;
gęstością.
Izotopy wodoru różnią się liczbą nukleonów. Różnica mas pomiędzy izotopami wodoru jest bardzo duża – atom deuteru ma masę dwukrotnie większą od masy atomu protu, a tryt – aż trzykrotnie. Wpływ zmiany masy atomowej na właściwości tych izotopów zamieszczono w tabeli poniżej.
Izotop | Symbol | Temperatura topnienia | Temperatura wrzenia |
|---|---|---|---|
Prot | |||
Deuter | |||
Tryt |
Cząsteczki ciężkiej wody () mają masę cząsteczkową większą o od cząsteczek wody , co powoduje jej większą gęstość. Dzięki tej właściwości można oddzielać wodę ciężką od „zwykłej” poprzez wirowanie.
Parametr | |||
|---|---|---|---|
Temperatura | |||
Temperatura | |||
Gęstość (, ) | |||
[w ] |
Ciężka woda występuje naturalnie w przyrodzie. W normalnej wodzie znajduje się ok. wody ciężkiej. W tych stężeniach jest nieszkodliwa dla organizmów, jednak badania eksperymentalne wykazały, że wysokie stężenia mogą prowadzić do bezpłodności, a nawet śmierci organizmów żywych.
Większość pierwiastków ma kilka izotopów, ale istnieją również takie, które mają tylko jeden stabilny izotop.
- Nazwa kategorii: pierwiastki posiadające[br]jeden stabilny izotop
- Nazwa kategorii: fluor
- Nazwa kategorii: sód
- Nazwa kategorii: glin
- Nazwa kategorii: fosfor
- Nazwa kategorii: skand
- Nazwa kategorii: mangan
- Nazwa kategorii: kobalt
- Nazwa kategorii: arsen
- Nazwa kategorii: itr
- Nazwa kategorii: niob
- Nazwa kategorii: jod
- Nazwa kategorii: cez
- Nazwa kategorii: bizmut
- Nazwa kategorii: rod
- Nazwa kategorii: złoto
- Nazwa kategorii: beryl
- Nazwa kategorii: prazeodym
- Nazwa kategorii: protaktyn
- Nazwa kategorii: terb
- Nazwa kategorii: holm
- Nazwa kategorii: tul Koniec elementów należących do kategorii pierwiastki posiadające[br]jeden stabilny izotop
- Elementy należące do kategorii pierwiastki posiadające[br]jeden stabilny izotop
Zapoznaj się z filmem edukacyjnym i odpowiedz pytania:

Film dostępny pod adresem /preview/resource/R1DpGHPijnXkO
Film nawiązujący do treści materiału – dotyczy opisu budowy atomów – protonów, neutronów i elektronów oraz izotopów tego samego pierwiastka.
Przeanalizuj symulację dotyczącą atomów przykładowych pierwiastków. Spróbuj policzyć liczbę izotopów poszczególnych pierwiastów, jakie uda Ci się zidentyfkować

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D4A6441GO
W symulacji przedstawiono, jak określić skład izotopowy pierwiastków. Najpierw podano definicję izotopu oraz odpowiednio liczby atomowej i liczby masowej.
Izotopy to odmiany tego samego pierwiastka chemicznego, które mają jednakową liczbę atomową oraz różną liczbę masową. Izotopy zajmują to samo miejsce w układzie okresowym pierwiastków chemicznych.
Liczba atomowa informuje nas o: miejscu danego pierwiastka w układzie okresowym; ilości protonów w jądrze, ilości elektronów w chmurze elektronowej atomu pierwiastka.
Liczba masowa jest sumą nukleonów, czyli sumą protonów i neutronów w jądrze atomu.
Masa atomowa
Masa atomowa pierwiastka jest średnią masą atomową, która wynika z procentowej zawartości izotopów tworzących dany pierwiastek. Możemy ją obliczyć według wzoru:
Gdzie:
– masa atomowa pierwiastka;
, , – masy atomowe poszczególnych izotopów;
, , – procentowe zawartości poszczególnych izotopów.
Obliczanie masy atomowej pierwiastka na podstawie jego składu izotopowego
Oblicz masę atomową bromu naturalnego, wiedząc, że zawiera on izotopu o masie atomowej i izotopu o masie atomowej .
Obliczenia składu izotopowego pierwiastka
Korzystając z powyższego wzoru, obliczymy zawartość procentową dwóch izotopów chloru. Wiemy, że chlor ma dwa izotopy: i . Znamy również masę atomową chloru, która wynosi . Masa ta bliższa jest wartości masy izotopu . Przyczyną jest znacznie większy udział tego izotopu w naturalnym chlorze, wynoszący ok. . Masa atomowa pierwiastka jest średnią ważoną mas atomowych jego izotopów oraz uwzględnia rozpowszechnienie izotopów pierwiastka. Załóż, że masa atomowa izotopów jest równa ich liczbie masowej. Czy wiesz, jak zapisać to równanie?
Określ liczbę protonów, elektronów i neutronów dla izotopu .
Tytan (, łac. titanium) to pierwiastek chemiczny o liczbie atomowej . Za pomocą symulacji wskaż, ile izotopów posiada ten pierwiastek oraz podaj ich liczby masowe.