Właściwości fizykochemiczne fluorowców
Znajdują się w jednej kolumnie układu okresowego, ale każdy z nich ma własny, niepowtarzalny charakter. Łączy je silna tendencja do tworzenia związków, często gwałtownie i z dużą energią.
Fluorowce
Fluorowce to pierwiastki należące do 17. grupy układu okresowego. Są to niemetale aktywne chemiczne. Tu ograniczymy się do właściwości fluoru, chloru, bromu i jodu, ponieważ duża część właściwości astatu jest nieznana. Jest to spowodowane jego krótkim czasem życia – czas połowicznego rozpadu najtrwalszego izotopu astatu o liczbie masowej 210 wynosi niewiele ponad osiem godzin.
Dane fizykochemiczne fluorowców:
Atomy fluorowców posiadają siedem elektronów walencyjnych. Konfiguracja elektronowa powłoki walencyjnej w stanie podstawowym ma postać , gdzie jeden niesparowany elektron znajduje się na orbitalu p. Można więc wnioskować, że do uzyskania stabilnej energetycznie konfiguracji elektronowej najbliższego helowca brakuje im tylko jednego elektronu. Fluorowce chętnie tworzą dwuatomowe cząsteczki , , , . Co ciekawe, w związkach chemicznych fluor ma zawsze taki sam stopień utlenienia , zaś pozostałe fluorowce przyjmują najczęściej stopnie utlenienia , , , i .
Wysoka elektroujemność fluorowców świadczy o ich tendencji do przyciągania elektronów z innych pierwiastków, w wyniku czego tworzą ujemne aniony , np. , , oraz . Im większy jest promień atomu fluorowca, tym „gorzej” przyjmuje kolejny elektron. Dlaczego? Im powłoka, na którą przyłączany jest elektron, jest bardziej oddalona od jądra (a zwykle jest to powłoka walencyjna), tym słabsze występuje przyciągnie elektronów przez jądro. Dominują tam efekty wzajemnego odpychania pomiędzy elektronami, dlatego jod ma najsłabsze właściwości utleniające. Natomiast najbardziej elektroujemnym, nie tylko spośród fluorowców, ale i wszystkich pierwiastków chemicznych, jest fluor. Jego elektroujemność wg skali Paulinga to 4,0.
Jak zmienia się aktywność fluorowców?
Fluor gwałtownie reaguje z wodą, tworząc kwas fluorowodorowy i tlen.
Chlor i brom reagują z wodą powoli, tworząc odpowiednio kwas chlorowodorowy i kwas chlorowy(
oraz kwas bromowodorowy i kwas bromowy(
Reaktywność fluorowców maleje w dół grupy.
Fluor jest tak aktywnym pierwiastkiem, że tworzy związki z gazami szlachetnymi. W wyniku ogrzewania, naświetlania lub poddawania wyładowaniami elektrycznymi ksenonu i fluoru powstają fluorki ksenonu.

Ważnym czynnikiem wpływającym na reaktywność fluorowców jest potencjał standardowy półogniw halogenowych.
Półogniwo | Potencjał standardowy EIndeks górny 00 [V] |
|---|---|
2,87 | |
1,36 | |
1,09 | |
0,54 |
Wartość potencjału standardowego ogniwa fluorowego wynosi 2,87 V, co skutkuje tym, że jest on najsilniejszym utleniaczem z całej grupy fluorowców. Teoretycznie może wypierać inne jony fluorowców z roztworu.
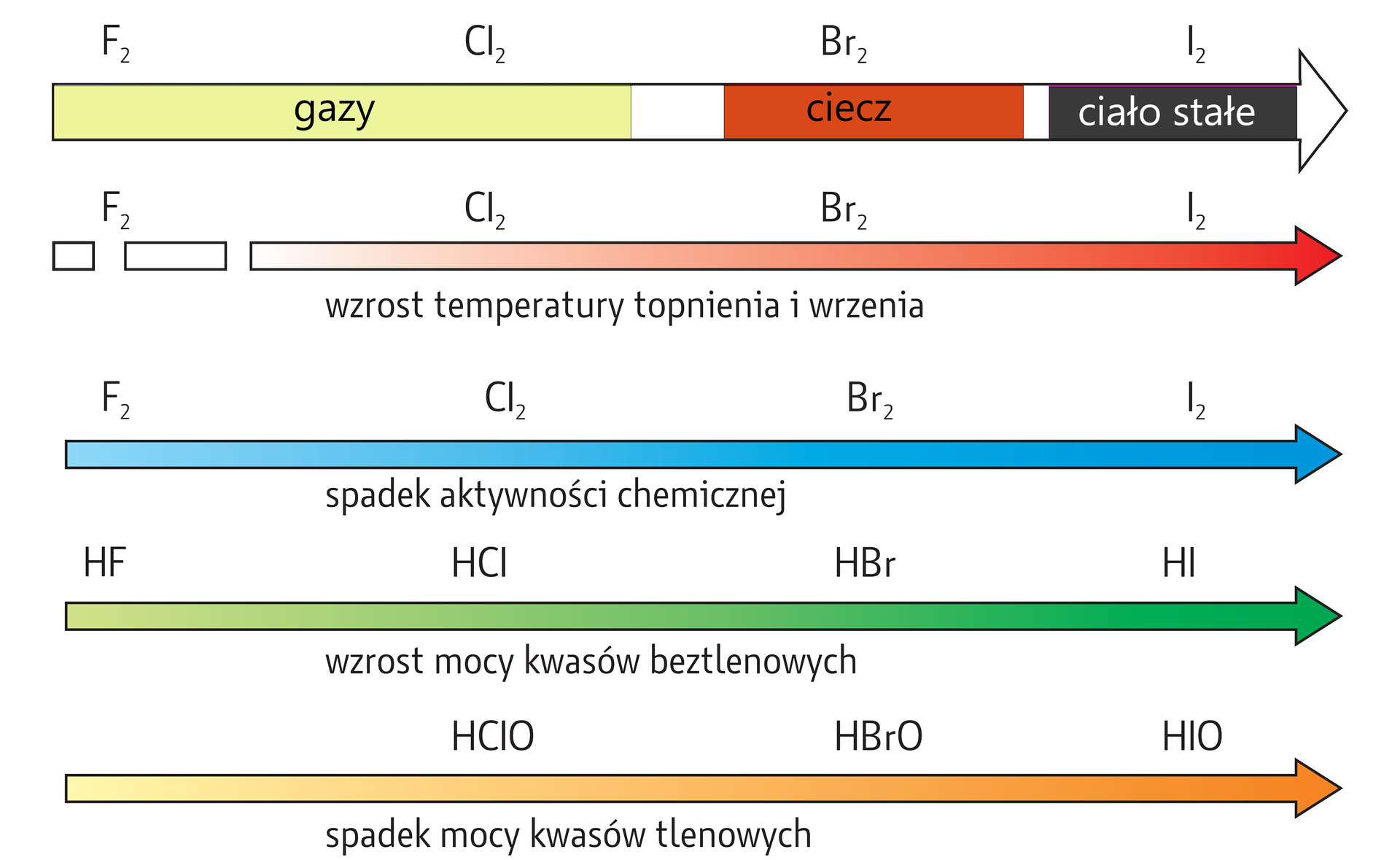
Wraz ze wzrostem liczby atomowej spada reaktywność fluorowców.
Moc kwasów beztlenowych rośnie w dół grupy. Moc kwasów tlenowych zależy od elektroujemności fluorowca – fluorowce o największej elektroujemności będą tworzyć mocniejsze kwasy.
Czy wiesz, jaki jest stan skupienia chloru, bromu i jodu? Znasz wszystkie właściwości fizyczne tych pierwiastków? Przeprowadź doświadczenie w laboratorium chemicznym, które dotyczy właściwości fizycznych fluorowców. Rozwiąż problem badawczy i zweryfikuj hipotezę. Zapisz swoje obserwacje i sformułuj wnioski. Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się w górnej części ekranu.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D4USBZLE6
Czy wiesz, jaki jest stan skupienia chloru, bromu i jodu? Znasz wszystkie właściwości fizyczne tych pierwiastków? Zapoznaj się z opisem doświadczenia chemicznego, które dotyczy właściwości fizycznych fluorowców. Na koniec rozwiąż zadania.
Analiza eksperymentu:
Właściwości fizyczne fluorowców.
Problem badawczy:
Jakie właściwości fizyczne są wspólne dla fluorowców?
Hipoteza:
Chlor, brom i jod charakteryzują się podobnymi właściwościami fizycznymi.
Doświadczenie 1
Sprzęt laboratoryjny:
- probówki z korkami - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
- pipety Pasteura - wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
- łyżeczki - długi trzonek wykonany ze szkła, porcelany lub metalu, zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych.
Odczynniki chemiczne:
- chlor;
- brom;
- jod;
- woda destylowana;
- etanol;
- trichlorometan;
- benzyna.
Przebieg doświadczenia:
1. W trzech probówkach przygotowano próbki bromu (ok. 1 cmIndeks górny 33) i jodu (kilka kryształków), próbki chloru zostały już przygotowane. Probówki z chlorem i bromem zatkano korkami.
2. Do każdej z probówek dodano po 3 cmIndeks górny 33 wody destylowanej. Zawartości probówek wytrząśnięto.
3. Przygotowano trzy zestawy, w każdym z nich po trzy probówki – z próbką chloru, bromu i jodu.
4. Do pierwszego zestawu probówek wlano po 3 cmIndeks górny 33 etanolu.
5. Do drugiego zestawu probówek wlano po 3 cmIndeks górny 33 trichlorometanu.
6. Do trzeciego zestawu probówek wlano po 3 cmIndeks górny 3 Indeks górny koniec3 benzyny.
7. Zatkano probówki korkami i wytrząśnięto. Obserwowano, czy i w jaki sposób badane substancje rozpuszczają się w poszczególnych rozpuszczalnikach.
Doświadczenie 2:
Sprzęt laboratoryjny:
- łyżeczka - długi trzonek wykonany ze szkła, porcelany lub metalu, zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
- kolba okrągłodenna - szklane naczynie laboratoryjne z zaokrąglonym dnem;
- zlewka - naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
- palnik gazowy - rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
- trójnóg laboratoryjny z płytą - umożliwia ustawianie nad palnikiem naczyń laboratoryjnych przeznaczonych do podgrzania.
Odczynniki chemiczne:
- jod.
Przebieg doświadczenia:
1. Na dno zlewki wsypano około pół łyżeczki kryształków jodu.
2. Zlewkę przykryto kolbą okrągłodenną (zawierającą kilka cmIndeks górny 33 zimnej wody).
3. Przykrytą kolbą zlewkę ustawiono na płycie nad palnikiem i delikatnie ogrzewano przez chwilę.
Obserwacje:
1. Chlor to zielonożółty gaz, rozpuszczalny w wodzie, etanolu, benzynie i trichlorometanie. We wszystkich przypadkach tworzy bezbarwny roztwór.
2. Brom to łatwo parująca brunatna ciecz. Rozpuszcza się w wodzie z wytworzeniem żółtobrązowego roztworu. Rozpuszcza się w etanolu, benzynie i trichlorometanie, tworząc pomarańczowe roztwory.
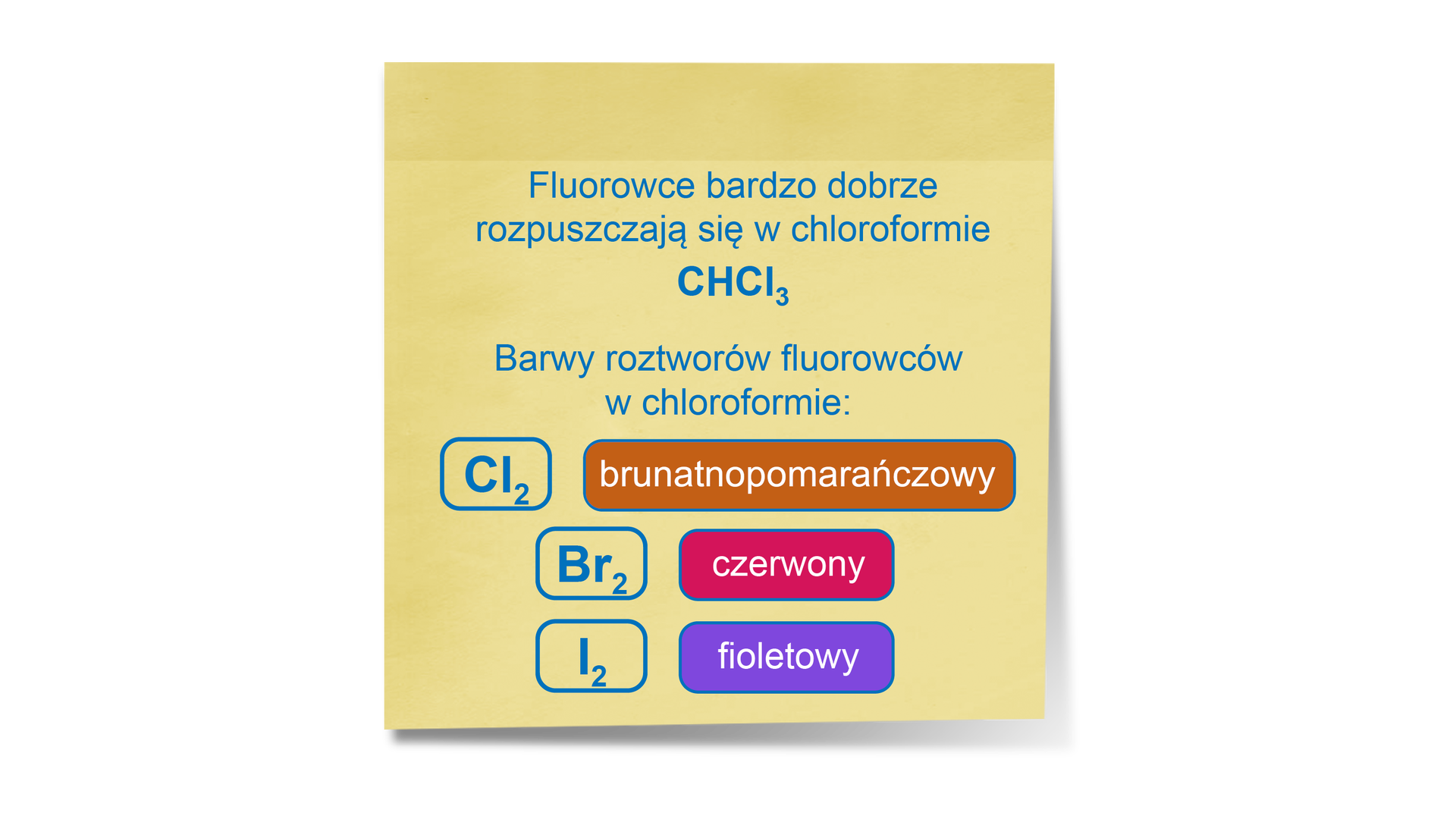
3. Jod to krystaliczne ciało stałe, przyjmuje formę czarno szarych kryształów z metalicznym połyskiem. Jod praktycznie nie rozpuszcza się w wodzie. W przypadku etanolu, rozpuszcza się i tworzy brązowy roztwór. W benzynie rozpuszcza się i tworzy fioletowy roztwór. W trichlorometanie rozpuszcza się z wytworzeniem fioletowo purpurowego roztworu.
4. W wyniku ogrzewania kryształów jodu wydziela się fioletowy gaz.
Wyniki:
Chlor, brom i jod występują w różnych stanach skupienia. Wszystkie dobrze rozpuszczają się w etanolu, benzynie i trichlorometanie. Chlor i brom dobrze rozpuszczają się również w wodzie. Jod jest praktycznie nierozpuszczalny w wodzie. Ich roztwory, podobnie jak same pierwiastki, różnią się barwami.
Wnioski:
Hipoteza nie została potwierdzona. Chlor, brom oraz jod, mimo że należą do tej samej grupy układu okresowego, występują w różnych stanach skupienia.
Wszystkie fluorowce reagują z wodorem cząsteczkowym, jednak czasami wymagane są odpowiednie warunki. Przeanalizuj symulację, która przedstawia zachowanie fluorowców w reakcji z wodorem, wybierając odpowiedni fluorowiec. W momencie, gdy reakcja nie zajdzie samoistnie, spróbuj ją zainicjować poprzez naświetlanie lub podwyższenie temperatury.
Wszystkie fluorowce reagują z wodorem cząsteczkowym, jednak czasami wymagane są odpowiednie warunki. Przeanalizuj opis symulacji, która przedstawia zachowanie fluorowców w reakcji z wodorem, wybierając odpowiedni fluorowiec.
Aktywność chemiczna fluorowców maleje wraz ze wzrostem liczby atomowej fluorowca. Im mniejszy jest promień atomowy (i większa elektroujemność) fluorowca, tym silniej elektrony są przyciągane przez jądro i tym łatwiej tworzy się anion XIndeks górny --. W reakcjach chemicznych fluorowiec bardziej aktywny wypiera z roztworu soli fluorowiec mniej aktywny.
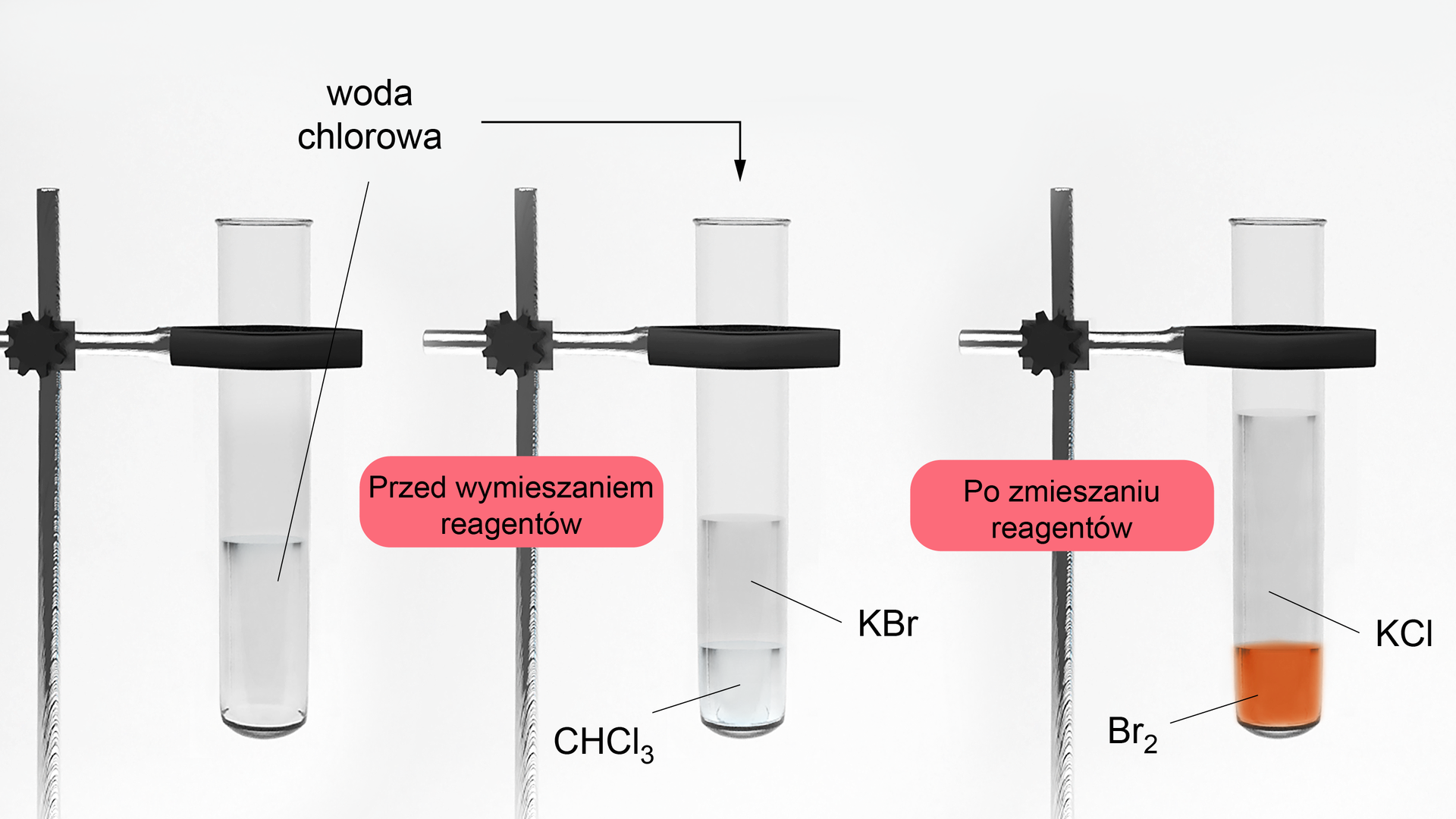
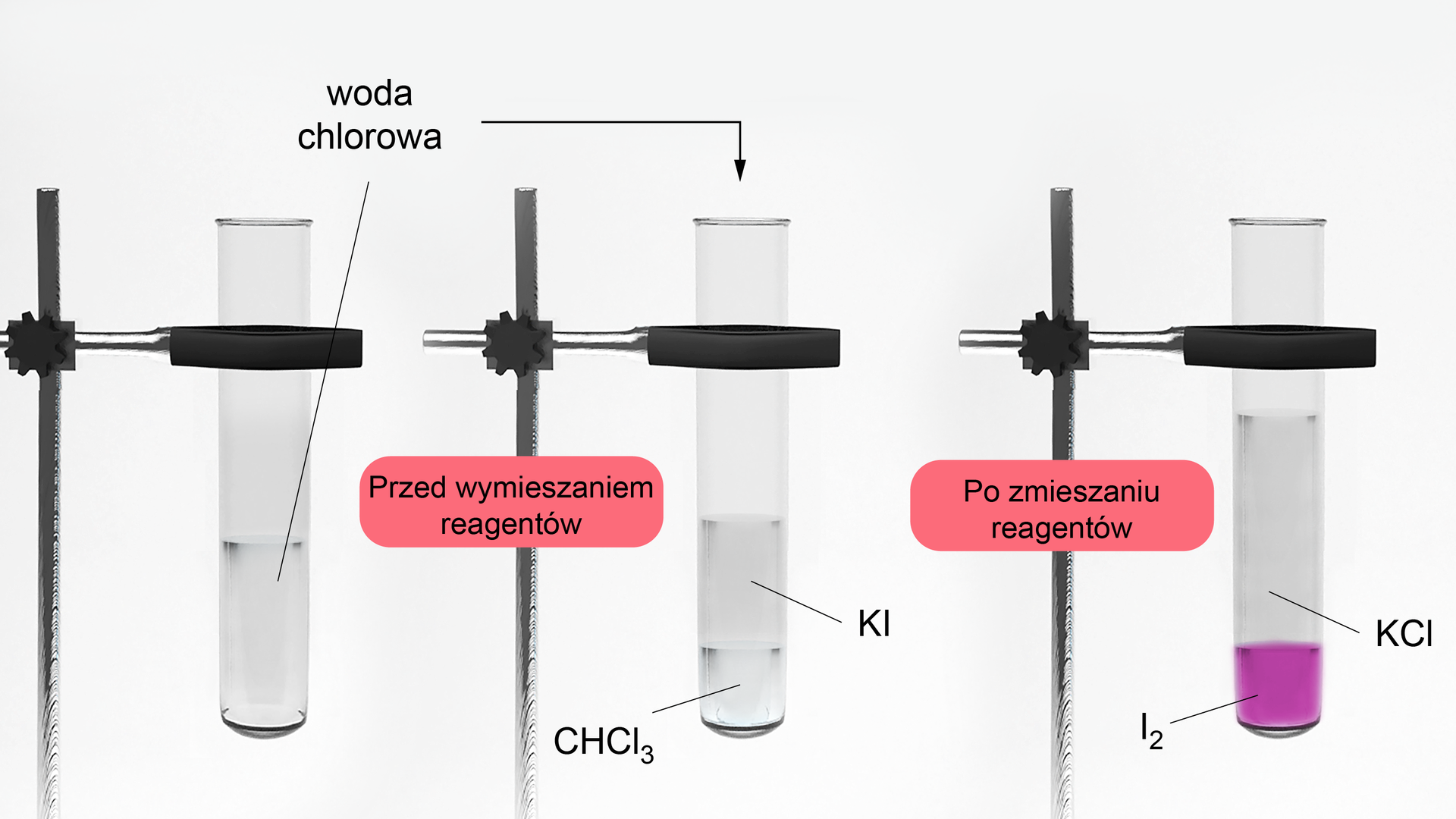
Zaprojektuj doświadczenie chemiczne pozwalające na zbadanie względnej aktywności chemicznej fluorowców. Na podstawie problemu badawczego postaw hipotezę. Opisz przewidywane obserwacje, a następnie napisz równania reakcji zachodzących w probówkach, kolejno porównaj je z tymi znajdującymi się w odpowiedziach. Na podstawie wyników doświadczeń uporządkuj badane fluorowce wg wzrastającej aktywności.
Jak prezentuje się szereg wzrastającej aktywności fluorowców?
Hipoteza: {duzepole‑Treść wewnątrz} Sprzęt i odczynniki laboratoryjne: chlor Ce el 2, roztwór bromku potasu Ka Be er; roztwór jodku potasu Ka i, chloroform, probówki. Instrukcja wykonania doświadczenia: uzupełnij Obserwacje: uzupełnij Wnioski: uzupełnij

Uwaga!
Fluor jest najbardziej reaktywnym (reaguje z wodą) z fluorowców, jednakże ze względu na wysoką toksyczność fluoru i jego związków, doświadczenie z jego użyciem zostało pominięte.
Pamiętaj!
Jakie produkty powstają w reakcji bromu i chloru z jodkiem potasu i o czym to świadczy? Odpowiedź uzasadnij, zapisując odpowiednia równania reakcji chemicznych.
Czy wiesz, w jaki sposób można zapisać równania reakcji z udziałem fluorowców? Zapoznaj się z filmem edukacyjnym i odpowiedz na pytanie.

Film dostępny pod adresem /preview/resource/RQok4r5zM7lrd
Film dotyczy ćwiczenia zapisu równań z udziałem fluorowców.
Fluor gwałtownie reaguje z wodą. Zapisz równanie reakcji.
Zapisz w sposób jonowy skrócony równania reakcji zachodzących pomiędzy azotanem(
a) jonami chloru;
b) jonami bromu;
c) jonami jodu.
![Ilustracja przedstawia podstawowe informacje na temat atomu fluoru. Jego liczba atomowa wynosi 9. Konfiguracja elektronowa podpowłokowa skrócona: [ H e ] 2 s 2 2 p 5 . Konfiguracja klatkowa elektronów walencyjnych: w kwadracie opisanym 2 s 2 znajdują się dwie pionowe równoległe strzałki o grotach skierowanych przeciwnie, dalej znajduje się prostokąt opisany 2 p 5 , jest on podzielony na trzy kwadraty. W pierwszym i drugim znajdują się po dwie pionowe równoległe strzałki o grotach skierowanych przeciwnie, w ostatnim kwadracie znajduje się jedna pionowa strzałka w pozycji równoległej do pozostałych. Ma grot skierowany ku górze. Podano promień atomowy fluoru: 58 pm. Promień jonowy anionu fluorkowego wynosi 133 pm.](https://static.zpe.gov.pl/portal/f/res-minimized/RJREu8ZNlrCef/1640879685/2jZb61ESclTUqcvqbtiIFFWAoxvG7lRY.png)
![Ilustracja przedstawia podstawowe informacje na temat atomu chloru. Jego liczba atomowa wynosi 17. Konfiguracja elektronowa podpowłokowa skrócona: [ N e ] 3 s 2 3 p 5 . Konfiguracja klatkowa elektronów walencyjnych: w kwadracie opisanym 3 s 2 znajdują się dwie, pionowe równoległe strzałki o grotach skierowanych przeciwnie, dalej znajduje się prostokąt opisany 3 p 5 , jest on podzielony na trzy kwadraty. W pierwszym i drugim znajdują się po dwie pionowe równoległe strzałki o grotach skierowanych przeciwnie, w ostatnim kwadracie znajduje się jedna pionowa strzałka w pozycji równoległej do pozostałych. Ma grot skierowany ku górze. Podano promień atomowy chloru: 99 pm. Promień jonowy anionu chlorkowego wynosi 181 pm.](https://static.zpe.gov.pl/portal/f/res-minimized/RCxcHB6Bpp5w3/1640879685/1sOhsW0ZeAxIrDugXvs8jj3MLswsXTpE.png)
![Ilustracja przedstawia podstawowe informacje na temat atomu bromu. Jego liczba atomowa wynosi 35. Konfiguracja elektronowa podpowłokowa skrócona: [ A r ] 4 s 2 3 d 10 4 p 5 . Konfiguracja klatkowa elektronów walencyjnych: w kwadracie opisanym 4 s 2 znajdują się dwie równoległe pionowe strzałki o grotach skierowanych przeciwnie, dalej znajduje się prostokąt opisany 4 p 5 , jest on podzielony na trzy kwadraty. W pierwszym i drugim znajdują się po dwie pionowe równoległe strzałki o grotach skierowanych przeciwnie, w ostatnim kwadracie znajduje się jedna strzałka w pozycji równoległej do pozostałych. Ma grot skierowany ku górze. Podano promień atomowy bromu: 114 pm. Promień jonowy anionu bromkowego wynosi 196 pm.](https://static.zpe.gov.pl/portal/f/res-minimized/R1Q8sQYzxZ0O5/1640879686/ey02R7yLGoiDptzxmsCcOPkzj9VbpZgb.png)
![Ilustracja przedstawia podstawowe informacje na temat atomu jodu. Jego liczba atomowa wynosi 53. Konfiguracja elektronowa podpowłokowa skrócona: [ K r ] 5 s 2 4 d 10 5 p 5 . Konfiguracja klatkowa elektronów walencyjnych: w kwadracie opisanym 5 s 2 znajdują się dwie równoległe, pionowe strzałki o grotach skierowanych przeciwnie, dalej znajduje się prostokąt opisany 5 p 5 , jest on podzielony na trzy kwadraty. W pierwszym i drugim znajdują się po dwie równoległe, pionowe strzałki o grotach skierowanych przeciwnie, w ostatnim kwadracie znajduje się jedna strzałka w pozycji równoległej do pozostałych. Jej grot jest skierowany ku górze. Podano promień atomowy jodu: 133 pm. Promień jonowy anionu bromkowego wynosi 220 pm.](https://static.zpe.gov.pl/portal/f/res-minimized/R1Y7llI3cAK2G/1640879686/1uCvj5vW58iorI40r48s7PiuuJ1S8sd0.png)
![Ilustracja przedstawia podstawowe informacje na temat atomu astatu. Jego liczba atomowa wynosi 85. Konfiguracja elektronowa podpowłokowa skrócona: [ X e ] 6 s 2 4 f 14 5 d 2 6 p 5 . Konfiguracja klatkowa elektronów walencyjnych: w kwadracie opisanym 6 s 2 znajdują się dwie równoległe, pionowe strzałki o grotach skierowanych przeciwnie, dalej znajduje się prostokąt opisany 6 p 5 , jest on podzielony na trzy kwadraty. W pierwszym i drugim znajdują się po dwie równoległe, pionowe strzałki o grotach skierowanych przeciwnie, w ostatnim kwadracie znajduje się jedna strzałka w pozycji równoległej do pozostałych. Jej grot jest skierowany ku górze. Podano promień atomowy astatu: 140 pm. Promień jonowy anionu astatu wynosi 227 pm.](https://static.zpe.gov.pl/portal/f/res-minimized/R3zafDsD0zquu/1640879687/sQBHeZpUWYuIg61LmUdRFHcIWYPdpvS4.png)