Miareczkowanie alkacymetryczne w obecności wskaźnika
Wprowadzenie do analizy objętościowej
Analiza ilościowa jest metodą, za pomocą której chemicy są w stanie określić ilości oraz stężenia substancji obecnych w próbce, np. zawartość kwasu askorbinowego (witaminy C) w tabletce. Jednym z rodzajów analizy ilościowej jest analiza miareczkowa (objętościowa). Podczas analizy miareczkowej do określonej objętości roztworu z oznaczoną substancją (analitemanalitem) dodawany jest porcjami roztwór z biurety, zwany titrantemtitrantem, który jest roztworem mianowanymroztworem mianowanym.
Zapoznaj się z poniższą grafiką interaktywną, przedstawiającą zestaw do miareczkowania, i odpowiedz na pytania.
Biurety, stosowane do miareczkowania, często charakteryzują się odwrotną skalą, tzn. wartość „” jest na górze biurety, a na samym dole jest największa wartość, jednocześnie stanowiąca objętość biurety. Wyjaśnij, dlaczego zastosowanie takiej skali w biurecie do miareczkowania jest wygodniejsze od standardowej skali?
Miareczkowanie alkacymetryczne
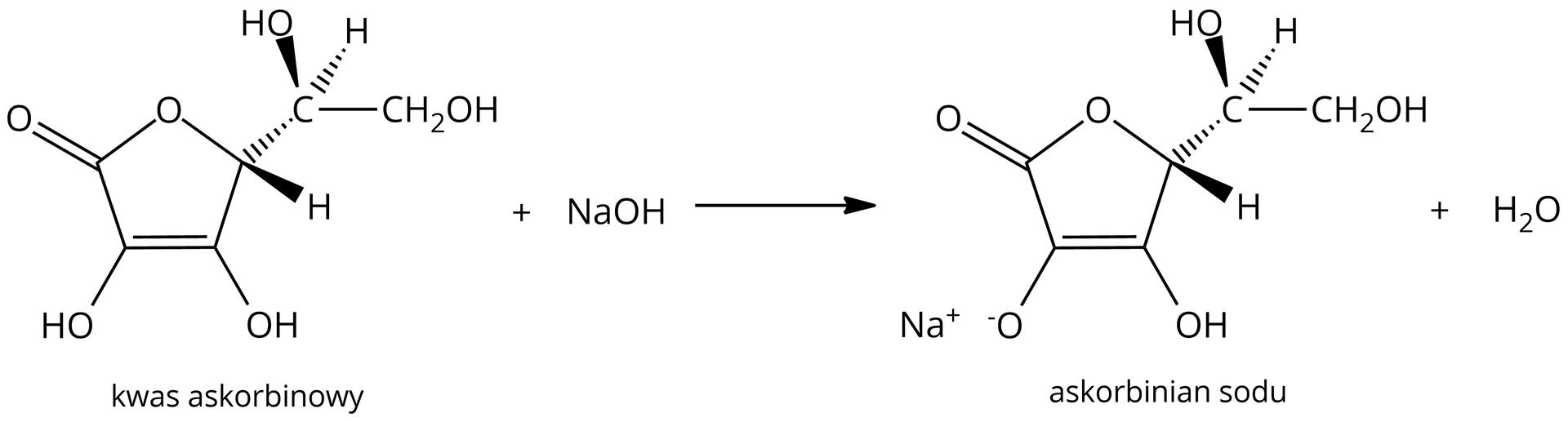
Z uwagi na typ reakcji zachodzącej pomiędzy oznaczanym składnikiem a titrantemtitrantem, analiza miareczkowa jest podzielona na określone działy. Jednym z nich jest alkacymetriaalkacymetria oparta na reakcji zobojętniania, czyli reakcji kwasu z zasadą:
W zależności od rodzaju używanego titranta, alkacymetria obejmuje dwie metody oznaczeń:
alkalimetrięalkalimetrię – titrantem jest zasada, a analitem kwas;
acydymetrięacydymetrię – titrantem jest kwas, a analitem zasada.
Objętość zużytego podczas miareczkowania titranta pozwala na obliczenie zawartości składnika w badanej próbce. Miareczkowanie powinno zostać zakończone w momencie, gdy titrant przereaguje ilościowo z oznaczanym składnikiem. Moment ten definiuje się jako punkt równoważnikowypunkt równoważnikowy (PR), a do jego określenia stosowane są metody instrumentalne (np. pehametr) lub wizulane (wskaźnik chemiczny).
Wskaźniki chemiczne
Aby wizualnie określić koniec miareczkowania alkacymetrycznego, stosuje się odpowiedni wskaźnikwskaźnik (indykator), który zmienia barwę roztworu w okolicach zakończenia reakcji pomiędzy roztworem miareczkowanym a titrantem. Do analitu dodawana jest zazwyczaj niewielka ilość wskaźnika. Jeśli zostanie użyta duża ilość, wskaźnik wpłynie na końcowe , obniżając dokładność eksperymentu.
Moment, w którym wskaźnik zmienia barwę, nazywa się punktem końcowym miareczkowania (PK). Punkt ten zasadniczo powinien pokrywać się z punktem równoważnikowym, jednak w praktyce prawie zawsze następuje przed lub po nim. Różnica między punktem końcowym a punktem równoważnikowym nazywa się błędem miareczkowania.
Indeks dolny /Źródło: Lipiec T., Szmal Z., Chemia analityczna z elementami analizy instrumentalnej, Warszawa 1980./ Indeks dolny koniec/Źródło: Lipiec T., Szmal Z., Chemia analityczna z elementami analizy instrumentalnej, Warszawa 1980./

Wskaźniki kwasowo–zasadowe zmieniają barwę w różnych zakresach . Zakres zmiany barwy wskaźnika powinien leżeć w zakresie skoku miareczkowania, czyli gwałtownej zmiany w pobliżu punktu równoważnikowego.
Nazwa wskaźnika | Zakres zmiany barwy | Barwa wskaźnika poniżej niższej wartości | Barwa wskaźnika powyżej wyższej wartości |
|---|---|---|---|
oranż metylowy | – | czerwona | żółtopomarańczowa |
tymoloftaleina | – | bezbarwna | niebieska |
fenoloftaleina | – | bezbarwna | malinowa |
Błękit tymolowy | – | czerwona | żółta |
– | żółta | niebieska | |
błękit bromotymolowy | – | żółta | niebieska |
błękit bromofenolowy | – | żołta | niebieskofioletowa |
czerwień metylowa | – | czerwona | żółta |
czerwień Kongo | – | niebieska | czerwona |
lakmus | – | czerwona | niebieska |
Krzywe miareczkowania alkacymetrycznego
Krzywa miareczkowaniaKrzywa miareczkowania dla miareczkowania kwasowo‑zasadowego jest wykresem zależności analizowanego roztworu od objętości dodanego titranta. Oznacza to, że w miarę dodawania titranta z biurety zmienia się roztworu analizowanego. Krzywe te są przydatne przy wyborze odpowiednich wskaźników kwasowo‑zasadowych, które pozwalają na dokładne określenie punktów końcowychpunktów końcowych miareczkowania. Z uwagi na stosowanie słabych, jak i mocnych elektrolitówmocnych elektrolitów (kwasów oraz zasad), w alkacymetrii możliwe są cztery przypadki. W każdym z nich obserwuje się inny kształt krzywej miareczkowania.
Kształt krzywych w przypadku słabych elektrolitów zależy w znacznym stopniu od ich mocy – roztworów słabych elektrolitów zależy od stężenia i stałej dysocjacji, a w konsekwencji wpływa to również na profil krzywej miareczkowania oraz położenie punktu równoważnikowego.
Przykładowe krzywe miareczkowania dla różnych typów badanych roztworów przedstawiono poniżej.
Jak obliczyć rzeczywistą masę kwasu askorbinowego w tabletce?
W laboratorium wykonano doświadczenie, w którym sprawdzano rzeczywistą zawartość kwasu askorbinowego w tabletce, komercyjnie dostępnego suplementu.
Na opakowaniu suplementu widnieje informacja, że tabletka zawiera kwasu askorbinowego.
Po rozpuszczeniu tabletki w wody destylowanej, do roztworu dodano niewielką ilość wskaźnika kwasowo‑zasadowego (błękitu bromotylowego).
Jak obliczyć rzeczywistą masę kwasu askorbinowego w tabletce, wiedząc, że jego masa molowa wynosi ?
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje i wyniki, a następnie sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D77HLN3QK
Przeprowadzono doświadczenie w wirtualnym laboratorium chemicznym. Rozwiązano problem badawczy i zweryfikowano hipotezę. W formularzu zapisano obserwacje i wyniki, a następnie sformułowano wnioski.
Analiza doświadczenia:
Miareczkowanie alkacymetryczne w obecności wskaźnika.
Problem badawczy:
Czy wykorzystując odpowiedni wskaźnik kwasowo‑zasadowy, można wyznaczyć punkt końcowy miareczkowania i obliczyć masę kwasu lub zasady w analizowany roztworze?
Hipoteza:
Wykorzystując odpowiedni wskaźnik kwasowo–zasadowy, można wyznaczyć punkt końcowy miareczkowania i obliczyć masę kwasu lub zasady w analizowany roztworze.
Sprzęt i szkło laboratoryjne:
biureta – podłużna szklana rurka zakończona kranikiem skalibrowana, na odpowiednią objętość z reguły z podziałką o dokładności mililitra;
kolby stożkowe – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szyjką;
lejek – szkło w kształcie odwróconego stożka, zwężającą się rurką służący do przelewania cieczy lub sączenia;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
pipeta – wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
kolba miarowa – kolba z reguły okrągła, płaskodenna z podłużną, wąską szyjką oraz korkiem skalibrowana na daną objętość, która zaznaczona jest za pomocą wyżłobionej w szkle kreski;
statyw – pionowy pręt ze stabilną podstawą umożliwiający mocowanie na wybranej wysokości, na przykład szkła laboratoryjnego umieszczonego w łapie;
łapa – rodzaj narzędzia wykorzystywanego w laboratorium do trzymania, na przykład kolb;
mieszadło magnetyczne – urządzenie umożliwiające mieszanie, dzięki wykorzystaniu dipola magnetycznego.
Odczynniki:
roztwór kwasu chlorowodorowego mol na decymetr sześcienny, roztwór wodorotlenku sodu mol na decymetr sześcienny, roztwór kwasu octowego, fenoloftaleina, oranż metylowy, woda destylowana.
Obserwacje:
Podczas miareczkowania wodnego roztworu kwasu octowego wskaźnik zabarwia się na jasnoróżowo.
Podczas miareczkowania wodnego roztworu kwasu chlorowodorowego barwa wskaźnika zmienia się z czerwonej na pomarańczową.
Podczas miareczkowania wodnego roztworu wodorotlenku sodu barwa wskaźnika zmienia się z żółtej na jasnopomarańczową.
Przebieg doświadczenia:
1. Korzystając z lejka, uzupełniono biuretę roztworem titranta (kwasu chlorowodorowego o stężeniu mol na decymetr sześcienny). Pamiętano, aby podczas tej czynności kranik na dole biuretu był zamknięty.
2. Pipetę przepłukano dwukrotnie niewielką ilością badanego roztworu, czyli wodnego roztworu wodorotlenku sodu.
3. Pobrano pipetą centymetrów sześciennych analizowanego roztworu wodorotlenku sodu (analitu) i przeniesiono do kolby stożkowej, dodano dwie lub trzy krople oranżu metylowego. Pamiętano o dodaniu mieszadełka magnetycznego.
4. Tak przygotowany roztwór ustawiono na mieszadle magnetycznym.
5. Mieszając roztwór w kolbie stożkowej, dodawano kroplami titrant z biurety, aż do pojawienia się pierwszego zauważalnego trwałego zabarwienia z żółtego na przejściowo jasno pomarańczowe. Odczytano z podziałki biurety objętość zużytego titranta i zanotowano wyniki.
6. Miareczkowanie powtórzono trzykrotnie. Jako wynik końcowy przyjęto średnią arytmetyczną wyników z wykonanych pomiarów.
7. Wykonano obliczenia zgodnie z równaniem stechiometrycznym zastosowanej reakcji, używając następujących danych: średnia objętość titranta, jaka została zużyta do miareczkowania, stężenie molowe titranta, objętość roztworu miareczkowanego, dokładna masa molowa oznaczanej substancji, obliczona na podstawie mas atomowych z układu okresowego pierwiastków.
Wyniki:
Zawartość kwasu octowego w miareczkowanej próbce analitu: .
Zawartość kwasu chlorowodorowego w miareczkowanej próbce analitu: .
Zawartość wodorotlenku sodu w miareczkowanej próbce analitu: .
Wnioski:
Prowadząc miareczkowanie alkacymetryczne, w obecności odpowiedniego wskaźnika kwasowo–zasadowego, można wyznaczyć końcowy punt miareczkowania i obliczyć zawartość kwasu lub zasady w analizowanym roztworze.