Chlor - ogólna charakterystyka i otrzymywanie
Chlor to pierwiastek, który wielu z nas kojarzy z ostrym zapachem basenu lub silnym środkiem dezynfekującym. Ale za tym intensywnym pierwszym wrażeniem kryje się znacznie więcej. Jako przedstawiciel fluorowców, chlor należy do grupy niezwykle reaktywnych pierwiastków, które mają ogromny wpływ na przebieg reakcji chemicznych i właściwości związków. Jego zdolność do tworzenia trwałych i różnorodnych połączeń sprawia, że odgrywa ważną rolę w chemii organicznej, nieorganicznej, a nawet w biochemii.
Właściwości fizyczne chloru
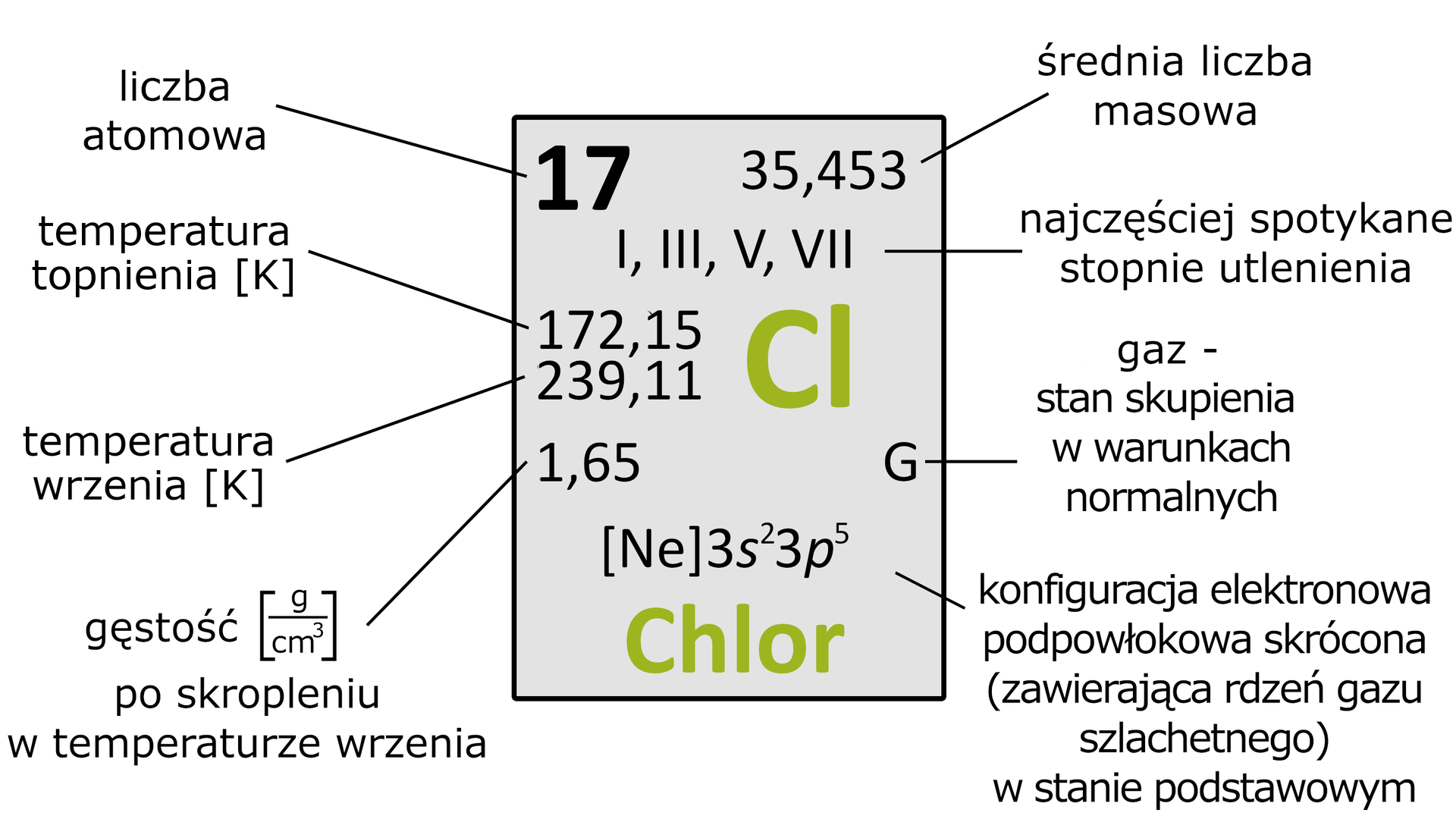
Przeanalizuj dane z tabeli i określ, w jakim stanie skupienia występuje chlor w warunkach normalnych.
chlorowiec | temperatura topnienia | temperatura wrzenia | promień jonowy [] | promień kowalencyjny [] |
|---|---|---|---|---|
Chlor | ||||
Brom | ||||
Jod |
Chlor jest gazem o barwie zielonożółtej, cięższym od powietrza. Charakteryzuje się ostrym, intensywnym zapachem i jest wyczuwalny w powietrzu przy stężeniu . Chlor rozpuszcza się w wodzie, tworząc tzw. wodę chlorową. Rozpuszczalność chloru w wodzie zależy od temperatury. W wody o temperaturze rozpuszcza się chloru (odmierzonego w warunkach normalnych). Chlor w reakcji z wodą ulega dysproporcjonowaniu na chlorowodór
() i kwas chlorowy() ().
Metody otrzymywanie chloru
Otrzymywanie chloru w reakcji tlenku manganu() i kwasu chlorowodorowego
Pierwsza opisana synteza chloru opierała się na reakcji chemicznej pomiędzy tlenkiem manganu(), a kwasem solnym (chlorowodorowym).
Schemat tej reakcji ma postać:
Jak łatwo zauważyć, w powyższej reakcji chemicznej następuje zmiana stopni utlenienia atomów pierwiastków chemicznych. Dlatego też powyższa reakcja jest reakcją typu redoks (utleniania‑redukcji). Współczynniki stechiometryczne należy więc dobrać metodą bilansu jonowo‑elektronowego:
Równanie procesu redukcji:
Równanie procesu utlenienia:
Sumaryczne równanie reakcji:
W tej reakcji chemicznej tlenek manganu() pełni funkcję utleniacza, a kwas solny (chlorowodorowy) funkcję reduktora.
Modyfikacją tej metody może być ogrzewanie roztworu solanki z kwasem siarkowym() i tlenkiem manganu().
Schemat tej reakcji ma postać:
Podobnie jak w poprzednim przypadku w reakcji tej następuje zmiana stopni utlenienia indywiduów, dlatego też współczynniki stechiometryczne należy dobrać metodą bilansu jonowo‑elektronowego:
Równanie procesu redukcji:
Równanie procesu utlenienia:
Sumaryczne równanie reakcji:
Otrzymywanie chloru w wyniku utleniania chlorowodoru
Z czasem zauważono, że chlor ma właściwości wybielające, co zwiększyło zapotrzebowanie na tę gazową substancję prostą. Jedną z pierwszych metod otrzymywania chloru była reakcja spalania chlorowodoru w tlenie, z chlorkiem miedzi() pełniącym funkcję katalizatora.
Schemat tej reakcji ma postać:
Podobnie jak we wcześniejszych reakcjach chemicznych możemy zauważyć zmiany stopni utlenienia indywiduów, dlatego też współczynniki stechiometryczne należy dobrać metodą bilansu elektronowego:
Równanie procesu redukcji:
Równanie procesu utlenienia:
Sumaryczne równanie reakcji:
Otrzymywanie chloru w reakcji kwasów lub bezwodników kwasowych z chloranem() wapnia
W warunkach laboratoryjnych chlor można również otrzymać w wyniku reakcji kwasów (lub bezwodników kwasowych kwasów nieorganicznych) z solami wapniowymi będącymi pochodnymi kwasu chlorowego() (kwasu podchlorawego), m.in. z chloranem() wapnia.
W wyniku działania kwasem solnym (chlorowodorowym) na chloran() wapnia otrzymuje się gazowy chlor.
Schemat analizowanej reakcji ma postać:
Aby dobrać współczynniki w powyższej reakcji chemicznej należy wykorzystać metodę bilansu jonowo‑elektronowego:
Równanie procesu redukcji:
Równanie procesu utlenienia:
Sumaryczne równanie reakcji:
Otrzymywanie chloru metodą elektrolizy
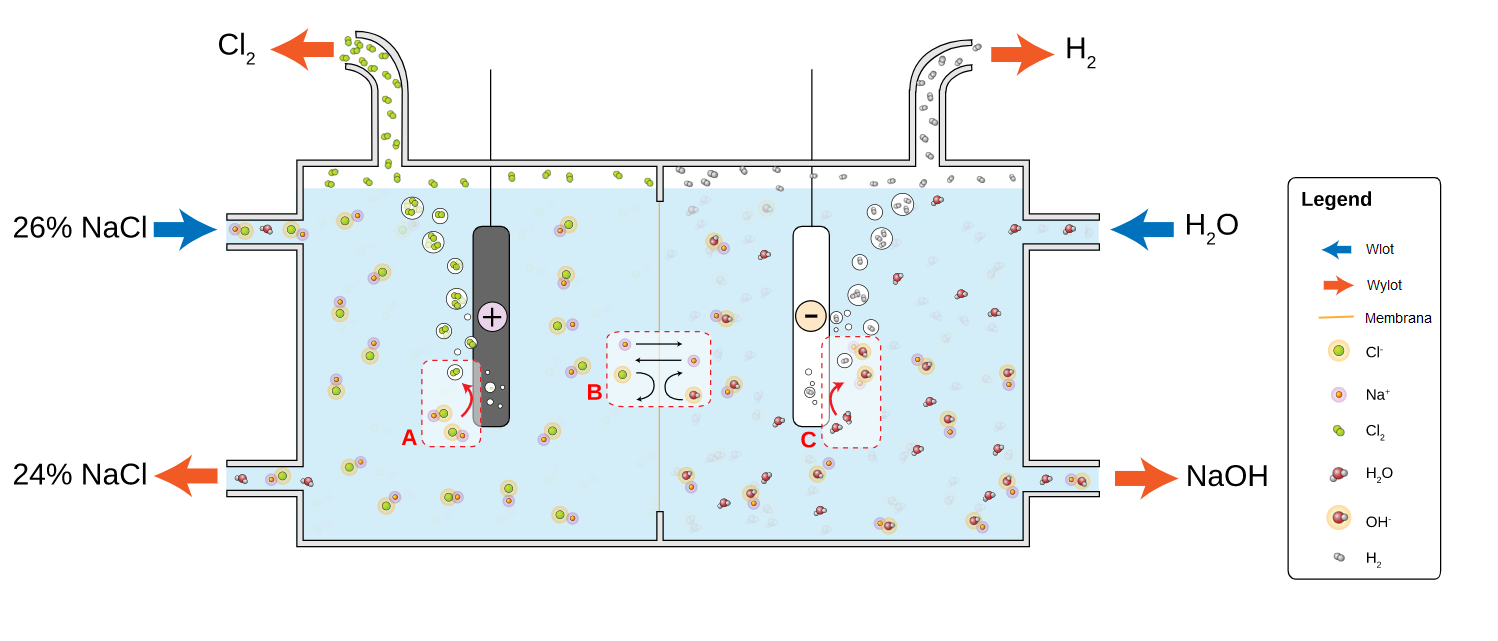
Inną wykorzystywaną w laboratorium metodą syntezy chloru jest metoda elektrolizy solanki. W trakcie procesu elektrolizy na elektrodach zachodzą odpowiednie procesy:
Równanie procesu katodowego:
Równanie procesu anodowego:
Sumaryczne równanie reakcji:
Produktami reakcji elektrolizy solanki są: chlor, wodór oraz wodorotlenek sodu.
Czy wiesz, w jaki sposób można otrzymać chlor w warunkach laboratoryjnych? Jaką reakcję należy przeprowadzić i w jakiej postaci otrzyma się taki produkt? Przeanalizuj przedstawione wirtualne laboratorium, rozwiąż problem badawczy i zweryfikuj hipotezę. Uzupełnij obserwacje, wyniki i wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D79TKA7QD
Czy wiesz, w jaki sposób można otrzymać chlor w warunkach laboratoryjnych? Jaką reakcję należy przeprowadzić i w jakiej postaci otrzyma się taki produkt? Przeanalizuj opis poniższego doświadczenia, w którym rozwiązano problem badawczy i zweryfikowano hipotezę. Następnie rozwiąż ćwiczenia sprawdzające.
Analiza doświadczenia:
Otrzymywanie chloru w warunkach laboratoryjnych.
Problem badawczy:
Jak otrzymać chlor w warunkach laboratoryjnych?
Hipoteza:
W reakcji manganianu potasu z kwasem chlorowodorowym wydziela się chlor.
Sprzęt i szkło laboratoryjne:
łyżeczka metalowa – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką;
pipeta Pasteura – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
palnik laboratoryjny – urządzenie techniczne umożliwiające podtrzymywanie płomienia spalanego gazu w kontrolowany sposób;
kolba stożkowa z korkiem – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szyjką;
drucik miedziany.
Odczynniki chemiczne:
manganian potasu;
stężony kwas chlorowodorowy.
Przebieg doświadczenia:
Umieszczenie manganianu potasu w kolbie stożkowej przy pomocy łyżki laboratoryjnej i lejka.
Odmierzenie dziesięciu centymetrów sześciennych stężonego roztworu kwasu chlorowodorowego przy pomocy cylindra miarowego. Umieszczenie odmierzonego kwasu we wkraplaczu.
Zatkanie wylotu kolby dwuszyjnej korkiem z gumowym wężykiem.
Dodawanie kwasu chlorowodorowego do kolby okrągłodennej. Zebranie wydzielającego się gazu.
Analiza produktu:
Rozgrzanie drucika miedzianego w płomieniu palnika.
Umieszczenie rozgrzanego drucika w kolbie z zebranym gazem.
Wyjęcie drucika z kolby i wlanie do niej niewielkiej ilości wody destylowanej. Wymieszanie zawartości kolby.
Obserwacje:
Po wprowadzeniu stężonego kwasu chlorowodorowego do manganianu potasu zaobserwowano wydzielanie się żółtozielonego gazu. Gaz ten zbierał się w pustej kolbie, opadając na jej dno. Po wprowadzeniu do kolby z zebranym gazem, żarzącego się miedzianego drucika, zaobserwowano powstawanie brunatnozielonego dymu. Po wlaniu wody destylowanej do tej kolby i po wymieszaniu zawartości otrzymano niebieski roztwór.
Wyniki:
Otrzymany żółtozielony gaz to chlor. Zostało to potwierdzone w reakcji z miedzią. Obserwowane brunatnozielone “dymy” to pary bezwodnego chlorku miedzi. Niebieska barwa roztworu potwierdza, że są w nim obecne jony miedzi.
Wnioski:
Otrzymano chlor w warunkach laboratoryjnych. Hipoteza została potwierdzona – w reakcji manganianu potasu z kwasem chlorowodorowym powstaje chlor.
Stosując zapis cząsteczkowy, zapisz równania reakcji przeprowadzonych w wirtualnym laboratorium. Współczynniki stechiometryczne dobierz metodą bilansu jonowo‑elektronowego.
Stosując zapis cząsteczkowy, zapisz równania reakcji przeprowadzonych w wirtualnym laboratorium. Współczynniki stechiometryczne dobierz metodą bilansu jonowo‑elektronowego.
Właściwości chemiczne chloru
Dlaczego atomy chloru łączą się, tworząc cząsteczki dwuatomowe? Jaki wpływ na konfigurację każdego z atomów chloru, tworzących cząsteczkę , ma uwspólnienie dodatkowego elektronu?
Chlor jest aktywnym chemicznie niemetalem, który w związkach może występować na , , , i stopniu utlenienia. Łączy się on bezpośrednio z większością pierwiastków. Z metalami tworzy sole – chlorki. Jest silnym utleniaczem, co sprawia, że w odpowiednich warunkach może utleniać wiele metali, w tym również metale szlachetne:
Metale, takie jak np. żelazo, utlenia do wyższych stopni utlenienia niż :
W przyrodzie najpopularniejszymi związkami chloru są:
W obecności światła łączy się z wodorem, tworząc chlorowodór:
Chlorowodór jest głównie otrzymywany przez działanie stężonych roztworów mocnych kwasów, np. kwasu siarkowego() na chlorki, np. chlorek sodu:
Od tej reakcji wywodzi się nazwa zwyczajowa kwasu chlorowodorowego – kwas solny, bo wypierany jest z soli kuchennej.
W reakcji z wodą tworzy mocny kwas chlorowodorowy:
Tlenki chloru są związkami generalnie nietrwałymi. Wszystkie mają charakter kwasowy.
stopień utlenienia chloru | wzór tlenku | wzór strukturalny tlenku | wzór kwasu tlenowego | wzór strukturalny kwasu | nazwa kwasu | wzrost mocy kwasów | wzrost właściwości utleniających |
|---|---|---|---|---|---|---|---|
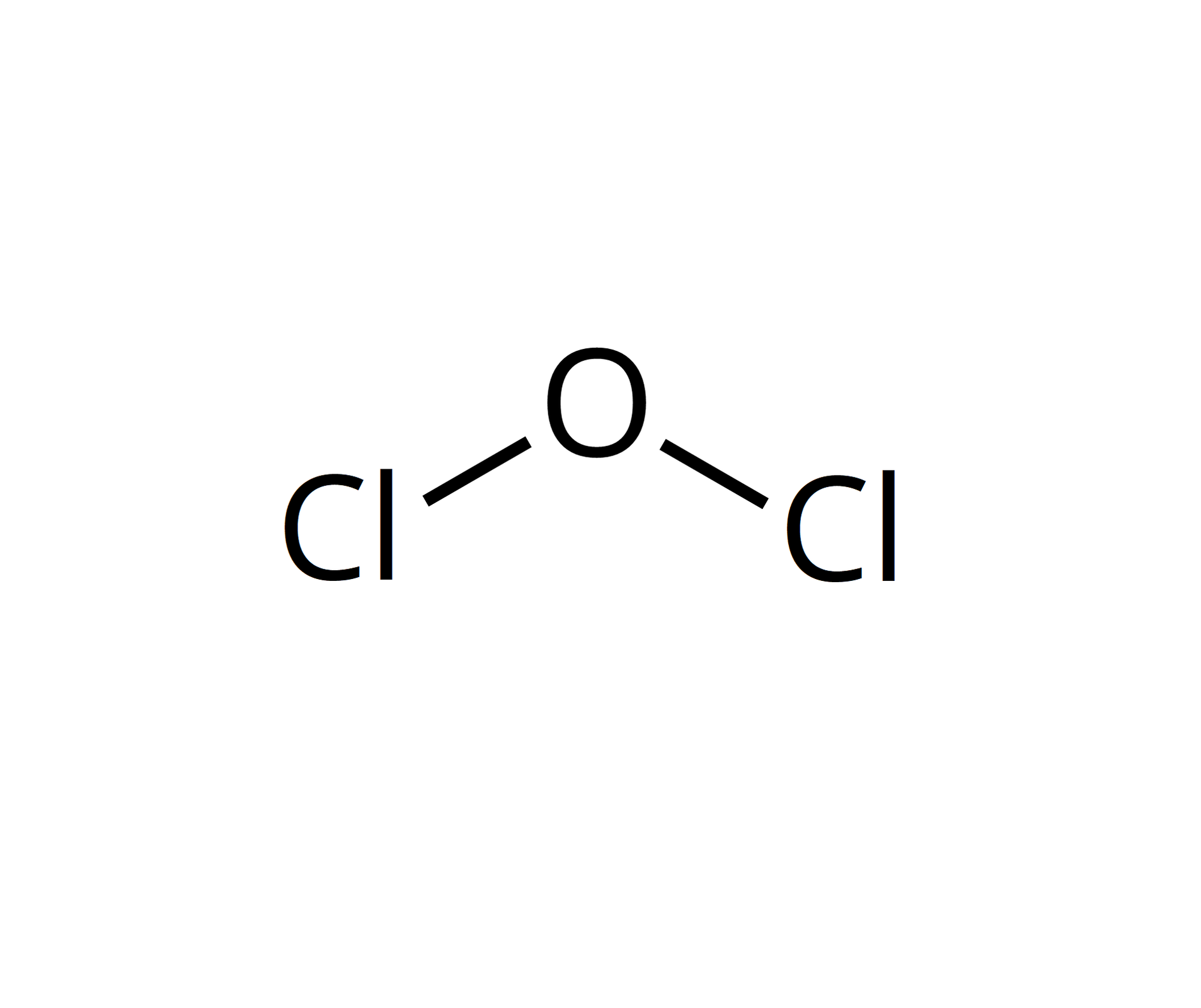 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | 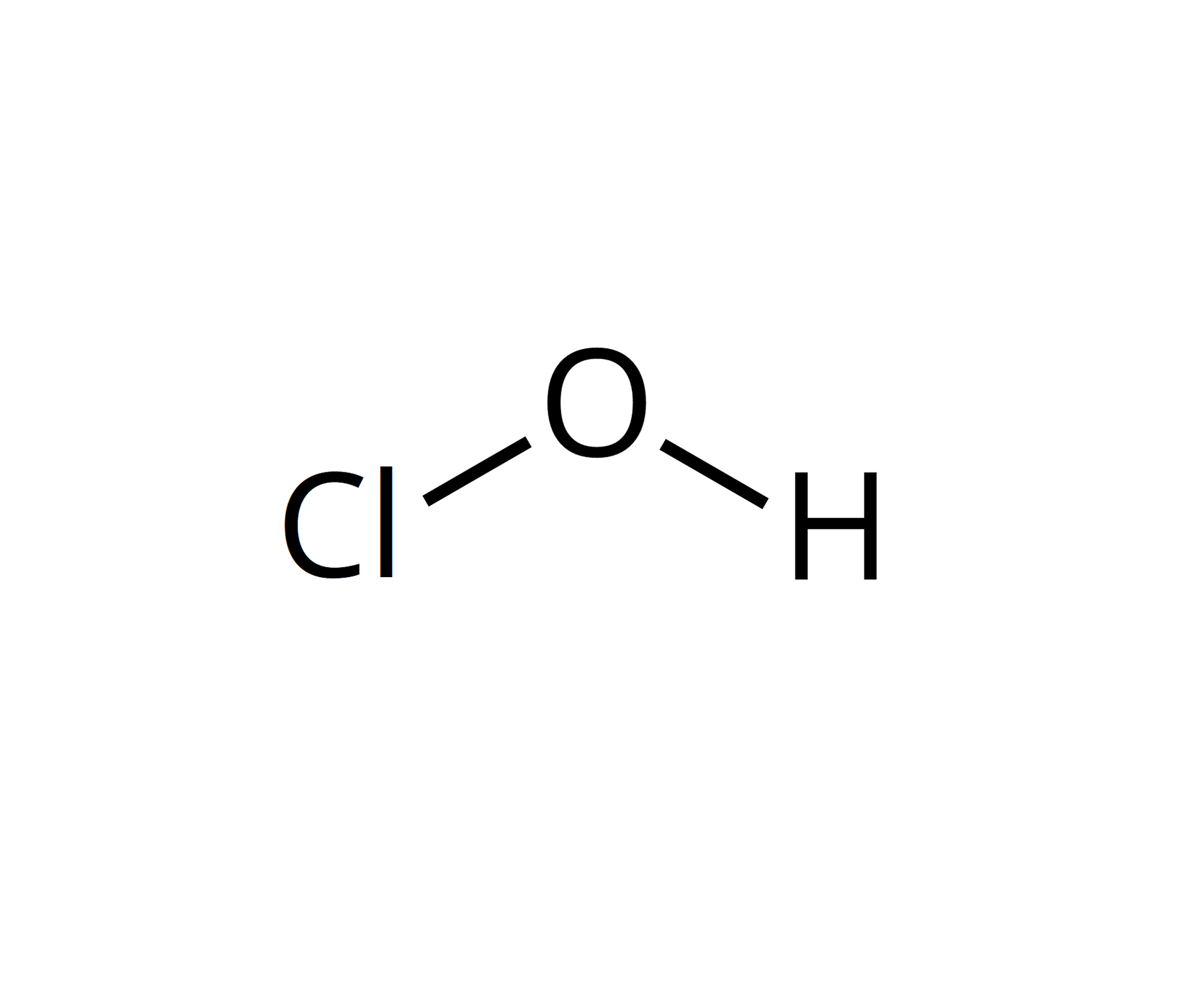 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas chlorowy |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | |||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | 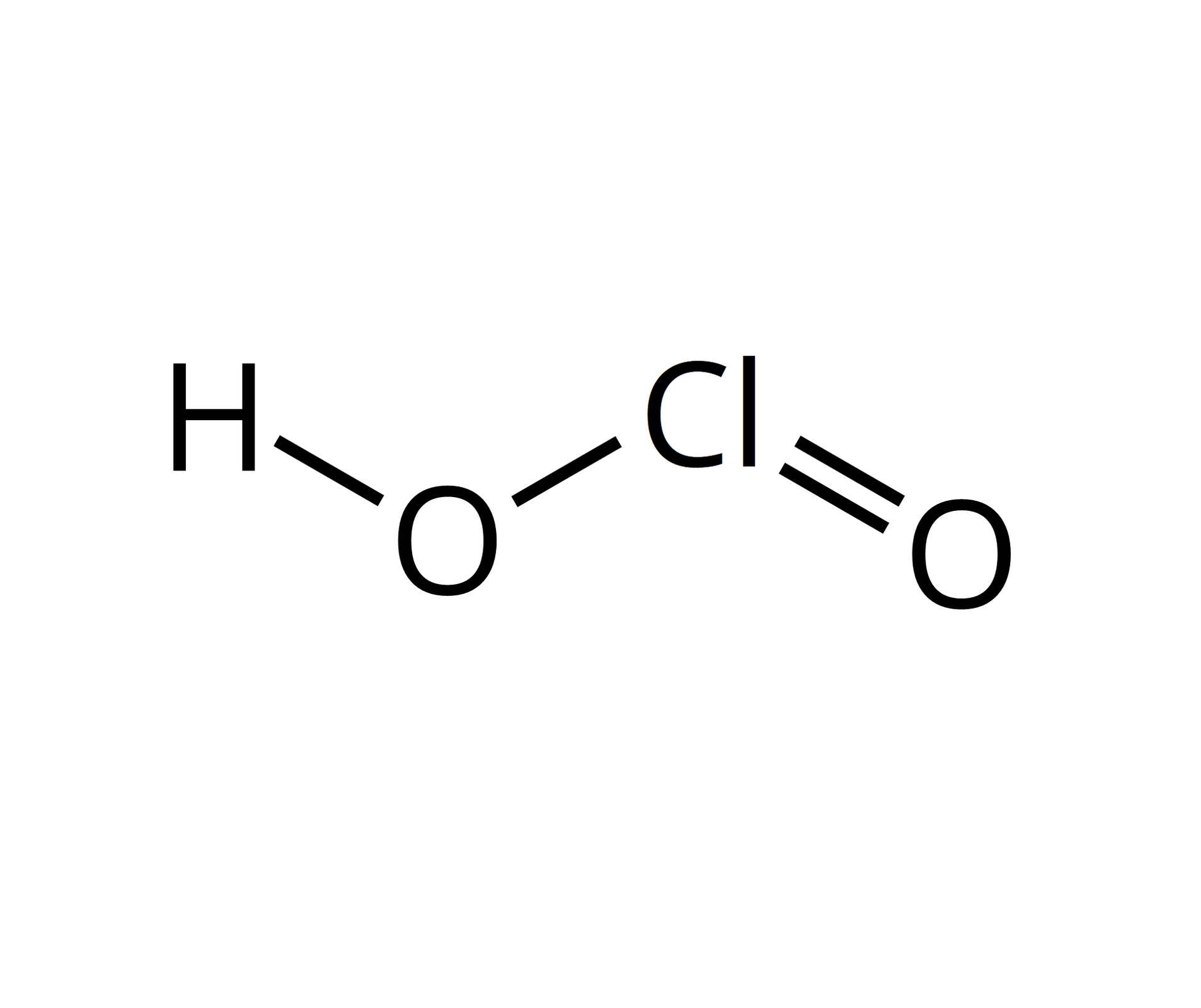 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas chlorowy | |||||
– | – | 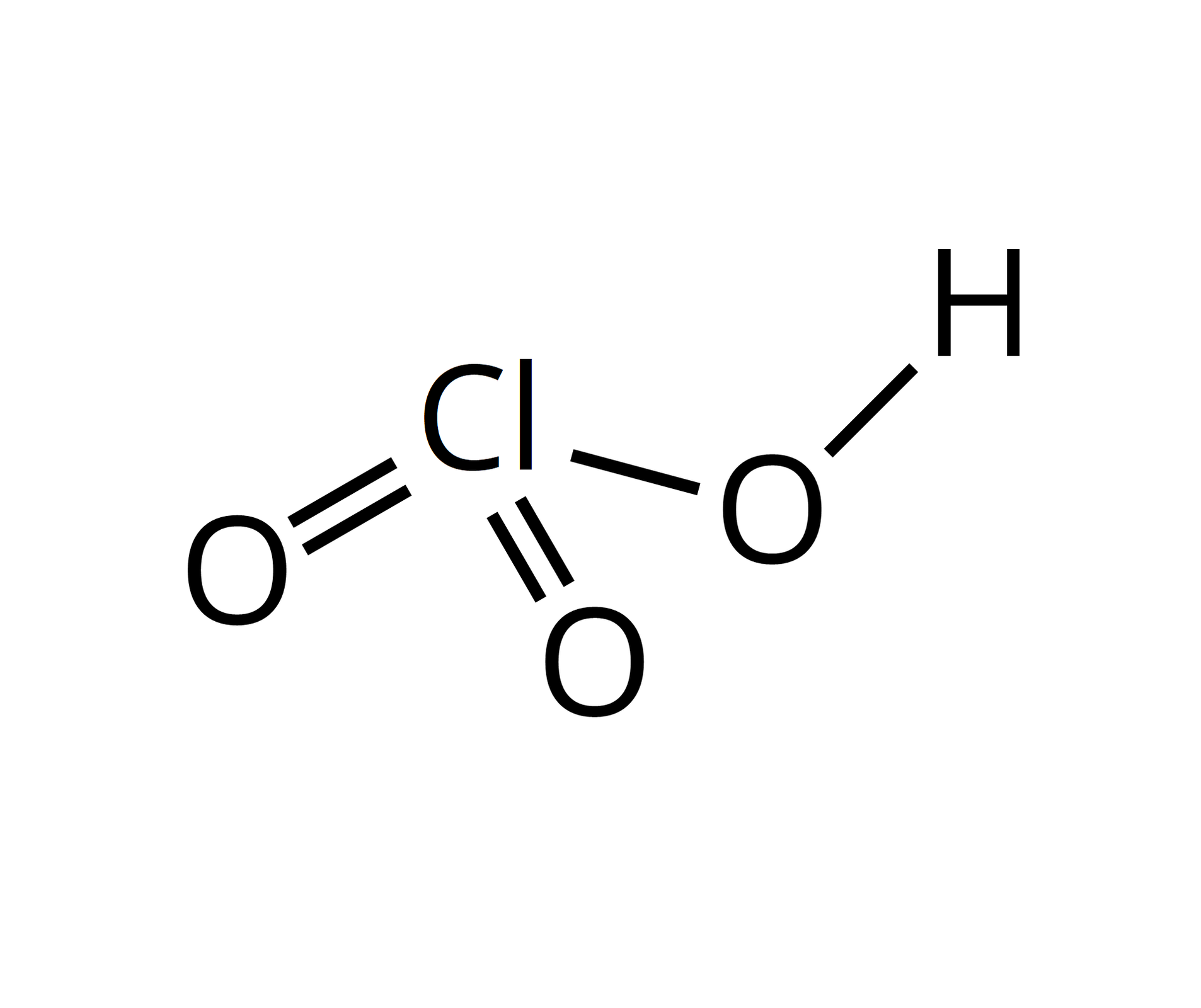 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas chlorowy | ||||
 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. |  Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. | kwas chlorowy |
Istnieją jeszcze dwa tlenki chloru: tlenek chloru(,) oraz tlenek
chloru(,) . Mówi się także o hipotetycznym istnieniu tlenku chloru o wzorze .
Najmocniejszym kwasem tlenowym chloru jest kwas chlorowy(). To wyjątkowo silny utleniacz. Jego sole – chlorany(), są substancjami o silnych właściwościach utleniających, a ich ucieranie w możdzierzu może wywołać reakcję wybuchową z tlenem.
Chlorany maja właściwości utleniające, np.:
To właśnie powstawanie aktywnego tlenu w reakcji rozkładu chloranu() decyduje o właściwościach wybielaczy zawierających chlor.
Czy wiesz, jakie właściwości fizykochemiczne posiada chlor? Zbadaj je przy pomocy poniższej symulacji, a następnie uzupełnij obserwacje oraz wnioski dla każdej z probówek.
Czy wiesz, jakie właściwości fizykochemiczne posiada chlor? Zapoznaj się z opisem symulacji interaktywnej, a następnie uzupełnij obserwacje oraz wnioski dla każdej z probówek.
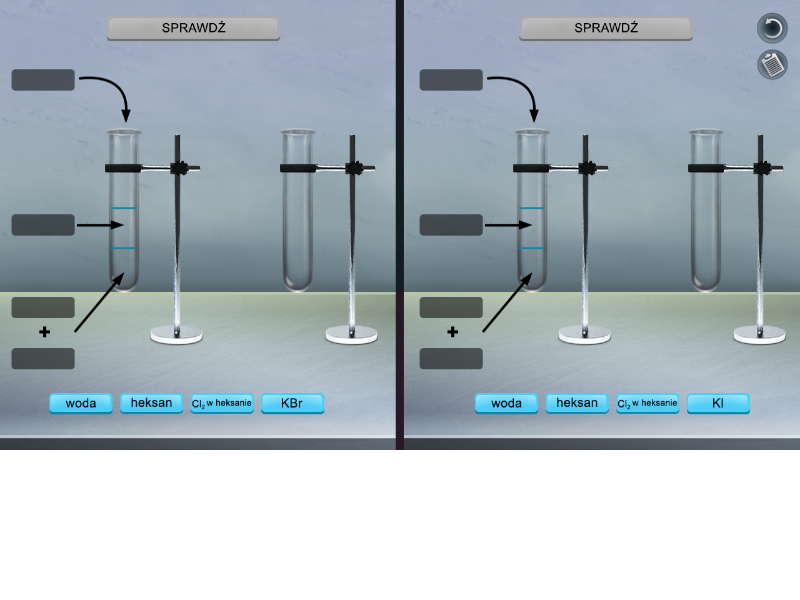
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D79TKA7QD
Wniosek: Zabarwienie heksanu pochodzi od 1. Potas, 2. chloru, 3. Chlor, 4. brom, 5. pomarańczowy, 6. chlor, 7. potasu, 8. bladozielony, 9. potas, 10. bromu, 11. ciemnofioletowy, 12. Brom. 1. Potas, 2. chloru, 3. Chlor, 4. brom, 5. pomarańczowy, 6. chlor, 7. potasu, 8. bladozielony, 9. potas, 10. bromu, 11. ciemnofioletowy, 12. Brom wypiera 1. Potas, 2. chloru, 3. Chlor, 4. brom, 5. pomarańczowy, 6. chlor, 7. potasu, 8. bladozielony, 9. potas, 10. bromu, 11. ciemnofioletowy, 12. Brom z roztworu soli.
Wniosek: Zabarwienie heksanu pochodzi od 1. Chlor, 2. chlor, 3. chloru, 4. jodu, 5. pomarańczowy, 6. jod, 7. Jod, 8. bladozielony, 9. fioletowy, 10. potas, 11. potasu, 12. Potas. 1. Chlor, 2. chlor, 3. chloru, 4. jodu, 5. pomarańczowy, 6. jod, 7. Jod, 8. bladozielony, 9. fioletowy, 10. potas, 11. potasu, 12. Potas wypiera 1. Chlor, 2. chlor, 3. chloru, 4. jodu, 5. pomarańczowy, 6. jod, 7. Jod, 8. bladozielony, 9. fioletowy, 10. potas, 11. potasu, 12. Potas z roztworu soli.
Czy wiesz, co dzieje się w kontakcie chloru z wodą na poziomie mikroświata? Zapoznaj się z poniższą symulacją interaktywną i odpowiedz na pytania.
Czy wiesz, co dzieje się w kontakcie chloru z wodą na poziomie mikroświata? Zapoznaj się z opisem symulacji interaktywnej i odpowiedz na pytania.
- W dwóch kolbach stożkowych umieszczono po sto pięćdziesiąt centymerów sześciennych wody destylowanej.
- Do pierwszej z nich wsypano pięć gramów K M n O indeks dolny, cztery, koniec indeksu dolnego.
- Kolby zatkano korkami, które połączono szklaną rurką. Wkraplacz umieszczono w korku kolby z roztworem K M n O indeks dolny, cztery, koniec indeksu dolnego, a następnie wlano do niego sześćdziesiąt centymetrów sześciennych H C l.
- Powoli wkraplano kwas do kolby i obserwowano zachodzące zmiany.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D79TKA7QD
Zapisz równanie reakcji chemicznej zachodzącej podczas kontaktu chloru z wodą (zastosuj zapis cząsteczkowy). Następnie zapisz równania dysocjacji elektrolitycznej powstałych produktów.
Odpowiedz, dlaczego wodę chlorową należy przechowywać w ciemnych naczyniach.



