Rozdzielanie mieszanin związków organicznych
Rozdzielanie mieszanin związków organicznych przy użyciu metod chromatograficznych
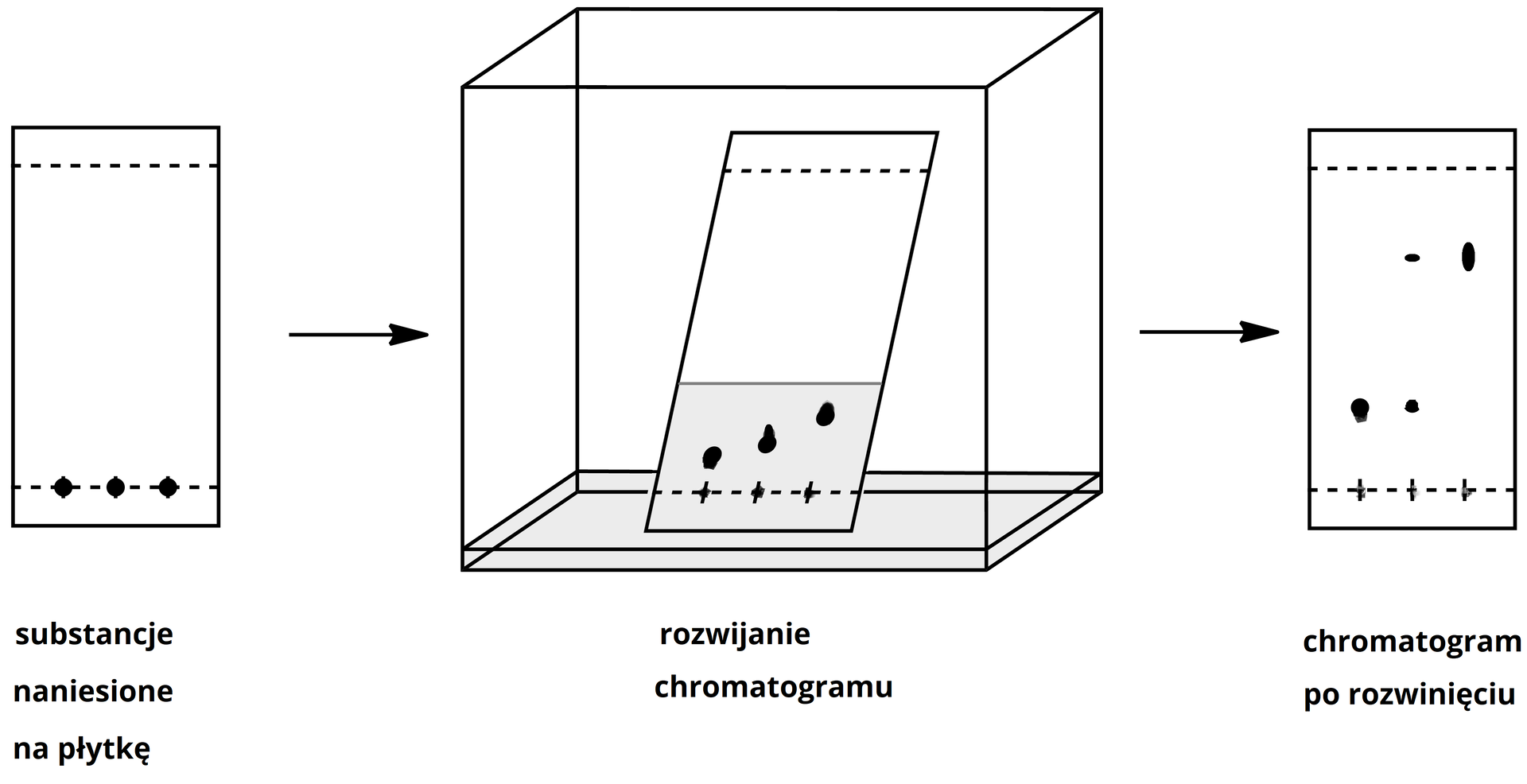
Techniki chromatograficzne (chromatografia gazowa, chromatografia cieczowa (kolumnowa, HPLC), chromatografia cienkowarstwowa TLC) pozwalają na sprawdzenie, czy dana substancja jest czysta, czy może jest mieszaniną kilku różnych związków. Ponadto, stosując specyficzne techniki rozdziału chromatograficznego, można dokonać rozdziału mieszaniny substancji, co w efekcie prowadzi do oczyszczenia analizowanego związku chemicznego. Techniki te bazują na prawie podziału Nerstaprawie podziału Nersta i adsorpcji substancji na nośniku.
Rozdzielane składniki mieszaniny charakteryzuje różnica w ich oddziaływaniu z dwiema fazami przemieszczającymi się względem siebie. Poszczególne składniki migrują z różną prędkością wraz z fazą ruchomą (gaz lub ciecz), która jest w kontakcie z fazą nieruchomą (ciało stałe lub ciecz na odpowiednim nośniku), i w ten sposób następuje ich rozdział.
W poniższym wirtualnym laboratorium możesz się zapoznać z często używanym szkłem laboratoryjnym. Masz możliwość sprawdzenia, jak wykorzystywana jest chłodnica Liebiga. Klikając na nią, przenosisz się do laboratorium, w którym poznasz jej zastosowanie. Podobnie klikając na syntezę preparatu możesz zobaczyć, jak wykorzystywane jest szkło laboratoryjne podczas reakcji otrzymywania benzenu.
Dodatkowo poznasz wyposażenie apteczki, która znajduje się w każdym laboratorium. Zobaczysz, co zalicza się do środków ochrony osobistej, a co do środków ochrony zbiorowej.
Zobaczysz również, jaki sprzęt laboratoryjny ułatwia pracę podczas wykonywania doświadczeń. Możesz sprawdzić, kiedy przydaje się przyrząd do pomiaru temperatury topnienia. Klikając właśnie w ten przyrząd, przeniesiesz się do laboratorium, gdzie zadaniem jest sprawdzenie, jaka substancja znajduje się w słoiczku podpisanym , a jaka w słoiczku podpisanym . Powodzenia.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D819H7HUX
Zapoznaj się z dwoma przeprowadzonymi doświadczeniami, a następnie wykonaj polecenie.
Doświadczenie
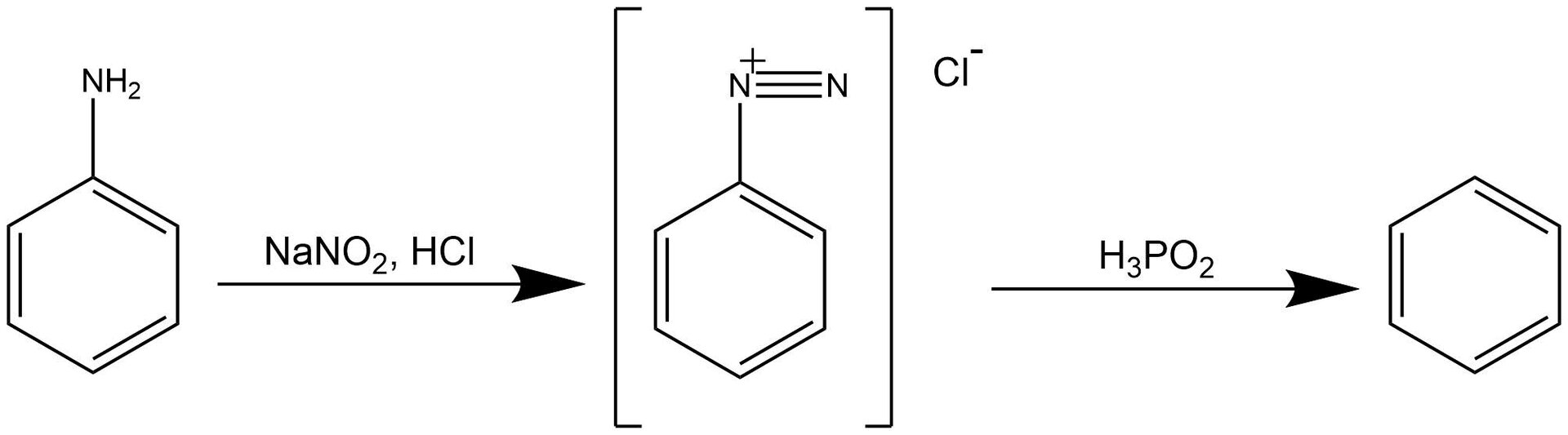
Analiza eksperymentu: Otrzymywanie benzenu.
Problem badawczy: Czy możliwe jest otrzymanie benzenu w reakcji z soli diazoniowej z trihydroksocynianem() sodu?
Hipoteza: Można otrzymać benzen w reakcji z soli diazoniowej z trihydroksocynianem() sodu.
Sprzęt laboratoryjny:
waga – urządzenie do odmierzania masy substancji chemicznych;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości. Służy do odmierzania cieczy;
pipety – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
kolba okrągłodenna – szklane naczynie laboratoryjne z zaokrąglonym dnem;
termometr ze szlifem – podłużny sprzęt laboratoryjny zawierający najczęściej skalę w stopniach Celsjusza oraz słup wypełniony rtęcią, który pod wpływem temperatury wskazuje pomiar;
płaszcz grzejny – urządzenie przeznaczone do prac laboratoryjnych i służy do podgrzewania różnego rodzaju cieczy;
chłodnica Liebiga – podłużne szkło laboratoryjne, wewnątrz którego znajduje się spiralna rurka, przez którą przepływa zimna woda schładzająca powstające podczas reakcji opary. Służy do skraplania gazów powstających podczas ogrzewania substancji;
kolba stożkowa – szklane naczynie laboratoryjne o kształcie stożka z płaskim dnem i wąską szeroką szyjką;
łaźnia lodowa – naczynie wypełnione lodem, służące do schładzania innych naczyń laboratoryjnych wraz z ich zawartością;
naczynko wagowe – sprzęt laboratoryjny służący do dokładnego odważania substancji stałych;
statyw – element sprzętu laboratoryjnego, rodzaj metalowego statywu służącego do montowania szklanej aparatury.
Odczynniki chemiczne:
anilina;
azotan() sodu;
kwas chlorowodorowy 35%;
wodorotlenek sodu;
chlorek cyny();
woda destylowana.
Przebieg eksperymentu:
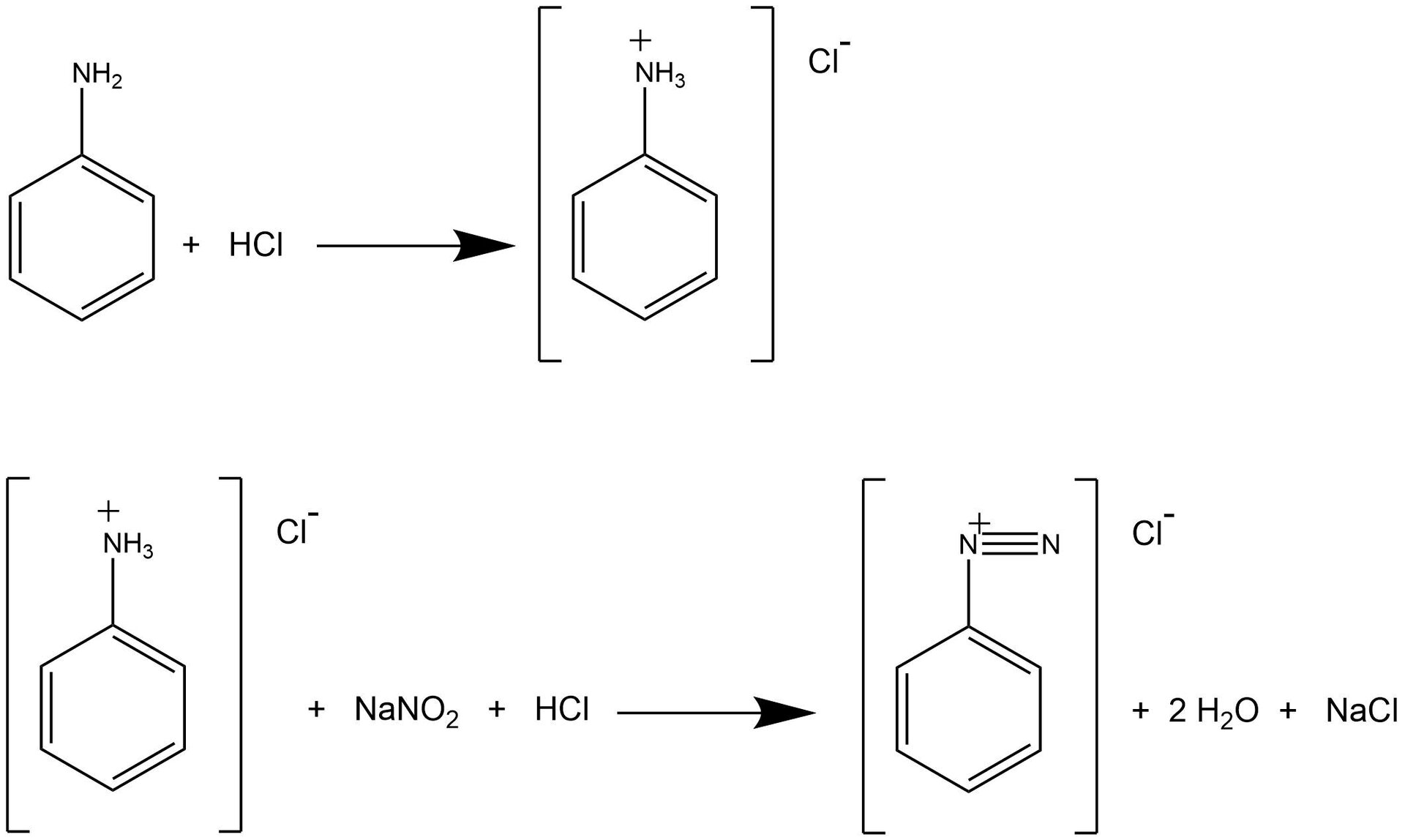
Dodano aniliny do kolby okrągłodennej, następnie stężonego kwasu chlorowodorowego.
Taką mieszaninę włożono do łaźni lodowej.
Kolejno dodano azotanu() sodu rozpuszczonego w wody.
chlorku cyny rozpuszczono w wody. Do sporządzonego roztworu dodano wodorotlenku sodu.
Do powstałego związku w kolbie okrągłodennej, dodawano małymi porcjami roztwór powstałego cynianu() sodu.
Po zakończeniu reakcji, przeprowadzono destylację prostą powstałego roztworu. Pierwszym zebranym produktem był spodziewany produkt.
Obserwacje:
Po dodaniu azotanu() sodu, mieszanina przybiera kolor pomarańczowy. Otrzymany produkt to bezbarwna ciecz.
Wyniki:
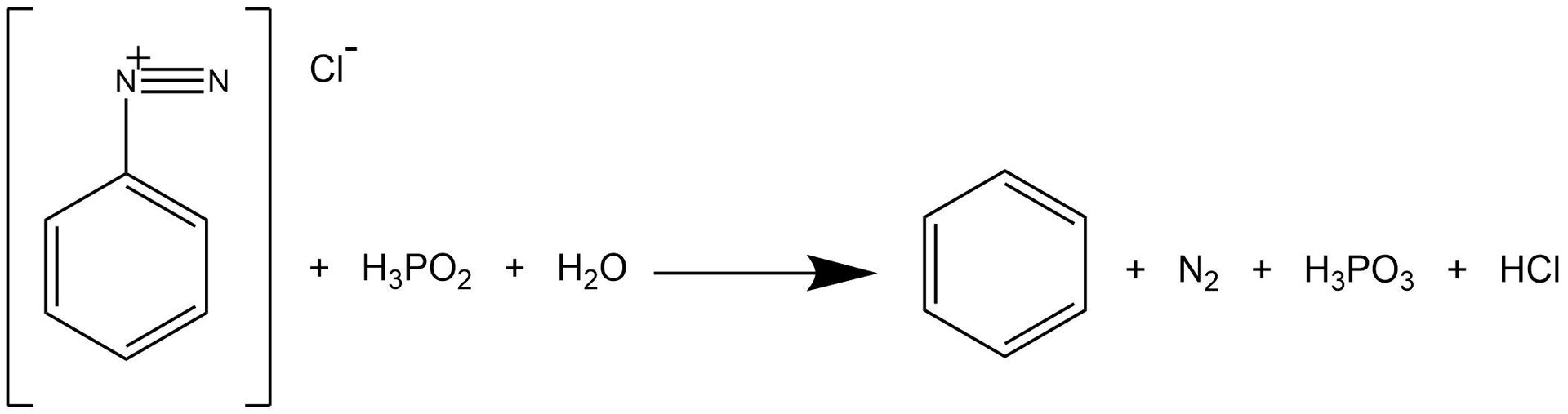
W wyniku reakcji otrzymano benzen.
Wnioski:
W wyniku reakcji aniliny z azotanem() sodu otrzymano jasnożółtą ciecz – jest to benzen. Hipoteza została potwierdzona.
Doświadczenie
Analiza eksperymentu: Wykorzystanie przyrządu do pomiaru temperatury topnienia.
Problem badawczy: Jak najłatwiej odróżnić dwie substancje: kwas benzoesowy od salicylowego?
Hipoteza: Badane kwasy posiadają różne temperatury topnienia.
Sprzęt laboratoryjny:
probówki w statywie – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych;
palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych;
krystalizator z wodą – płaskie naczynie laboratoryjne, które służy do procesu krystalizacji;
przyrząd do pomiaru temperatury topnienia
uniwersalne papierki wskaźnikowe – kawałek bibuły najczęściej w kształcie paska, nasączony roztworem substancji chemicznej będącej indykatorem i wysuszony;
drewniana łapa do probówek – rodzaj trzymaka, służący do uchwycenia probówki lub małej kolby stożkowej.
Odczynniki chemiczne:
eter dietylowy;
etanol;
woda destylowana.
Przebieg eksperymentu:
Zbadano rozpuszczalność substancji oraz w zimnej wodzie. Następnie sprawdzono rozpuszczalność tych substancji, ale po ogrzaniu. W tym celu probówki z badanymi substancjami (, ) oraz wodą ogrzano w łaźni wodnej.
Sprawdzono odczyn badanych roztworów za pomocą papierka uniwersalnego.
Zbadano rozpuszczalność substancji oraz w eterze dietylowym oraz w etanolu.
Sprawdzono temperaturę topnienia badanych substancji.
Obserwacje:
Badane substancje oraz to białe ciała stałe, nierozpuszczalne w zimnej wodzie, lecz po podgrzaniu. Uniwersalne papierki wskaźnikowe zmieniły barwę z żółtej na czerwoną w obu przypadkach. Substancje rozpuszczają się w eterze dietylowym oraz w etanolu; różnią się temperaturą topnienia.
Wyniki:
Czerwona barwa uniwersalnych papierków wskaźnikowych świadczy o kwasowym odczynie roztworów obu substancji. Związek posiada temperaturę topnienia , natomiast .
Wnioski:
Związek to kwas benzoesowy, a związek to kwas salicylowy. Hipoteza została potwierdzona.
Przeprowadź doświadczenie w laboratorium chemicznym. Metodą chromatografii kolumnowej rozdziel mieszaninę -nitrofenol i -nitrofenolu. Jako eluent zastosuj dichlorometan. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D819H7HUX
Zapoznaj się z opisem doświadczenia, w którym metodą chromatografii kolumnowej rozdzielono mieszaninę -nitrofenol i -nitrofenolu. Jako eluent zastosowano dichlorometan. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje wyniki, a następnie sformułuj wnioski.
Analiza doświadczenia:
Chromatografia kolumnowa.
Problem badawczy:
Czy za pomocą chromatografii kolumnowej można rozdzielić -nitrofenol oraz -nitrofenol?
Hipoteza:
Za pomocą chromatografii kolumnowej można rozdzielić -nitrofenol oraz -nitrofenol.
Sprzęt laboratoryjny:
statyw – pionowy pręt ze stabilną podstawą, umożliwiający mocowanie na wybranej wysokości, na przykład szkła laboratoryjnego umieszczonego w łapie;
łapa – rodzaj narzędzia, wykorzystywanego w laboratorium do trzymania, na przykład kolb;
szklana kolumna chromatograficzna – szklana rurka zakończona u dołu kranikiem;
kolby stożkowe – szklane naczynia laboratoryjne o kształcie stożka z płaskim dnem i wąską szyjką;
lejek – szkło w kształcie odwróconego stożka, ze zwężającą się rurką, służący do przelewania cieczy lub sączenia;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca, z umieszczoną na ściance podziałką objętości, służące do odmierzania cieczy;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu, zakończony z jednej strony łyżeczką;
bagietka szklana – szklany pręt laboratoryjny służący do mieszania;
pipeta – wąska rurka służąca do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
mieszanina -nitrofenolu i -nitrofenolu, dichlorometan, silikażel
Przebieg doświadczenia:
Do zlewki dodano pięć łyżek silikażelu, a następnie około mililitrów dichlorometanu. Zawartość dokładnie wymieszano przy pomocy szklanej bagietki.
Przygotowany silikażel wraz z dichlorometanem przeniesiono do kolumny z wykorzystaniem lejka.
Łyżeczkę mieszaniny nitrofenoli rozpuszczono w jak najmniejszej ilości dichlorometanu i naniesiono na kolumnę przy pomocy pipety, lejąc bardzo powoli po ściankach kolumny.
Kolejno dokonano rozdziału mieszaniny, używając jako eluentu dichlorometanu, który w miarę przepływu fazy ruchomej uzupełniano tak, by jego poziom zawsze znajdował się ponad fazą stacjonarną.
Z zebranych frakcji odparowano rozpuszczalnik przy pomocy wyparki laboratoryjnej.
Obserwacje:
Po wprowadzeniu mieszaniny dwóch związków na kolumnę chromatograficzną, barwna smuga przesuwa się po silikażelu, a następnie rozdziela się w miarę postępującej elucji.
Wyniki: W wyniku przeprowadzenia chromatografii kolumnowej, mieszaniny -nitrofenolu oraz -nitrofenolu, otrzymano dwa czyste związki: -nitrofenol oraz -nitrofenol.
Wnioski: Chromatografia kolumnowa pozwala na rozdział badanej mieszaniny dwóch związków.
Hipoteza została potwierdzona.