Wodorotlenki – otrzymywanie
W wyniku jakich reakcji powstają wodorotlenki?
Istnieje kilka metod na otrzymanie wodorotlenków, które różnią się w zależności od zdolności wodorotlenków do rozpuszczania w wodzie oraz od położenia metalu w układzie okresowym. Wodorotlenki rozpuszczalne w wodzie to wodorotlenki metali i (z wyjątkiem berylu) grupy układu okresowego pierwiastków, które można otrzymać m.in. czterema poniższymi metodami:
Reakcja aktywnego metalu z wodą
Wykorzystując poniższą symulację, sprawdź, w jaki sposób użyte w niej metale zachowują się wobec wody. Następnie zapisz obserwacje. Ponadto, korzystając z dostępnych źródeł informacji przeanalizuj właściwości fizyczne użytych metali i wskaż jaki błąd popełniono w poniższej symulacji.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D919HXUPR
Wykonano doświadczenie, w którym sprawdzono, w jaki sposób reagują z wodą magnez i miedź. W tym celu próbki metali wrzucono do probówek z wodą destylowaną z dodatkiem alkoholowego roztworu fenoloftaleiny. Potem je ogrzano, a do ich wylotu zbliżono zapaloną zapałkę. Zaznacz zdanie, które poprawnie opisuje obserwacje, poczynione podczas doświadczenia.
Tą metodą można otrzymać wodorotleneki litowców i berylowców (za wyjątkiem wodorotlenku berylu). Przykładowo, reakcję sodu z wodą, w wyniku której powstaje wodorotlenek sodu, można opisać równaniem:
Litowce reagują gwałtowniej z wodą niż berylowce. W obrębie tych grup aktywność metali rośnie w dół. Magnez reaguje z wodą w widoczny sposób dopiero w podwyższonej temperaturze, zgodnie z równaniem:
Reakcja tlenku metalu z wodą
Wykorzystując poniższą symulację, sprawdź, w jaki sposób użyte w niej tlenki metali zachowują się wobec wody. Następnie zapisz obserwacje.
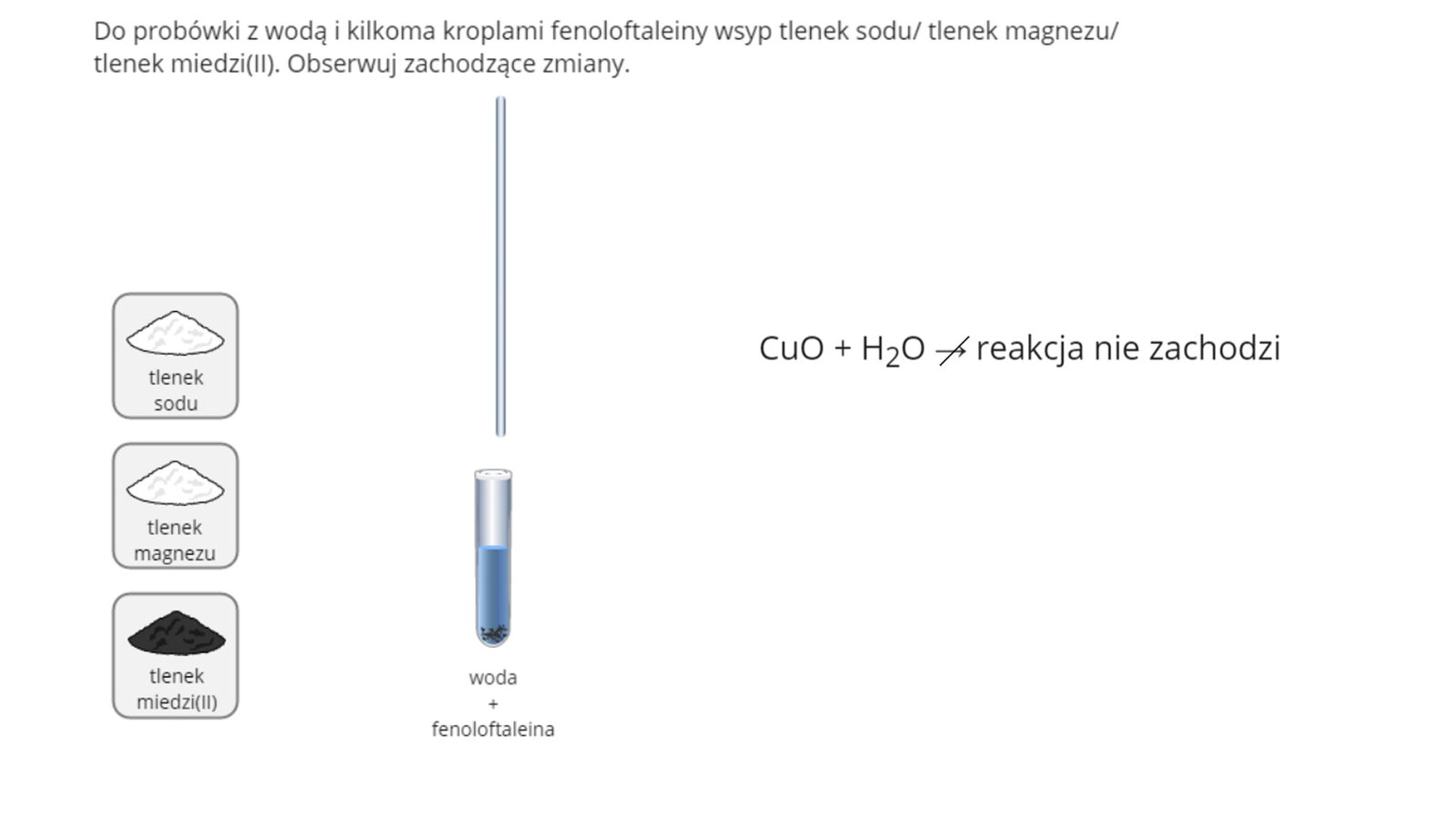
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D919HXUPR
Wykonano doświadczenie, w którym sprawdzono reaktywność wybranych tlenków metali z wodą. W tym celu do trzech probówek, zawierających wodę destylowaną z dodatkiem alkoholowego roztworu fenoloftaleiny, dodano kolejno tlenek sodu, tlenek magnezu i tlenek miedzi(). Zawartość każdej probówki dokładnie wymieszano za pomocą szklanej bagietki. Zaznacz zdanie, które poprawnie opisuje obserwacje poczynione podczas doświadczenia.
Ta metoda sprwadzi się do otrzymywania wodorotlenków litowców oraz wodorotlenku wapnia, strontu i baru. W wyniku reakcji tlenku z wodą powstaje odpowiedni wodorotlenek. Przykładowo, reakcje tlenku sodu i tlenku wapnia z wodą obrazują poniższe równania reakcji:
Reakcja wodorków typu soli ( i grupy układu okresowego pierwiastków) z wodą
Otrzymywanie wodorotlenków z wodorków to jedna z metod syntezy tych związków. Proces ten opiera się na reakcji wodorków metali (np. wodorku sodu, wodorku wapnia) z wodą. W reakcji tej wodorek reaguje z cząsteczkami wody, co prowadzi do powstania odpowiedniego wodorotlenku oraz wydzielenia wodoru w postaci gazowej.
Reakcja nadtlenków z wodą
Wodorotlenki można otrzymać z nadtlenków metali pierwszej i drugiej grupy układu okresowego poprzez ich reakcję z wodą (za wyjątkiem magnezu i berylu). Proces ten polega na rozkładzie nadtlenków i powstawaniu odpowiednich wodorotlenków oraz nadtlenku wodoru.
Wytrącanie wodorotlenków z roztworów soli
Trudnorozpuszczalne w wodzie wodorotlenki można otrzymać poprzez reakcję rozpuszczalnej w wodzie soli danego metalu z wodnym roztworem wodorotlenku, który jest mocnym elektrolitem, np. lub .
Otrzymywanie większości wodorotlenków metali grup od trzeciej do oraz wodorotlenku magnezu i berylu polega na zastosowaniu tzw. metody strąceniowej. Chcąc otrzymać dany wodorotlenek metalu, należy do wodnego roztworu dobrze rozpuszczalnej soli, zawierającej kationy metalu, dodać wodnego roztworu wodorotlenku sodu, potasu, wapnia, litu bądź baru. Wówczas zaobserwujemy wytrącanie osadu trudno rozpuszczalnego w wodzie wodorotlenku. Metodę tę możemy opisać schematem:
Przykładowo wodorotlenek żelaza(III) można wytrącić w postaci brunatnego osadu z roztworu chlorku żelaza(III) za pomocą wodorotlenku sodu, co obrazuje poniższe równanie:
Eksperymentuj1
Przeprowadź eksperyment w laboratorium chemicznym. Sformułuj i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D919HXUPR
Zapoznaj się z opisem przeprowadzonego doświadczenia i wykonaj ćwiczenie.
Analiza eksperymentu: Otrzymywanie wodorotlenków różnymi metodami.
Problem badawczy: Czy wszystkie wodorotlenki można otrzymać w wyniku reakcji metali i tlenków metali z wodą?
Hipoteza: Wszystkie wodorotlenki można otrzymać w wyniku reakcji metali i tlenków metali z wodą.
Sprzęt laboratoryjny:
cztery probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
łyżeczki – długie trzonki wykonane ze szkła, porcelany lub metalu, zakończone z jednej strony łyżeczką. Służą do nabierania sypkich substancji chemicznych;
pipety jednorazowe – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
tlenek wapnia;
tlenek cynku;
lit;
żelazo;
fenoloftaleina;
woda destylowana.
Przebieg eksperymentu:
Do wszystkich probówek wprowadzono wodę destylowaną, a następnie kilka kropel fenoloftaleiny.
Następnie za pomocą łyżeczek umieszczono osobno w każdej probówce kolejno tlenek wapnia, tlenek cynku i żelazo, a za pomocą pęsety laboratoryjnej lit.
Obserwacje:
Probówka : Tlenek wapnia rozpuszcza się, roztwór zmienia zabarwienie na kolor malinowy.
Probówka : Tlenek cynku opada na dno probówki, brak widocznych zmian.
Probówka : Żelazo opada na dno probówki, brak widocznych zmian.
Probówka : Lit pływa po powierzchni i rozpuszcza się, roztwór zmienia zabarwienie na kolor malinowy. Wydziela się bezbarwny gaz.
Wyniki:
W probówkach, w których roztwór zmienił zabarwienie na kolor malinowy, obecne są jony , co świadczy o powstaniu wodorotlenków. Wydzielającym się gazem w probówce zawierającej lit jest wodór.
Wnioski:
Nie wszystkie wodorotlenki można otrzymać w wyniku reakcji metali i tlenków metali z wodą, ponieważ niektóre metale lub tlenki metali są nierozpuszczalne w wodzie.
Hipoteza została odrzucona.
Zagraj w grę, w której zadaniem jest pomóc Czarodziejowi przygotować mikstury złożone z dwóch reagentów. Zbieraj monety u Mistrza Czarodzieja i zdobądź ich przynajmniej , aby wygrać grę.
Uwaga!
W przypadku, gdy współczynnik stechiometryczny wynosi , należy wybrać z listy cyfrę .
W etapach od do przynajmniej jeden związek chemiczny w przedstawionym równaniu reakcji musi być wodorotlenkiem.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D919HXUPR
Wykonaj poniższe ćwiczenia dotyczące reakcji, w których wodorotlenki pełnią rolę substratów lub są produktami reakcji.
Zapisz cząsteczkowe równania reakcji przedstawiające dwie metody otrzymywania wodorotlenku magnezu.
W ramach podsumowania1
Dodając sód do wody, można otrzymać wodorotlenek sodu. Czy dodając srebro do wody, można otrzymać wodorotlenek srebra? Zapoznaj się z samouczkiem, a następnie rozwiąż ćwiczenia pod filmem.

Film dostępny pod adresem /preview/resource/RuU9Ovq67j8Gp
Film nawiązujący do zagadnienia otrzymywania wodorotlenków.
Otrzymywanie wodorotlenków