Badanie wpływu różnych czynników (stężenia ciśnienia) substratów, temperatury, obecności katalizatora i stopnia rozdrobnienia substratów) na szybkość reakcji
Czym jest szybkość reakcji chemicznej?
Szybkość reakcji chemicznejSzybkość reakcji chemicznej definiowana jest przez zmianę stężeniastężenia substratów lub zmianę stężenia produktów w jednostce czasu.
Ilość substratu podczas reakcji maleje w jednostce czasu, dlatego przed zmianą stężenia substratu jest znak minus.
Szybkość reakcji chemicznych zależy od:
- Nazwa kategorii: Szybkość reakcji chemicznych zależy od:
- Nazwa kategorii: Rodzaju oraz chemicznego charakteru reagujących substancji
- Nazwa kategorii: Stężenia substratów
- Nazwa kategorii: Ciśnienia (w przypadku substancji gazowych)
- Nazwa kategorii: Temperatury
- Nazwa kategorii: Obecności katalizatora Koniec elementów należących do kategorii Szybkość reakcji chemicznych zależy od:
- Elementy należące do kategorii Szybkość reakcji chemicznych zależy od:
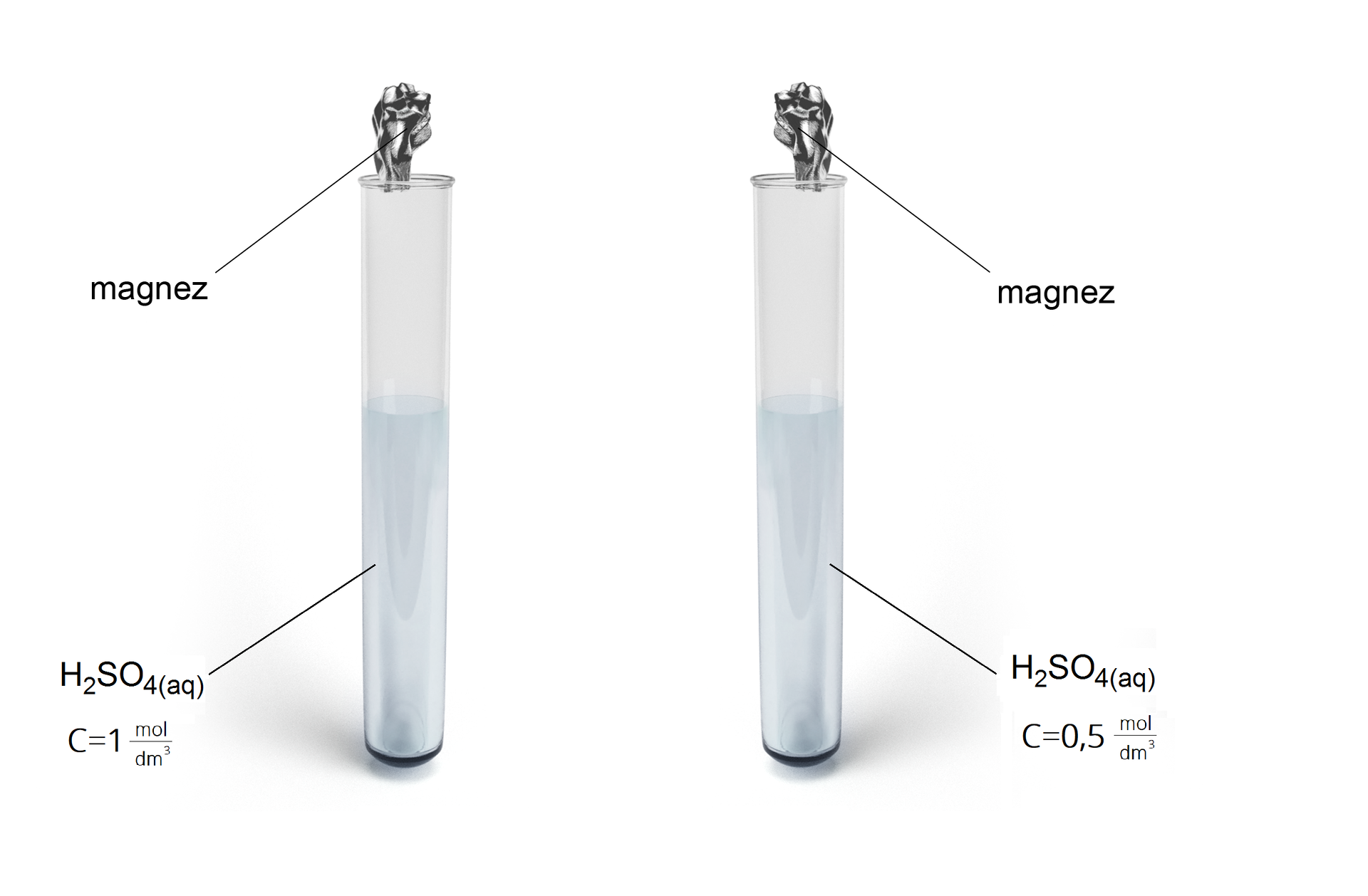
Badanie zależności szybkości reakcji metalu z kwasem siarkowym() od stężenia użytego kwasu.
Schemat doświadczenia:
Badanie wpływu temperatury na szybkość reakcji.
Schemat doświadczenia:

Sprawdź się! Zaprojektuj doświadczenie
Zaproponuj doświadczenie, w którym zbadasz wpływ stopnia rozdrobnienia substratu na szybkość zachodzącej reakcji na podstawie reakcji kwasu solnego z metalicznym magnezem. Uzupełnij w formularzu niezbędny sprzęt i odczynniki, instrukcję wykonania doświadczenia, obserwacje oraz wnioski.
Doświadczenie
Badanie wpływu stopnia rozdrobnienia substratu na szybkość reakcji.
Schemat doświadczenia:

Zaproponuj doświadczenie, w którym zbadasz wpływ dodatku katalizatorakatalizatora na szybkość zachodzącej reakcji na podstawie reakcji kwasu solnego z cynkiem, używając roztworu siarczanu() miedzi() jako katalizatora. Uzupełnij w formularzu niezbędny sprzęt i odczynniki, instrukcję wykonania doświadczenia, obserwacje oraz wnioski.
Doświadczenie 4
Badanie wpływu obecności katalizatora na szybkość reakcji
Schemat doświadczenia:

Przeprowadź eksperyment w laboratorium chemicznym. Sformułuj i zweryfikuj własną hipotezę. W formularzu zanotuj obserwacje i wyniki, a następnie zapisz wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D9BLNGCNL
Zadanie: Badanie wpływu różnych czynników (stężenia (ciśnienia) substratów, temperatury, obecności katalizatora i stopnia rozdrobnienia substratów) na szybkość reakcji.
Analiza eksperymentu: Badanie wpływu różnych czynników na szybkość reakcji.
Problem badawczy: Czy podwyższenie temperatury oraz obecność innych substancji wpływa na rozkład nadtlenku wodoru?
Hipoteza: Obecność niektórych substancji oraz podwyższenie temperatury zwiększa szybkość reakcji rozkładu nadtlenku wodoru.
Sprzęt laboratoryjny: palnik – rodzaj sprzętu z regulacją płomienia, umożliwiający podgrzewanie substancji chemicznych; probówki w statywie – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych; pipety – wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki; łyżeczki – długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych; łuczywko – kawałek drewna przesyconego żywicą, służy do utrzymania płomienia; drewniana łapa – rodzaj trzymaka służący do uchwycenia probówki lub małej kolby stożkowej.
Odczynniki chemiczne: nadtlenek wodoru ; tlenek manganu(); jodek potasu; kwas ortofosforowy().
Przebieg eksperymentu: Do probówek dodano taką samą ilość (około centymetrów sześciennych) wody utlenionej (nadtlenku wodoru ). Pierwszą probówkę ogrzewano w łaźni wodnej, po chwili do wylotu probówki zbliżono palące się łuczywko. Do drugiej probówki dodano odrobinę tlenku manganu(), po chwili do wylotu probówki zbliżono palące się łuczywko. Do trzeciej probówki dodano odrobinę jodku potasu, po chwili do wylotu probówki zbliżono palące się łuczywko. Do probówki czwartej dodano kwas ortofosforowy(), po chwili do wylotu probówki zbliżono palące się łuczywko.
Obserwacje: Podczas ogrzewania roztwór w probówce zaczyna się pienić, wydzielana jest para, zbliżone łuczywko pali się intensywniej. W probówkach z tlenkiem manganu() oraz jodkiem potasu również roztwór się pieni, wydzielana jest para, zbliżone łuczywko pali się intensywniej. Brak objawów reakcji po dodaniu kwasu ortofosforowego().
Wyniki: Podczas przeprowadzanych reakcji następował rozkład nadtlenku wodoru, w wyniku reakcji powstawał gaz, który powodował intensywniejsze palenie się łuczywka (po zbliżeniu do wylotu probówki). Gazem tym jest tlen. Brak reakcji w probówce, do której dodano kwas ortofosforowy().
Wnioski: Hipoteza została potwierdzona. Podwyższenie temperatury oraz obecność katalizatora (tlenek manganu(), jodek potasu) zwiększa szybkość reakcji nadtlenku wodoru. Kwas ortofosforowy() jest inhibitorem tej reakcji.