Jakie właściwości mają tlenki?
Właściwości tlenków w głównej mierze zależą od położenia pierwiastka tworzącego dany tlenek w układzie okresowym. Ogólnie można wywnioskować, że tlenki niemetali są w dużej mierze tlenkami wykazującymi charakter kwasowy, natomiast tlenki metali wykazują zazwyczaj charakter zasadowy. Mimo to tej tendencji nie powinno się traktować w sposób bezwzględny.
Badanie charakteru chemicznego wybranych tlenków1
Czy wiesz, w jaki sposób zbadać charakter chemiczny następujących tlenków: , , ? Zapoznaj się z poniższym laboratorium i zbadaj charakter chemiczny tych związków chemicznych. Następnie uzupełnij dzienniczek, wpisując do niego sprzęt laboratoryjny oraz odczynniki chemiczne, z których korzystałeś, a także instrukcję wykonywanego eksperymentu. Na koniec rozwiąż ćwiczenia sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBJHP2UJG
Analiza doświadczenia: Badanie charakteru chemicznego tlenków.
Problem badawczy: Jaki charakter chemiczny posiadają tlenki: magnezu, glinu oraz fosforu()?
Hipoteza: Tlenek magnezu ma charakter zasadowy, tlenek glinu ma charakter amfoteryczny, a tlenek fosforu() ma charakter kwasowy.
Odczynniki: wodny roztwór wodorotlenku sodu o stężeniu ; kwas chlorowodorowy o stężeniu ; , , ; roztwór oranżu metylowego; alkoholowy roztwór fenoloftaleiny.
Sprzęt laboratoryjny: probówek – podłużnych naczyń szklanych do przeprowadzania prostych reakcji chemicznych; łyżki laboratoryjne – długie trzonki wykonane ze szkła, porcelany lub metalu zakończone z jednej strony łyżeczką. Służą do nabierania sypkich substancji chemicznych; statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki; szklanych bagietek – sprzętów laboratoryjnych, o kształcie prostego pręta szklanego, czasami zakończonego z jednej strony małą rączką, a z drugiej małą łopatką; pipety Pasteura – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Instrukcja wykonania doświadczenia:
1. Do trzech probówek wlano po kwasu chlorowodorowego, a następnie dodano kilka kropli roztworu oranżu metylowego
2. Do każdej z trzech probówek dodano kolejno niewielką ilość (pół łyżeczki) tlenków: , ,.
3. Zawartość probówek zamieszano.
4. Do kolejnych trzech probówek wlano po wodnego roztworu wodorotlenku sodu, a następnie dodano kilka kropli alkoholowego roztworu fenoloftaleiny.
5. Do każdej z trzech probówek dodano kolejno niewielką ilość (pół łyżeczki) tlenków: , , .
6. Zawartość probówek zamieszano.
Obserwacje:
Po dodaniu roztworu oranżu metylowego do probówek z kwasem chlorowodorowym roztwory w probówkach zabarwiły się na czerwono, a po dodaniu alkoholowego roztworu fenoloftaleiny do probówek z wodnym roztworem wodorotlenku sodu roztwory w probówkach zabarwiły się na malinowo.
Po wprowadzeniu tlenku magnezu oraz tlenku glinu do probówek z kwasem chlorowodorowym i oranżem metylowym zaobserwowano roztworzenie się obydwu tlenków oraz zmianę zabarwienia roztworów z czerwonego na żółtopomarańczowe. Po wprowadzeniu tlenku fosforu() do probówki z kwasem chlorowodorowym i oranżem metylowym zaobserwowano roztworzenie się tlenku (roztwór pozostał jednak czerwony).
Po wprowadzeniu tlenku glinu oraz tlenku fosforu() do probówek z wodnymi roztworami wodorotlenku sodu i fenoloftaleiną zaobserwowano roztworzenie się obydwu tlenków oraz odbarwienie się malinowych roztworów. Po wprowadzeniu tlenku magnezu do probówki z wodnym roztworem wodorotlenku sodu i fenoloftaleiną zaobserwowano roztwarzanie się tlenki i wytrącanie się białego osadu (uzyskano zmętniony malinowy roztwór).
Wyniki:
Tlenek magnezu zareagował z kwasem chlorowodorowym, czego skutkiem był wzrost pH roztworu, nie zareagował on z kolei z wodnym roztworem wodorotlenku.
W przypadku tlenku glinu doszło do reakcji zarówno z kwasem chlorowodorowym, jak i wodnym roztworem wodorotlenku sodu – w obydwóch przypadkach doszło do zmiany pH.
Tlenek fosforu() zareagował z wodnym roztworem wodorotlenku, czego wynikiem był spadek pH roztworu, nie uległ on jednak reakcji z kwasem chlorowodorowym.
Wnioski:
Tlenek magnezu nie uległ reakcji z wodnym roztworem wodorotlenku, nie doszło do zmiany pH, a roztworzenie tlenku wynika z jego reakcji z wodą. Uległ on z kolei reakcji z kwasem, w wyniku czego nastąpił wzrost pH – była to zatem reakcja neutralizacji. Tlenek magnezu jest więc tlenkiem zasadowym.
Tlenek glinu uległ reakcji w obydwóch przypadkach i w obydwóch przypadkach doszło do zmiany pH – w reakcji z kwasem nastąpił wzrost, a w reakcji z wodnym roztworem wodorotlenku nastąpił spadek pH. Jest on zatem tlenkiem amfoterycznym.
Tlenek fosforu() uległ reakcji z wodnym roztworem wodorotlenku, czego skutkiem był spadek pH i nie zareagował on z kwasem (roztworzenie tlenku w tym przypadku było skutkiem jego reakcji z wodą). Jest to więc tlenek kwasowy.
Hipoteza została potwierdzona.
Równania reakcji chemicznych:
1.
2.
3.
4.
5.
6.
7.
8.
Hipoteza została potwierdzona.
Tlenki kwasowe
Doświadczenie: Badanie charakteru chemicznego tlenku siarki().
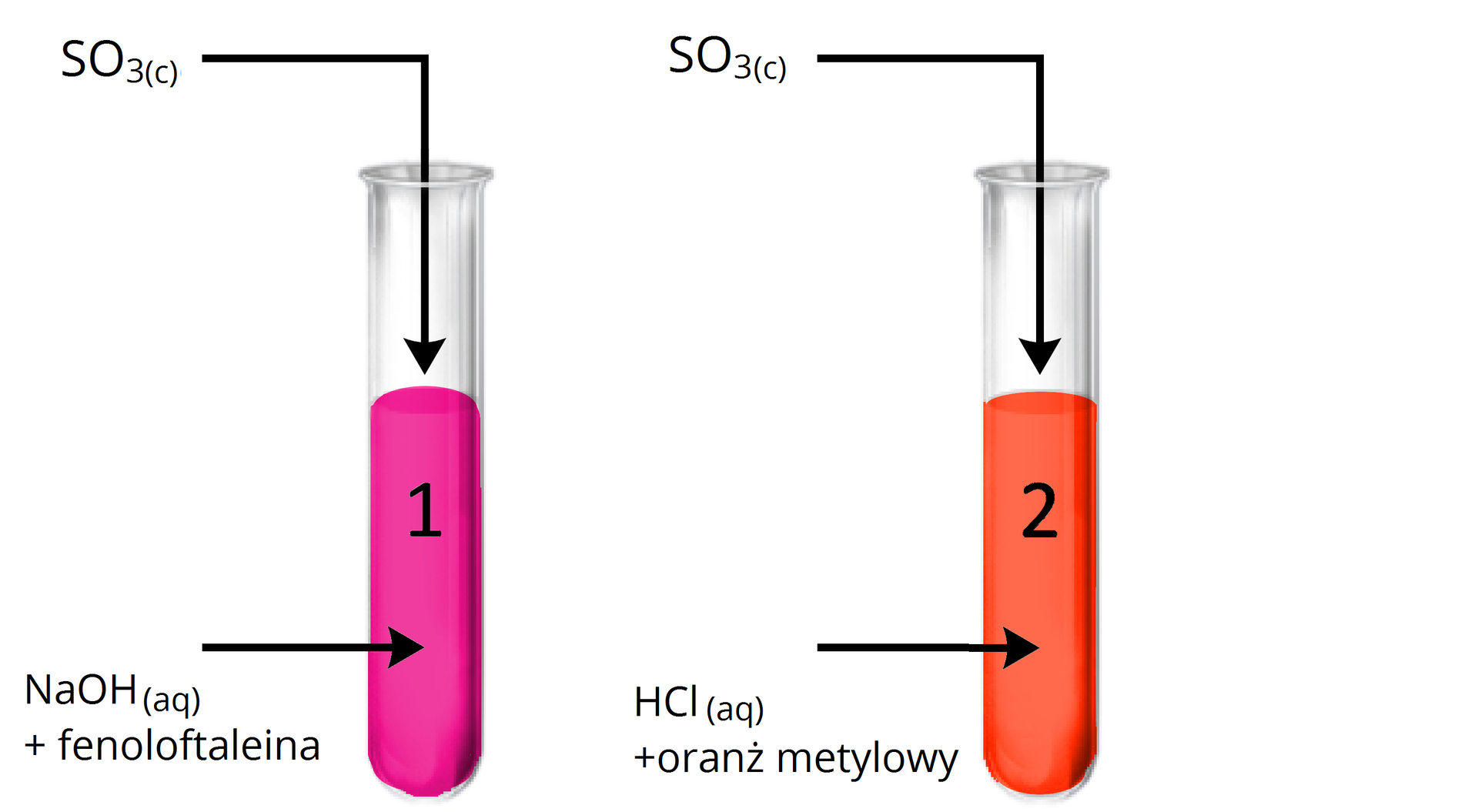
Obserwacje:
Probówka : Malinowy roztwór uległ odbarwieniu.
Probówka : Brak widocznych objawów reakcji.
Wniosek:
Tlenek siarki() jest tlenkiem kwasowym, ponieważ reaguje z zasadą (wodnym roztworem wodorotlenku), a nie reaguje z kwasem.
Równanie reakcji chemicznej z zasadą:
W formie cząsteczkowej:
W formie jonowej – skróconej:
Równanie reakcji chemicznej z kwasem:
Tlenki kwasowe są to tlenki niemetali oraz tlenki niektórych metali, które reagują z wodnymi roztworami wodorotlenków, a nie reagują z kwasami.
Tlenki kwasowe pierwiastków | ||
bloku | bloku | bloku |
brak | - | - |
W reakcjach tlenków kwasowych z roztworami wodorotlenków powstaje sól i woda. Reakcję tą można zapisać w sposób ogólny jako:
Tlenki zasadowe
Doświadczenie: Badanie charakteru chemicznego tlenku baru.
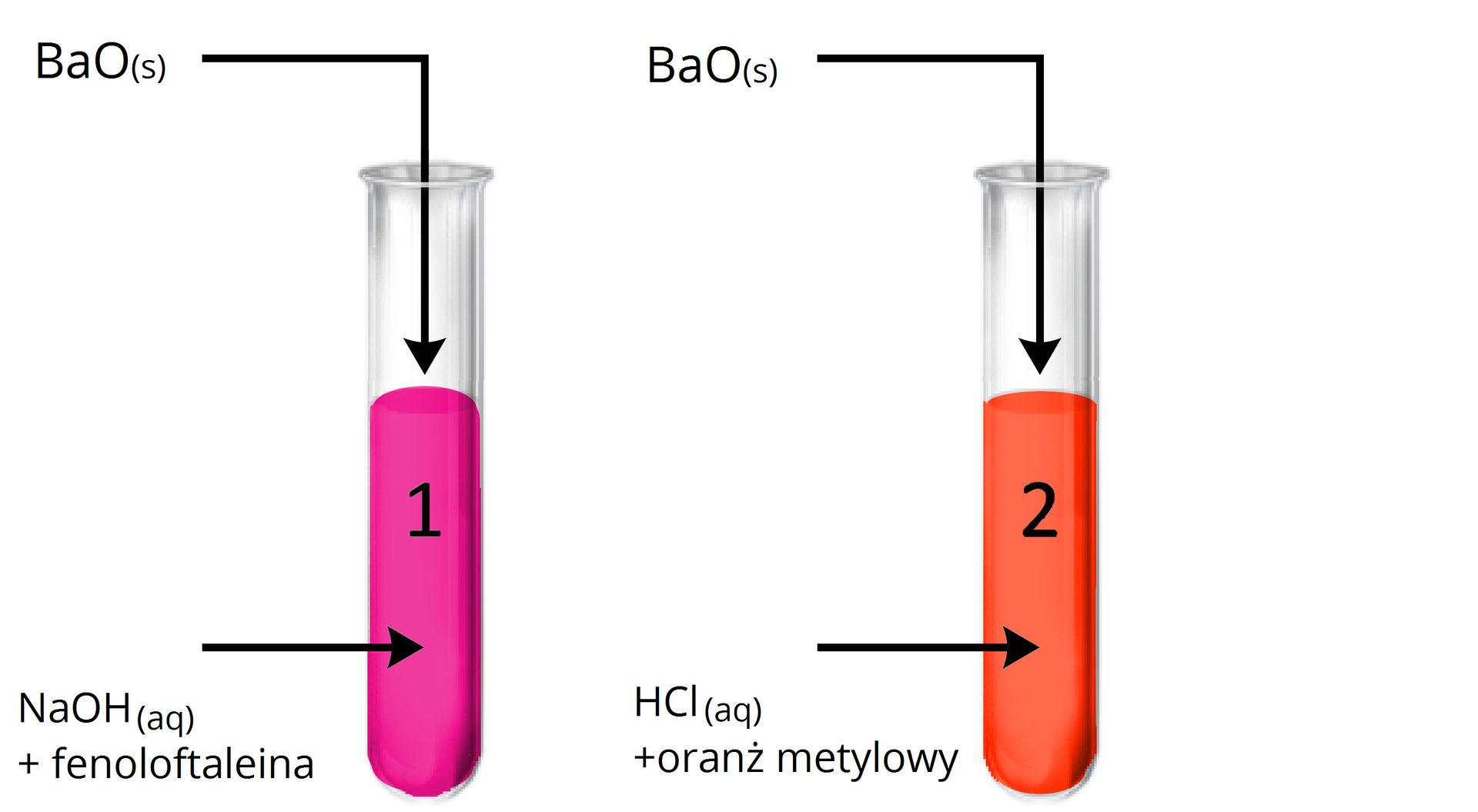
Obserwacje:
Probówka : Brak widocznych oznak reakcji z wodnym roztworem wodorotlenku sodu (Tlenek ulega rozpuszczeniu, ale roztwór nie zmienia zabarwienia).
Probówka : Ciało stałe uległo roztworzeniu. Roztwór zmienił barwę z czerwonej na żółtopomarańczową.
Wniosek:
Tlenek baru jest tlenkiem zasadowym, ponieważ reaguje z kwasem, a nie reaguje z zasadą (wodnym roztworem wodorotlenku).
Równanie reakcji chemicznej z kwasem:
W formie cząsteczkowej:
W formie jonowej – skróconej:
Równanie reakcji chemicznej z wodorotlenkiem:
Tlenki zasadowe, to tlenki metali, które reagują z kwasami, a nie reagują z wodorotlenkami.
Tlenki zasadowe metali | ||
bloku | bloku | bloku |
Wszystkie za wyjątkiem na przykład: | - | - |
W reakcjach tlenków zasadowych z kwasem powstaje sól i woda. Równanie tej reakcji można zapisać w sposób ogólny jako:
Tlenki amfoteryczne
Czy wiesz, jak zbadać właściwości amfoteryczne tlenków? Wprowadź do kolejnych probówek z tlenkiem cynku i tlenkiem glinu odpowiednio: kwas solny, wodny roztwór wodorotlenku sodu i wodę, a następnie rozwiąż poniższe ćwiczenia.
Zapoznaj się z opisem symulacji. Sprawdź, jak zbadać właściwości amfoteryczne tlenków.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DBJHP2UJG
Zapisz obserwacje i wnioski dotyczące właściwości chemicznych badanych tlenków.
Klasyfikacja tlenków według charakteru chemicznego
- Nazwa kategorii: Charakter chemiczny tlenków
- Nazwa kategorii: Kwasowy
- Nazwa kategorii: Reagują z wodnymi roztworami wodorotlenków tworząc sole.
- Nazwa kategorii: W większości reagują z wodą tworząc odpowiednie kwasy.
- Nazwa kategorii: Tworzą sole z tlenkami zasadowymi. Koniec elementów należących do kategorii Kwasowy
- Nazwa kategorii: Zasadowy
- Nazwa kategorii: Reagują z kwasami tworząc sole.
- Nazwa kategorii: Tlenki litowców i berylowców reagują z wodą tworząc odpowiedni wodorotlenek. Koniec elementów należących do kategorii Zasadowy
- Nazwa kategorii: Amfoteryczny
- Nazwa kategorii: Reagują z kwasami i wodnymi roztworami wodorotlenków tworząc sole.
- Nazwa kategorii: Zazwyczaj nie reagują z wodą. Koniec elementów należących do kategorii Amfoteryczny
- Nazwa kategorii: Obojętny
- Nazwa kategorii: Nie reagują z kwasami, wodnymi roztworami wodorotlenków ani z wodą. Koniec elementów należących do kategorii Obojętny
- Elementy należące do kategorii Charakter chemiczny tlenków
- Elementy należące do kategorii Kwasowy
- Elementy należące do kategorii Zasadowy
- Elementy należące do kategorii Amfoteryczny
- Elementy należące do kategorii Obojętny
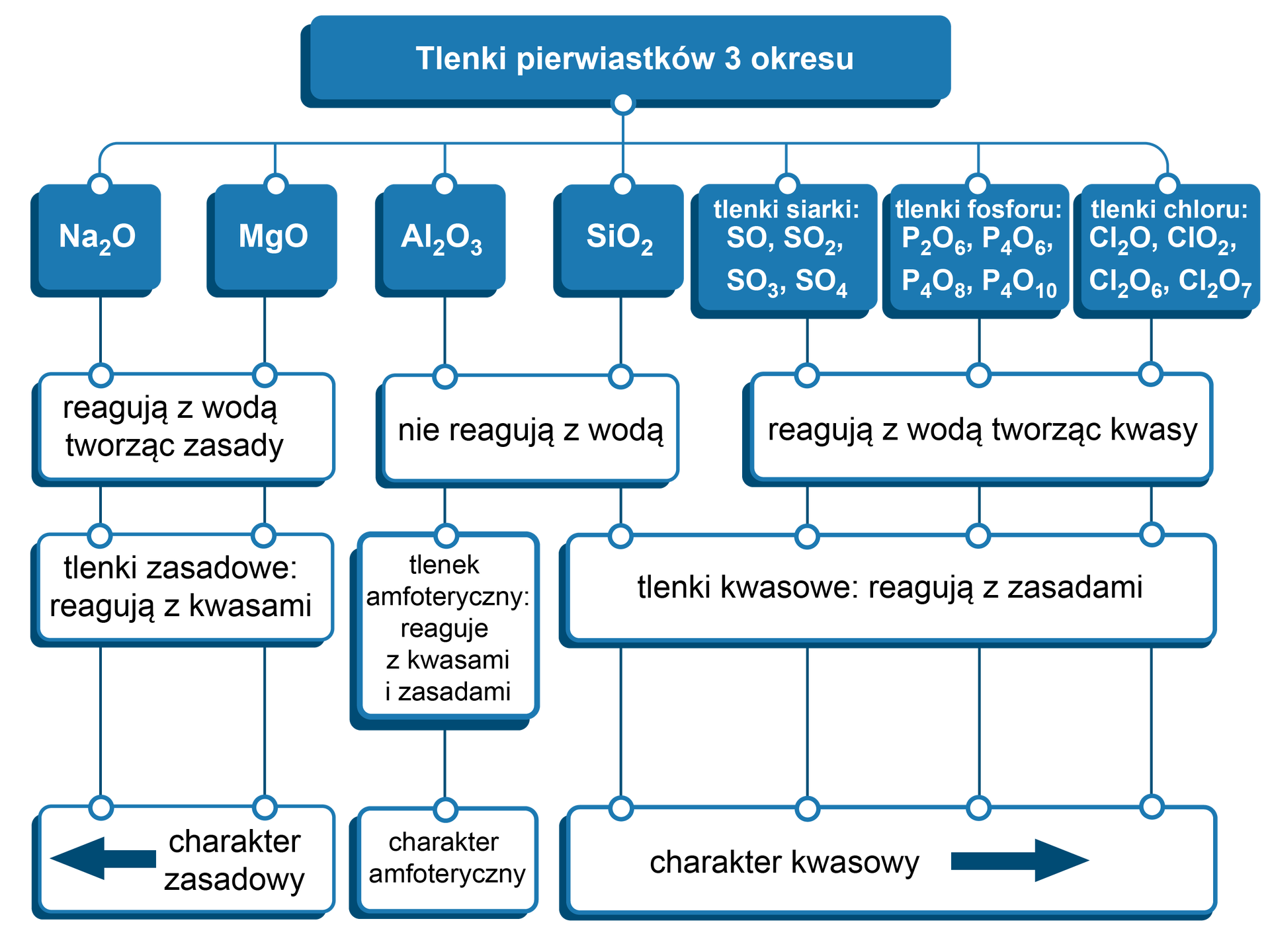
Ze względu na jakie czynniki klasyfikuje się tlenki? Przeanalizuj mapę interaktywną, uzupełnij ją o inne przykłady tlenków pasujących do róznych kategorii, a następnie rozwiąż ćwiczenia znajdujące się pod mapą.
Mapa pojęciowa dotycząca klasyfikacji tlenków ze względu na: charakter chemiczny, stan skupienia, charakter wiązania chemicznego, zachowanie wobec wody i rodzaj pierwiastka wchodzącego w skład tlenku, wraz z przykładami.
Nazwa kategorii: Klasyfikacja tlenków.
Elementy należące do kategorii Klasyfikacja tlenkówNazwa kategorii: ze względu na charakter chemiczny
Elementy należące do kategorii ze względu na charakter chemicznyNazwa kategorii: kwasowe
Elementy należące do kategorii kwasoweKoniec elementów należących do kategorii kwasowe
Nazwa kategorii: obojętne
Elementy należące do kategorii obojętneKoniec elementów należących do kategorii obojętne
Nazwa kategorii: zasadowe
Elementy należące do kategorii zasadoweKoniec elementów należących do kategorii zasadowe
Nazwa kategorii: amfoteryczne
Elementy należące do kategorii amfoteryczneKoniec elementów należących do kategorii amfoteryczne
Koniec elementów należących do kategorii ze względu na charakter chemiczny
Nazwa kategorii: ze względu na stan skupienia
Elementy należące do kategorii ze względu na stan skupieniaNazwa kategorii: ciecze
Elementy należące do kategorii cieczeKoniec elementów należących do kategorii ciecze
Nazwa kategorii: gazy
Elementy należące do kategorii gazyKoniec elementów należących do kategorii gazy
Nazwa kategorii: ciała stałe
Elementy należące do kategorii ciała stałeKoniec elementów należących do kategorii ciała stałe
Koniec elementów należących do kategorii ze względu na stan skupienia
Nazwa kategorii: ze względu na charakter wiązania chemicznego
Elementy należące do kategorii ze względu na charakter wiązania chemicznegoNazwa kategorii: zawierające wiązanie kowalencyjne
Elementy należące do kategorii zawierające wiązanie kowalencyjneKoniec elementów należących do kategorii wiązanie kowalencyjne
Nazwa kategorii: zawierające wiązanie jonowe
Elementy należące do kategorii zawierające wiązanie jonoweKoniec elementów należących do kategorii wiązanie jonowe
Koniec elementów należących do kategorii ze względu na charakter wiązania chemicznego
Nazwa kategorii: ze względu na zachowanie wobec wody
Elementy należące do kategorii ze względu na zachowanie wobec wodyNazwa kategorii: reagujące z wodą
Elementy należące do kategorii reagujące z wodąNazwa kategorii: zasadotwórcze
Elementy należące do kategorii zasadotwórczeKoniec elementów należących do kategorii zasadotwórcze
Nazwa kategorii: kwasotwórcze
Elementy należące do kategorii kwasotwórczeKoniec elementów należących do kategorii kwasotwórcze
Koniec elementów należących do kategorii reagujące z wodą
Nazwa kategorii: niereagujące z wodą
Elementy należące do kategorii niereagujące z wodąKoniec elementów należących do kategorii niereagujące z wodą
Koniec elementów należących do kategorii ze względu na zachowanie wobec wody
Nazwa kategorii: ze względu na rodzaj pierwiastka wchodzącego w skład tlenku
Elementy należące do kategorii ze względu na rodzaj pierwiastka wchodzącego w skład tlenkuNazwa kategorii: tlenki metali
Elementy należące do kategorii tlenki metaliKoniec elementów należących do kategorii tlenki metali
Nazwa kategorii: tlenki niemetali
Elementy należące do kategorii tlenki niemetaliKoniec elementów należących do kategorii tlenki niemetali
Koniec elementów należących do kategorii ze względu na rodzaj pierwiastka wchodzącego w skład tlenku
Koniec elementów należących do kategorii Klasyfikacja tlenków
Do jakiej grupy klasyfikuje się tlenek glinu ze względu na charakter chemiczny? Zapisz równania reakcji chemicznych, które potwierdzają tę tezę.