Badanie odczynu oraz pH wodnych roztworów kwasów, zasad i soli
Wielkościami liczbowo charakteryzującymi odczynodczyn roztworu są oraz :
Odczyn roztworu zależy zatem od stężenia molowego jonów i od stężenia molowego jonów oraz ich wzajemnej relacji:
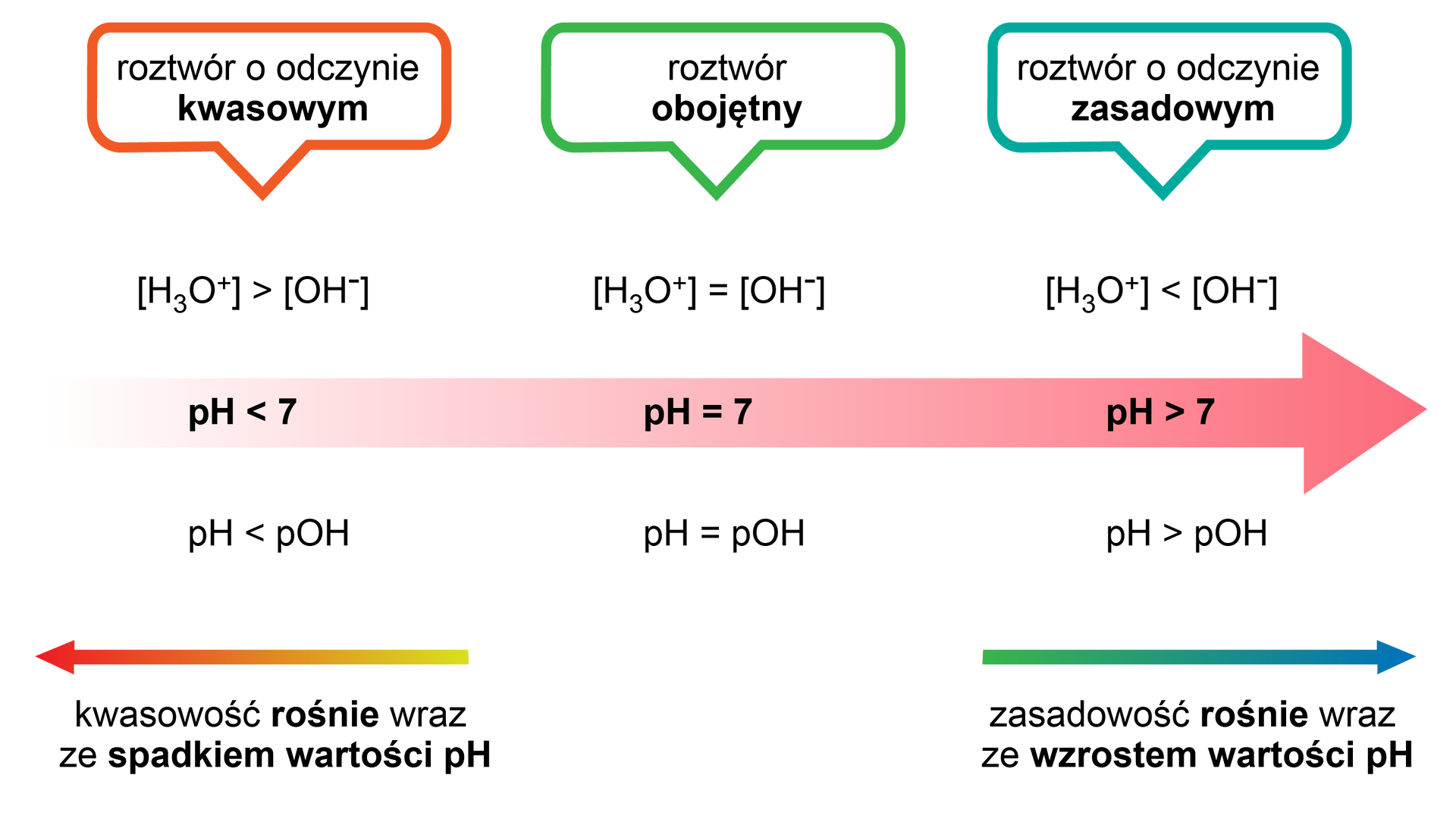
Przykłady wskaźników kwasowo‑zasadowych
WskaźnikiWskaźniki kwasowo–zasadowe to zwykłe związki typu słabych kwasów lub słabych zasad organicznych. Barwy, które nadają roztworom forma zdysocjowana i forma niezdysocjowana są różne. Przewaga danej formy (zdysocjowanej lub niezdysocjowanej), a więc i barwa roztworu jest zatem zależna od jego pH. Najpopularniejszym wskaźnikiem jest papierek uniwersalnypapierek uniwersalny, zwany wskaźnikowym. W roztworze o odczynie kwasowym przyjmuje on barwę czerwoną, o odczynie zasadowym przyjmuje barwę zieloną lub niebieską, a w roztworze obojętnym pozostaje zółty. Inne popularne wskaźnikiwskaźniki przedstawiono w tabeli.
Warto znać też inne wskaźniki kwasowo–zasadowe.
Wskaźnik | Barwa wskaźnika poniżej niższej wartości pH | Zakres pH zmiany barwy | Barwa wskaźnika powyżej wyższej wartości pH |
|---|---|---|---|
błękit tymolowy | czerwona | –; – | niebieska |
błękit bromofenolowy | żółta | – | niebieskofioletowa |
czerwień Kongo | niebieska | – | czerwona |
zieleń bromokrezolowa | żółta | – | niebieska |
błękit bromotymolowy | żółta | – | niebieska |
Aby zbadać odczyn roztworu, możemy nanieść kroplę roztworu na uniwersalny papierek wskaźnikowyuniwersalny papierek wskaźnikowy:
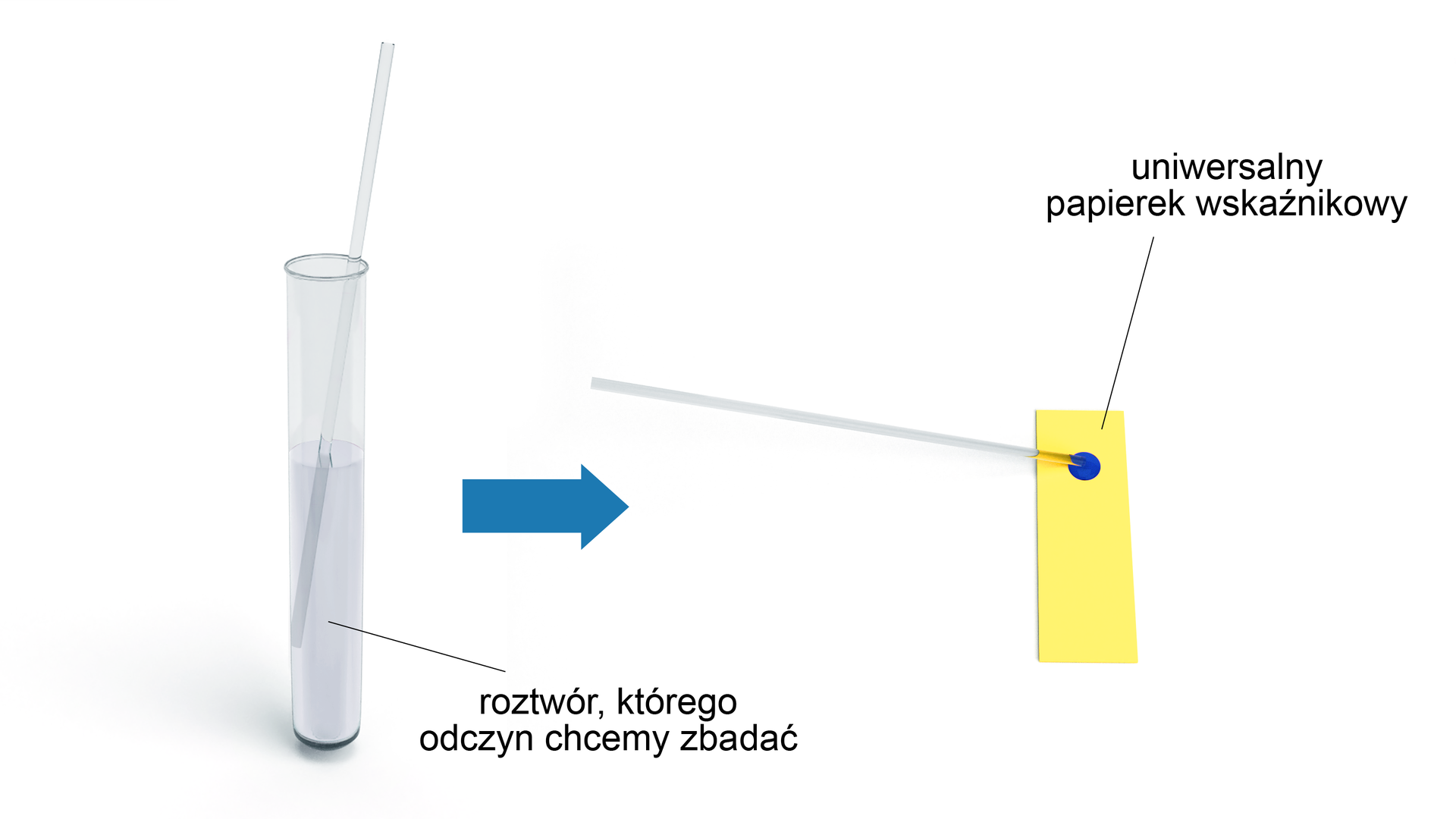
Następnie należy porównać barwę uniwersalnego papierka wskaźnikowego ze skalą barw.

Odczyn roztworu
Generalnie wodne roztwory kwasów mają odczynodczyn kwasowy, natomiast zasad – zasadowy. A jaki odczyn mają wodne roztwory soli?
Rozpuszczalne w wodzie sole nie tylko ulegają procesowi dysocjacji elektrolitycznej, ale również hydroliziehydrolizie. To reakcja odwracalna, która zachodzi między kationem lub/i anionem, pochodzącym z dysocjacji soli, a cząsteczkami wody. Hydrolizie ulegają wszystkie sole z wyjątkiem soli mocnych kwasów i mocnych zasad, np. (odczyn roztworu wodnego tej soli jest obojętny). Reakcja hydrolizy pozwala na przewidywanie odczynu roztworu. Jony powstałe podczas hydrolizy odpowiedzialne są za odczyn roztworu. Za odczyn zasadowy odpowiada obecność jonów (przewaga liczby jonów w stosunku do jonów obecnych w roztworze), natomiast za odczyn kwasowy odpowiada obecność jonów (większa liczba jonów w roztworze niż ). W przypadku odczynu obojętnego liczba jonów i jest taka sama.
Przypomnienie o hydrolizie
Przeprowadź eksperyment w laboratorium chemicznym. Zapisz problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie sformułuj wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DDN55ES1X
Przeprowadzono eksperyment w laboratorium chemicznym. Zapisano problem badawczy i zweryfikowano hipotezę. W formularzu zanotowano obserwacje i wyniki, a następnie sformułowano wnioski.
Analiza eksperymentu:
Badanie odczynu oraz wodnych roztworów kwasów, zasad i soli.
Problem badawczy:
Czy roztworu zależy od rodzaju substancji rozpuszczonej?
Hipoteza:
Rodzaj substancji rozpuszczonej wpływa na jej roztworu.
Sprzęt laboratoryjny:
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
pręcik szklany – szklany pręt laboratoryjny służący do mieszania;
tryskawka z wodą destylowaną;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości, służące do odmierzania cieczy;
–metr – aparat służący do pomiaru pH wyposażony elektrodę wskaźnikową i porównawczą;
uniwersalne papierki wskaźnikowe – kawałek bibuły nasączonej indykatorem służący do pomiaru .
Odczynniki chemiczne:
Roztwory wodne o stężeniach na decymetr sześcienny, na decymetr sześcienny i na decymetr sześcienny następujących substancji: chlorek sodu; chlorowodór; chlorek amonu; węglan potasu; wodorotlenek sodu; kwas octowy; octan amonu; amoniak; N–metylometanoamina (dimetyloamina).
Przebieg eksperymentu:
Wybrano roztwór do badania i przeniesiono go na blat stołu laboratoryjnego.
Wybrano stężenie roztworu oraz metodę pomiarową (papierki wskaźnikowe, –metr). Podczas korzystania z uniwersalnych papierków wskaźnikowych zanurzano szklany pręcik w roztworze, a następnie dotykano nim papierka wskaźnikowego. Podczas korzystania z –metru używano cylindra miarowego o pojemności mililitrów dla wybranego roztworu i przenoszono go do zlewki. Pamiętano przed i po dokonaniu pomiaru o przemyciu elektrody wodą dejonizowaną.
Obserwacje:
Kolory papierków wskaźnikowych dla roztworów wodnych ( na decymetr sześcienny; na decymetr sześcienny; na decymetr sześcienny): chlorku sodu (żółty; żółty; żółty); chlorowodoru (brunatny; brunatny; czerwonawy); chlorku amonu (ciemnopomarańczowy; ciemnopomarańczowy; ciemnopomarańczowy); węglanu potasu (niebieski; niebieskozielony; niebieskozielony); wodorotlenku sodu (granatowy; ciemnoniebieski; ciemnoniebieski); kwasu octowego (ciemnoczerwony; ciemnoczerwony; ciemnoczerwony); octanu amonu (żółty; żółty; żółty); amoniaku (niebieskozielony; niebieskozielony; niebieskozielony); N–metylometanoaminy (niebieski; niebieski; niebieskozielony);
Wyniki:
roztworów wodnych ( na decymetr sześcienny; na decymetr sześcienny; na decymetr sześcienny):
chlorku sodu (; ; );
chlorowodoru (; ; );
chlorku amonu (; ; );
węglanu potasu (; ; );
wodorotlenku sodu (; ; );
kwasu octowy (; ; );
octan amonu (; ; ); amoniaku (; ; );
N–metylometanoaminy (; ; ).
Wnioski:
Roztwór wodny chlorku sodu posiada odczyn obojętny. Kwas chlorowodorowy posiada odczyn silnie kwasowy. Roztwór wodny wodorotlenku sodu posiada odczyn silnie zasadowy. Roztwór wodny chlorku amonu posiada odczyn kwasowy. Roztwór wodny węglanu potasu posiada odczyn zasadowy. Roztwór wodny kwasu octowego posiada odczyn kwasowy. Roztwór wodny octanu amonu posiada odczyn obojętny. Roztwór wodny amoniaku posiada odczyn zasadowy. Roztwór wodny dimetyloaminy posiada odczyn zasadowy.
Wodne roztwory kwasów mają odczyn kwasowy, a wodne roztwory zasad – odczyn zasadowy. Wodne roztwory soli wykazują zróżnicowany odczyn – od kwasowego, poprzez obojętny do zasadowego.
Wartości wodnych roztworów kwasów, zasad i soli zależą m.in. od rodzaju substancji użytej do sporządzenia roztworu oraz od stężenia tego roztworu.
Hipoteza została potwierdzona.