Jak się zmieniają promienie atomów i jonów w układzie okresowym?
Rozmiar atomu jest jedną z wielkości fizycznych, dzięki którym możliwe jest przedstawienie zmian właściwości chemicznych pierwiastków w zależności od położenia w układzie okresowym. Wielkość atomów jest ważna przy próbie wyjaśnienia zachowania atomów, cząsteczek lub jonów.
Czym są promienie atomowe i jonowe oraz jak się zmieniają w układzie okresowym pierwiastków?
Jednym ze sposobów wyrażania wielkości atomów jest promień atomowypromień atomowy. Za rozmiar atomu lub jonu odpowiada głównie rozmiar chmury elektronowej. Pomimo, że w naszym postrzeganiu sam atom jest bardzo mały to porównując rozmiar jądra atomowego do rozmiaru samego atomu może zauważyć, że rozmiar atomu jest nieporównywalnie większy od rozmiaru jego jądra (ok. razy mniejszych od rozmiarów atomu).
Chmury elektronówChmury elektronów nie mają wyraźnych granic, więc nie możemy zmierzyć dokładnego promienia atomu. Jednak gdy atomy łączą się ze sobą tworząc cząsteczki, ich centra (jądrajądra) znajdują się wtedy w określonych odległościach od siebie. W celu standaryzacji pomiaru promieni atomowych, mierzy się odległość między jądrami dwóch identycznych atomów połączonych ze sobą.
Promień atomu
Promień atomowy jest zdefiniowany jako połowa odległości pomiędzy jądrami dwóch atomów tego samego pierwiastka, połączonych wiązaniem chemicznym.

Jak zmieniają się promienie atomów pierwiastków leżących w tym samym okresie?
Nasze rozważania zawęzimy do pierwiastków usytuowanych w grupach głównych układu okresowego , oraz – W ramach danego okresu, największe promienie mają te atomy, które rozpoczynają dany okres. Prócz wodoru, są to zatem atomy litowców. Wraz ze wzrostem liczby atomowej dla atomów kolejnych pierwiastków danego okresu, można zaobserwować zapełnianie danej powłoki kolejnymi elektronami. Objawia się to zmniejszeniem promienia atomu w danym okresie. Wynika to stąd, że im większy ładunek jądra (równy liczbie atomowej), tym silniej przyciąga ono elektrony wszystkich powłok (również elektrony znajdujące się na najbardziej zewnętrznej powłoce, która decyduje o wielkości atomu).
Jak zmieniają się promienie atomów pierwiastków leżących w tej samej grupie?
W grupach głównych promienie atomowe kolejnych pierwiastków rosną w dół grupy. Łatwo to zrozumieć biorąc pod uwagę wielkość chmury elektronowej atomów pierwiastków. Poruszając się w dół grupy, atomy kolejnych pierwiastków rozmieszczają elektrony na coraz bardziej oddalonych od jądra powłokach elektronowych, np. beryl rozmieszcza elektrony na dwóch powłokach, magnez już na trzech, wapń na czterech, stront na pięciu, a bar na sześciu. Skoro elektrony zajmują coraz bardziej oddalone od jądra powłoki, rośnie zatem rozmiar chmury elektronowej, a w konsekwencji także promień atomowy.
![Ilustracja przedstawia układ okresowy pierwiastków z wartościami promieni atomowych (zaznaczonych przy każdym symbolu jako zielone półkole) i promieni jonowych pierwiastków (zaznaczonych przy każdym symbolu jako półkole pomarańczowe dla kationów lub niebieskie dla anionów). Na przykład dla fransu Fr: liczba atomowa 87, średnia masa atomowa 223,02 unita, promień atomowy zaznaczony na zielonym półkolu wynosi 270 pikometrów [pm], na mniejszym pomarańczowym półkolu stykającym się z półkolem zielonym znajduje się wartość promienia jonowego wynoszącego 180 pikometrów. jeżeli jest niebieski oznacza anion. 7 s 1 , w prawym dolnym rogu kwadratu, oznacza konfigurację elektronów walencyjnych. Pod symbolem pierwiastka Fr jest F r + - symbol jonu; oraz litera k oznaczająca, że jon występuje tylko w kryształach, a nie w roztworach wodnych. Dla wodoru podano wartości zarówno promienia atomowego równą 30 pikometrów oraz wartości promieni jonowych dla kationu równą 105-, zaś dla anionu równą 154 pikometry. Podano również odpowiednio wartości promieni jonowych kationów i promieni atomowych dla następujących pierwiastków: lit (78; 152), sód (98; 186), potas (133; 227), rubid (149; 248), cez (165; 265), frans (180; 270), beryl (34; 114), magnez (78; 160), wapń (106; 197), stront (127; 215), bar (143; 217), rad (152; 223), skand (83; 161), itr (106; 181), tytan (60; 145), cyrkon (87; 160), hafn (84; 157), wanad (65; 132), niob (72; 143), tantal (72; 143), chrom (64; 125), molibden (96; 136), wolfram (68; 137), mangan (70; 129), technet (72; 130), ren (72; 137), żelazo (67; 124), ruten (77; 134), osm (81; 134), kobalt (64; 125), rod (75; 134), iryd (75; 136), nikiel (78; 127), pallad (86; 138), platyna (85; 138), miedź (72; 128), srebro (113; 144), złoto (91; 144), cynk (83; 133), kadm (103; 149); rtęć (112; 160), bor (23; 88), glin (57; 143), gal (72; 122), ind (92; 163), tal (105; 170), german (53; 122), cyna (74; 140), ołów (84; 175), arsen (69; 121), antymon (89; 141), bizmut (96; 155). Ponadto, podano wartości promieni jonowych i atomowych dla większości lantanowców i aktynowców: lantan (122; 188), cer (107; 182), prazeodym (106; 183), neodym (104; 182), promet (99; 181), samar (96; 180), europ (95; 204), gadolin (94, 180), terb (93, 178), dyspoz (91; 177), holm (90; 177), erb (89; 176), tul (87; 175), lutet (85; 173), aktyn (118; 188), tor (99; 180), proaktyn (98; 161), uran (97; 138), neptun (95; 131), pluton (93; 151), ameryk (92; 184). Oprócz tego, wartości promieni jonowych anionów i promieni atomowych podano dla następujących pierwiastków, wyrażając je w pikometrach: węgiel (260; 77), krzem (271; 117), azot (171; 70), fosfor (212; 110), tlen (132; 66), siarka (184; 104), selen (191; 117), tellur (211; 143), polon (240; 153), fluor (133; 58), chlor (181; 99), brom (196; 114), jod (220; 133), astat (227; 140). Dla pozostałych pierwiastków grup od pierwszej do piętnastej podano wartości promieni jonowych dla kationów, z wyjątkiem pierwiastków, dla których nie wyznaczono jeszcze dokładnych wartości.](https://static.zpe.gov.pl/portal/f/res-minimized/RD2WjveAYjym8/1622537373/DZNX8neyb7O1ztGXCxQtLl3ZNV8TslT5.png)
Podsumowując dyskusję dotyczącą promieni poszczególnych atomów, można powiedzieć, że promieniem atomowy rośnie w układzie okresowym (w grupach głównych) w lewo i w dół, a zatem w stronę atomu fransu.
Promień jonu
odległość najbardziej oddalonych elektronów od jądra atomu, w przypadku jonów utworzonych z jednego atomu, lub też od geometrycznego centrum jonów, złożonych z większej liczby atomów.
Przeanalizuj symulację pod kątem zmian promieni atomów i jonów dla pierwiastków podczas odrywania kolejnych elektronów od atomu danego pierwiastka: , , , , , , , , , , , i . Zmiany wartości promienia możesz obserwować wyciągając odpowiednią ilość elektronów z niebieskiej chmury do szarego pola. Jak myślisz, w jaki sposób będzie zmieniać się promień, jeżeli do atomu będą dołączane kolejne elektrony?
Źródło danych: Dayah M., Periodic Table - Ptable, online: https://ptable.com, dostęp: 29.06.2022.
Co dzieje się za promieniem atomu, gdy odrywa się od atomu kolejne elektrony?
Jak będzie zmieniać się promień, gdy do atomu będą przyłączane elektrony?
W wyniku oderwania elektronu lub elektronów, atom przechodzi w kation (jon o ładunku dodatnim), ponieważ liczba elektronów na powłokach jest mniejsza od liczby protonów w jądrze. Dokładnie można to zobrazować, zapisując konfigurację elektronową atomu pierwiastka oraz jego kationów:
konfiguracja elektronowa:
:
Atom żelaza w czasie jonizacji oddaje najpierw elektrony z podpowłoki . Po oddaniu obu elektronów powstaje kation dwudodatni:
konfiguracja elektronowa:
:
Jeśli ulega dalszej jonizacji, to kolejny elektron jest usuwany już z podpowłoki . Powstaje w ten sposób kation trójdodatni:
konfiguracja elektronowa:
:
Promienie jonowe kationów są mniejsze od promienia atomu, od którego pochodzą te jony. Im większy ładunek dodatni ma kation (im więcej elektronów oddał), tym jego promień jest mniejszy. Dlaczego? Można to wyjaśnić, biorąc pod uwagę dwie poniższe informacje:
usuwanie elektronów z powłok elektronowych może prowadzić do utraty najbardziej zewnętrznych powłok elektronowych, a więc do zmniejszenia rozmiaru chmury elektronowej;
utrata elektronu oznacza, że w drobinie jest więcej protonów niż elektronów. Im więcej elektronów zostanie usuniętych z powłok, tym z większą siłą jądro atomowe (którego ładunek dodatni przecież nie zmienia się) będzie przyciągać elektrony, które pozostały jeszcze w chmurze elektronowej.
Podsumowując – jeżeli porównujemy wielkość atomu żelaza i jego jonów, to:

Odwrotną zależność można zaobserwować dla anionów (jonów o ładunku ujemnym), powstałych w wyniku przyłączenia elektronów do atomu. Promienie jonowe anionów są większe niż atom, z którego pochodzą. Im większy ładunek ujemny posiada dany anion, tym jego promień jest większy. Elektrony są dodawane do zewnętrznej powłoki elektronowej zwiększającej rozmiar chmury elektronowej, a zatem również promień. Ponadto, ze wzrostem ujemnego ładunku anionu, jądro o stałym i niezmienny ładunku dodatnim musi przyciągać i utrzymywać coraz większą liczbę elektronów. W konsekwencji elektrony te są przyciągane słabiej, co również wpływa na rozmiar chmury elektronowej.

Podobnie jak w przypadku promienia atomowego, promienie jonów o tym samym ładunku są coraz większe dla kolejnych pierwiastków danej grupy układu okresowego.
Przeanalizuj poniższą grafikę interaktywną. Zwróć uwagę na podane wielkości promieni dla poszczególnych atomów i ich jonów, a także na podane konfiguracje elektronowe atomów pierwiastków. Następnie, w oparciu o grafikę, rozwiąż poniższe zadania.
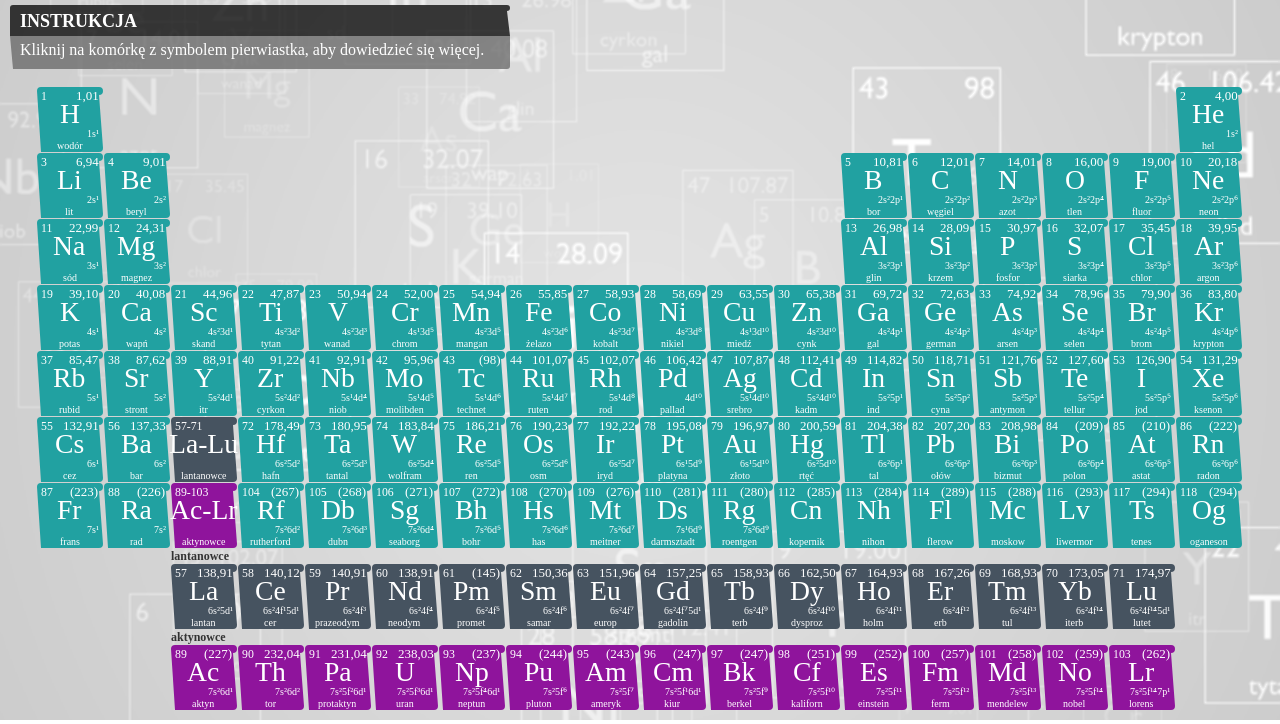
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DEMV7FMJH
Czy wiesz, jak zmieniają się promienie atomów i jonów pierwiastków w układzie okresowym? Zapoznaj się z opisem grafiki. Zwróć uwagę na podane wielkości promieni dla poszczególnych atomów i ich jonów, a także na podane konfiguracje elektronowe atomów pierwiastków. Następnie, w oparciu o grafikę, rozwiąż poniższe zadania.
- W okresach dwa-siedem największy promień atomowy mają fluorowce/ litowce/ tlenowce.
- Biorąc pod uwagę tylko pierwiastki grup głównych układu okresowego, w danym okresie promień rośnie/ maleje ze wzrostem liczby atomowej.
- Zwiększająca się liczba powłok elektronowych decyduje o tym, że w grupach głównych obserwuje się wzrost/ zmniejszenie się promienia atomowego w miarę wzrostu liczby atomowej.
- Wybierz atom, który ma większy promień atomu: N a czy C l?
- Wybierz atom, który ma większy promień atomu: C a czy F?
- Wybierz atom, który ma mniejszy promień atomu: L i czy C s?
- Kation ma promień jonowy mniejszy niż/ większy niż/ taki sam jak atom macierzysty.
- Anion ma promień jonowy mniejszy niż/ większy niż/ taki sam jak atom macierzysty.
Konfiguracja elektronowa M g indeks górny, dwa, plus, koniec indeksu górnego: 1. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, cztery, koniec indeksu górnego, 2. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 3. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, jeden, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 4. dwa, 5. cztery, 6. pięć, 7. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, pięć, koniec indeksu górnego, 8. dwa, 9. trzy, 10. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 11. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, cztery, koniec indeksu górnego, 12. pięć, 13. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, pięć, koniec indeksu górnego, 14. cztery, 15. trzy, 16. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, jeden, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego .
Liczba powłok N a indeks górny, plus, koniec indeksu górnego: 1. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, cztery, koniec indeksu górnego, 2. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 3. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, jeden, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 4. dwa, 5. cztery, 6. pięć, 7. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, pięć, koniec indeksu górnego, 8. dwa, 9. trzy, 10. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 11. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, cztery, koniec indeksu górnego, 12. pięć, 13. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, pięć, koniec indeksu górnego, 14. cztery, 15. trzy, 16. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, jeden, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego .
Liczba powłok M g indeks górny, dwa, plus, koniec indeksu górnego: 1. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, cztery, koniec indeksu górnego, 2. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 3. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, jeden, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 4. dwa, 5. cztery, 6. pięć, 7. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, pięć, koniec indeksu górnego, 8. dwa, 9. trzy, 10. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego, 11. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, cztery, koniec indeksu górnego, 12. pięć, 13. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, dwa, koniec indeksu górnego, dwa p indeks górny, pięć, koniec indeksu górnego, 14. cztery, 15. trzy, 16. jeden s indeks górny, dwa, koniec indeksu górnego, dwa s indeks górny, jeden, koniec indeksu górnego, dwa p indeks górny, sześć, koniec indeksu górnego .
Odpowiedz, który z promieni jonowych jest większy i uzasadnij dlaczego.