Węglowodory aromatyczne – areny. Metylobenzen (toluen) - właściwości
Właściwości fizykochemiczne toluenu
Toluen zawiera zarówno część alifatyczną, jak i aromatyczną, dzięki czemu przejawia właściwości dwojakiego rodzaju. Występowanie pierścienia aromatycznego wskazuje na to, że ów związek ulega m.in. reakcjom substytucji elektrofilowej, natomiast występowanie łańcucha bocznego – substytucji rodnikowej. Co więcej, oba fragmenty – alifatyczny i aromatyczny – wpływają na siebie. Grupa metylowa oddziałuje na zmianę właściwości aromatycznych pierścienia, natomiast ten z kolei decyduje o właściwościach alifatycznych łańcucha bocznego. Przykładowo, w wyniku obecności grupy metylowej nitrowanie pierścienia zachodzi łatwiej niż w samym benzenie. I odwrotnie – halogenowanie (np. bromowanie) grupy metylowej zachodzi łatwiej w obecności pierścienia niż dla samego metanu. Dlatego należy pamiętać, że każdy fragment cząsteczki wpływa na reaktywność drugiego fragmentu, wobec całego związku.

Toluen ulega reakcjom substytucji elektrofilowej analogicznie jak benzen. Do reakcji substytucji elektrofilowej należą reakcje nitrowania, halogenowania (bromowania, chlorowania), alkilowania, acylowania czy sulfonowania.

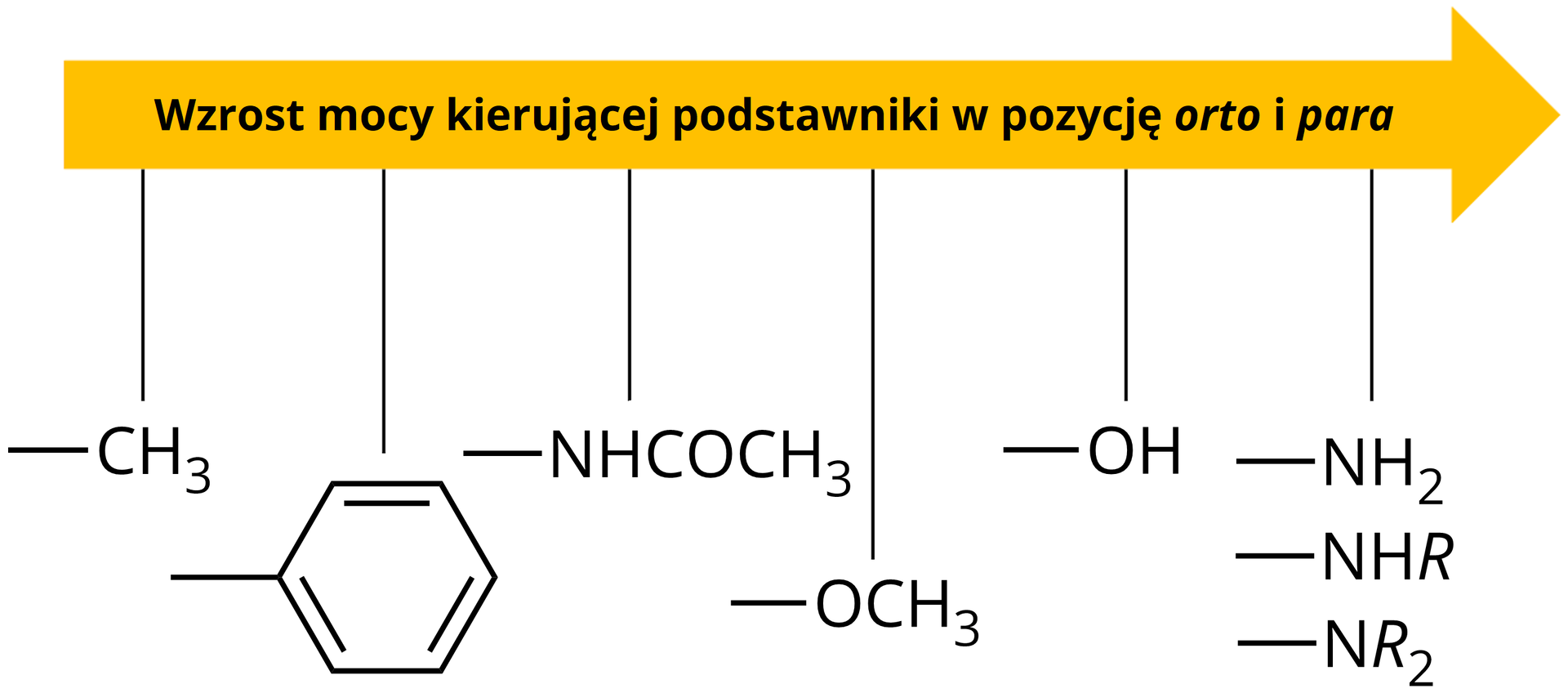
Atomy wodoru pierścienia aromatycznego toluenu nie są równocenne chemicznie, więc w odróżnieniu od benzenu nie bez znaczenia jest to, który atom wodoru ulega podstawieniu. Grupa metylowa, należąca do grup alkilowych w reakcjach aromatycznego podstawienia elektrofilowego (substytucji elektrofilowej), silnie aktywuje pierścień, czyli wzbogaca go w elektrony. O takiej grupie mówi się wówczas jako o aktywującej lub elektrodonorowejelektrodonorowej. Tego typu grupy są podstawnikami I rodzaju i kierują inne podstawniki w położenie orto i para.

W wyniku każdej reakcji substytucji elektrofilowej powstaje zatem mieszanina produktów w postaci izomerów orto i para.
Podstawniki przyłączone do pierścienia aromatycznego mają wpływ na jego reaktywność.
Podstawnikami aktywującymi nazywamy podstawniki kierujące w położenie orto i para. Podstawniki takie aktywują pierścień, przez co staje się on bardziej reaktywny niż benzen.
Podstawniki decydują również o położeniu kolejnego podstawnika w pierścieniu, a zatem mają wpływ na kierunek reakcji. Reaktywność i położenie są związane z dwoma efektami: efektem indukcyjnym i efektem rezonansowym.
Ten pierwszy – efekt indukcyjny – powstaje, kiedy w grupach funkcyjnych cząsteczki znajdują się wiązania spolaryzowane. Powodują one oddawanie lub przyciąganie elektronów w relacji z pierścieniem aromatycznym.
Efekt rezonansowy opiera się na nakładaniu orbitalami p pierścienia aromatycznego z orbitalem podstawnika. Efekt jest taki sam, a nakładanie powoduje wyciąganie elektronów z pierścienia lub ich dostarczanie do pierścienia aromatycznego.
Niektóre podstawniki orto i para mogą mieć funkcję dezaktywującą pierścień.
Część podstawników działa dezaktywująco na pierścień aromatyczny, powodując, że kolejne podstawienia zachodzą głównie w pozycję meta (w położenie 2 pierścienia aromatycznego). Obejrzyj symulację i określ, które podstawniki należą do tej grupy. Nazywamy je podstawnikami II rodzaju.
Przeanalizuj poniższą symulację interaktywną. Sprawdź, czy możliwe jest dołączenie kolejnych podstawników do pochodnych benzenu. W tym celu określ typ podstawnika przyłączonego do cząsteczki benzenu, a następnie zaznacz miejsca, do których mogą być przyłączone pozostałe podstawniki, oraz określ ich rodzaje. Aby sprawdzić swoją wiedzę, rozwiąż kolejno zadania sprawdzające.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DQX18HLRC
W symulacji przedstawiono szereg różnie podstawionych pochodnych benzenu, dla których określono, czy podstawnik w pierścieniu jest aktywujący czy dezaktywujący.
1. Nitrobenzen - podstawnik dezaktywujący i kierujący w pozycje meta.
2. Fenol - podstawnik aktywujący i kierujący w pozycje orto i para.
3. Benzaldehyd - podstawnik dezaktywujący i kierujący w pozycję meta.
4. Chlorobenzen - podstawnik dezaktywujący, z uwagi na rezonans wpływ kierujący w pozycję orto i para.
5. Anilina - grupa aminowa jest podstawnikiem aktywującym i kierujący w pozycje orto i para.
6. Etylobenzen - podstawnik aktywujący i kierujący w pozycję orto i para.
7. Kwas benzoesowy - podstawnik dezaktywujący i kierujący w pozycję meta.
Nitrowanie toluenu
Zgodnie z wpływem kierującym podstawnika metylowego, produktami reakcji nitrowania toluenu są o-nitrotoluen
(-metylo--nitrobenzen) oraz p-nitrotoluen (-metylo--nitrobenzen), czytane jako „orto-nitrotoluen” oraz „para-nitrotoluen”.

Halogenowanie toluenu
Do reakcji halogenowaniahalogenowania zalicza się m.in. bromowanie oraz chlorowanie, które zachodzą pod wpływem katalizatorów, odpowiednio i lub samego żelaza. Dla przykładu, zgodnie z wpływem kierującym podstawnika metylowego, produktami reakcji bromowania toluenu są -bromo--metylobenzen oraz -bromo--metylobenzen.

Alkilowanie toluenu
Reakcja alkilowaniaalkilowania katalizowana jest , reagującym z dowolnym halogenkiem alkilu.Zgodnie z wpływem kierującym podstawnika metylowego, produktami reakcji alkilowania, w poniższym przykładzie metylowania, są ,-dimetylobenzen oraz
,-dimetylobenzen.

Sulfonowanie toluenu
Zgodnie z wpływem kierującym podstawnika metylowego produktami reakcji sulfonowania toluenu są kwas -metylobenzenosulfonowy oraz
-metylobenzenosulfonowy.

Hydrogenacja pierścienia toluenu
Kolejnym typem reakcji, w której uczestniczy pierścień aromatyczny, jest reakcja addycji wodoru. Toluen w odpowiednich warunkach ulega hydrogenacji, czyli uwodornieniuuwodornieniu, pod wpływem katalizatorakatalizatora – np. , lub . Taka reakcja zachodzi zgodnie z mechanizmem addycji na katalizatorze i prowadzi do powstania metylocykloheksanu.

Reakcja ta wiąże się z utratą aromatyczności produktu, należącego do grupy cykloalkanów.
Substytucja rodnikowa w łańcuchu bocznym
Grupa metylowa w cząsteczce toluenu ulega zatem reakcji substytucji wolnorodnikowej w wyniku fluorowcowania za pomocą lub w obecności światła.

W wyniku chlorowania toluenu otrzymuje się chlorofenylometan o zwyczajowej nazwie chlorek benzylu.
Utlenianie łańcucha bocznego
Kolejnym typem reakcji, która dotyczy łańcucha bocznego, jest jego utlenianieutlenianie za pomocą silnego utleniaczautleniacza, np. , czy . Utlenianie toluenu prowadzi do otrzymania kwasu benzoesowego (kwasu benzenokarboksylowego). ReduktoremReduktorem w tej reakcji jest natomiast sama cząsteczka toluenu.

Pozostałe produkty reakcji zależą od użytego utleniacza oraz warunków prowadzenia reakcji, tak jak pokazano na poniższych przykładach, gdzie utleniaczem jest np. manganian() potasu oraz dichromian() potasu w środowisku kwasowym.
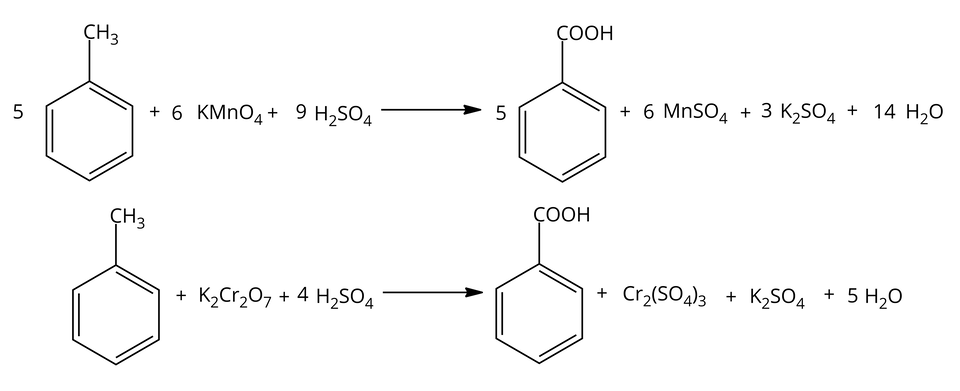
Przeprowadź poznane reakcje chemiczne toluenu w poniższym wirtualnym laboratorium oraz wykonaj zawarte pod nim ćwiczenia.
Na pewno wiesz już, jaki jest wzór toluenu i do jakiej grupy związków należy, ale czy wiesz, jakim reakcjom ulega? Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym, uzupełnij formularz, a następnie rozwiąż zadania.
Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod znakiem zapytania w prawym górnym rogu.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DQX18HLRC
Na pewno wiesz już, jaki jest wzór toluenu i do jakiej grupy związków należy, ale czy wiesz, jakim reakcjom ulega? Zapoznaj się z opisem przeprowadzonego doświadczenia, a następnie rozwiąż zadania.
Analiza doświadczenia: Badanie reaktywności toluenu wobec bromu.
Problem badawczy: Czy toluen reaguje z bromem w obecności światła lub bromku żelaza()?
Hipoteza: Toluen ulega reakcji z bromem zarówno w obecności światła, jak i bromku żelaza().
Odczynniki:
toluen
bromek żelaza()
woda bromowa
Sprzęt laboratoryjny:
probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
pipety – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżki laboratoryjne – długie trzonki wykonane ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką, służące do nabierania sypkich substancji chemicznych;
uniwersalne papierki wskaźnikowe – kawałek bibuły najczęściej w kształcie paska, nasączony roztworem substancji chemicznej będącej indykatorem i wysuszony.
Instrukcja wykonania doświadczenia:
Do dwóch probówek ostrożnie wprowadzono za pomocą pipety szklanej po około toluenu.
Następnie do obu probówek dodano za pomocą pipety szklanj po około kropli wody bromowej.
Pierwsza probókę przesieniono w zaciemnione miejsce, a następnie dodano do niej niewielką ilość . Zamieszano zawartość ostrożnie wstrząsając. Do wylotu probówki zbliżono zwilżony wodą uniwersalny papierek wskaźnikowy.
Druga probówkę zamknięto korkiem, a następnie wystawiono na działanie światła słonecznego lub silnej żarówki. Po kilku minutach zbliżono zwilżony wodą uniwersalny papierek wskaźnikowy do wylotu probówki.
Zanotowano obserwacje i wnioski.
Obserwacje:
W obu probówkach ich zawartość odbarwia się, a zwilżony uniwersalny papierek wskaźnikowy zabarwia się na czerwono.
Wyniki:
W obu probówkach zaszła reakcja. Czerwona barwa uniwersalnego papierka wskaźnikowego świadczy o powstaniu substancji, której wodny roztwór wykazuje odczyn kwasowy.
Wnioski:
W obydwu przypadkach reakcje zachodzą pod wpływem katalizatorów: dla reakcji w pierwszej probówce jest nim światło, a dla reakcji w drugiej probówce – bromek żelaza(). Produktem obu reakcji jest bromowodór (kolor czerwony uniwersalnego papierka wskaźnikowego). Hipoteza została potwierdzona.
Wiedząc, że mimo bardzo podobnych obserwacji w obu probówkach w wyniku reakcji powstały różne produkty organiczne, uzupełnij poniższe równania reakcji, dorysowując wzory odpowiednich związków chemicznych.
Uzupełnij zdania, wstawiając w puste pola odpowiednie wyrazy spośród wymienionych możliwości.
Przeanalizuj poniższą symulację interaktywną i sprawdź, czy metylobenzen reaguje z . W tym celu, za pomocą jednorazowej pipety, wprowadź do probówek metylobenzen, a następnie klika kropli roztworu . Kolejno, do wybranych probówek dodaj kwas siarkowy(), wodorotlenek potasu oraz wodę destylowaną. Wypełnioną probówkę umieść w zlewce, włącz płytę grzejną i obserwuj, co się stanie. Na końcu wykonaj załączone do medium ćwiczenia sprawdzające.
Zapoznaj się z opisem symulacji interaktywnej i sprawdź, czy metylobenzen reaguje z . Na końcu wykonaj załączone do medium ćwiczenia sprawdzające.
Metylobenzen jest związkiem organicznym i: Możliwe odpowiedzi: 1. o działaniu drażniącym., 2. łatwopalnym., 3. żrącym., 4. rakotwórczym., 5. wybuchowym.
