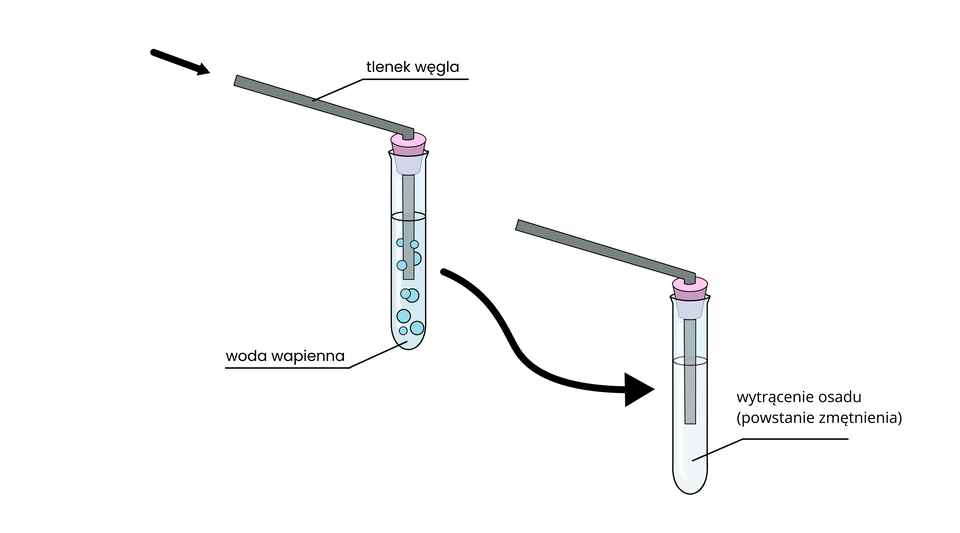
Składniki powietrza - tlenek węgla(IV)
Poniższy materiał jest uzupełnieniem treści zawartych w materiale: Właściwości tlenku węgla()
Czy powietrze jest potrzebne? Spróbuj zadać to pytanie swoim znajomym. Prawdopodobnie każdy bez wahania odpowie twierdząco. Niektórzy może nawet przyjrzą Ci się z pobłażaniem, że zadajesz tak trywialne pytania.
Każdy z nas wie, iż powietrze jest nam potrzebne choćby do oddychania. Ale czy całe? Czy do oddychania nie wystarczyłby nam tylko jeden jego składnik? Jeśli tak, to który? Jakie gazy są składnikami powietrza? Czy skoro ich nie widać, to można w jakiś sposób potwierdzić ich obecność?
definicje: powietrza, mieszaniny jednorodnej, substratów, produktów;
sposób zapisu równań reakcji chemicznych;
doświadczalne sposoby pozwalające na potwierdzenie istnienia powietrza;
nazwy oraz symbole i wzory chemiczne gazów będących składnikami powietrza;
właściwości fizykochemiczne poszczególnych gazów będących składnikami powietrza;
właściwości fizykochemiczne powietrza;
sposoby identyfikacji tlenu, tlenku węgla() (dwutlenku węgla) oraz pary wodnej.
projektować i przeprowadzać doświadczenia pozwalające na potwierdzenie obecności tlenu, tlenku węgla() i pary wodnej w powietrzu;
projektować i przeprowadzać doświadczenia pozwalające na porównanie zawartości tlenu i tlenku węgla() w powietrzu wdychanym do płuc i wydychanym z płuc;
wyjaśniać różnice w składzie powietrza wdychanego do płuc i wydychanego z płuc.
1. Czym jest powietrze?
PowietrzePowietrze jest jednorodną, wieloskładnikową mieszaniną różnych gazów, które tworzą atmosferę ziemską. Tym samym, powietrze stanowi jeden z podstawowych składników środowiska przyrodniczego.
To, że powietrze jest mieszaniną jednorodnąmieszaniną jednorodną oznacza, że nie jesteśmy w stanie rozpoznać jego składników ani „gołym” okiem, ani za pomocą prostych przyrządów optycznych.
W starożytności powietrze uznawane było za jeden z czterech żywiołów – podstawowych elementów, z których zbudowany jest świat.
Do około połowy wszystkie substancje i mieszaniny w stanie gazowym nazywano powietrzem.
2. Jakie substancje wchodzą w skład powietrza?
Głównym składnikiem czystego powietrza jest azot (), stanowiący około jego objętości. Drugim pod względem zawartości w powietrzu gazem jest tlen (). Gaz ten stanowi około objętości powietrza.
Azot i tlen nie są jednak jedynymi substancjami zawartymi w powietrzu. Około objętości powietrza stanowią bowiem inne gazy. Wśród nich znajdują się między innymi gazy szlachetne (hel, neon, argon, krypton), para wodna () oraz tlenek węgla() (dwutlenek węgla, ). Zawartość niektórych gazów w powietrzu może wahać się w zależności od różnych czynników (np. powietrze znajdujące się nad oceanem będzie różniło się zawartością pary wodnej od powietrza, znajdującego się bezpośrednio nad lądem).
3. Czy obecność poszczególnych gazów w powietrzu można potwierdzić doświadczalnie?
Na postawione powyżej pytanie spróbujesz odpowiedzieć samodzielnie, przeprowadzając odpowiednie eksperymenty w wirtualnym laboratorium. Zanim jednak to nastąpi, zapoznaj się z poniższymi informacjami, które ułatwią Ci zrozumienie obserwowanych w wirtualnym laboratorium zmian. W tym celu kliknij na każdy z poniższych kafelków i przeanalizuj ich zawartość.
Przeprowadź eksperyment w wirtualnym laboratorium. Przyjrzyj się dostępnym w nim odczynnikom i sprzętowi laboratoryjnemu. Na podstawie analizy powyższego materiału zastanów się i odpowiedz na pytanie: Obecność, których gazów można potwierdzić w powietrzu, mając do dyspozycji wspomniane wyposażenie? Wykonaj odpowiednie eksperymenty, a w ich trakcie uzupełnij dziennik laboratoryjny (polecenie ).
Na podstawie przeprowadzonych eksperymentów porównaj zawartość badanych gazów w powietrzu wdychanym do płuc i wydychanym z płuc. Odpowiednie informacje na ten temat zapisz we wspomnianym dzienniku laboratoryjnym.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DjTfCycY7
Analiza Eksperymentu Badania Składu Powietrza z Wykorzystaniem Miedzi
Na podstawie laboratorium przedstawiono oznaczanie zawartości tlenu w powietrzu atmosferycznym przy użyciu reakcji utleniania miedzi. Eksperyment ten stanowi klasyczny przykład zastosowania reakcji chemicznej do analizy ilościowej składników powietrza i demonstruje fundamentalne zasady chemii analitycznej.
1. Skład procentowy powietrza atmosferycznego
a. Identyfikacja Odczynników i Elementów Widocznych w Eksperymencie
Główne Składniki Eksperymentu:
Głównym elementem widocznym w eksperymencie jest miedź w postaci wiórów (Cu), która została umieszczona w rurce reakcyjnej. Miedź stanowi kluczowy element eksperymentu, gdyż jej właściwości chemiczne umożliwiają selektywną reakcję z tlenem zawartym w powietrzu atmosferycznym.
Powietrze atmosferyczne występujące w układzie eksperymentalnym zawiera następujące składniki: azot (N₂) stanowiący 78% objętości, tlen (O₂) stanowiący 21% objętości, argon (Ar) oraz inne gazy szlachetne łącznie 0,94%, dwutlenek węgla (CO₂) około 0,04%, oraz śladowe ilości innych gazów. Skład ten ma fundamentalne znaczenie dla interpretacji wyników eksperymentu, gdyż tylko tlen będzie reagował z miedzią w warunkach eksperymentu.
b. Aparatura i Narzędzia Pomiarowe
Cylinder miarowy o pojemności 200 cm³, który służy do precyzyjnego pomiaru objętości gazów przed i po reakcji.
Strzykawki laboratoryjne umożliwiają kontrolowane przemieszczanie powietrza przez nagrzaną miedzią rurką reakcyjną, co zapewnia pełny kontakt reagentów.
Rurka reakcyjna z miedzią stanowi centralne miejsce przebiegu reakcji chemicznej, gdzie zachodzi proces utleniania miedzi.
Analiza Reagujących Substancji Chemicznych.
2. Główna Reakcja Chemiczna
Jedyną reakcją chemiczną zachodzącą w przedstawionym eksperymencie jest reakcja utleniania miedzi tlenem zawartym w powietrzu atmosferycznym. Reakcja ta przebiega według równania stechiometrycznego: 2Cu + O₂ → 2CuO. Proces ten charakteryzuje się wysoką selektywnością - jedynie tlen z powietrza reaguje z miedzią, podczas gdy pozostałe składniki powietrza (azot, argon, dwutlenek węgla) pozostają obojętne chemicznie.
Warunki reakcji wymagają podwyższonej temperatury, co zostało zapewnione przez system grzewczy widoczny w eksperymencie. Temperatura jest niezbędna do przezwyciężenia energii aktywacji reakcji i umożliwienia efektywnego przebiegu procesu utleniania. Dostęp powietrza do nagrzanej miedzi jest zapewniony przez system strzykawek umożliwiających wielokrotne przepuszczanie powietrza przez strefę reakcji.
3. Produkty Reakcji i Ich Właściwości
Głównym produktem reakcji jest tlenek miedzi(II) o wzorze CuO, charakteryzujący się czarną barwą. Związek ten różni się znacząco od metalicznej miedzi pod względem właściwości fizycznych i chemicznych, co stanowi ważny wskaźnik przebiegu reakcji chemicznej.
Nierozpuszczalność tlenku miedzi(II) w wodzie oraz jego stabilność termiczna umożliwiają łatwe rozpoznanie produktu reakcji.
4. Charakterystyka Wszystkich Możliwych Reakcji Chemicznych
Reakcja Syntezy
Przedstawiona reakcja utleniania miedzi stanowi przykład reakcji syntezy (łączenia), w której dwa prostsze substancje - miedź i tlen - łączą się w celu utworzenia bardziej złożonego związku chemicznego. Reakcja ta może być zapisana jako proces łączenia atomów miedzi z cząsteczkami tlenu w proporcji stechiometrycznej 2:1. Mechanizm reakcji obejmuje przeniesienie elektronów z atomów miedzi na atomy tlenu, co prowadzi do powstania wiązań jonowych w strukturze krystalicznej tlenku miedzi(II).
Reakcja Utleniania‑Redukcji
Z punktu widzenia procesów elektronowych, reakcja stanowi przykład procesu redoks. Miedź ulega utlenieniu, oddając elektrony i zwiększając swój stopień utlenienia z 0 do +2, podczas gdy tlen ulega redukcji, przyjmując elektrony i obniżając stopień utlenienia z 0 do -2. Równanie elektronowe procesu można przedstawić jako: Cu → Cu²⁺ + 2e⁻ oraz O₂ + 4e⁻ → 2O²⁻.
Reakcja Egzotermiczna
Proces utleniania miedzi charakteryzuje się uwolnieniem energii w postaci ciepła, co klasyfikuje ją jako reakcję egzotermiczną. Entalpia reakcji ma wartość ujemną, wskazującą na spontaniczność procesu w warunkach eksperymentu. Uwolniona energia przyczynia się do podtrzymania reakcji po osiągnięciu odpowiedniej temperatury inicjującej proces.
5. Porównanie składu powietrza wdychanego i wydychanego
Wskaźniki Świadczące o Przebiegu Reakcji Chemicznej
Zmiany Właściwości Fizycznych
Najważniejszym wskaźnikiem przebiegu reakcji jest zmiana barwy miedzi z charakterystycznego czerwonobrązowego koloru metalicznej miedzi na intensywnie czarną barwę tlenku miedzi(II). Ta zmiana jest nieodwracalna i wyraźnie widoczna dla obserwatora, stanowiąc jednoznaczny dowód na przebieg reakcji chemicznej. Powierzchnia miedzi pokrywa się równomierną, przywierającą powłoką czarnego tlenku, co różni się od powierzchownych nalotów czy zanieczyszczeń.
Zmiana objętości gazów w układzie eksperymentalnym stanowi kolejny kluczowy wskaźnik. Objętość powietrza w układzie zmniejsza się o około 20‑21%, co odpowiada ilości tlenu zużytego w reakcji. To zmniejszenie objętości jest trwałe i może być precyzyjnie zmierzone za pomocą aparatury pomiarowej.
Efekty Energetyczne
Wydzielanie ciepła podczas reakcji stanowi dowód na przebieg procesu chemicznego o charakterze egzotermicznym. Wzrost temperatury w strefie reakcji jest obserwowany podczas aktywnego przebiegu procesu utleniania. Po zakończeniu reakcji temperatura układu stopniowo obniża się, co umożliwia wykonanie dokładnych pomiarów objętościowych w warunkach standardowych.
Nieodwracalność Procesu
Trwałość zmian zachodzących podczas reakcji stanowi istotny wskaźnik przebiegu reakcji chemicznej. Powstały tlenek miedzi(II) nie ulega spontanicznemu rozkładowi w warunkach eksperymentu, a przywrócenie pierwotnych właściwości miedzi wymagałoby dodatkowych procesów chemicznych, takich jak redukcja wodorem lub węglem. Ta nieodwracalność różni proces chemiczny od przemian fizycznych, które mogą być łatwo odwrócone.
Powstanie Nowej Substancji
Kluczowym dowodem na przebieg reakcji chemicznej jest powstanie nowej substancji - tlenku miedzi(II) - o właściwościach całkowicie różnych od substratów wyjściowych. Nowy związek chemiczny wykazuje inne właściwości fizyczne (barwa, przewodnictwo elektryczne, rozpuszczalność) i chemiczne (reaktywność, stabilność) w porównaniu z metaliczną miedzią i gazowym tlenem. Struktura krystaliczna tlenku miedzi(II) różni się fundamentalnie od struktury metalicznej miedzi, co stanowi dowód na głębokie przekształcenia na poziomie atomowym.
Znaczenie Edukacyjne i Praktyczne
Przedstawiony eksperyment stanowi doskonały przykład zastosowania reakcji chemicznej do analizy ilościowej. Umożliwia precyzyjne określenie składu powietrza atmosferycznego, demonstrując praktyczne zastosowania wiedzy chemicznej w badaniach środowiskowych. Metodyka eksperymentu ilustruje podstawowe zasady stechiometrii, kinetyki reakcji chemicznych oraz analizy ilościowej gazów.
Spośród zapisanych poniżej informacji wybierz i zaznacz te, które stanowią poprawne obserwacje i wnioski do przeprowadzonego przez ucznia doświadczenia. Możliwe odpowiedzi: 1. Obserwacje: Płomień świecy przykrytej kolbą pierwszą zgasł szybciej niż płomień świecy przykrytej kolbą drugą.
Wnioski: Powietrze wdychane do płuc zawiera więcej tlenu niż powietrze wydychane z płuc., 2. Obserwacje: Płomień świecy przykrytej kolbą drugą zgasł szybciej niż płomień świecy przykrytej kolbą pierwszą.
Wnioski: Powietrze wdychane do płuc zawiera więcej tlenu niż powietrze wydychane z płuc., 3. Obserwacje: Płomienie obydwu świec zgasły jednocześnie.
Wnioski: Powietrze wdychane do płuc zawiera tyle samo tlenu, co powietrze wydychane z płuc., 4. Obserwacje: Płomień świecy przykrytej kolbą drugą zgasł szybciej niż płomień świecy przykrytej kolbą pierwszą.
Wnioski: Powietrze wydychane z płuc zawiera więcej tlenu niż powietrze wdychane do płuc.
Uczeń przeprowadził doświadczenie zilustrowane na poniższym schemacie:
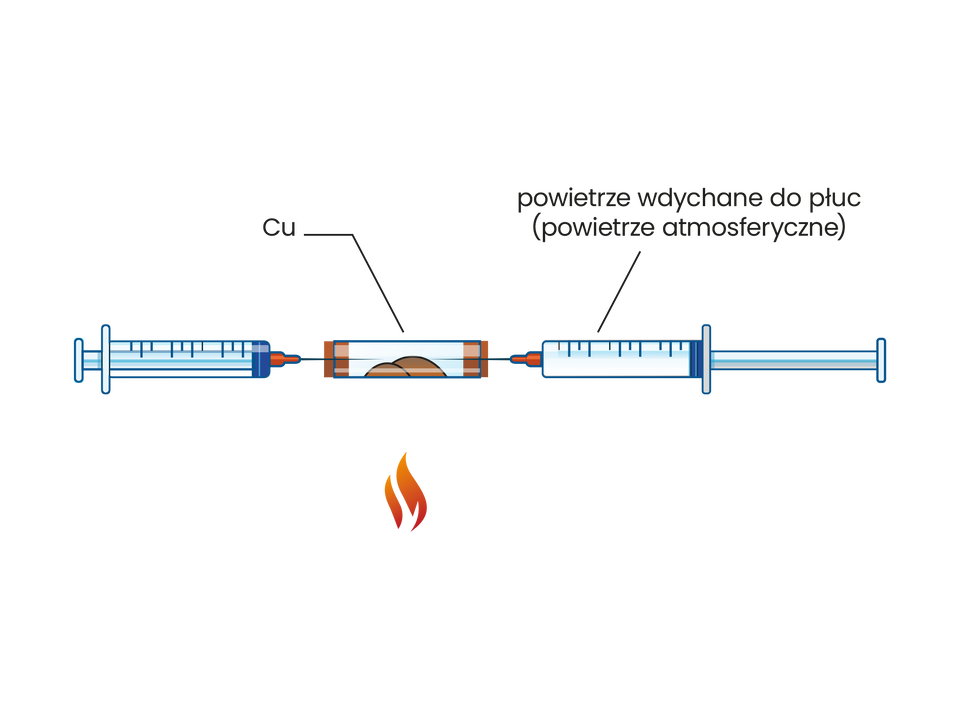
Uczeń przeprowadził doświadczenie polegające na umieszczeniu w zamkniętym, ogrzewanym od spodu naczyniu kawałka miedzi. Od dwóch stron naczynie przekłuto strzykawkami. Strzykawka z lewej strony była pusta (tłok był wciśnięty do środka), a strzykawka z prawej strony zawierała powietrze wdychane do płuc (powietrze atmosferyczne).
W czasie trwania doświadczenia, uczeń przesuwał tłoki strzykawek do momentu, aż przestał obserwować zmiany świadczące o przebiegu reakcji chemicznej.
Zaproponuj i przeprowadź doświadczenie pozwalające na potwierdzenie obecności pary wodnej w powietrzu wydychanym z płuc. Krótko opisz przebieg tego doświadczenia oraz przewidywane obserwacje i wnioski.
4. Czy powietrze wdychane do płuc ma taki sam skład, jak powietrze wydychane z płuc?
Na podstawie eksperymentów wykonanych w wirtualnym laboratorium oraz w oparciu o zdobytą wiedzę możesz wnioskować, że w skład powietrza wydychanego z płuc wchodzą te same substancje, które znajdują się w powietrzu wdychanym do płuc. Jednak zawartość niektórych ze wspomnianych substancji w obydwu rodzajach powietrza jest różna.
Na poniższym wykresie zamieszczono przybliżone wartości zawartości procentowej wybranych gazów w powietrzu wdychanym do płuc i w powietrzu wydychanym z płuc.
Zwróć uwagę, że w procesie oddychania zawartość tlenu w powietrzu zmniejsza się, przy jednoczesnym wzroście zawartości tlenku węgla() (dwutlenku węgla).
Jak już wspomniano, tlen jest substratem procesów spalaniaspalania. Oddychanie, z punktu widzenia chemika, jest spalaniem – zatem tlen zużywa się w tym procesie. Jednym z produktówproduktów spalania pokarmu w komórkach organizmu jest tlenek węgla() (dwutlenek węgla) – zatem jego ilość w wyniku oddychania wzrasta. Wśród gazów zawartych w powietrzu, oznaczonych na wykresie jako „inne”, znajduje się para wodna. Jej ilość w powietrzu w procesie oddychania również nieznacznie wzrasta. Para wodna, podobnie jak tlenek węgla(), jest produktem spalania pokarmu.

Obecność pary wodnej w powietrzu wdychanym do płuc (w powietrzu atmosferycznym) można wykazać, wykorzystując do tego celu substancje o właściwościach higroskopijnychhigroskopijnych. Do substancji tych należy między innymi stały wodorotlenek sodu. Wodorotlenek sodu jest jednym ze składników popularnego granulatu do udrażniania rur. Substancja ta jest bardzo dobrze rozpuszczalna w wodzie.
Składnikiem powietrza, bezpośrednio wykorzystywanym w procesie oddychania, jest tlen. Czy w związku z tym stwierdzenie, że powietrze jest nam potrzebne do oddychania, jest poprawne? Co by się stało gdybyśmy przez dłuższy czas oddychali czystym tlenem?
W przypadku utraty przytomności lub niedotlenienia, pacjentom bardzo często podawany jest do oddychania czysty tlen. W momencie kiedy do płuc zamiast powietrza trafia sam tlen, oddech pacjenta staje się szybszy. To z kolei skutkuje szybszym usuwaniem tlenku węgla() (dwutlenku węgla) z naczyń krwionośnych oraz ich zwężeniem. Może się zdarzyć, że średnica naczyń krwionośnych będzie na tyle mała, że nie będą one zdolne do transportowania odpowiednich ilości tlenu do poszczególnych narządów. W efekcie, podanie tlenu może skutkować jeszcze większym niedotlenieniem.
W związku z powyższym, czysty tlen powinien być podawany zgodnie z zaleceniem lekarza, a sama tlenoterapia powinna być prowadzona przez odpowiedni, ustalony przez lekarza, czas.
Słownik
jednorodna mieszanina gazów tworzących atmosferę ziemską
mieszanina co najmniej dwóch substancji, których nie można rozróżnić gołym okiem, ani za pomocą prostych przyrządów optycznych
substancja, która bierze udział w przemianie chemicznej (ulega przemianie chemicznej)
roztwór (mieszanina jednorodna), w którym znajduje się maksymalna ilość (liczba gramów) substancji rozpuszczonej, jaka wynika z jej rozpuszczalności w podanych warunkach temperatury (i ciśnienia)
nasycony wodny roztwór wodorotlenku wapnia w wodzie (); stosowana często jako odczynnik laboratoryjny, który umożliwia identyfikację tlenku węgla() – w obecności tlenku węgla(IV) woda wapienna mętnieje
gwałtowna reakcja, której towarzyszy wydzielenie się dużej ilości energii (między innymi na sposób ciepła i/lub światła); w niniejszym materiale jako reakcje spalania rozpatrywano reakcje odpowiednich substancji z tlenem; jako spalanie można jednak definiować również reakcje z innymi gazami, np. z chlorem
substancja, która powstaje w wyniku reakcji chemicznej
w uproszczeniu, zdolność niektórych substancji do pochłaniania pary wodnej i wody w postaci ciekłej
Ćwiczenia
Zawartość tego gazu w powietrzu w czasie oddychania nie ulega zmianie/zmniejsza się. Para wodna stanowi mniej/więcej niż jeden procent objętości czystego (suchego) powietrza.
Uczeń przeprowadził następujące doświadczenie:
Do zlewki wlał niewielką ilość wody wapiennej. Następnie za pomocą słomki do napojów wdmuchiwał do niej powietrze (wydychane z płuc).
Bibliografia
Burewicz A., Jagodziński P., Wolski R., Metodyka eksperymentu chemicznego, Poznań 2008.
Encyklopedia PWN
Gulińska H., Smolińska J., Ciekawa chemia. Podręcznik do gimnazjum 1, Warszawa 2014, wyd. 6.
Stradowski J., Tlen: życiodajna trucizna. Daje nam energię i truje nas wolnymi rodnikami, 2014, online: https://www.focus.pl/artykul/tlen-zyciodajna-trucizna, dostęp: 08.04.2022.