Różnice między zjawiskiem fizycznym a przemianą chemiczną
Poniższy materiał stanowi uzupełnienie treści zawartych w materiale: https://zpe.gov.pl/a/zjawisko-fizyczne-a-przemiana-chemiczna/DBKPFQFTj
Lanie wosku to jedna z najpopularniejszych wróżb andrzejkowych. Czy wiesz, jakie procesy (fizyczne czy chemiczne) zachodzą podczas topienia wosku i przelewania go przez dziurkę od klucza do naczynia z zimną wodą? Czy w wyniku tych procesów powstają nowe substancje chemiczne?

przykładowe właściwości fizyczne i chemiczne, które mogą posiadać substancje chemiczne;
procesy umożliwiające zmianę stanu skupienia substancji;
metody rozdzielania mieszanin na składniki.
wymieniać przykłady zjawisk fizycznych i przemian chemicznych zachodzących w otoczeniu człowieka;
opisywać efekty świadczące o przebiegu reakcji chemicznych;
projektować i wykonywać proste doświadczenie ilustrujące zjawiska fizyczne i reakcje chemiczne;
formułować obserwacje do przeprowadzanych doświadczeń i eksperymentów.
1. Zjawisko fizyczne a przemiana chemiczna
Podstawowym sposobem poznawania otaczającego nas świata jest obserwacja zachodzących w nim procesów. Procesy te możemy podzielić na dwie grupy. Pierwsza z nich to procesy (zjawiska) fizyczneprocesy (zjawiska) fizyczne, a więc takie, które nie prowadzą do powstawania nowych substancji, ale do zmian właściwości fizycznych substancji już istniejących. Drugą grupę stanowią przemiany (reakcje) chemiczneprzemiany (reakcje) chemiczne, prowadzące do otrzymywania nowych substancji chemicznych o właściwościach fizykochemicznych, odmiennych od substancji, z których powstały.
Do przemian fizycznych zaliczamy między innymi otrzymywanie oraz rozdzielanie mieszanin, a także zmiany stanu skupienia substancji, zachodzące na skutek zmian warunków temperatury i ciśnienia.
Przemianami chemicznymi są między innymi procesy zachodzące w ludzkim organizmie (np. trawienie, oddychanie), spalanie różnego rodzaju paliw oraz korozjakorozja metali. Wybrane przykłady zjawisk fizycznych i przemian chemicznych, obserwowanych w codziennym życiu, przedstawiono w poniższej galerii zdjęć.










Czasem zdarza się tak, że mamy wątpliwości, czy obserwowany proces jest zjawiskiem fizycznym, czy też przemianą chemiczną. W takich przypadkach, oprócz zmysłów, za pomocą których dokonujemy obserwacji, potrzebna jest również wiedza o właściwościach fizykochemicznych poszczególnych substancji.
2. Efekty świadczące o przebiegu reakcji chemicznych
Mimo że jednoznaczne określenie rodzaju przemiany bywa czasem dość trudne, możemy wskazać kilka obserwacji (efektów), które mogą świadczyć o danej przemianie – fizycznej lub chemicznej. Na poniższej mapie myśli opisano typowe efekty, które mogą świadczyć o przebiegu w układzie reakcji chemicznej.
Mapa myśli przedstawia efekty, które mogą świadczyć o przebiegu w układzie reakcji chemicznej. Są to: pojawienie się (wytrącenie się) osadu o określonej barwie, zmiana zabarwienia osadu, zanik osadu (roztwarzanie się osadu), wydzielanie się bezbarwnego gazu lub gazu o określonej barwie, wydzielanie się bezwonnego gazu lub gazu o charakterystycznym zapachu, pojawienie się charakterystycznego zapachu nie związanego z wydzielaniem się gazu (np. pojawienie się zapachu octu), zmiana zabarwienia roztworu, odbarwienie się roztworu, pojawienie się zabarwienia roztworu, zmiana temperatury układu reakcyjnego odnotowana z użyciem termometru lub za pomocą dotyku.
Formułując obserwacje do prowadzonych doświadczeń i eksperymentów, podczas których zachodzą przemiany chemiczne, nie podajemy nazw i wzorów chemicznych powstających w wyniku zachodzących przemian substancji (czasem zdarza się tak, że nie wiemy, co to za substancje i musimy je zidentyfikować, przeprowadzając dalsze badania). W obserwacjach wymieniamy wszystko to, co jesteśmy w stanie ustalić za pomocą zmysłów: wzroku, węchu, dotyku i słuchu.
Efektem świadczącym o przebiegu reakcji chemicznej jest wydzielanie się gazu. Gaz ten może być bezbarwny lub mieć określone zabarwienie (np. brunatne). Wydzielający się gaz może mieć również charakterystyczny zapach lub może być bezwonny (pozbawiony zapachu). Zapach obecny w trakcie wykonywania niektórych doświadczeń może nie być związany z wydzielaniem się gazu. W wyniku niektórych reakcji chemicznych powstają substancje, które nie są gazami, ale mają charakterystyczne zapachy (np. kwas octowy o zapachu octu, czy też etanol o zapachu alkoholu).
O przebiegu reakcji chemicznej może również świadczyć wytrącanie się osadu z roztworu. Osad ten może być biały lub mieć inne zabarwienie (np. niebieskie, czarne, brunatne itp.). Powstawanie osadu w wyniku reakcji chemicznej świadczy o tym, że w układzie powstała przynajmniej jedna substancja trudno rozpuszczalna w wodzie (lub w innym znajdującym się w roztworze rozpuszczalniku). Skutkiem reakcji chemicznej może być również zanikanie obecnego już w układzie osadu, co świadczy o tym, że substancja, będąca osadem, przekształciła się w substancję dobrze rozpuszczalną w wodzie (lub w innym użytym rozpuszczalniku).
Klasyfikując przemiany materii w odniesieniu do pojawiania się i zanikania osadu, należy być czujnym. Obydwa procesy, zarówno wytrącanie się osadu, jak i jego zanik, mogą być także skutkiem przemian fizycznych (np. krystalizacji, w wyniku której powstaje osad, lub rozpuszczania substancji stałej w ciekłym rozpuszczalniku).
Jeżeli reakcję chemiczną prowadzimy w roztworze (np. w roztworze wodnym), to w jej wyniku może dojść do zmiany zabarwienia tego roztworu. Jeśli roztwór przed reakcją był bezbarwny, skutkiem tej reakcji może być zabarwienie go na określony kolor. Barwne roztwory, w wyniku zachodzących reakcji chemicznych, mogą również ulec odbarwieniu.
Reakcjom chemicznym mogą także towarzyszyć efekty cieplne – wydzielanie się energii na sposób ciepła (reakcje egzotermicznereakcje egzotermiczne) lub pobieranie energii do układu reakcyjnego (reakcje endotermicznereakcje endotermiczne).
W pierwszym przypadku, kiedy energia jest wydzielana z układu reakcyjnego, temperatura tego układu (np. roztworu) wzrasta. Możemy to stwierdzić, używając odpowiedniego termometru lub dotykając naczynia reakcyjnego, które jest cieplejsze niż przed reakcją. Sprawdzając temperaturę naczynia za pomocą dotyku, musimy być jednak bardzo ostrożni. Jego temperatura może być bowiem tak wysoka, że możemy się poparzyć. Między innymi z tego powodu nie powinno się trzymać naczyń reakcyjnych „gołymi” dłońmi w czasie przeprowadzania doświadczeń (można je trzymać za pomocą łap laboratoryjnych, umieścić je w statywie lub ustawić na blacie laboratoryjnym).
W przypadku, gdy układ pobiera energię z otoczenia, temperatura układu maleje. Wówczas po dotknięciu naczynia reakcyjnego stwierdzimy, że jest ono chłodniejsze niż przed reakcją. Zmiany temperatury układu mogą również towarzyszyć rozpuszczaniu substancji w wodzie, a więc zjawiskom fizycznym. Przykładowo, roztwór uzyskany po rozpuszczeniu w wodzie stałego wodorotlenku sodu będzie miał temperaturę wyższą niż składniki użyte do jego przygotowania.
Jeżeli w czasie trwania doświadczenia lub eksperymentu nie odnotujemy w analizowanym układzie zmian, które świadczyłyby o przebiegu reakcji chemicznej, musimy to odnotować w obserwacjach. Zapisujemy wówczas komentarz: „brak objawów reakcji” lub „brak zmian świadczących o przebiegu reakcji chemicznej”.
Wodny roztwór wodorotlenku sodu jest bezbarwny, podobnie jak kwas chlorowodorowy (wodny roztwór chlorowodoru). Po zmieszaniu ze sobą wspomnianych roztworów, otrzymamy większą ilość bezbarwnego, klarownego roztworu. Z obserwacji mogłoby wynikać, że zmieszanie tych roztworów to wyłącznie zjawisko fizyczne, w wyniku którego powstała mieszanina jednorodna wody oraz rozpuszczone w niej wodorotlenek sodu i chlorowodór. Okazuje się jednak, że po zmieszaniu analizowanych roztworów wodnych, wodorotlenek sodu i kwas chlorowodorowy reagują ze sobą, przekształcając się w chlorek sodu (ten sam, który stanowi sól kuchenną) i wodę. Finalnie otrzymujemy więc wodny roztwór innej (niż wyjściowa) substancji. Można to potwierdzić, używając w trakcie doświadczenia odpowiedniego wskaźnika kwasowo‑zasadowegowskaźnika kwasowo‑zasadowego, który zmienia zabarwienie, w zależności od odczynu roztworu. Wskaźnikiem takim jest np. wywar z czerwonej kapusty, który w wodnym roztworze wodorotlenku sodu ma barwę zieloną, a w wodnym roztworze chlorku sodu – fioletową.
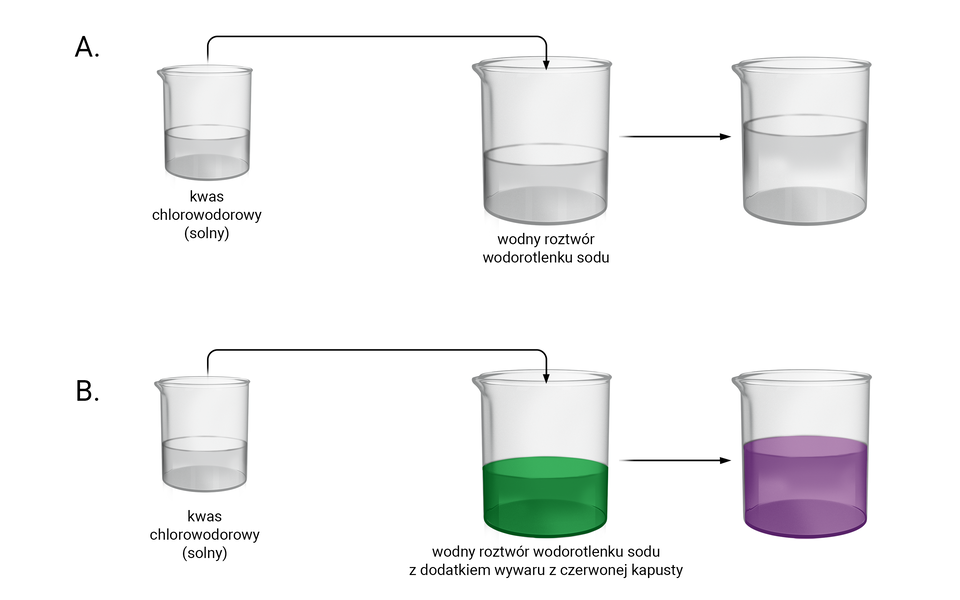
A – bez użycia wskaźnika
B – z użyciem wywaru z czerwonej kapusty jako wskaźnika kwasowo‑zasadowego
Mając do dyspozycji kwasek cytrynowy, sodę oczyszczoną oraz wodę destylowaną, oceń, czy proces , który zachodzi po zmieszaniu wodnych roztworów kwasku cytrynowego i sody oczyszczonej, to zjawisko fizyczne, czy przemiana chemiczna? Przeprowadź eksperyment i uzupełnij dziennik laboratoryjny.
Zapoznaj się z poniższym opisem przeprowadzonego eksperymentu, a następnie wykonaj polecenie.
Problem badawczy:
Czy proces, który zachodzi po zmieszaniu wodnych roztworów kwasku cytrynowego i sody oczyszczonej, to zjawisko fizyczne, czy przemiana chemiczna?
Hipoteza:
Po zmieszaniu wodnych roztworów kwasku cytrynowego i sody oczyszczonej, zachodzi przemiana chemiczna.
Co było potrzebne:
kwasek cytrynowy;
soda oczyszczona;
woda destylowana;
dwie zlewki (szklanki lub słoiki);
dwie łyżeczki.
Przebieg doświadczenia:
Do obydwu zlewek wlano po około wody destylowanej. Do jednej wsypano dwie łyżeczki kwasku cytrynowego, a następnie wymieszano zawartość. Do drugiej wsypano dwie łyżeczki sody oczyszczonej i również wymieszano zawartość naczynia. Roztwór jednej ze zlewek przelano do roztworu znajdującego się w drugiej zlewce.
Obserwacje:
Wydziela się bezbarwny, bezwonny gaz. Zlewka staje się zimna w dotyku.
Wnioski:
Wydzielanie się gazu świadczy o tym, że w układzie reakcyjnym powstały nowe substancje. Postawiona hipoteza jest zatem prawdziwa – po zmieszaniu wodnych roztworów, kwasku cytrynowego i sody oczyszczonej, zachodzi reakcja chemiczna. Reakcja ta jest endotermiczna.
Wykorzystując odczynniki i sprzęt laboratoryjny, uwzględniony w eksperymencie z polecenia nr , możesz przygotować „chemiczny wulkan”. Jeden z przygotowanych wodnych roztworów przelej do naczynia z wąską szyjką, np. do kolby Erlenmeyera lub butelki, i dodaj do niego płyn do mycia naczyń (roztwór ten możesz dodatkowo zabarwić, używając np. farbki lub barwnika spożywczego w dowolnym kolorze). Do roztworu z płynem do mycia naczyń wlej drugi z przygotowanych roztworów.
3. Opisywanie reakcji chemicznych
Substancje, które ulegają danej przemianie (reakcji) chemicznej, to substratysubstraty, a substancje powstające w jej wyniku to produktyprodukty. Wszystkie substraty i produkty, uczestniczące w określonej reakcji chemicznej, nazywane są reagentamireagentami.

Reakcje chemiczne możemy opisywać za pomocą odpowiednich równań. Równanie reakcji chemicznejRównanie reakcji chemicznej to matematyczny zapis jej przebiegu, wykorzystujący symbole i wzory chemiczne substancji uczestniczących w danej reakcji, a więc reagentów. Przyjęło się, że w równaniach reakcji, po lewej stronie zapisuje się symbole i wzory substratów, a po prawej stronie – symbole i wzory produktów reakcji. Pomiędzy substratami i produktami umieszcza się strzałkę obrazującą kierunek przebiegu reakcji – od substratów do produktów. Schemat zapisu równania reakcji chemicznej przedstawiono na poniższej grafice.
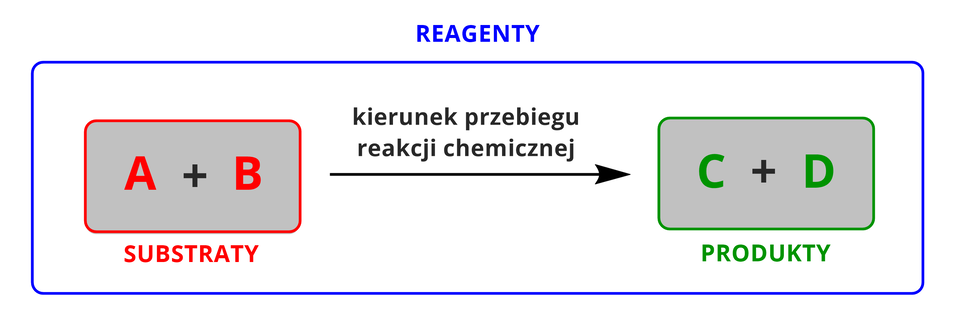
Na powyższym schemacie uwzględniono dwa substraty (A i B) i dwa produkty (C i D) reakcji. W rzeczywistości liczby poszczególnych reagentów mogą być inne, w zależności od rodzaju rozpatrywanej przemiany chemicznej. Dla przykładu, schemat równania reakcji chemicznej, która zachodzi po zmieszaniu wodnych roztworów kwasku cytrynowego i sody oczyszczonej (polecenie ), ma postać:
Strzałka zapisana za nazwą tlenku węgla() oznacza, że substancja ta wydziela się z układu w formie gazu.
Zbadaj zachowanie wody utlenionej (wodnego roztworu nadtlenku wodoru) w obecności soku z ziemniaka. W tym celu wykonaj doświadczenie według załączonej instrukcji i uzupełnij dziennik laboratoryjny.
Zapoznaj się z poniższym opisem doświadczenia, a następnie wykonaj polecenie.
Problem badawczy:
Czy proces, który zachodzi po wprowadzeniu wody utlenionej do soku z ziemniaka, to zjawisko fizyczne, czy przemiana chemiczna?
Hipoteza:
Po wprowadzeniu wody utlenionej do soku z ziemniaka, zachodzi reakcja chemiczna.
Co było potrzebne:
ziemniak średniej wielkości;
woda utleniona;
tarka do warzyw;
krystalizator, talerz lub miska;
dwie zlewki lub szklanki.
Przebieg doświadczenia:
Do jednej ze zlewek wlano około wody utlenionej. Ziemniaka starto na tarce, odciśnięto z niego sok i przelano go do drugiej zlewki. Następnie do soku wlano przygotowaną wcześniej wodę utlenioną.
Obserwacje:
Po wlaniu wody utlenionej do pustej zlewki, nie zaobserwowano objawów reakcji. Po wprowadzeniu wody utlenionej do soku z ziemniaka, wydziela się bezbarwny, bezwonny gaz (lub zawartość naczynia reakcyjnego pieni się).
Zapisz wnioski z przeprowadzonego doświadczenia.
Głównym składnikiem wody utlenionej jest substancja o nazwie nadtlenek wodoru (o wzorze ). Substancja ta samoistnie ulega bardzo powolnej przemianie (rozkładowi) na tlen i wodór. Rozkład ten można jednak przyspieszyć poprzez zastosowanie odpowiednich warunków. Do takich zaliczamy między innymi odpowiednią temperaturę, ciśnienie oraz obecność tak zwanego katalizatorakatalizatora, czyli substancji przyspieszającej przebieg reakcji chemicznej. Wymienione warunki uwzględnia się w zapisie równań reakcji nad strzałką obrazującą kierunek jej przebiegu. Rolę katalizatora w przemianie nadtlenku wodoru pełni zawarty w soku z ziemniaka enzym – katalaza. Schemat równania opisanej reakcji ma postać:
Powyższy zapis (podobnie jak zapis dotyczący polecenia ) to jedynie schemat zapisu równania reakcji chemicznej, w którym podano nazwy jej substratów i produktów. W najbliższym czasie poznasz reguły zapisu samych równań reakcji chemicznych. Dla przykładu, równanie analizowanej w doświadczeniu reakcji chemicznej ma postać:
Woda utleniona wykorzystywana jest jako środek dezynfekujący. Być może miałaś/miałeś okazję przemywać tym preparatem jakieś powierzchowne rany. W kontakcie z krwią, woda utleniona pieni się, podobnie jak to miało miejsce po wprowadzeniu jej do soku z ziemniaka. We krwi (podobnie jak w ziemniaku) zawarta jest bowiem katalaza, czyli enzym umożliwiający rozkład nadtlenku wodoru. W wyniku zachodzącej przemiany chemicznej gwałtownie wydziela się tlen, który to (w uproszczeniu) pełni niejako funkcję bakteriobójczą. Stosowanie wody utlenionej do odkażania świeżych ran nie jest jednak zalecane, ponieważ może utrudniać ich gojenie.
4. Wirtualne laboratoria
Przeprowadź eksperyment w wirtualnym laboratorium chemicznym. Sprawdź, które z odczynników chemicznych dostępnych w laboratorium reagują ze sobą. Zastanów się, które z obserwowanych efektów świadczą o tym, że zachodzi reakcja chemiczna.
Wykonując doświadczenia, uzupełnij dziennik laboratoryjny. Następnie przejdź do rozwiązywania ćwiczeń.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DmAiwUuUC
Analiza Odczynników Chemicznych i Reakcji w Laboratorium
Na podstawie występujących w laboratorium odczynników i sprzętu laboratoryjnego możliwe jest przeprowadzenie reakcji chemicznych oraz zaobserwowanie efektów przeprowadzenia doświadczeń.
1. . Lista odczynników i zastosowanego sprzętu laboratoryjnego
Odczynniki chemiczne:
HCl (aq) - kwas solny (chlorowodorowy) w roztworze wodnym - silny kwas, bezbarwny roztwór
CuSO₄ (aq) - siarczan miedzi(II) w roztworze wodnym - charakterystyczny niebieski roztwór, substancja żrąca
K₂S (aq) - siarczek potasu w roztworze wodnym - roztwór o charakterystycznym zapachu siarkowodoru
Mg - magnez w postaci metalicznej - szary metal o wysokiej aktywności chemicznej.
Sprzęt laboratoryjny:
Kolba stożkowa (Erlenmeyera)
Probówki szklane
Pręciki szklane do mieszania
Palnik gazowy
Termometr (widoczny na ścianie)
Statyw laboratoryjny
Pudełko zapałek
Półka na odczynniki
2. Analiza reaktywności dostępnych odczynników
Na podstawie analizy stwierdzono, że kluczowym czynnikiem decydującym o zachodzeniu reakcji jest szereg napięciowy metali oraz właściwości kwasów i zasad.
Magnez jest metalem wysoce aktywnym chemicznie, znajdującym się w szeregu napięciowym znacznie przed wodorem, co oznacza, że może wypierać wodór z kwasów.
Kwas solny jako silny kwas nieutleniający reaguje z aktywnymi metalami.
Siarczan miedzi jako sól metalu aktywnego może uczestniczyć w reakcjach wymiany z bardziej aktywnymi metalami.
Siarczek potasu jako sól słabego kwasu (H₂S) reaguje z mocnymi kwasami.
3. Reakcje chemiczne:
A. Reakcje zachodzące:
Reakcja 1: Magnez + kwas solny
Mg + 2HCl --> MgCl₂ + H₂↑
Typ: reakcja wymiany pojedynczej
Mechanizm: magnez wypiera wodór z kwasu solnego
Produkty: chlorek magnezu + wodór gazowy
Reakcja 2: Magnez + siarczan miedzi
Mg + CuSO₄ --> MgSO₄ + Cu↓
Typ: reakcja wymiany pojedynczej
Mechanizm: magnez wypiera miedź z jej soli
Produkty: siarczan magnezu + miedź metaliczna
Reakcja 3: Siarczek potasu + kwas solny
K₂S + 2HCl --> 2KCl + H₂S↑
Typ: reakcja wymiany podwójnej
Mechanizm: mocny kwas wypiera słaby kwas z jego soli
Produkty: chlorek potasu + siarkowodór gazowy
Reakcja 4: Siarczek potasu + siarczan miedzi
K₂S + CuSO₄ --> K₂SO₄ + CuS↓
Typ: reakcja wymiany podwójnej (strąceniowa)
Mechanizm: powstanie trudnorozpuszczalnego siarczku miedzi
Produkty: siarczan potasu + siarczek miedzi (osad)
B. Reakcje niezachodzące:
CuSO₄ + HCl - brak reakcji, ponieważ kwas solny nie może wyprzeć mocniejszego kwasu siarkowego z jego soli.
Cu + HCl - brak reakcji, ponieważ miedź w szeregu napięciowym metali znajduje się po wodorze i nie może go wypierać z kwasów nieutleniających.
4. Efekty świadczące o zachodzeniu reakcji chemicznej
Reakcje chemiczne można rozpoznać po charakterystycznych objawach, które można zaobserwować za pomocą zmysłów:
Główne efekty wizualne:
Wydzielanie gazów - pojawienie się pęcherzyków, syczenie, pienienie
Powstanie osadów - wytrącenie substancji stałych o charakterystycznych barwach
Zmiana barwy roztworu - odbarwienie lub zmiana kolorystyki
Rozpuszczanie substancji stałych - zanikanie metali w roztworach kwasów
Efekty termiczne i sensoryczne:
Wydzielanie lub pochłanianie ciepła - reakcje egzo- lub endotermiczne
Charakterystyczne zapachy - wydzielanie gazów o specyficznych zapachach
Efekty dźwiękowe - syczenie, bulgotanie, trzaskanie
Wydzielanie światła - możliwość zapłonu wydzielonych gazów
Konkretne objawy dla reakcji z dostępnymi odczynnikami:
Mg + 2HCl → MgCl₂ + H₂↑
Intensywne wydzielanie bezbarwnych pęcherzyków gazu (wodór)
Syczenie i bulgotanie
Wydzielanie ciepła (reakcja egzotermiczna)
Stopniowe rozpuszczanie się szarego metalu
Możliwość zapłonu wodoru przy kontakcie z płomieniem
Mg + CuSO₄ → MgSO₄ + Cu↓
Wytrącanie czerwonawego, metalicznego osadu (miedź)
Odbarwienie charakterystycznego niebieskiego roztworu CuSO₄
Rozpuszczanie się magnezu
Wydzielanie ciepła
K₂S + 2HCl → 2KCl + H₂S↑
Intensywny, nieprzyjemny zapach zgniłych jaj (siarkowodór)
Wydzielanie bezbarwnego, toksycznego gazu H₂S
Syczenie i pienienie roztworu
Lekkie podgrzanie się mieszaniny reakcyjnej
K₂S + CuSO₄ → K₂SO₄ + CuS↓
Natychmiastowe wytrącenie czarnego osadu (siarczek miedzi)
Zmiana barwy roztworu z niebieskiej na bezbarwną
Powstanie intensywnej mętności
5. Znaczenie praktyczne i zastosowania
Przedstawione reakcje mają istotne znaczenie w praktyce laboratoryjnej i przemysłowej:
Reakcja Mg + HCl wykorzystywana jest do otrzymywania wodoru w warunkach laboratoryjnych
Reakcja Mg + CuSO₄ służy do demonstracji szeregu napięciowego metali
Reakcja K₂S + HCl jest klasyczną próbą na wykrywanie siarczków w analizie jakościowej
Reakcja strąceniowa K₂S + CuSO₄ znajduje zastosowanie w analizie chemicznej i oczyszczaniu roztworów.
Zapoznaj się z poniższym opisem doświadczenia, a następnie wykonaj polecenia.
Hipoteza: Obserwując efekty towarzyszące przemianom substancji, można ustalić, czy w analizowanym układzie zaszła reakcja chemiczna.
Co było potrzebne (sprzęt laboratoryjny i odczynniki):
kolba Erlenmeyera;
zapałki;
termometr szklany (laboratoryjny);
magnez (wiórki);
kwas chlorowodorowy (solny);
siarczan() miedzi() (roztwór wodny);
siarczek potasu (roztwór wodny).
Przebieg doświadczenia:
Próba
W kolbie Erlenmeyera umieszczono niewielką ilość wiórek magnezu.
Następnie do kolby wlano niewielką ilość kwasu chlorowodorowego.
Do wylotu kolby zbliżono zapaloną zapałkę.
W momencie, kiedy obserwowane objawy przemian ustały, do roztworu w kolbie wprowadzono termometr i odczytano temperaturę roztworu.
Próba
Do kolby Erlenmeyera wlano niewielką ilość wodnego roztworu siarczanu() miedzi().
Następnie do kolby wprowadzono niewielką ilość wiórek magnezu.
Próba
Do kolby Erlenmeyera wlano niewielką ilość wodnego roztworu siarczku potasu.
Następnie do kolby wlano niewielką ilość kwasu chlorowodorowego.
Próba
Do kolby Erlenmeyera wlano niewielką ilość wodnego roztworu siarczanu() miedzi().
Następnie do kolby wlano niewielką ilość kwasu chlorowodorowego.
Próba
Do kolby Erlenmeyera wlano niewielką ilość wodnego roztworu siarczanu() miedzi().
Następnie do kolby wlano niewielką ilość wodnego roztworu siarczku potasu.
Próba
Do kolby Erlenmeyera wlano niewielką ilość wodnego roztworu siarczku potasu.
Następnie do kolby wsypano niewielką ilość wiórek magnezu.
Obserwacje:
Próba
Ciało stałe (magnez) stopniowo się roztwarza (zanika). Wydziela się bezbarwny gaz. Po zbliżeniu do wylotu kolby zapalonej zapałki, słychać charakterystyczny trzask. W kolbie pozostaje klarowny, bezbarwny roztwór. Temperatura uzyskanego w kolbie roztworu jest większa niż temperatura roztworu wyjściowego.
Próba
Ciało stałe (magnez) stopniowo się roztwarza (zanika). Wytrąca się różowy osad. Niebieski roztwór się odbarwia.
Próba
Wydziela się bezbarwny gaz o zapachu zgniłych jaj.
Próba
Brak objawów reakcji.
Próba
Wytrąca się czarny osad. Niebieski roztwór się odbarwia.
Próba
Brak objawów reakcji (wiórki magnezu opadają na dno naczynia).
Wnioski:
Obserwacje, odnotowane w opisanych powyżej próbach oznaczonych numerami , , oraz , pozwalają na stwierdzenie, że w czasie prowadzenia doświadczenia zaszły odpowiednie reakcje chemiczne. W przypadku wykonanych prób, oznaczonych numerami i , nie odnotowano objawów, które świadczą o przebiegu reakcji chemicznych, zatem można wnioskować, że w czasie tych doświadczeń przemiany chemiczne nie miały miejsca. Postawiona hipoteza jest zatem prawdziwa – obserwując efekty towarzyszące przemianom substancji, można ustalić, czy w analizowanym układzie zaszła reakcja chemiczna.
Spośród podanych poniżej substancji wybierz i zaznacz wszystkie te, które są substratami opisanej reakcji chemicznej.
Przeprowadź eksperyment w wirtualnym laboratorium chemicznym. Wykorzystując odczynniki dostępne w laboratorium, zaprojektuj doświadczenia ilustrujące zjawiska fizyczne i przemiany chemiczne.
Wykonując doświadczenia, uzupełnij dziennik laboratoryjny. Następnie przejdź do rozwiązywania ćwiczeń.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DmAiwUuUC
Zapoznaj się z poniższym opisem doświadczenia, a następnie wykonaj polecenia.
Hipoteza: Obserwując efekty towarzyszące przemianom substancji, można ustalić, czy analizowanym układzie zaszła reakcja chemiczna, czy przemiana fizyczna.
Co było potrzebne (sprzęt laboratoryjny i odczynniki):
zlewki;
metalowy statyw z łapą;
kolba okrągłodenna;
palnik;
trójnóg;
siatka ceramiczna;
szklana parownica;
szkiełko zegarkowe;
mages;
bagietka laboratoryjna;
łyżka laboratoryjna;
jod (kryształy);
sproszkowana siarka;
żelazo (pył);
azotan() srebra() (roztwór wodny);
chlorek potasu (stały);
lód;
woda destylowana.
Przebieg doświadczenia:
Próba
Wykorzystując łyżkę laboratoryjną, pobrano niewielką ilość jodu i umieszczono go w jednej ze zlewek.
Zlewkę z jodem ustawiono na siatce ceramicznej położonej na trójnogu, nad palnikiem.
W kolbie okrągłodennej (zamontowanej na statywie) umieszczono kostki lodu (tak, by zakryły dno kolby).
Kolbę z lodem obniżono tak, by jej dno zakryło wylot zlewki z jodem.
Zapalono palnik.
Próba
Wykorzystując łyżkę laboratoryjną, pobrano niewielką ilość siarki i umieszczono ją w szklanej parownicy.
Parownicę z siarką ustawiono na siatce ceramicznej położonej na trójnogu, nad palnikiem.
Przygotowano zlewkę z zimną wodą i ustawiono ją obok zmontowanego zestawu.
Zapalono palnik.
W momencie, gdy w parownicy znajdowała się tylko ciecz, wyłączono palnik, a następnie ostrożnie przelano zawartość parownicy do zlewki z zimną wodą.
Uzyskaną substancję wyjęto z wody i odłożono na szkiełko zegarkowe.
Po pewnym czasie sprawdzono wygląd substancji znajdującej się na szkiełku zegarkowym.
Próba
Wykorzystując łyżkę laboratoryjną, pobrano niewielką ilość kostek lodu i umieszczono je w jednej ze zlewek.
Zlewkę z kostkami lodu ustawiono na siatce ceramicznej, położonej na trójnogu, nad palnikiem.
W kolbie okrągłodennej (zamontowanej na statywie) umieszczono kolejną porcję kostek lodu (tak, by zakryły one dno kolby).
Zapalono palnik.
W momencie, gdy zawartość zlewki zaczęła wrzeć, obniżono kolbę z lodem tak, by jej dno zakryło wylot zlewki.
Próba
Do jednej ze zlewek wlano niewielką ilość wody.
Zlewkę z wodą ustawiono na siatce ceramicznej, położonej na trójnogu, nad palnikiem.
W kolbie okrągłodennej (zamontowanej na statywie) umieszczono kilka/kilkanaście kostek lodu (tak, by zakryły one dno kolby).
Zapalono palnik.
W momencie, gdy zawartość zlewki zaczęła wrzeć, obniżono kolbę z lodem tak, by jej dno zakryło wylot zlewki.
Próba
Do zlewki nalano niewielką ilość wody destylowanej.
Za pomocą łyżki laboratoryjnej pobrano z pojemnika niewielką ilość chlorku potasu i wsypano go do zlewki z wodą.
Zawartość zlewki dokładnie wymieszano bagietką.
Po kilku sekundach zlewkę z uzyskanym roztworem ustawiono na siatce ceramicznej, położonej na trójnogu, nad palnikiem.
Zapalono palnik i ogrzewano zawartość zlewki aż pozostała w niej sama substancja stała.
Próba
W jednej ze zlewek umieszczono niewielką ilość wodnego roztworu azotanu() srebra().
Za pomocą łyżki laboratoryjnej pobrano z pojemnika niewielką ilość żelaza i wprowadzono go do zlewki z roztworem.
Próba
W jednej ze zlewek umieszczono niewielką ilość wodnego roztworu azotanu() srebra().
Do drugiej ze zlewek nalano niewielką ilość wody destylowanej.
Za pomocą łyżki laboratoryjnej pobrano z pojemnika niewielką ilość chlorku potasu i wsypano go do zlewki z wodą. Zawartość zlewki dokładnie wymieszano bagietką, a następnie przelano do zlewki z wodnym roztworem azotanu() srebra().
Próba
Wykorzystując łyżkę laboratoryjną, pobrano niewielką ilość siarki i umieszczono ją w szklanej parownicy.
Za pomocą łyżki laboratoryjnej, pobrano niewielką ilość żelaza i przesypano je do parownicy z siarką. Zawartość parownicy wymieszano bagietką.
Do zawartości parownicy zbliżono magnes. Po zaobserwowaniu, że magnes przyciągnął mieszaninę z parownicy (lub któryś z jej składników), zdjęto ją i wprowadzono z powrotem do parownicy.
Parownicę z mieszaniną siarki i żelaza ustawiono na siatce ceramicznej, położonej na trójnogu, nad palnikiem.
Zapalono palnik i ogrzewano zawartość parownicy.
W momencie, gdy w parownicy powstała czarna masa zgaszono palnik. Następnie zdjęto ostrożnie parownicę i odstawiono do wystudzenia.
Po wystudzeniu zawartości parownicy, zbliż do niej magnes.
Obserwacje:
Próba
W czasie ogrzewania, w zlewce pojawiają się fioletowe pary. Po chwili, na dnie kolby okrągłodennej (od strony zlewki) pojawiają się fioletowe kryształy. Część kostek lodu w kolbie przekształca się w bezbarwną ciecz.
Próba
Siarka w trakcie ogrzewania topi się, zmieniając się w ciecz o jasnożółtej barwie. Podczas dalszego ogrzewania, jej barwa zmienia się na ciemnobrunatną. Substancja, uzyskana po przelaniu cieczy do zimnej wody, ma ciemnobrunatne zabarwienie i jest plastyczna. Po pewnym czasie powraca do początkowej postaci – substancji stałej, o żółtej barwie.
Próba
Podczas ogrzewania lód w zlewce stopniowo przekształca się w ciecz. Po chwili ciecz zaczyna wrzeć. Po zakryciu wylotu zlewki kolbą okrągłodenną z lodem, na dnie kolby (od strony zlewki) pojawiają się krople bezbarwnej cieczy, które po chwili „spadają” z powrotem do zlewki. Część kostek lodu w kolbie przekształca się w bezbarwną ciecz.
Próba
Po chwili ogrzewania, woda w zlewce zaczyna wrzeć. Po zakryciu wylotu zlewki kolbą okrągłodenną z lodem, na dnie kolby (od strony zlewki) pojawiają się krople bezbarwnej cieczy, które po chwili „spadają” z powrotem do zlewki. Część kostek lodu w kolbie przekształca się w bezbarwną ciecz.
Próba
Po wprowadzeniu chlorku potasu do wody, otrzymano klarowny bezbarwny roztwór. W czasie ogrzewania, objętość roztworu stopniowo malała. Ostatecznie w zlewce pozostał bezbarwny osad (kryształki).
Próba
Ciało stałe (żelazo) stopniowo się roztwarza. Roztwór w zlewce zabarwia się na żółtopomarańczowo. Wytrąca się srebrzystoszary osad.
Próba
Po wprowadzeniu chlorku potasu do wody, otrzymano klarowny bezbarwny roztwór. Po wymieszaniu roztworów, wytrąca się biały osad (nad osadem znajduje się klarowny bezbarwny roztwór).
Próba
Siarka, po zmieszaniu z żelazem, tworzy mieszaninę barwy szarej. Zbliżony do jej powierzchni magnes przyciąga pył żelaza. Po ogrzaniu, mieszanina się zapala. Żar obejmuje całą mieszaninę. Po zakończeniu żarzenia się, powstaje masa o czarnej barwie. Magnes nie oddziałuje z nią.
Wnioski:
Obserwacje, odnotowane w opisanych powyżej próbach oznaczonych numerami: , , , oraz , pozwalają na stwierdzenie, że w czasie prowadzenia doświadczenia zaszły wyłącznie przemiany fizyczne. Obserwacje, wykonane w przypadku wykonanych prób oznaczonych numerami , i , świadczą o przebiegu reakcji chemicznych (przy czym w próbach i miały miejsce także przemiany fizyczne – rozpuszczanie chlorku potasu w wodzie, przygotowywanie mieszaniny siarki z żelazem i rozdzielanie tej mieszaniny za pomocą magnesu). Postawiona hipoteza jest zatem prawdziwa – obserwując efekty towarzyszące przemianom substancji, można ustalić, czy w analizowanym układzie zaszła reakcja chemiczna, czy przemiana fizyczna.
Przeanalizuj schemat opisanej reakcji chemicznej i spośród podanych poniżej stwierdzeń wybierz wszystkie te, które są prawdziwe.
azotanu(pięć) srebra(jeden) zachodzi reakcja chemiczna.
Słownik
proces, w wyniku którego zmieniają się właściwości fizyczne substancji (np. ich stan skupienia); w wyniku przemian fizycznych nie powstają nowe substancje chemiczne
proces, w którym z jednej lub kilku substancji powstaje jedna lub więcej nowych substancji o właściwościach odmiennych od substancji wyjściowych
(łac. corrosio „zżeranie”) proces niszczenia materiałów, zachodzący pod wpływem reakcji chemicznych, przebiegających na granicy ze środowiskiem zewnętrznym; przykładami korozji są rdzewienie stalowych przedmiotów i czernienie przedmiotów wykonanych ze srebra
substancje, których roztworu zmieniają barwę na skutek zmiany odczynu roztworu
reakcja, w wyniku której do otoczenia wydzielane jest ciepło
reakcja, do której przebiegu potrzebne jest ciepło; układ reakcyjny pochłania energię (ciepło) z otoczenia
substancje, które biorą udział w przemianie chemicznej (ulegają przemianie chemicznej)
substancje, które powstają w wyniku reakcji chemicznej
substancje, które uczestniczą w reakcji chemicznej; reagentem jest każdy substrat i każdy produkt danej reakcji chemicznej
matematyczny zapis przebiegu reakcji chemicznej za pomocą symboli i wzorów chemicznych; przedstawia substraty i produkty reakcji oraz często warunki zachodzenia danej reakcji; w równaniach reakcji, po lewej stronie zapisuje się symbole i wzory substratów, a po prawej stronie symbole i wzory produktów reakcji; pomiędzy substratami a produktami umieszcza się strzałkę obrazującą kierunek przebiegu reakcji – od substratów do produktów (nad strzałką można zapisać warunki przebiegu reakcji, np. ogrzewanie)
w uproszczeniu: substancja, która po dodaniu do układu reakcyjnego przyspiesza przebieg zachodzącej w nim reakcji chemicznej
Ćwiczenia
Poniżej zapisano schematy równań czterech reakcji chemicznych:
sód woda wodorotlenek sodu wodór;
węgiel tlen tlenek węgla();
azot wodór amoniak;
węglan wapnia tlenek wapnia tlenek węgla().
chemicznych (od jeden do cztery).
Pozostawione w otwartej butelce wino, po pewnym czasie kwaśnieje. Dzieję się tak, ponieważ zawarty w winie etanol, pod wpływem tlenu zawartego w powietrzu (oraz odpowiednich bakterii), przekształca się w kwas octowy (etanowy). Drugim z produktów opisanego procesu jest woda. Proces ten to tak zwana fermentacja octowa. Wykorzystuje się go między innymi w produkcji octu winnego.
Zadaniem ucznia było sprawdzenie czy zmieszanie sody oczyszczonej i octu będzie skutkowało przebiegiem reakcji chemicznej, czy też będzie to przemiana fizyczna.
Uczeń przeprowadził doświadczenie, które zilustrował za pomocą schematycznego rysunku.
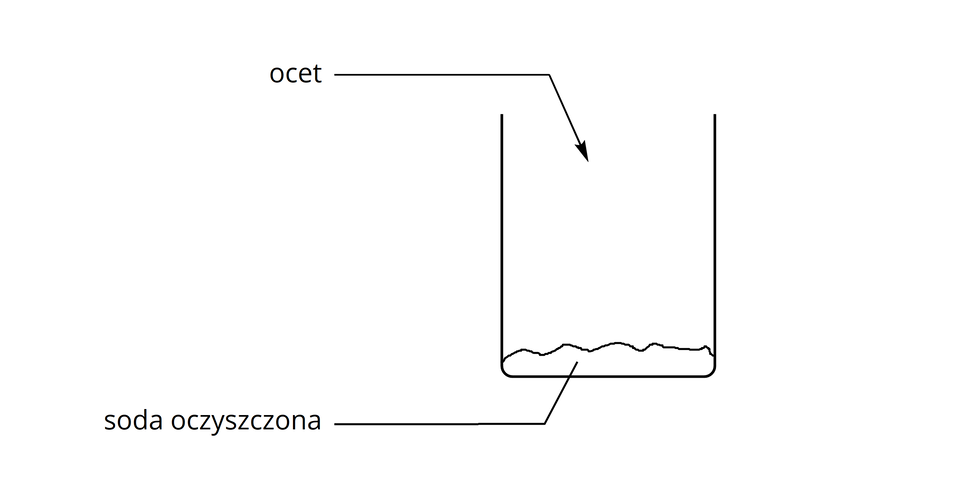
Napisz, jakie obserwacje powinien odnotować uczeń podczas wykonywania doświadczenia. Następnie sformułuj odpowiedni wniosek.
Uczeń przeprowadził doświadczenie, które polegało na dodaniu octu do znajdującej się w zlewce sody oczyszczonej.
Uczeń przeprowadził eksperyment zilustrowany na poniższym schemacie.

Uczeń przeprowadził eksperyment, polegający na wprowadzeniu białka oraz żółtka jaja kurzego do zlewki z octem.
Physical transformations are often associated with a change in the state of matter of a given chemical substance. Complete the diagram below by dragging to the indicated places the names of appropriate processes that result in a change in the state of matter of the substance.
Physical transformations are often associated with a change in the state of matter of a given chemical substance. Match the names of the processes (written in English) to the pairs of states of matter between which they occur.
Bibliografia
Encyklopedia PWN
Krzeczkowska M., Loch J., Mizera A., Repetytorium chemia. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko‑Biała 2010.
Szczypiński R., Projektowanie doświadczeń chemicznych, Warszawa 2019.


