Alkany - właściwości fizyczne i chemiczne
Poniższy materiał stanowi uzupełnienie treści zawartych w materiale: https://zpe.gov.pl/a/wlasciwosci-alkanow/Dw3ToRi0J
Czy wiesz, jaki gaz spalany jest podczas używania palników w kuchence gazowej? Najczęściej taka kuchenka podłączona jest do gazu ziemnegogazu ziemnego z sieci, którego głównym składnikiem, stanowiącym około , jest metan. To najprostszy alkan zbudowany z jednego atomu węgla i czterech atomów wodoru, jest gazem łatwopalnym i spala się niebieskim płomieniem. Czy wiesz, jakie produkty powstają w wyniku reakcji spalania metanu?
charakterystykę węglowodorów nasyconych i grupę węglowodorów, którą do nich zaliczamy;
sposób tworzenia wzorów sumarycznych alkanów i ich nazewnictwo;
sposób zapisu wzorów strukturalnych i półstrukturalnych (grupowych) alkanów.
badać i opisywać właściwości fizyczne alkanów;
analizować zależności pomiędzy długością łańcucha węglowego a właściwościami fizycznymi alkanów;
badać i opisywać właściwości chemiczne alkanów;
zapisywać równania reakcji spalania alkanów.
AlkanyAlkany należą do grupy węglowodorów nasyconych, czyli związków węgla i wodoru, w których pomiędzy atomami węgla występują wyłącznie wiązania pojedyncze. Charakteryzują się wzorem ogólnym:
gdzie n stanowi liczbę atomów węgla, dlatego pierwszy alkan w szeregu homologicznym alkanówszeregu homologicznym alkanów ma wzór , a kolejne: , , , itd.
AlkanyAlkany pod względem właściwości fizycznychwłaściwości fizycznych wykazują wiele podobieństw, ale również różnic. Przeanalizujmy zatem poniższą tabelę i sprawdźmy, czym wybrane alkany różnią się od siebie.
W poniższej tabeli przedstawiono wybrane właściwości fizyczne niektórych alkanów:
Wzór sumaryczny alkanu | Nazwa systematyczna | Masa cząsteczkowa | Gęstość | Temperatura wrzenia | Temperatura topnienia | Stan skupienia w warunkach normalnych |
|---|---|---|---|---|---|---|
metan | gaz | |||||
etan | gaz | |||||
propan | gaz | |||||
butan | gaz | |||||
pentan | ciecz | |||||
oktan | ciecz | |||||
heksadekan | ciało stałe | |||||
ikozan | ciało stałe |
Analizując wartości w powyższej tabeli, możemy zauważyć, że wraz ze wzrostem długości nierozgałęzionego łańcucha węglowego alkanów wzrasta zarówno ich gęstość, jak i temperatury wrzenia i topnienia. W związku z tym zmienia się również ich stan skupienia – od gazowego, przez ciekły po stały. Zmiany właściwości fizycznych są wynikiem wzrostu mas cząsteczkowych w szeregu homologicznym nierozgałęzionych alkanów. Im dłuższe łańcuchy węglowe (większe masy cząsteczkowe), tym więcej oddziaływań pomiędzy cząsteczkami (sił van der Waalsa), zatem większe ich uporządkowanie. Pamiętajmy bowiem, że największe uporządkowanie cząsteczek obserwujemy w stanie stałym, mniejsze w stanie ciekłym, a najmniejsze w stanie gazowym. Dlatego alkany o najkrótszych, nierozgałęzionych łańcuchach węglowych (najniższych masach cząsteczkowych, czyli alkany od do atomów węgla w cząsteczce) to gazy, te o średniej długości łańcuchach węglowych (alkany od do atomów węgla w cząsteczce) to ciecze, a te o najdłuższych łańcuchach węglowych (alkany, w których jest powyżej atomów węgla) to ciała stałe. Ponadto należy pamiętać, że im dłuższe łańcuchy węglowe alkanów, tym należy dostarczyć więcej energii, aby rozerwać oddziaływania międzycząsteczkowe, co z kolei wiąże się ze zmianą stanu skupienia.
W jaki sposób określić stan skupienia danego związku chemicznego, analizując jego temperaturę topnienia i wrzenia?
Przeanalizuj poniższy przykład, a następnie rozwiąż ćwiczenie. Pewien alkan charakteryzuje się temperaturą wrzenia równą , a temperaturą topnienia równą . W jakim stanie skupienia występuje ten związek w temperaturze pokojowej () i pod ciśnieniem normalnym ()?
Krok
Narysuj oś i zaznacz na niej wartości temperatury topnienia i wrzenia.
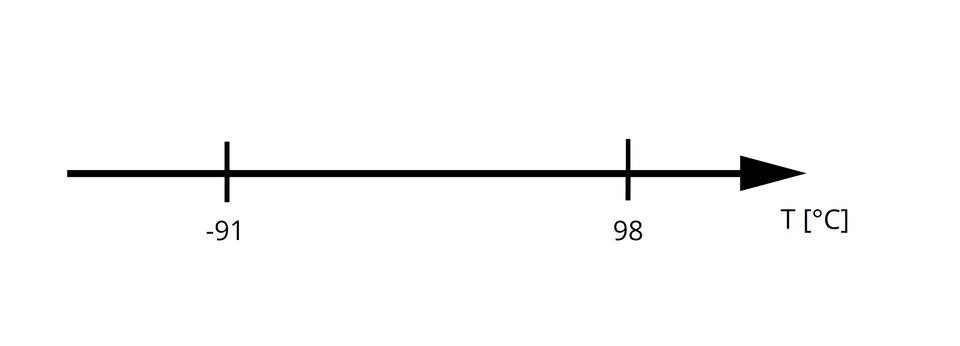
Krok
Wrzenie to zmiana stanu skupienia z ciekłego na gazowy, a topnienie to zmiana stanu skupienia ze stałego na ciekły. Dlatego poniżej temperatury omawiany alkan występuje w postaci ciała stałego, powyżej jest gazem. Pomiędzy tymi wartościami temperatur alkan ten jest cieczą. Zaznacz te informacje na osi.
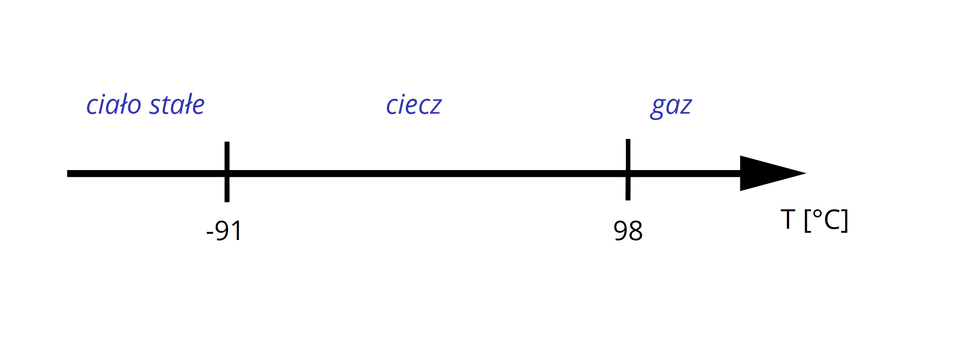
Krok
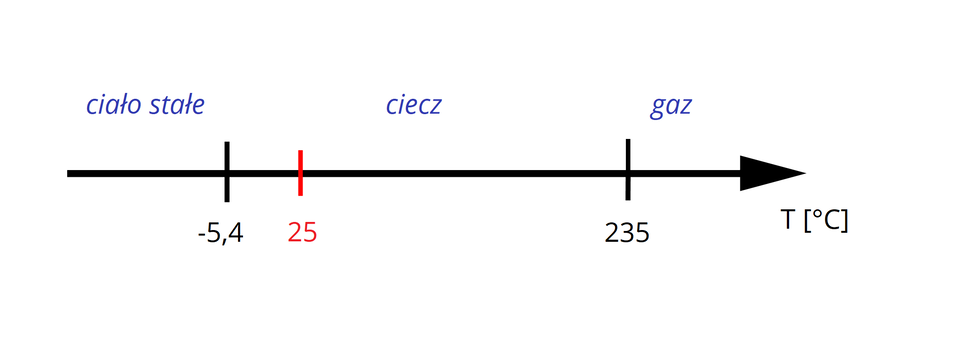
Zaznacz na osi szukaną temperaturę i odczytaj stan skupienia alkanu.
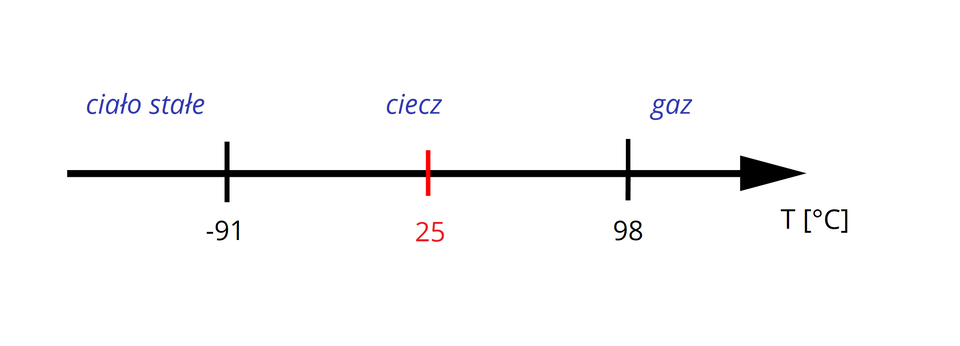
Zatem szukany alkan w temperaturze równej jest cieczą.
Zapisz, w jakim stanie skupienia występuje omówiony alkan w temperaturze równej .
Do właściwości fizycznych alkanów należy również ich rozpuszczalność w różnych rozpuszczalnikach. Substancje polarne, czyli takie, w których występują przede wszystkim wiązania jonowe i kowalencyjne spolaryzowane, z reguły dobrze rozpuszczają się w rozpuszczalnikach polarnych, takich jak np. woda, etanol czy metanol. Substancje niepolarne, czyli takie, w których występują przede wszystkim wiązania kowalencyjne niespolaryzowane, z reguły dobrze rozpuszczają się w rozpuszczalnikach niepolarnych, takich jak np. benzyna czy nafta (które stanowią mieszaninęmieszaninę ciekłych węglowodorów). Warto pamiętać zatem zasadę „podobne rozpuszcza się w podobnym”. Dlatego też alkany bardzo słabo rozpuszczają się w wodzie, a bardzo dobrze w ciekłych węglowodorach (alkanach) czy innych rozpuszczalnikach organicznych.

Heksan z wodą tworzą mieszaninę niejednorodnąmieszaninę niejednorodną. Ten pierwszy jest rozpuszczalnikiem niepolarnym, a drugi – polarnym. Substancje te nie mieszają się ze sobą. Z kolei heksan z naftą (mieszaniną węglowodorów, których cząsteczki zawierają od do atomów węgla) tworzą mieszaninę jednorodnąmieszaninę jednorodną, gdyż obie stanowią substancje niepolarne.
Do właściwości chemicznychwłaściwości chemicznych alkanów zaliczamy przede wszystkim ich palność. Wszystkie alkany są palne, a produkty ich spalania zależą od dostępności tlenu. Przy nieograniczonym dostępie powietrza (tlenu) następuje spalanie alkanów do tlenku węgla(). Jest to spalanie całkowite.
Przy ograniczonym dostępie powietrza (tlenu) następuje spalanie węglowodorów do węgla, czyli sadzy. Jest to jeden z typów spalania niecałkowitego.
Możliwe jest również spalanie węglowodorów do tlenku węgla(), czyli czadu. Jest to drugi rodzaj spalania niecałkowitego.
Wirtualne laboratorium
Alkany charakteryzują się różnymi wartościami temperatur wrzenia. Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym polegające na zbadaniu temperatur wrzenia wybranych alkanów. Czy długość łańcucha węglowego alkanu ma wpływ na jego temperaturę wrzenia? Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Zapoznaj się z opisem doświadczenia zamieszczonym poniżej, a następnie wykonaj polecenia.
Hipoteza:
Im dłuższy łańcuch węglowy alkanu, tym wyższa temperatura wrzenia.
Sprzęt laboratoryjny:
mieszadło magnetyczne z funkcją grzania;
kamyczki wrzenne;
termometr;
kolba okrągłodenna;
chłodnica;
kolba płaskodenna;
cylinder miarowy;
łyżeczka.
statyw.
Odczynniki chemiczne:
pentan;
heksan;
heptan;
oktan;
nonan;
dekan.
Przebieg eksperymentu:
Do kolby okrągłodennej odmierzono za pomocą cylindra miarowego pięćdziesiąt wybranego alkanu. Następnie dodano do kolby kamyczki wrzenne. W kolejnym kroku umieszczono kolbę w płaszczu grzejnym znajdującym się w zamontowanym zestawie. Następnie odkręcono wodę i włączono ogrzewanie kolby. Dalej obserwowano moment, w którym ciecz zaczęła parować, a następnie pary zaczęły się skraplać. Odczytano temperaturę na wyświetlaczu i zanotowano ją.
Obserwacje:
Pentan zaczął wrzeć w temperaturze .
Heksan zaczął wrzeć w temperaturze .
Heptan zaczął wrzeć w temperaturze .
Oktan zaczął wrzeć w temperaturze .
Nonan zaczął wrzeć w temperaturze .
Dekan zaczął wrzeć w temperaturze .
Wyniki:
Im dłuższy łańcuch węglowy alkanu, tym wyższa temperatura wrzenia.
Wnioski:
Hipoteza została potwierdzona.
Aplikacja
Słownik
mieszanina gazowych węglowodorów, w tym przede wszystkim metanu i etanu;
Związki węgla i wodoru, należące do węglowodorów nasyconych, czyli takich, w których pomiędzy atomami węgla występują wyłącznie wiązania pojedyncze
zestawienie alkanów uporządkowanych według zwiększającej się liczby atomów węgla w cząsteczce. W szeregu tym każdy następny węglowodór różni się od poprzedniego o jeden atom węgla i dwa atomy wodoru
charakterystyczne cechy danej substancji, takie jak: stan skupienia, barwa, rozpuszczalność (rozpuszczanie to zjawisko fizyczne), przewodnictwo elektryczne, przewodnictwo cieplne, temperatury wrzenia i topnienia, twardość, kruchość, kowalność, połysk, gęstość, właściwości magnetyczne
cechy substancji, które można określić na podstawie jej zachowania wobec innych substancji; do właściwości chemicznych zaliczamy między innymi: palność, reaktywność, zapach, smak
Jest to układ składający się z co najmniej dwóch substancji zmieszanych w dowolnych proporcjach, np. siarki i oleju, piasku i magnezu
Jest to układ składający się z co najmniej dwóch substancji, których nie można odróżnić gołym okiem lub za pomocą prostych przyrządów optycznych, takich jak np. lupa bądź woda z sokiem z malin
Jest to układ składający się z co najmniej dwóch substancji, które można odróżnić gołym okiem lub za pomocą prostych przyrządów, takich jak np. lupa bądź woda z oliwą z oliwek
Ćwiczenia
Gazowe alkany zbiera się najczęściej do probówki umieszczonej do góry dnem, wypełnionej wodą i umieszczonej w krystalizatorze z wodą w sposób, jaki przedstawiono na poniższym rysunku.
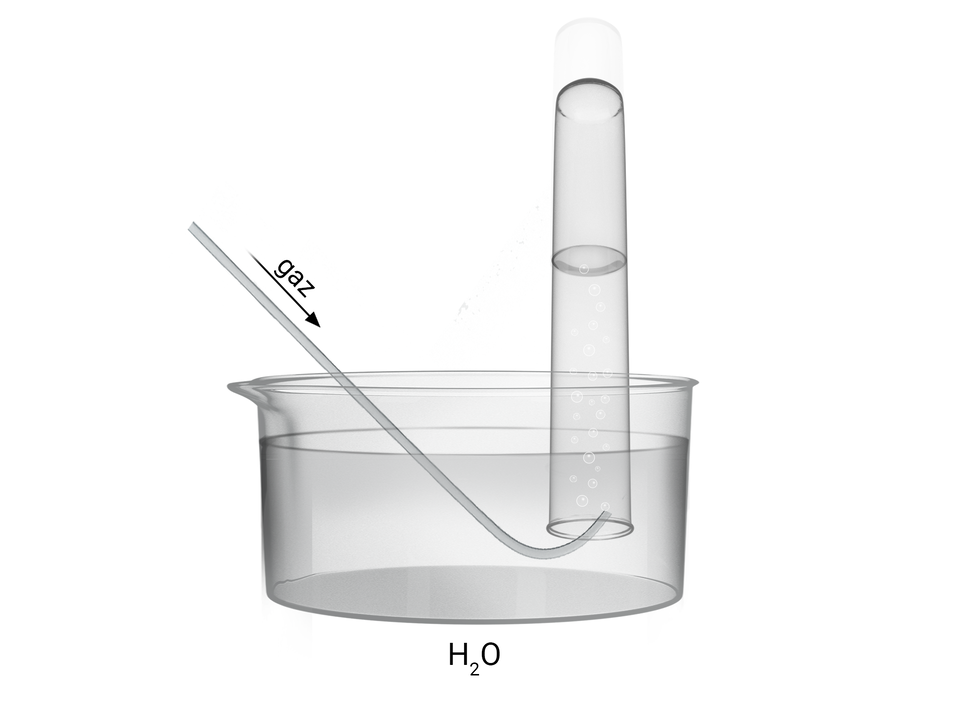
Gazowe alkany zbiera się najczęściej do probówki umieszczonej do góry dnem, wypełnionej wodą i umieszczonej w krystalizatorze z wodą. Do probówki włożona jest rurka, przez którą wprowadzany jest gaz.
Na poniższym schematycznym rysunku przedstawiono mieszaninę dwóch substancji. Która lub które z poniższych mieszanin mogły znaleźć się w probówce?
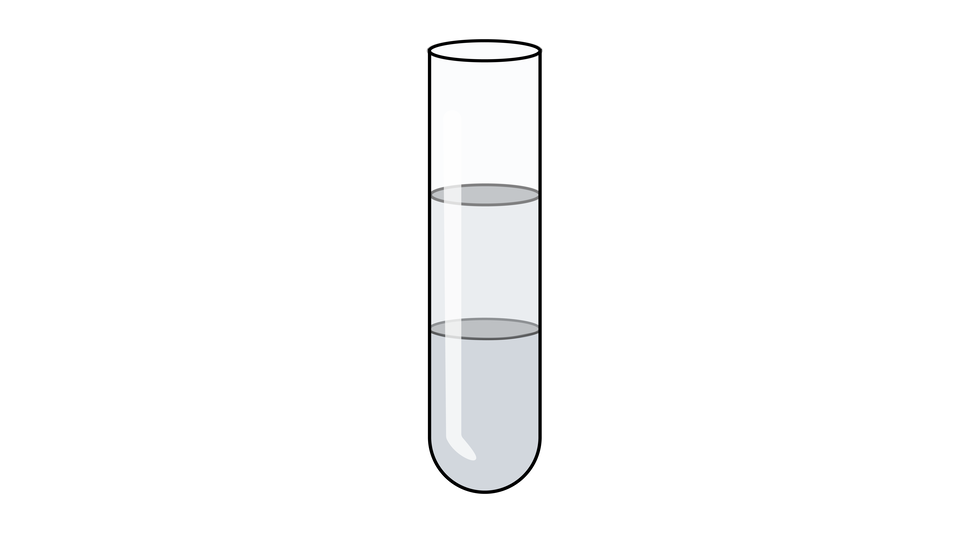
W probówce znajduje się mieszanina dwóch substancji, które nie mieszają się ze sobą, tworząc dwie warstwy.
Analizują budowę cząsteczek alkanów, wskaż zależność pomiędzy długością łańcucha węglowego a ich gęstością, temperaturą wrzenia i topnienia.
Zapalniczki gazowe zawierają w zbiorniczkach butan w stanie skroplonym. Po naciśnięciu przycisku (spustu), butan w postaci gazowej wydostaje się na zewnątrz. Otwiera się wówczas zaworek zbiornika, a ciśnienie powoduje wyrzucanie gazu i jego zmieszanie z powietrzem.
Przeprowadzono doświadczenie chemiczne, w których sprawdzano palność butanu. W tym celu napełniano probówkę butanem z zapalniczki przez kilkanaście sekund. Probówkę z gazem trzymano ustawioną do góry dnem. Następnie przystawiono do wylotu probówki źródło ognia. Pojawił się wówczas pomarańczowy płomień u wylotu probówki, a jej wnętrze pokryło się czarnym osadem. Zapisz równanie reakcji, która zaszła.
Bibliografia
Bielański A., Podstawy chemii nieorganicznej, Warszawa, 2022.
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy siódmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy siódmej szkoły podstawowej, Mac Edukacja 2020.
Jones L., Atkins P., Leroy L., Warszawa 2020, wyd. 2.