Budowa atomu
Czy możliwe jest, że już dwa i pół tysiąca lat temu ktoś wpadł na pomysł, że wszystko składa się z maleńkich, niepodzielnych cząstek? Choć nie mieli mikroskopów ani laboratoriów, starożytni myśliciele zaczęli snuć odważne wizje budowy materii. Z czasem, dzięki naukowcom takim jak Dalton, Thomson czy Bohr, te idee przekształciły się w coraz dokładniejsze modele atomu. Historia teorii atomistycznych to nie tylko zbiór nazwisk i dat – to opowieść o ludzkiej ciekawości, błędach, poprawkach i wielkich odkryciach, które doprowadziły nas do dzisiejszego rozumienia tego, czego nie widać gołym okiem.
Teorie atomistyczne i ich twórcy
Ostatecznie, dokładna fizyczna natura atomów wyłoniła się z serii eksperymentów przeprowadzonych w latach –. Jednym z najbardziej wyrazistych osiągnięć był słynny eksperyment rozpraszania promieniowania alfa, przeprowadzony w roku przez Ernesta Rutherforda.
Rutherford ustalił, że prawie cała masa atomu jest zawarta w maleńkim (a zatem niezwykle gęstym) jądrze, które niesie dodatni ładunek elektryczny.
Budowa atomu
Jądro jest centralną częścią każdego atomu. Posiada ładunek dodatni.
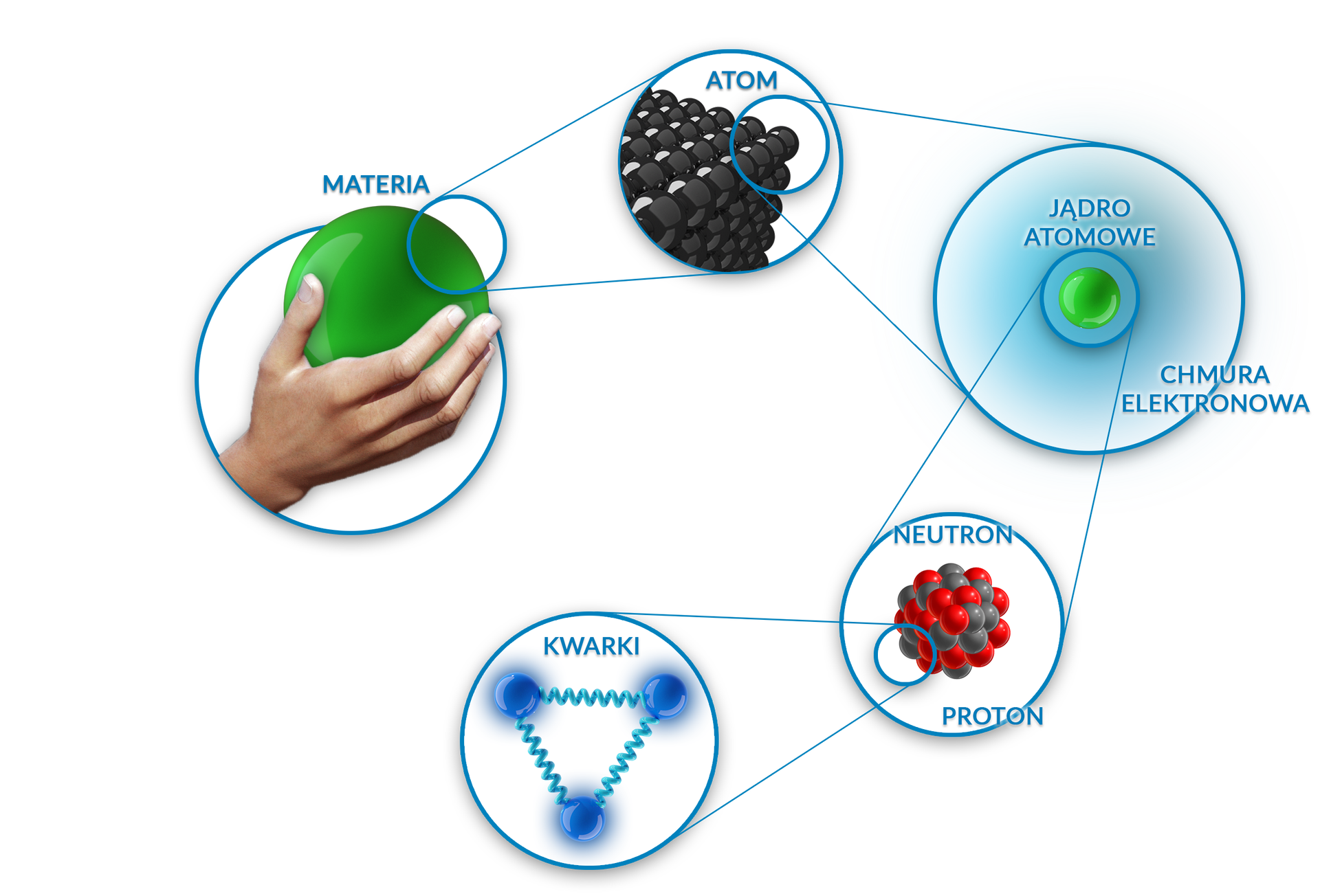
Atom jako całość jest elektrycznie obojęny. Dodatni ładunek jądra równoważony jest przez otaczające jądro elektrony, które tworzą tzw. chmurę elektronową.

Jądro atomu zbudowane jest z protonów oraz neutronów.
Protony są nośnikami dodatniego ładunku elektrycznego w jądrze. Neutron nie zawiera ładunku elektrycznego, a jego masa jest prawie taka sama jak masa protonu.
Znajdujące się w przestrzeni wokół jądra elektrony mają ładunek ujemny. Oznacza to, że w każdym (elektrycznie obojętnym) atomie liczba protonów w jądrze (często określana jako ładunek jądrowy) jest równoważona przez tę samą liczbę elektronów poza jądrem.
W poniższej tabeli przedstawiono właściwości elektronów, protonów i neutronów.
Cząstka | Ładunek | Symbol | Masa | Promień |
|---|---|---|---|---|
elektron | mniej niż | |||
proton | ||||
neutron |
Czy protony i neutrony są cząstkami elementarnymi?
Cząstki elementarne to cząstki, które według współczesnej fizyki (głównie Modelu Standardowego) nie mają żadnej wewnętrznej struktury — są fundamentalnymi składnikami materii i oddziaływań. Innymi słowy, nie da się ich „rozłożyć” na mniejsze składniki (przynajmniej na obecnym poziomie wiedzy).
Protony i neutrony posiadają wewnętrzną strukturę. Nie są więc cząstkami elementarnymi. W skład każdego z nich wchodzą trzy cząstki – kwarki.
Istnieją tzw. trzy pokolenia kwarków: górne i dolne (pokolenie ), dziwne i powabne (pokolenie ), prawdziwe i piękne (pokolenie ).
W skład zwykłej materii wchodzą jedynie kwarki górne i dolne. Proton złożony jest z trzech kwarków: dwóch górnych i jednego dolnego, a neutron z dwóch dolnych i jednego górnego. Kwarki górne mają ładunek dodatni ładunku protonu, a kwarki dolne ładunek ujemny ładunku protonu. Inne cząstki, które zawarte są we wnętrzu protonów i neutronów, to gluony. Ich zadaniem jest utrzymywanie kwarków razem.
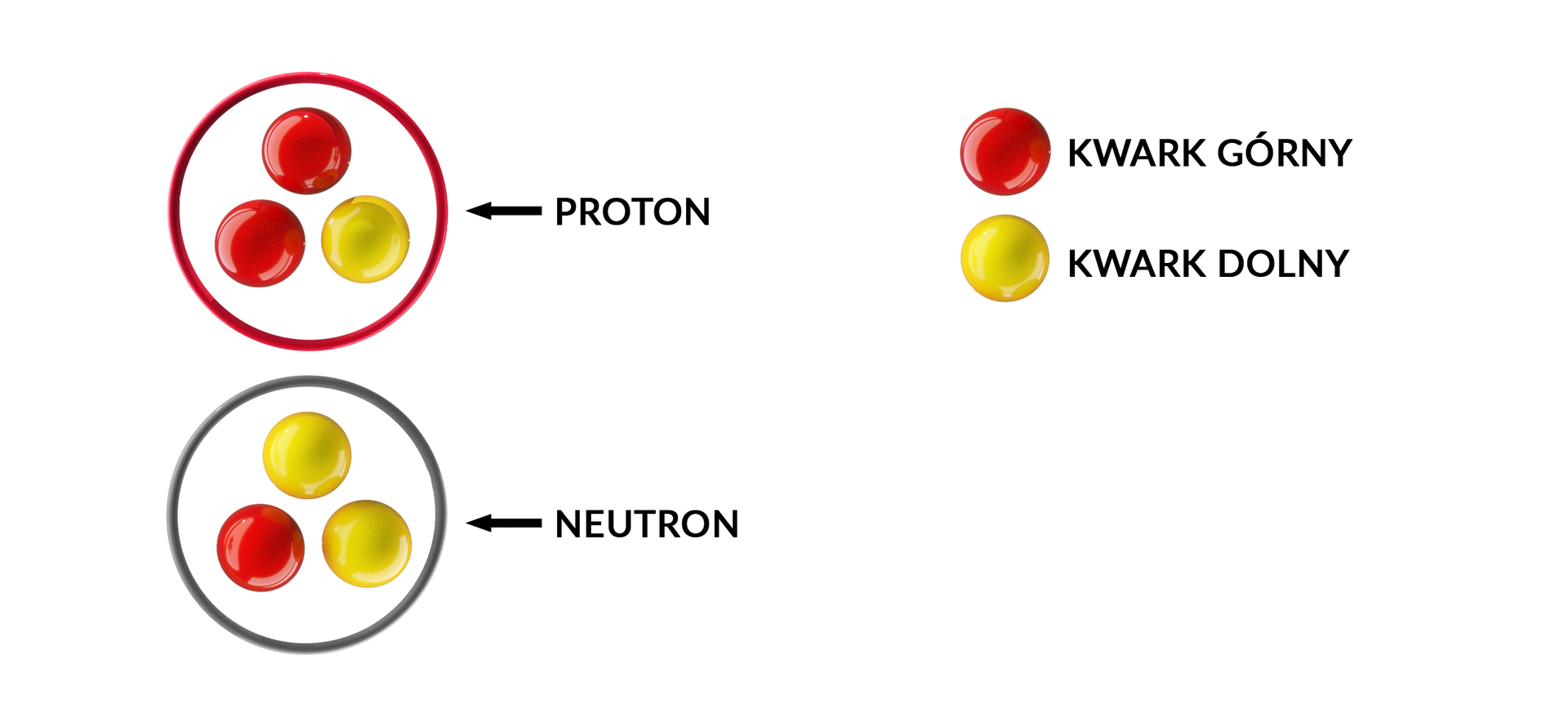
Zapoznaj się z poniższym multimedium, a następnie rozwiąż ćwiczenia.
Zapoznaj się z opisami multimedium, a następnie rozwiąż ćwiczenia.
Czy wszystkie atomy są identyczne?
Nie, nie wszystkie atomy są identyczne – choć każdy atom ma podobną budowę (jądro + chmura elekrtonowa), różnią się liczbą protonów, neutronów i elektronów, a co za tym idzie – właściwościami chemicznymi i fizycznymi.
Te atomy, które mają taką samą liczbe protonów w jądrze tworzą określony pierwiastek chemiczny
Pierwiastek chemiczny
Wszystkie atomy danego pierwiastka mają taką samą liczbę protonów w swoim jądrze. Na przykład, wszystkie atomy wodoru – gdziekolwiek we wszechświecie – mają jeden proton. Wszystkie atomy helu mają dwa protony. Wszystkie atomy tlenu mają osiem protonów.
Chemicy używają terminu liczba atomowa (symbol ) w odniesieniu do liczby protonów w jądrze każdego atomu pierwiastka. Jądro atomu zawiera także neutrony. W rzeczywistości masa atomu wynika z połączonych mas jego protonów i neutronów. Dlatego liczba masowa elementu (symbol ) to całkowita liczba protonów i neutronów w jądrze jednego z jego atomów. Każdy proton lub neutron jest liczony jako jedna jednostka liczby masowej. Na przykład atom tlenu, który ma osiem protonów i osiem neutronów w swoim jądrze, ma liczbę masową . Atom uranu, który ma protony i neutronów, ma liczbę masową .
Informację o liczbie protonów i neutronów atomu danego pierwiastka często podsumowuje się za pomocą notacji chemicznej, którą pokazano poniżej:
– liczba masowa;
– liczba atomowa;
E – symbol pierwiastka.
Wskaż rolę oddziaływania silnego w utrzymywaniu stabilności jądra atomowego.
Antymateria
Większość cząstek elementarnych posiada również swoje odpowiedniki zwane antycząstkami. Antycząstki charakteryzują się takimi samymi cechami jak cząstki, ale mają przeciwny ładunek. Antyproton posiada ładunek ujemny, a antyelektron (pozyton) ma ładunek dodatni. W pewnych warunkach istnieje możliwość laboratoryjnego wytworzenia tych cząstek. Antyprotony wraz z otaczającymi ich pozytonami tworzą tzw. antymaterię.