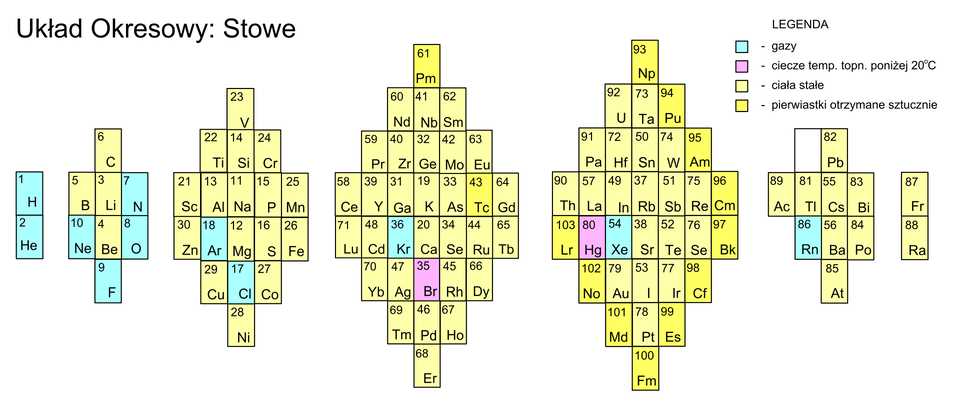
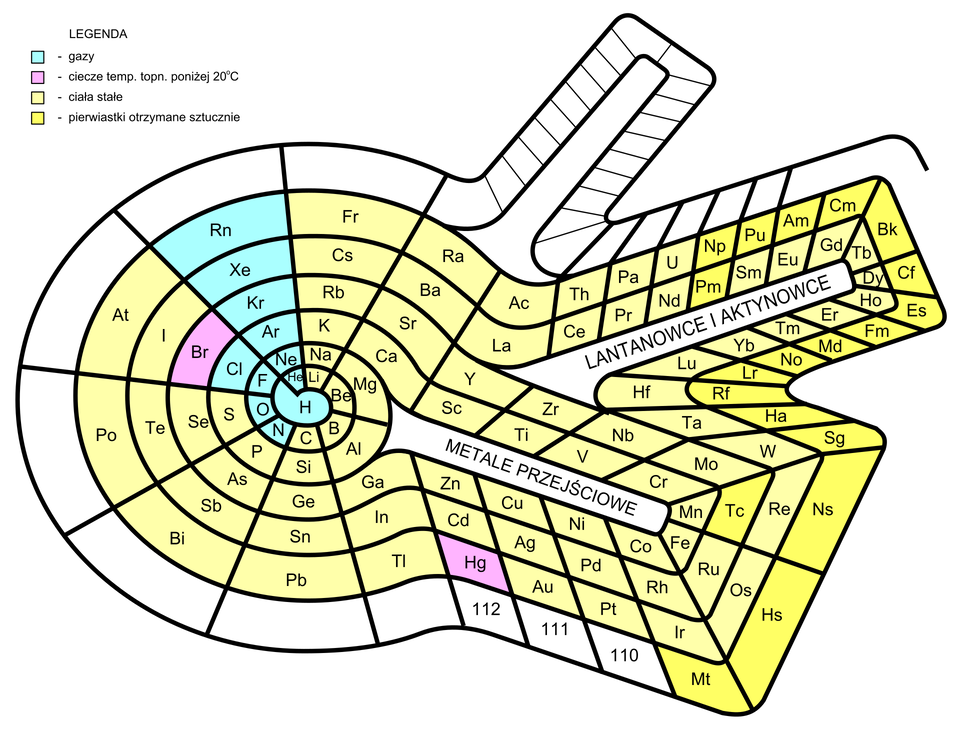
Jak zbudowany jest układ okresowy
Jak klasyfikowano pierwiastki chemiczne?
to czas, kiedy uczeni znali już kilkadziesiąt pierwiastków chemicznych. Były one już przez nich wówczas zbadane i opisane. Ówcześni naukowcy zauważyli, że wśród pierwiastków są takie, które wykazują podobne właściwości. Poszukiwali więc klucza, wg którego mogliby je uporządkować i sklasyfikować. Zauważyli, że jeśli ułoży się je w szeregu, zgodnie ze wzrastającą masą atomową, to na początku co ósmy, a potem co osiemnasty pierwiastek wykazuje podobne cechy. To spostrzeżenie pozwoliło jednemu z uczonych sformułować ogólne prawo, które nazwano prawem okresowości (na cześć twórcy Dymitra MendelejewaDymitra Mendelejewa – prawem okresowości Mendelejewa).
W poniższej animacji ukazano w skrócie, jak wyglądały pierwsze próby uporządkowania pierwiastków chemicznych, znanych już w
W poniższym filmie przedstawiono aktualny układ okresowy pierwiastków chemicznych. Jego dokładny opis znajduje się pod filmem. Po odtworzeniu filmu, zapoznaj się z opisem.

Film dostępny pod adresem /preview/resource/RG7AOREF9VLF5
W filmie opisano historię systematyki pierwiastków. Przedstawiono chemików, którzy zajmowali się systematyzacją pierwiastków, byli to: Johann Wolfgang Döbereiner, John Alexander Reina Newlands, Dymitr Mendelejew oraz Julius Lothar Meyer.
Opis układu okresowego pierwiastków chemicznych. Kliknij, aby rozwinąć opis.
Obecny wygląd układu okresowego różni się od tego, który zaproponował Mendelejew. Na podstawie odkrycia i analizy budowy jądra atomowego oraz badań nad widmami rentgenowskimi, emitowanymi przez znane pierwiastki chemiczne, stwierdzono, że lepszym kryterium, wg którego należy uporządkować pierwiastki chemiczne, jest liczba protonów w jądrze atomowym (liczba atomowaliczba atomowa). Dlatego też współcześnie funkcjonuje inna niż za czasów Mendelejewa treść prawa okresowościprawa okresowości.
Prawo okresowości — właściwości pierwiastków chemicznych, uszeregowane wg rosnącej liczby atomowej , powtarzają się okresowo.
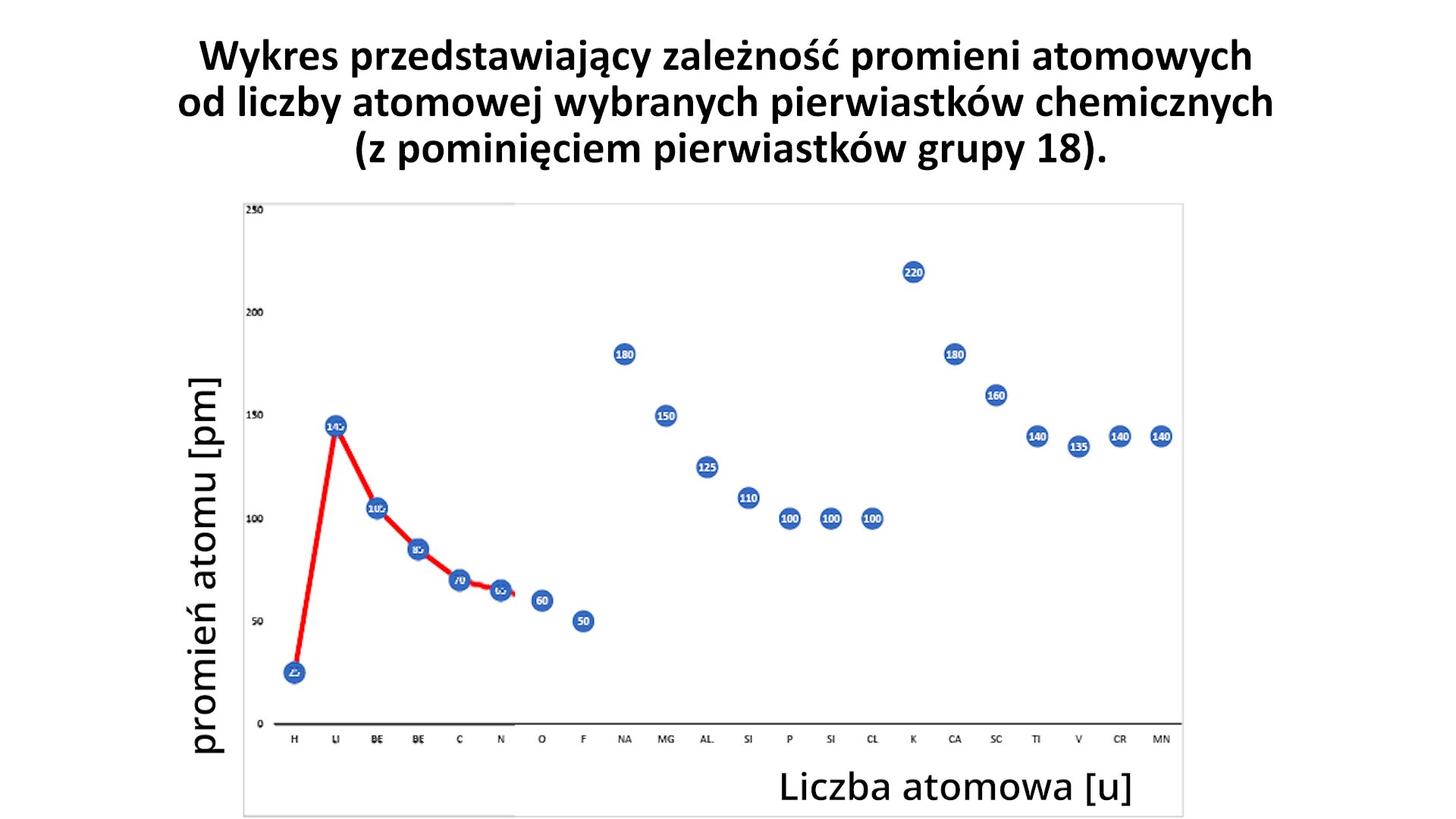
W poniższej animacji ukazano odzwierciedlenie prawa okresowości w długościach promieni atomowych wybranych pierwiastków chemicznych.
Film dostępny pod adresem /preview/resource/R1MTPTV3AVSNU
Na filmie ukazano pierwiastki uporządkowane według wzrastającej liczby atomowej. Na wykresie przedstawiono zależność pomiędzy długością promieni atomowych a liczbą atomową pierwiastków.
Jak zbudowany jest współczesny układ okresowy pierwiastków?
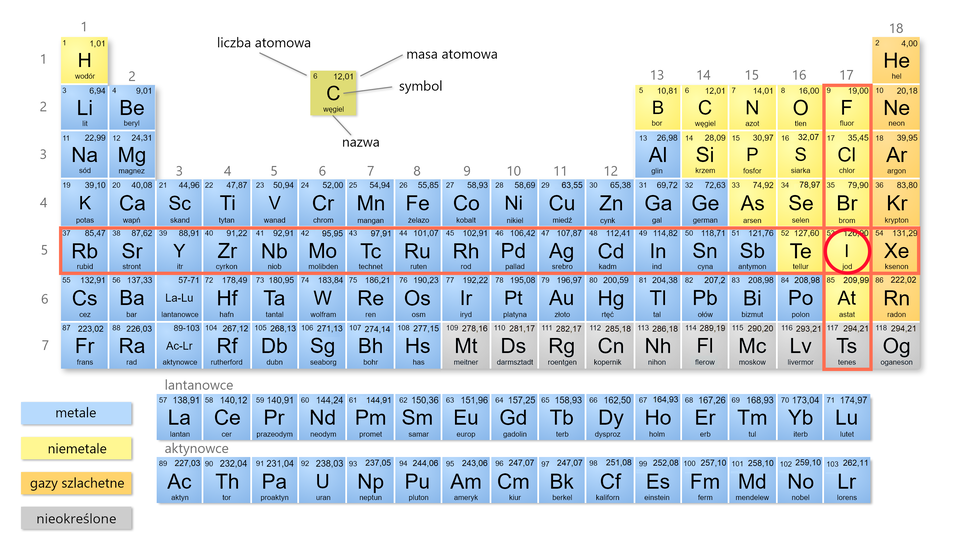
Układ okresowy pierwiastkówUkład okresowy pierwiastków to zestawienie w tabeli wszystkich pierwiastków chemicznych, uporządkowanych na podstawie rosnącej liczby atomowej. Pierwiastki są pogrupowane wg cyklicznie powtarzających się podobieństw ich właściwości. Kolumny określa się mianem grup, a wiersze — mianem okresów. Grupy i okresy są ponumerowane.
Przeanalizuj budowę zamieszczonego poniżej układu okresowego.
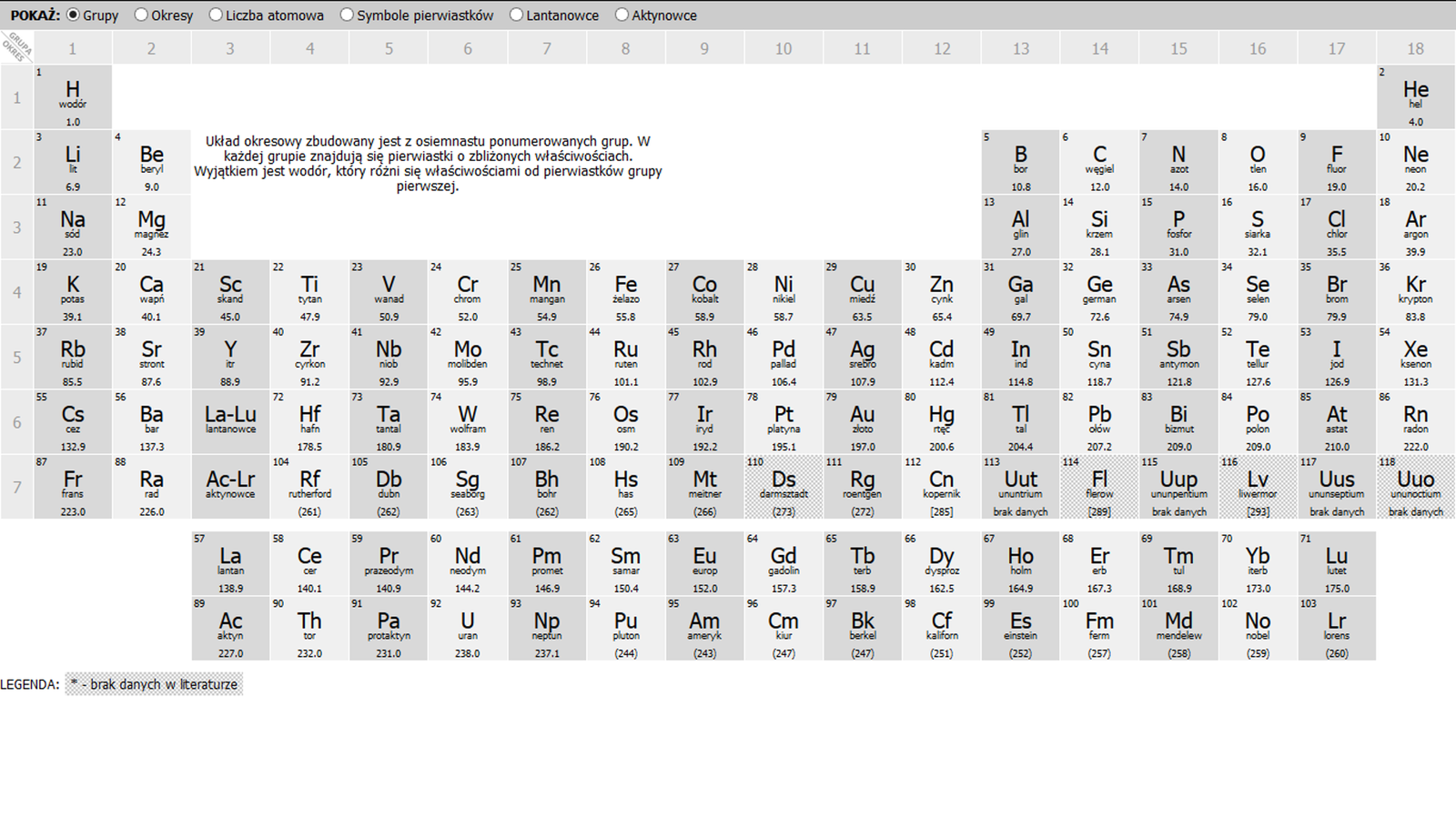
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D38LS1AZF
Zastanów się i odpowiedz na pytanie, jakie dwa parametry należy podać, aby określić położenie pierwiastka chemicznego w układzie okresowym.
Na podstawie znajomości numeru grupy i numeru okresu, możemy w prosty sposób zlokalizować dany pierwiastek w układzie okresowym.
Podaj nazwę oraz symbol pierwiastka chemicznego, który znajduje się w grupie i w okresie układu okresowego.
Jaką formę może przyjąć układ okresowy?
Niektórzy uczeni opracowywali układy okresowe o różnych kształtach. Jednak sposób prezentowania pierwiastków w formie tabeli jest najpowszechniej stosowany. Został zaakceptowany przez Międzynarodową Unię Chemii Czystej i Stosowanej — The International Union of Pure and Applied Chemistry, skrót IUPACIUPAC (czyt. internaszional junion of piur end eplajd kemistry), organizację zajmującą się głównie ujednolicaniem symboliki, nazewnictwa i wzorów, stosowanych przez chemików na całym świecie.
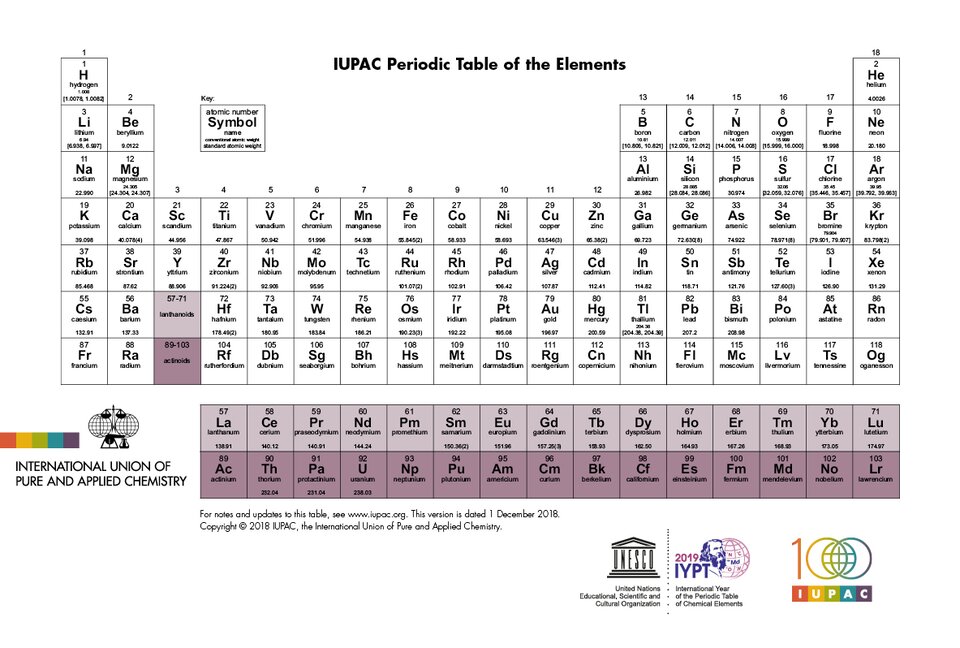
Najprostsza wersja układu okresowego zawiera symbole pierwiastków chemicznych, ich liczby atomowe (porządkowe) oraz numery grup i okresów. Istnieją jednak i takie wersje układów okresowych, które prezentują inne dodatkowe dane (np. nazwy pierwiastków i ich właściwości, budowę ich atomów, ich wielkość itp.). W niektórych układach okresowych stosuje się również kolory, np. do wskazania, które z pierwiastków chemicznych należą do metali, a które do niemetali, czy też do oznaczenia stanu skupienia poszczególnych pierwiastków chemicznych. Niezależnie od tego, ile informacji o pierwiastkach zawierają układy okresowe, zawsze kolejność pierwiastków, liczba grup oraz rodzaj pierwiastków w grupie i okresie w każdym układzie okresowym są identyczne.
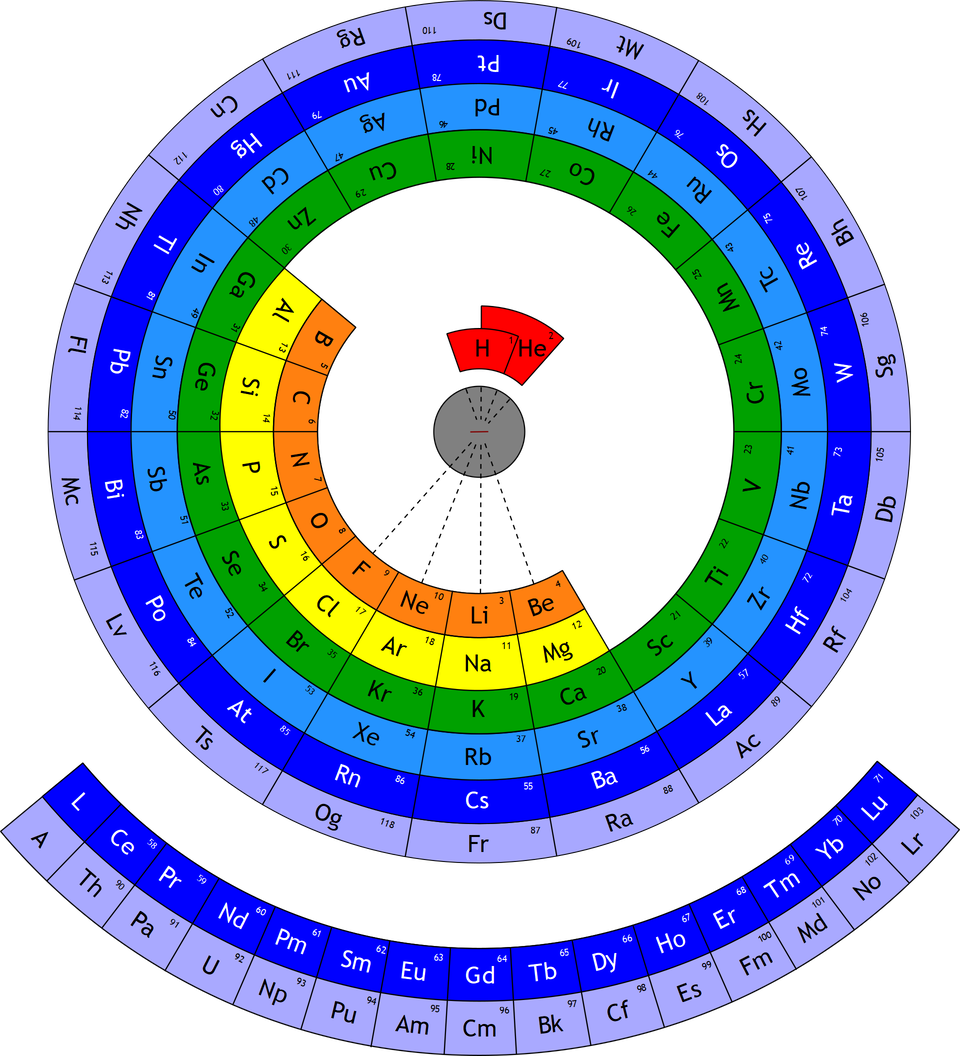
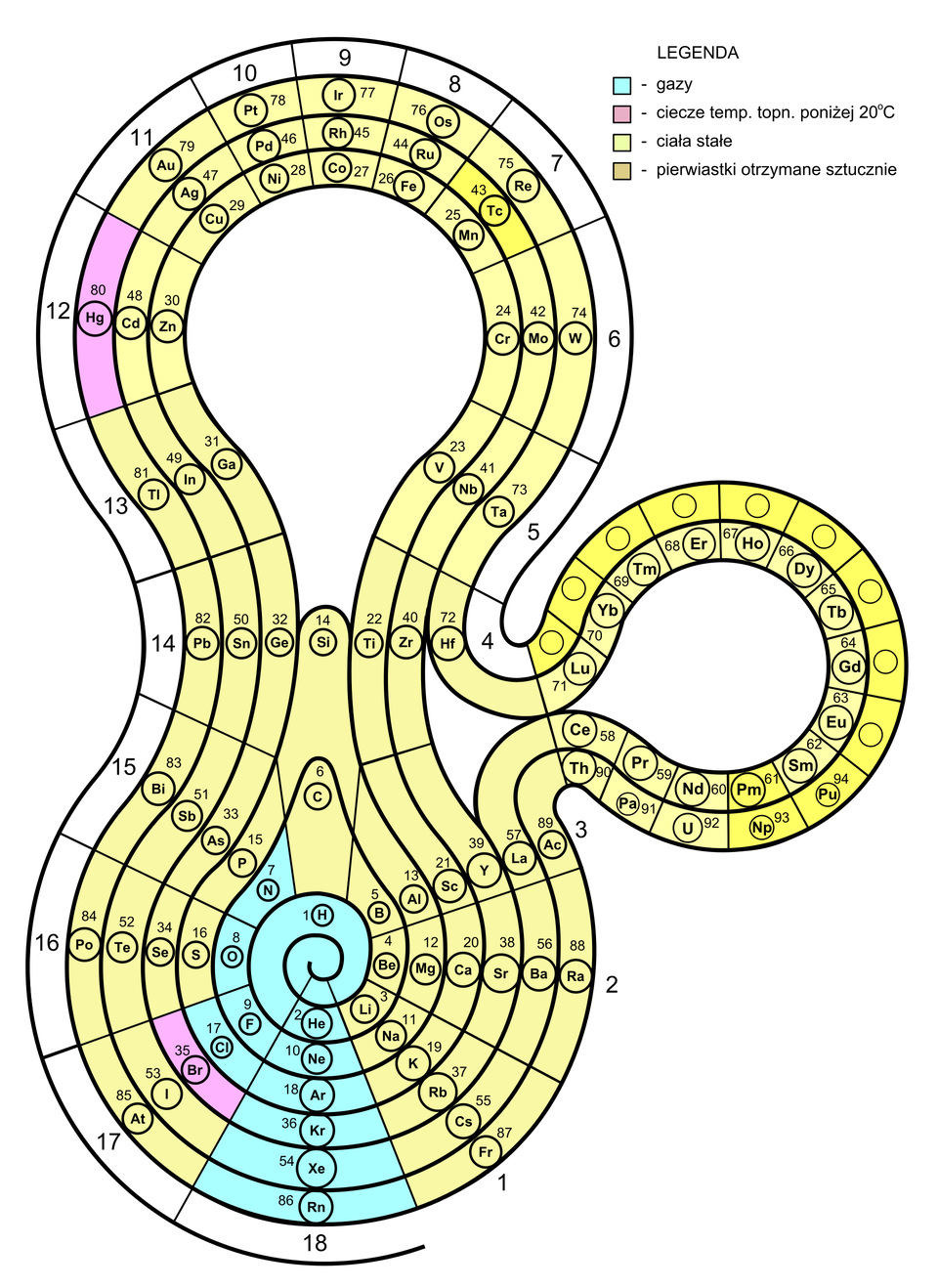
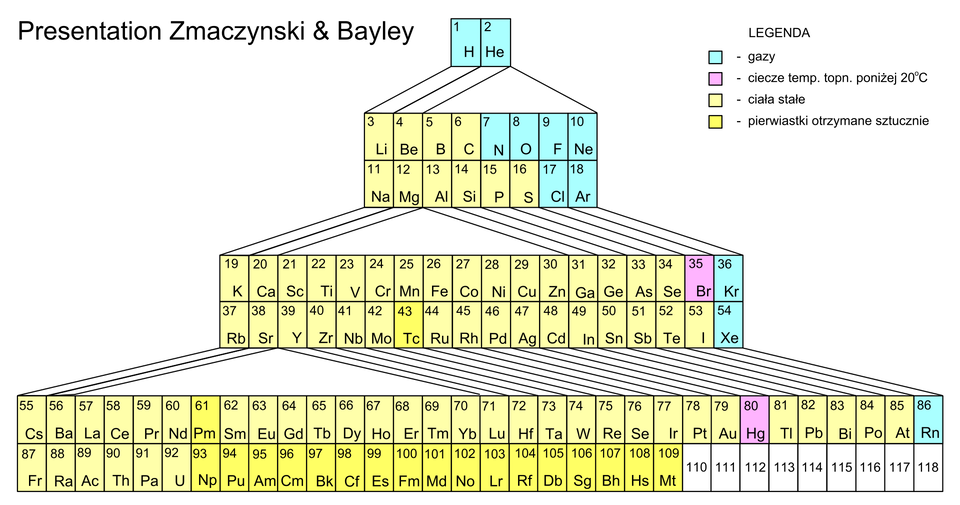
Przez wiele lat różni uczeni wychodzili z różnymi propozycjami porządkowania znanych im pierwiastków chemicznych, tworząc niejednokrotnie układy okresowe o przeróżnych kształtach. W poniższej galerii znajduje się kilka z nich.
Najmniejszy układ okresowy świata – wyczyn wpisany do Księgi rekordów Guinnessa (czyt. ginesa).
Naukowcy w Wielkiej Brytanii zapisali na ludzkim włosie cały układ okresowy pierwiastków. Użyli do tego bardzo precyzyjnych narzędzi (m.in. specjalnego rodzaju mikroskopu) i otrzymali układ o wymiarach na mikrometrów. Jak wiemy, mikrometr odpowiada jednej tysięcznej milimetra. Tego układu okresowego nie bylibyśmy w stanie zobaczyć nieuzbrojonym w odpowiedni sprzęt okiem.

Co łączy pierwiastki chemiczne należące do jednej grupy?
Czy grupy mają swoje nazwy?
Wszystkim grupom w układzie okresowym nadano nazwy, które pochodzą od nazw pierwiastków, znajdujących się na początku grupy. Pierwiastki z tej samej grupy mają podobne właściwości. Mogą one chociażby tworzyć podobne typy związków chemicznych z innymi pierwiastkami czy też wykazują podobne zachowanie wobec tych samych substancji chemicznych (np. wobec wody). Wyjątkiem jest wodór. Chociaż jest położony w grupie metali, to w rzeczywistości jest niemetalem i wykazuje odmienne właściwości od pozostałych pierwiastków chemicznych, które należą do pierwszej grupy układu okresowego. Stąd też nazwa wspomnianej grupy nie wywodzi się od wodoru, ale od znajdującego się tuż pod nim litu.
Nazwy poszczególnych grup układu okresowego przedstawiono na poniższym układzie okresowym.
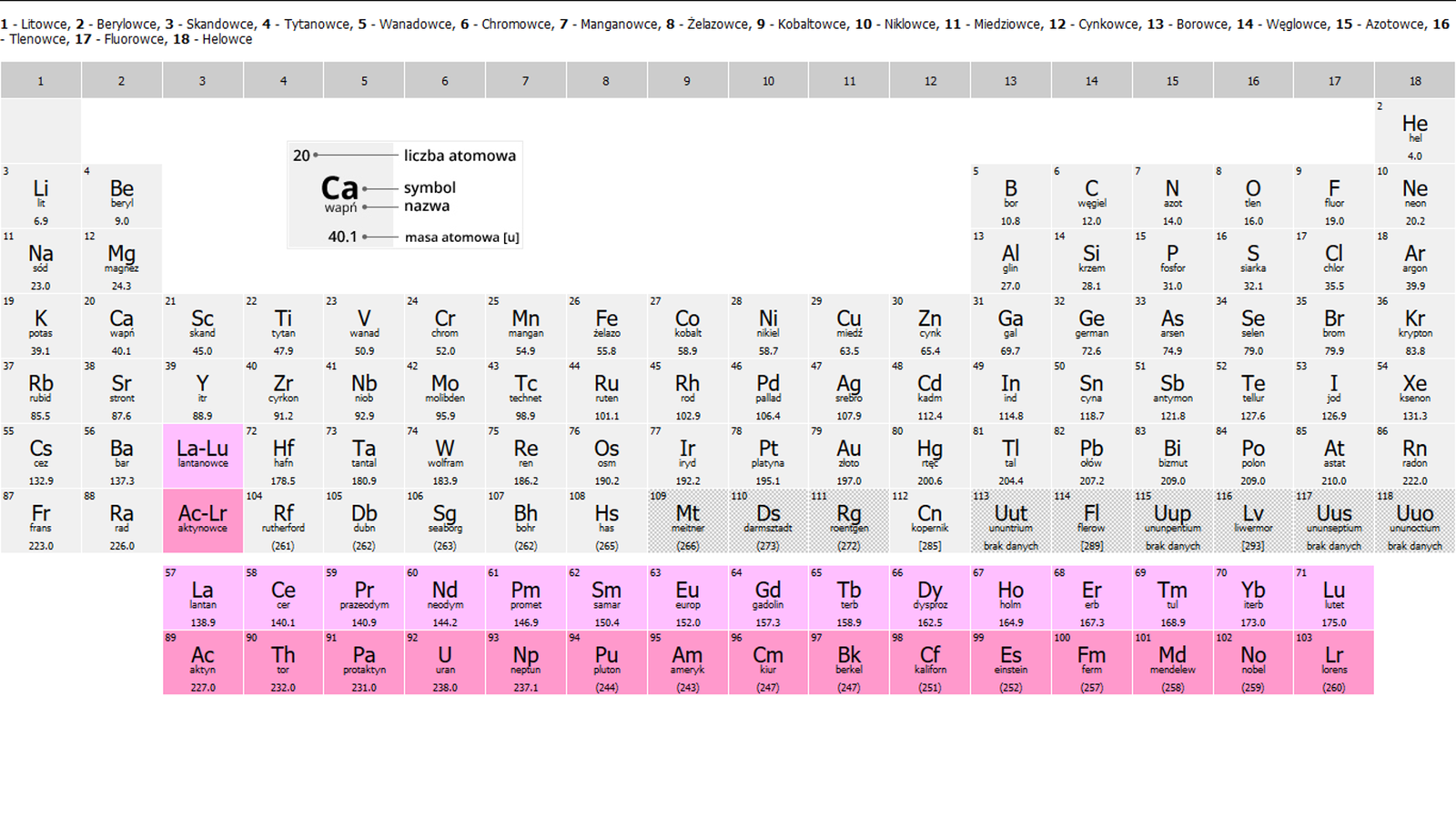
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D38LS1AZF
Pierwiastki chemiczne, należące do grupy układu okresowego, nazywane są fluorowcami, ale często również halogenami, a pierwiastki chemiczne należące do grupy układu okresowego określa się mianem helowców, a także gazami szlachetnymi.
Jak układ okresowy odzwierciedla podział pierwiastków na metale i niemetale?
Układ okresowy można umownie podzielić na dwie części, tak jak to przedstawiono na poniższej grafice. Pierwiastki chemiczne, zaznaczone na prezentowanym układzie okresowym na niebiesko, są metalami, a te, które zaznaczono na żółto, to niemetale.
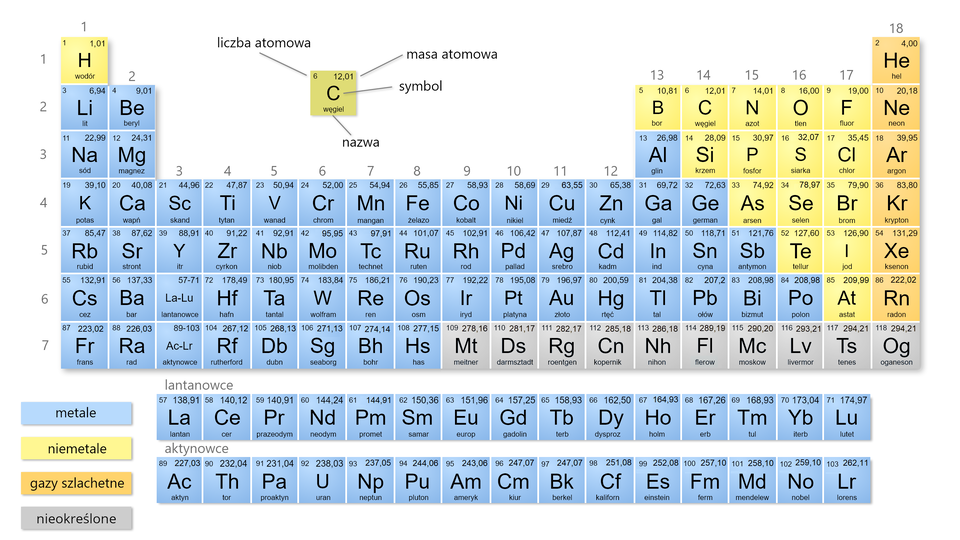
Układ okresowy, nawet wtedy, gdy jest przedstawiony w najprostszej formie, może dostarczyć nam cennych informacji na temat poszczególnych pierwiastków chemicznych. Zapoznaj się z poniższą animacją, a dowiesz się, jakie wiadomości o tlenie można uzyskać z układu okresowego. Następnie wykonaj polecenie .

Film dostępny pod adresem /preview/resource/R16DFKQX8ZQX9
Film pokazujący, jakie informacje o tlenie można uzyskać z układu okresowego.
Korzystając z poniższej aplikacji potrenuj odczytywanie informacji z układu okresowego.
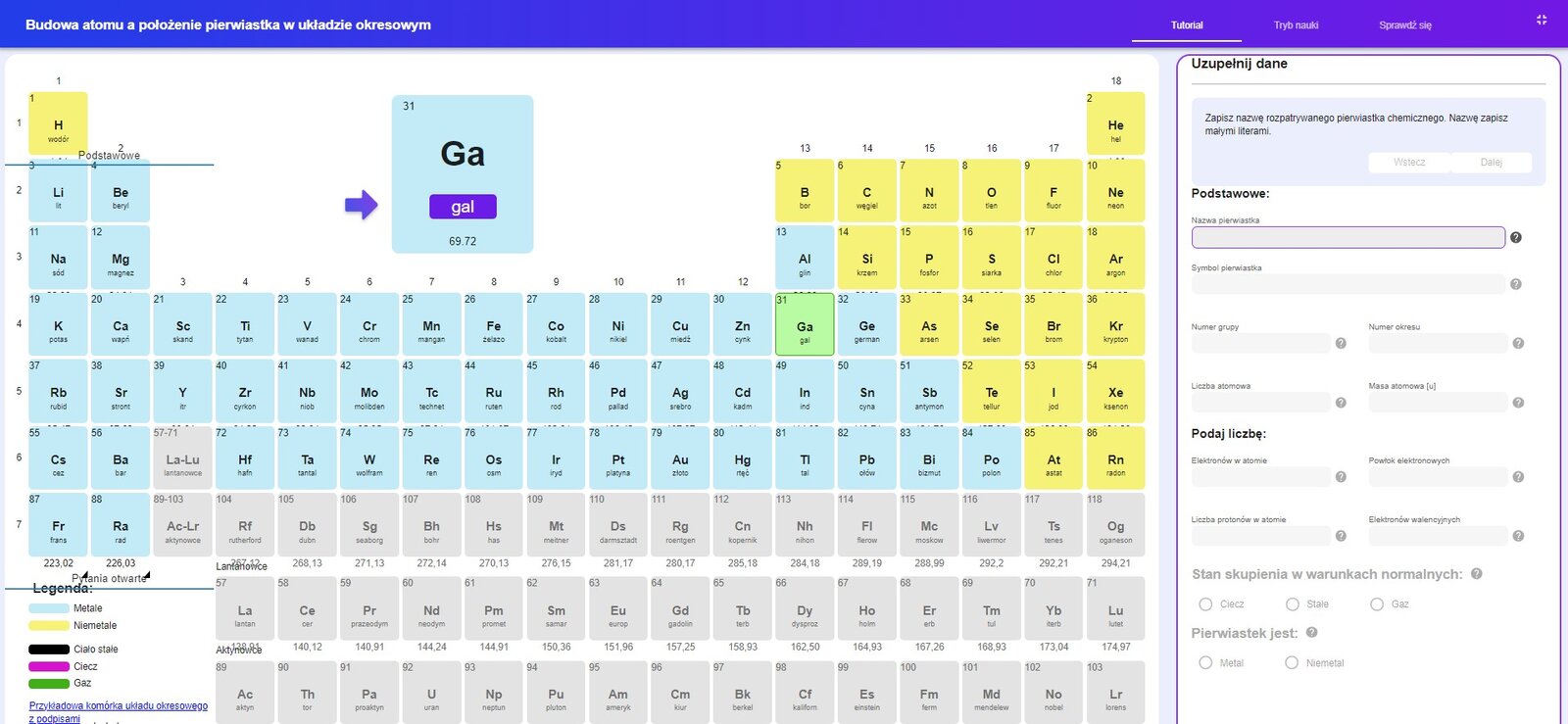
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D38LS1AZF
Poniżej znajdują się wybrane informacje dotyczące budowy atomów niektórych pierwiastków chemicznych. Do każdej z informacji dopasuj nazwę pierwiastka chemicznego, dla którego jest ona prawdziwa. Dana informacja może być prawdziwa dla kilku pierwiastków jednocześnie.
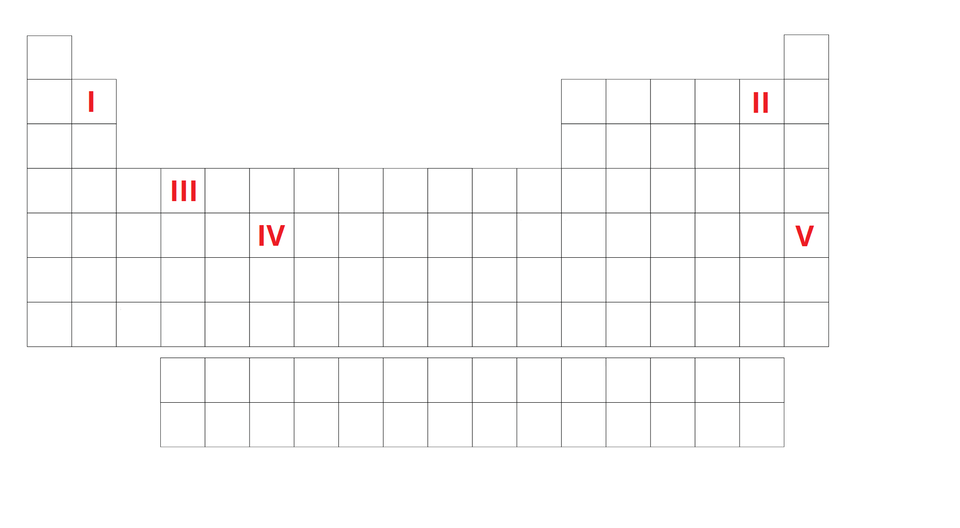
Na poniższym schemacie układu okresowego zaznaczono cyframi położenia pięciu różnych pierwiastków chemicznych ().
W załączonym układzie okresowym odszukaj pierwiastki chemiczne o nazwach: fosfor, potas, glin oraz brom, a potem uzupełnij poniższą tabelę. Masę atomową wskazanych pierwiastków chemicznych zaokrąglij do jedności.
Wyszukaj w układzie okresowym następujące pierwiastki:
— pierwiastek chemiczny z grupy helowców, używany do napełniania balonów; dostarczony do płuc, powoduje zmianę wysokości głosu;
— pierwiastek chemiczny z grupy borowców, stosowany do wyrobu puszek do napojów oraz folii do pakowania żywności;
— pierwiastek chemiczny z drugiej grupy układu okresowego, główny składnik kości;
— pierwiastek chemiczny z czwartego okresu, będący głównym składnikiem stali;
— pierwiastek chemiczny z piątego okresu, będący surowcem do tworzenia biżuterii.
Podsumowanie
Układ okresowy pierwiastków chemicznych jest uniwersalnym sposobem prezentacji pierwiastków chemicznych i różnorodnych danych na ich temat.
W układzie okresowym pierwiastki chemiczne (ich symbole i/lub nazwy) są umieszczone kolejno w tabeli, zgodnie z rosnącą liczbą atomową.
Pionowe kolumny tabeli nazywa się grupami, zaś poziome rzędy okresami. Wszystkie grupy i okresy są ponumerowane.
Każda z grup układu okresowego ma swoją nazwę, która pochodzi od nazwy rozpoczynającego ją pierwiastka chemicznego (z wyjątkiem grupy pierwszej, której nazwa pochodzi od drugiego z kolei pierwiastka).
Pierwiastki chemiczne należące do jednej grupy układu okresowego mają zbliżone właściwości (wyjątkiem jest wodór).