Budowa i nazewnictwo amin
Czym są aminy?
AminyAminy są związkami organicznymi, pochodnymi amoniaku. Mają swoją charakterystyczną grupę aminową (w przypadku amin pierwszorzędowych).
Aminy można uważać za pochodne amoniaku, w którego cząsteczce jeden, dwa lub trzy atomy wodoru zostały zastąpione resztami węglowodorowymi (alkilowymi lub/i arylowymi).

Rzędowość amin określona jest liczbą grup węglowodorowych, związanych z atomem azotu.



Właściwości fizyczne amin
Niższe alifatycznealifatyczne aminy w temperaturze pokojowej są gazami dobrze rozpuszczalnymi w wodzie.

Wyższe aminy alifatyczne są cieczami lub ciałami stałymi. Cząsteczki amin pierwszo- i drugorzędowych ulegają asocjacji (pomiędzy cząsteczkami tworzą się wiązania wodorowe) i stąd aminy te mają wyższe temperatury wrzenia niż węglowodory nasycone o identycznej liczbie atomów węgla w cząsteczce.
Cząsteczki amin pierwszorzędowych mogą tworzyć więcej wiązań wodorowychwiązań wodorowych z cząsteczkami wody niż cząsteczki amin drugo- i trzeciorzędowych, dlatego rozpuszczalność w wodzie amin pierwszorzędowych jest większa od rozpuszczalności amin drugo- i trzeciorzędowych.

Właściwości chemiczne amin

O zasadowymzasadowym charakterze amin, podobnie jak w przypadku amoniaku, decyduje atom azotu, który, mając wolną parę elektronową, jest zdolny do przyłączenia jonów . Wniosek więc jest taki, że aminy mogą reagować z kwasami i wodą.
Aminy mają charakterystyczny rybi zapach, a niektóre, np. N‑metylometanoamina (dimetyloamina) i N,N‑dimetylometanoamina (trimetyloamina) można znaleźć w zalewie śledziowej. Wodne roztwory amin mają odczyn zasadowy.
Rzędowość amin | Przykład reakcji |
|---|---|
aminy pierwszorzędowe | |
aminy drugorzędowe | |
aminy trzeciorzędowe |
Wniosek: w czasie rozpuszczania aminy w wodzie następuje wzrost stężenia jonów , powstaje zasada amoniowa.
Aminy mają charakter zasadowy, więc reagują z kwasami, np.:
Rzędowość amin | Przykład reakcji |
|---|---|
aminy pierwszorzędowe | |
aminy drugorzędowe | |
aminy trzeciorzędowe |
Wniosek: w reakcji amin z powstają odpowiednie chlorowodorki, np. chlorowodorek metyloaminy – . Jest to związek o budowie jonowej (typu soli): .
Aminy alifatyczne są silniejszymi zasadami od amoniaku. Ich zasadowość rośnie wraz ze wzrostem rzędowości.

Zwiększona w porównaniu z amoniakiem zasadowość jest skutkiem efektu indukcyjnego grup alkilowych, które odpychają elektrony w kierunku atomu azotu. Należy pamiętać, że każdy czynnik (podstawniki, elektroujemne atomy itp.) „angażujący” wolną parę elektronową atomu azotu, osłabia zasadowość związku, a każdy czynnik „dopychający” elektrony w kierunku atomu azotu – zwiększa zasadowość.
Aminy, jako słabe zasady, mogą być wyparte ze swoich soli pod wpływem działania mocnych zasad, np.:
Trzeciorzędowe aminy mają zdolność reagowania z halogenkami alkilowymi i tworzenia czwartorzędowych soli amoniowych. Sole te można potraktować częściowo jako pochodne soli amonowych, w których każdy atom wodoru w jonie amonowym został zastąpiony grupą węglowodorową.
Czwartorzędowe sole amoniowe odgrywają ważną rolę biologiczną; w organizmach naturalnie występują np. cholina (kation -hydroksyetylo(trimetylo)amoniowy), acetylocholina (-(acetyloksy)-N,N,N-trimetyloetanoamina).
Czy wiesz, jak zbudowane są aminy? Dowiesz się tego w poniższej symulacji. Następnie sprawdź, czy wszystko zostało zapamiętane i rozwiąż zadania.

Film dostępny pod adresem /preview/resource/R14eoUzh4UFBF
Film nawiązujący do treści materiału dotyczącej budowy amin.
Jakie znasz przykłady amin , lub -rzędowych? Do której klasy amin należą trietyloamina lub etyloamina? Zapoznaj się z grafiką interaktywną, a następnie wykonaj odpowiednie ćwiczenia.
Jakie znasz przykłady amin , lub -rzędowych? Do której klasy amin należą trietyloamina lub etyloamina? Zapoznaj się z opisem grafiki interaktywnej, a następnie wykonaj odpowiednie ćwiczenia.
Wzór sumaryczny: C indeks dolny, dwa, koniec indeksu dolnego, H indeks dolny, siedem, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór szkieletowy cząsteczki etanoaminy: C H indeks dolny, 3, koniec indeksu dolnego, C H indeks dolny, 2, koniec indeksu dolnego, N H indeks dolny, 2, koniec indeksu dolnego.
Nazwa: n-butanoamina (n-butyloamina);
Wzór sumaryczny: C indeks dolny, cztery, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór szkieletowy cząsteczki butanoaminy: C H indeks dolny, trzy, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, N H indeks dolny, dwa, koniec indeksu dolnego., 2. Do amin alifatycznych drugo-rzędowych należą: Nazwa: N-etyloetanoamina (dietyloamina);
Wzór sumaryczny: C indeks dolny, cztery, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór szkieletowy cząsteczki N‑etyloetanoaminy:C H indeks dolny, 3, koniec indeksu dolnego, C H indeks dolny, 2, koniec indeksu dolnego, N H C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, trzy, koniec indeksu dolnego.
Nazwa: N-butylobutanoamina (dibutyloamina);
Wzór sumaryczny: C indeks dolny, osiem, koniec indeksu dolnego, H indeks dolny, dziewiętnaście, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór szkieletowy cząsteczki N‑butylobutanoaminy: C H indeks dolny, trzy, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, N H C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, trzy, koniec indeksu dolnego., 3. Do amin alifatycznych trzecio-rzędowych należą: Nazwa: N,N-dietyloetanoamina (trietyloamina);
Wzór sumaryczny: C indeks dolny, sześć, koniec indeksu dolnego, H indeks dolny, piętnaście, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór szkieletowy cząsteczki N,N‑dietyloetanoaminy zbudowanej z atomu azotu połączonego z trzema grupami etylowymi C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, trzy, koniec indeksu dolnego.
Nazwa: N,N-dibutylobutanoamina (tributyloamina);
Wzór sumaryczny: C indeks dolny, dwanaście, koniec indeksu dolnego, H indeks dolny, dwadzieścia siedem, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór szkieletowy cząsteczki N,N‑dibutylobutanoaminy zbudowanej z atomu azotu połączonego z trzema podstawnikami n‑butylowymi C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, dwa, koniec indeksu dolnego, C H indeks dolny, trzy, koniec indeksu dolnego., 4. Do amin aromatycznych pierwszo-rzędowych należą: Nazwa: trzy-metyloanilina (trzy-metylobenzenoamina, m-metyloanilina, m-toluidyna);
Wzór sumaryczny: C indeks dolny, siedem, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór trzy-metyloaniliny zbudowanej z sześcioczłonowego pierścienia aromatycznego, w którym jeden z atomów węgla podstawiony jest grupą aminową N H indeks dolny, dwa, koniec indeksu dolnego, zaś drugi w położeniu trzecim grupą metylową C H indeks dolny, trzy, koniec indeksu dolnego.
Nazwa: 1‑naftyloamina;
Wzór sumaryczny: C indeks dolny, dziesięć, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór jeden-naftyloaminy, którą tworzą dwa pierścienie benzenu posiadające dwa wspólne atomy węgla, tak zwane atomy mostkowe, do jednego z atomów węgla sąsiadującego z atomem mostkowym przyłączona jest grupa aminowa N H indeks dolny, dwa, koniec indeksu dolnego., 5. Do amin aromatycznych drugo-rzędowych należą: Nazwa: N-fenyloanilina (difenyloamina);
Wzór sumaryczny: C indeks dolny, dwanaście, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N;
Wzór chemiczny:
oIlustracja przedstawia wzór półstrukturalny N‑fenyloanilinyzbudowanej z atomu azotu podstawionego atomem wodoru oraz dwiema grupami fenylowymi, to jest sześcioczłonowymi pierścieniami aromatycznymi.
Nazwa: N-metyloanilina (N-metylobenzenoamina);
Wzór sumaryczny: C indeks dolny, siedem, koniec indeksu dolnego, H indeks dolny, dziewięć, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór N‑metyloaniliny. Do pierścienia benzenu przyłączony jest atom azotu połączony z atomem wodoru i grupą metylową C H indeks dolny, trzy, koniec indeksu dolnego., 6. Do amin aromatycznych trzecio-rzędowych należą: Nazwa: N,N-dimetyloanilina;
Wzór sumaryczny: C indeks dolny, osiem, koniec indeksu dolnego, H indeks dolny, jedenaście, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór N,N‑dimetyloaniliny. Do pierścienia benzenu przyłączony jest atom azotu połączony z dwiema grupami C H indeks dolny, trzy, koniec indeksu dolnego.
Nazwa: N,N-dimetylo‑1-naftyloamina;
Wzór sumaryczny: C indeks dolny, dwanaście, koniec indeksu dolnego, H indeks dolny, trzynaście, koniec indeksu dolnego, N;
Wzór chemiczny:
Ilustracja przedstawia wzór N,N‑dimetylo-jeden-naftyloaminy, którą tworzą dwa skondensowane, sześcioczłonowe pierścienie aromatyczne posiadające dwa wspólne atomy węgla, tak zwane atomy mostkowe, do jednego z atomów węgla sąsiadującego z atomem mostkowym przyłączony jest atom azotu związany z dwiema grupami C H indeks dolny, trzy, koniec indeksu dolnego.
Określ typ aminy przedstawionej na poniższym rysunku oraz jej rzędowość.
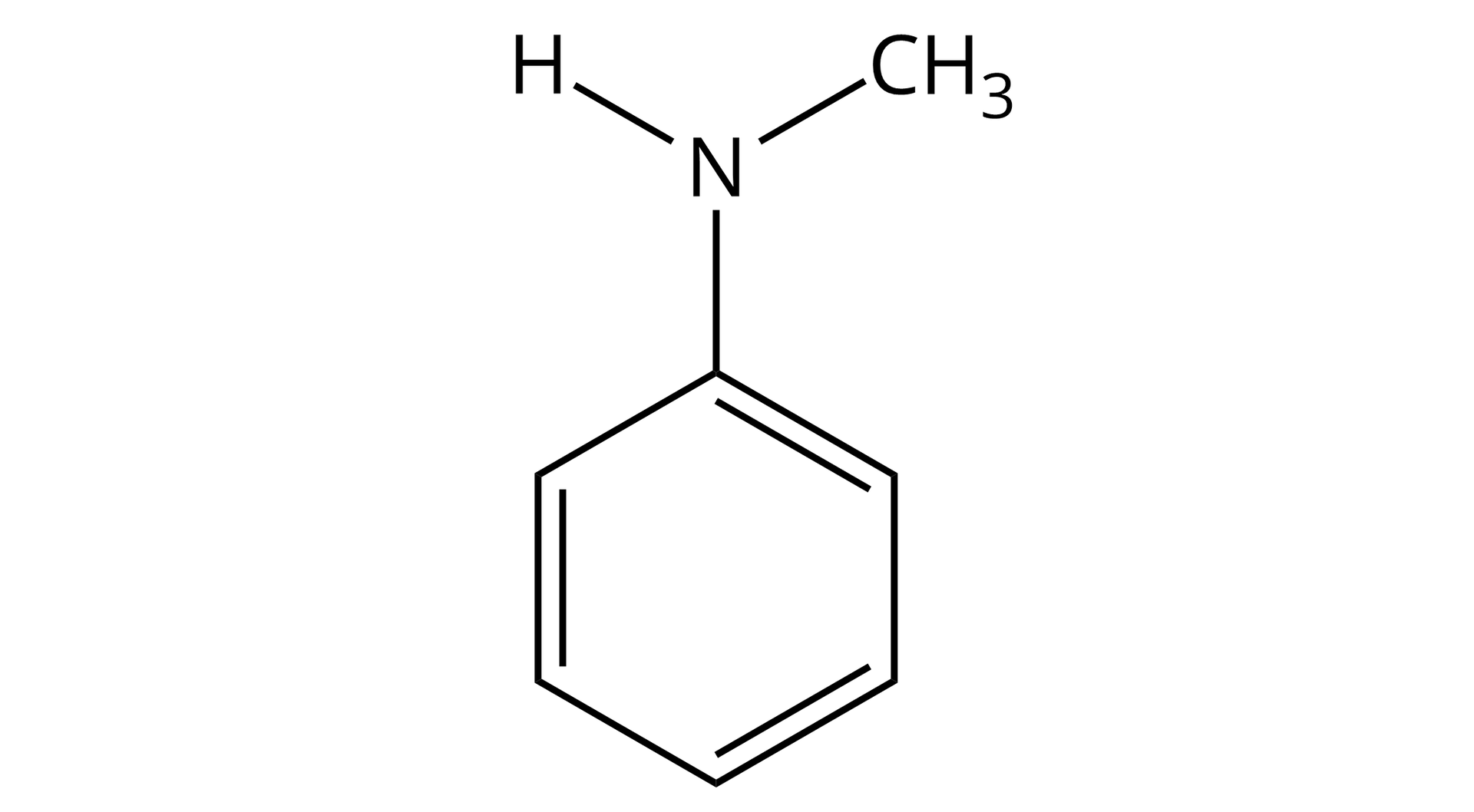
Określ typ aminy oraz jej rzędowość.
Nomenklatura amin
AminyAminy możemy podzielić na alifatycznealifatyczne z podstawnikami alkilowymialkilowymi (), a także aromatycznearomatyczne z podstawnikami arylowymiarylowymi (). Rozróżniamy aminy pierwszorzędowe, drugorzędowe oraz trzeciorzędowe. Rzędowość określa się na podstawie liczby atomów węgla, połączonych z atomem azotu. Aminy drugo– i trzeciorzędowe mogą należeć do grupy amin symetrycznych lub niesymetrycznych, w zależności od rodzaju grup występujących w związku oraz sposobu rozmieszczenia względem atomu azotu. Aminy można nazwać symetrycznymi, gdy jedna strona związku ma odbicie lustrzane po drugiej stronie względem atomu azotu. Niesymetryczne aminy mają różne grupy i nie można określić symetrii cząsteczki. Określenie symetrii oraz rzędowości jest niezwykle ważne przy tworzeniu nazw amin. Zasady nazewnictwa przedstawiają podrozdziały poniżej.
- Nazwa kategorii: Aminy
- Nazwa kategorii: Alifatyczne[br](podstawniki alkilowe)
- Nazwa kategorii: pierwszo rzędowe
- Nazwa kategorii: drugo rzędowe
- Nazwa kategorii: trzecio rzędowe Koniec elementów należących do kategorii Alifatyczne[br](podstawniki alkilowe)
- Nazwa kategorii: Aromatyczne[br](podstawniki arylowe)
- Nazwa kategorii: pierwszo rzędowe
- Nazwa kategorii: drugo rzędowe
- Nazwa kategorii: trzecio rzędowe Koniec elementów należących do kategorii Aromatyczne[br](podstawniki arylowe)
- Elementy należące do kategorii Aminy
- Elementy należące do kategorii Alifatyczne[br](podstawniki alkilowe)
- Elementy należące do kategorii Aromatyczne[br](podstawniki arylowe)
Aminy –rzędowe
Nazwy -rzędowych amin-rzędowych amin konstruuje się poprzez dodanie nazwy „amina” do nazwy węglowodoru macierzystego.
Na przykład, w przedstawionym niżej wzorze widzimy, że grupa aminowa jest przyłączona do węglowodorowego łańcucha butanu – zatem jej nazwa to butano––amina. Atom węgla, bezpośrednio połączony z grupą aminową, nie musi być zawsze oznaczony lokantem . Ważniejsze jest bowiem, aby łańcuch węglowy był jak najdłuższy.

Inne przykłady amin –rzędowych wraz z ich nazwami systematycznymi podano poniżej:
Aminy – i –rzędowe
W celu nazwania aminy -- lub -rzędowej-rzędowej należy:
Wybrać najdłuższy łańcuch (lub pierścień) węglowy i nazwać aminę, tak jak to czyniliśmy w przypadku amin –rzędowych.
Dodać nazwy podstawników na atomie azotu, wskazując ich usytuowanie literą N.
Na przykład:

Poniżej przeanalizujemy inne wzory – i –rzędowych amin wraz z ich nazwami, pamiętając, że nazwa, zalecana dla pierścienia benzenowego podstawionego grupą aminową (benzenoaminy), to anilina. Właśnie tej nazwy powinniśmy używać.
Jak tworzy się nazwy amin? Aby poznać odpowiedź na to pytanie, zapoznaj się z poniższymi informacjami.
Aby określić nazwę aminy, co należy wziąć pod uwagę? Na przykładzie dwóch nazw amin przedstawionych poniżej przeanalizuj, jak one powstały.
Nazwij podany poniżej związek.

Podaj nazwę związku o wzorze grupowym .







