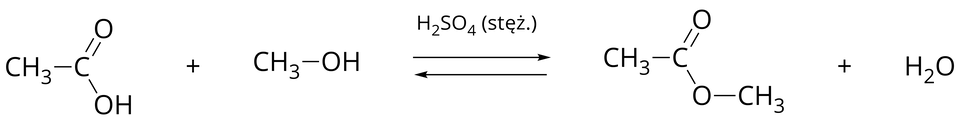
Budowa i właściwości estrów
Poniższy materiał stanowi uzupełnienie treści zawartych w materiale: https://zpe.gov.pl/a/estry–budowa-i-wlasciwosci/D19BFjfMU
Zamknij oczy i wyobraź sobie, że przed Tobą postawiono talerz pełen owoców. Wyczuwasz wiele różnych zapachów. Jesteś w stanie rozpoznać zapach ananasów, bananów, gruszek, jabłek i wiele innych. Czy wiesz, jakie substancje dotarły do receptorów węchowych w Twojej jamie nosowej? Te substancje to estry, które odpowiadają między innymi za charakterystyczne zapachy różnych owoców.
budowę alkoholi i kwasów karboksylowych;
właściwości fizyczne i chemiczne alkoholi i kwasów karboksylowych.
opisywać budowę estrów kwasów karboksylowych;
wyjaśniać, w jaki sposób tworzy się nazwy systematyczne estrów kwasów karboksylowych;
przedstawić, na czym polega reakcja estryfikacji i w jakich warunkach zachodzi;
projektować doświadczenie, które pozwoli zbadać właściwości fizykochemiczne estrów na przykładzie etanianu etylu;
projektować doświadczenie, dzięki któremu otrzymasz wybrane estry.
Estry kwasów karboksylowych to związki chemiczne bardzo szeroko rozpowszechnione w przyrodzie. Stanowią podstawowy składnik substancji zapachowych wielu roślin. Są to produkty reakcji alkoholi i kwasów karboksylowych. Estry kwasów karboksylowych należą zatem do grupy pochodnych węglowodorów. Ich cechą charakterystyczną jest posiadanie grupy estrowej, łączącej reszty węglowodorowe, które z kolei pochodzą od kwasu karboksylowego i alkoholu.
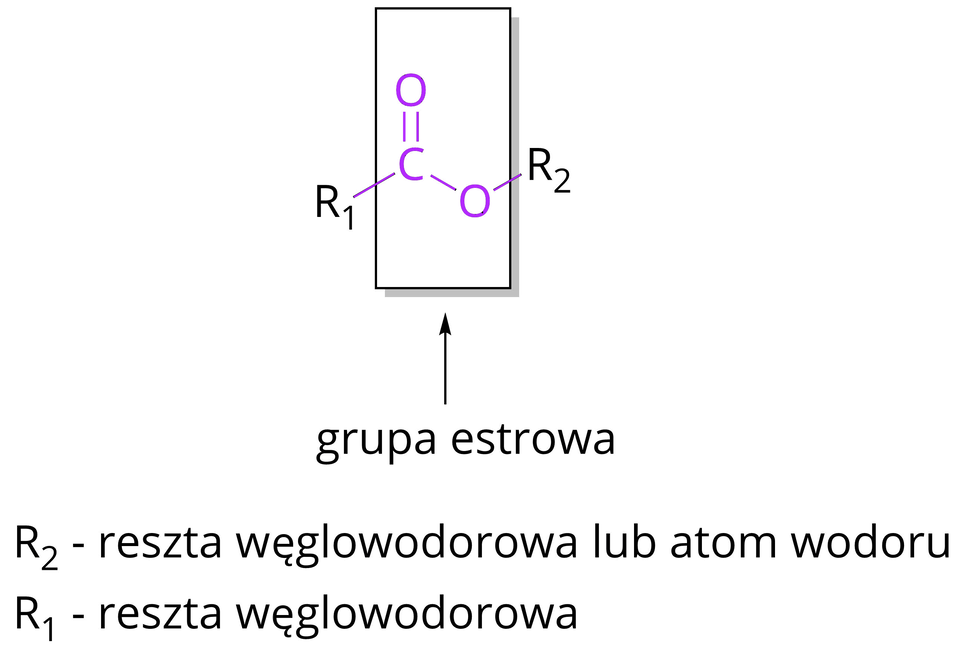
Na poniższej grafice przedstawiono budowę estrów z wyszczególnieniem pochodzenia poszczególnych jego części.
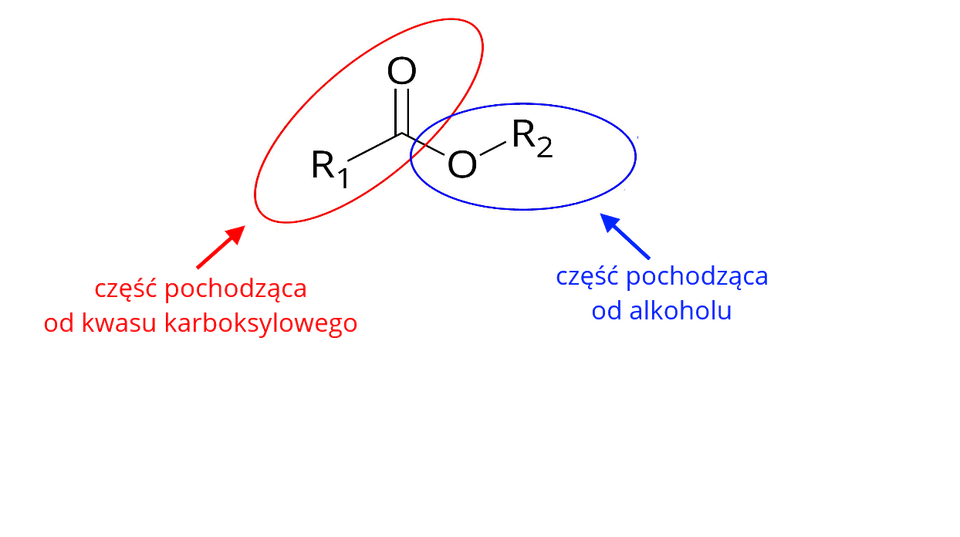
W poniższej tabeli zebrano przykładowe wzory i nazwy estrów. Przeanalizuj je, a następnie rozwiąż ćwiczenie.
Wzór półstrukturalny i nazwa estru zalecana przez IUPAC | Pochodzenie | |
|---|---|---|
Kwas karboksylowy | Alkohol | |
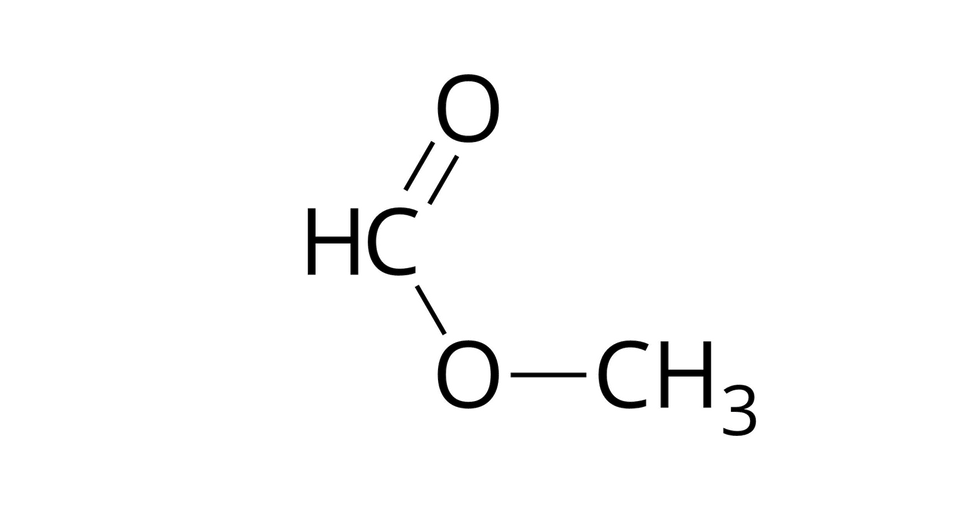 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. metanian metylu | 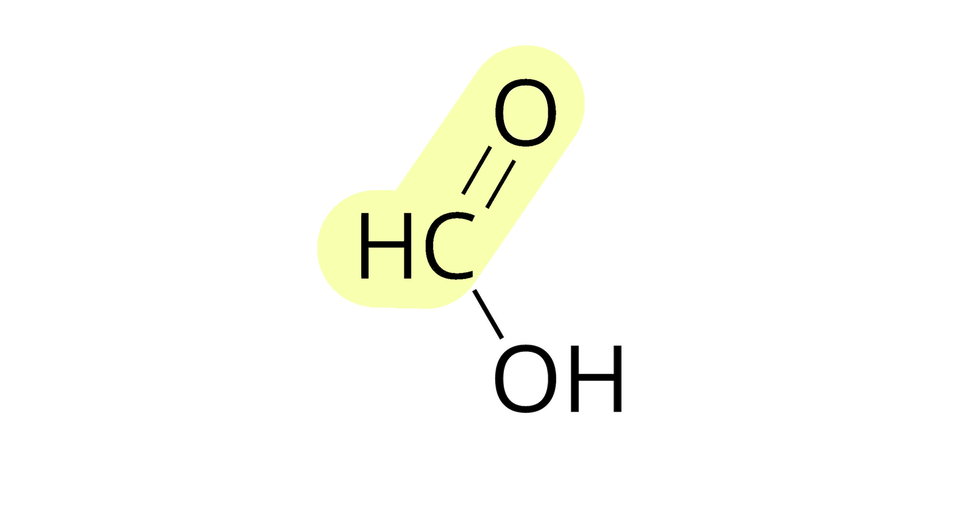 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. kwas metanowy | 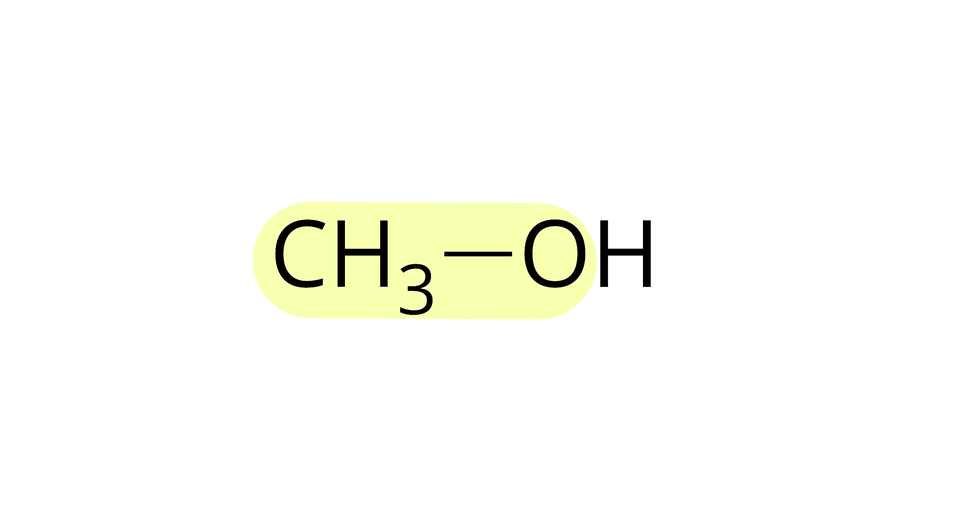 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. metanol |
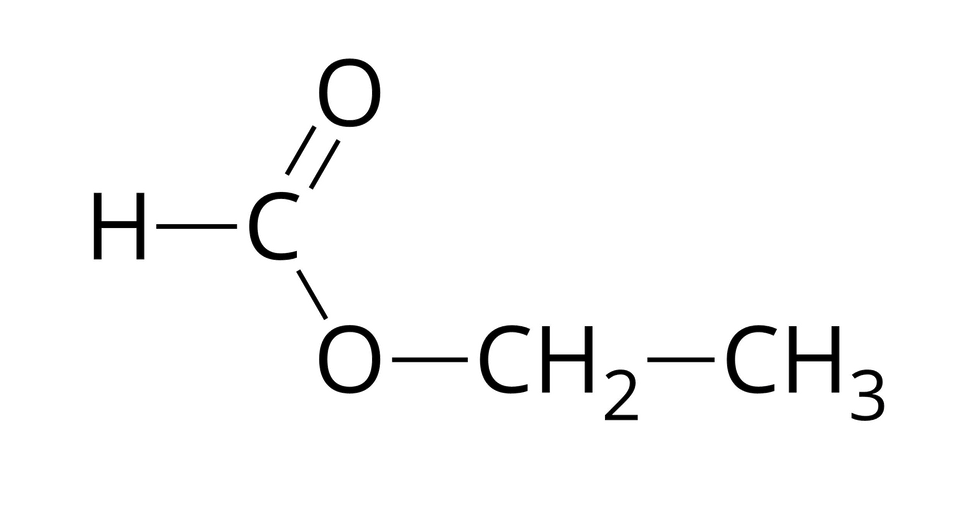 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. metanian etylu | 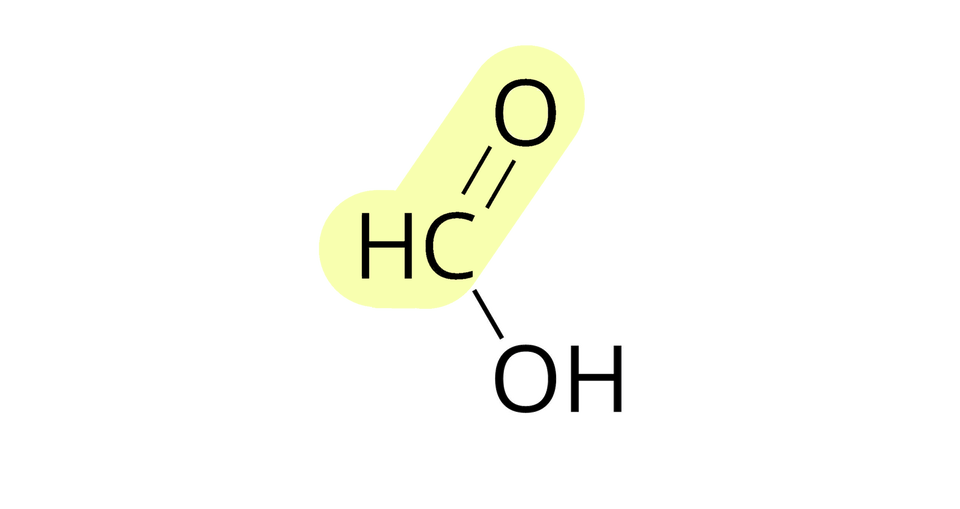 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. kwas metanowy | 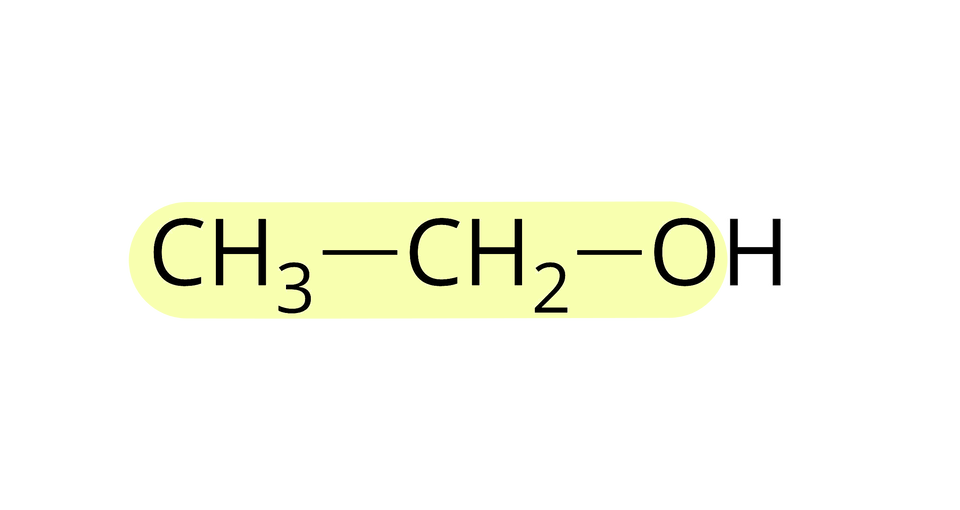 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. etanol |
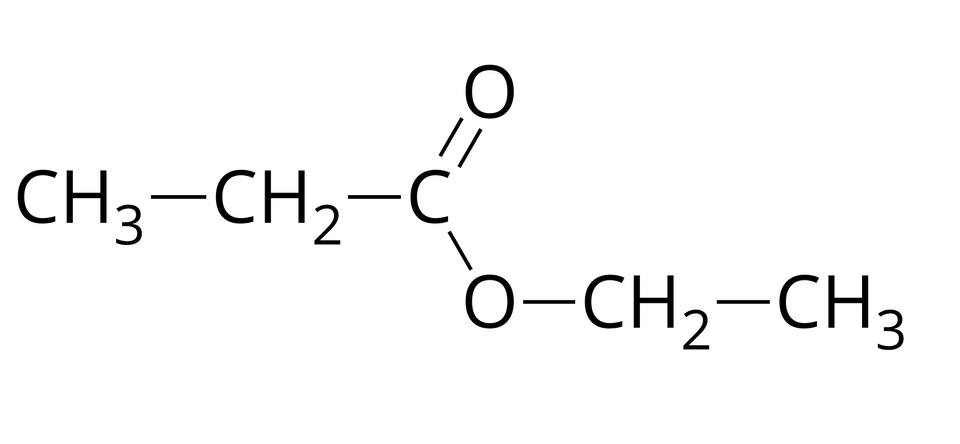 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. propanian etylu | 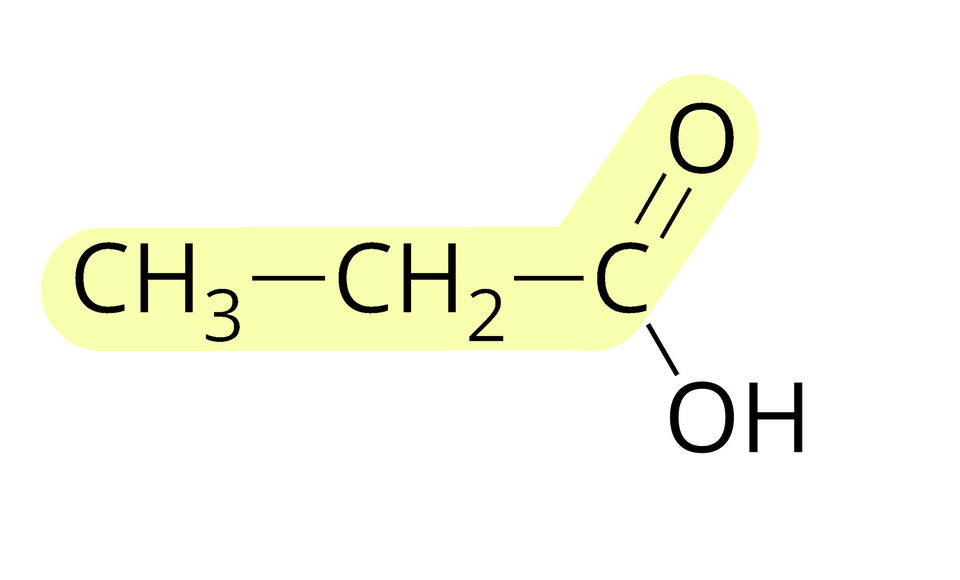 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. kwas propanowy | 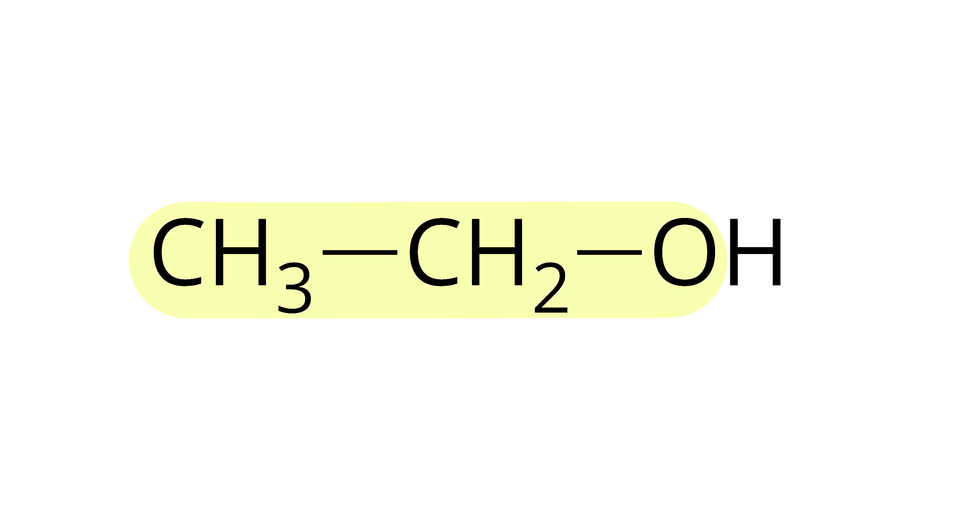 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. etanol |
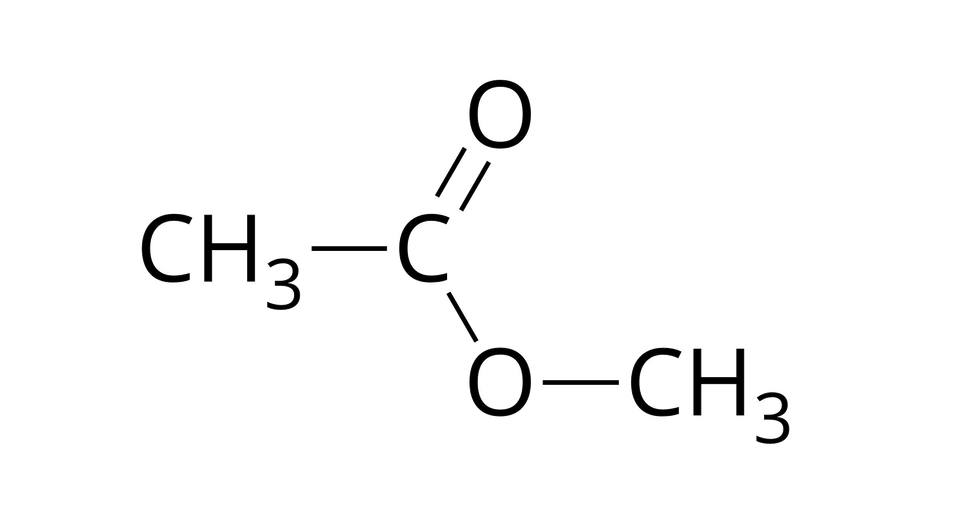 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. etanian metylu | 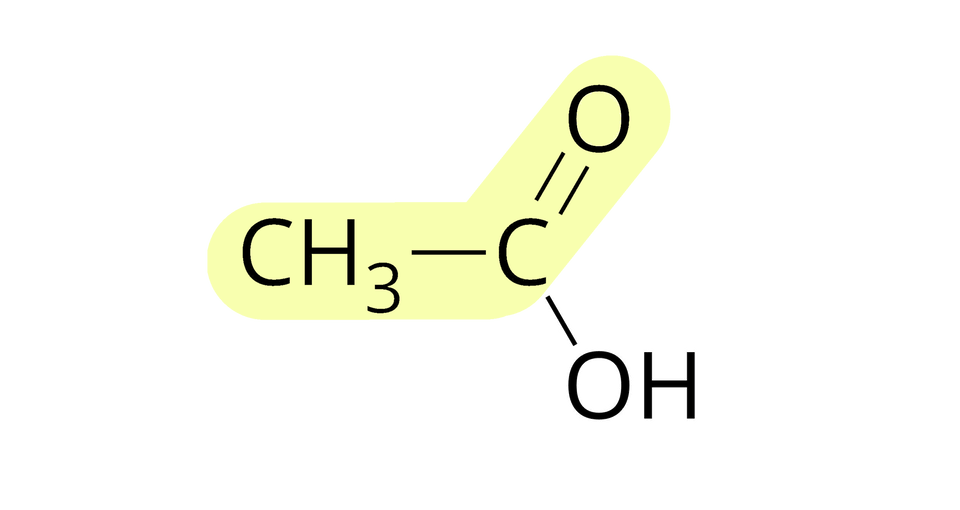 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. kwas etanowy | 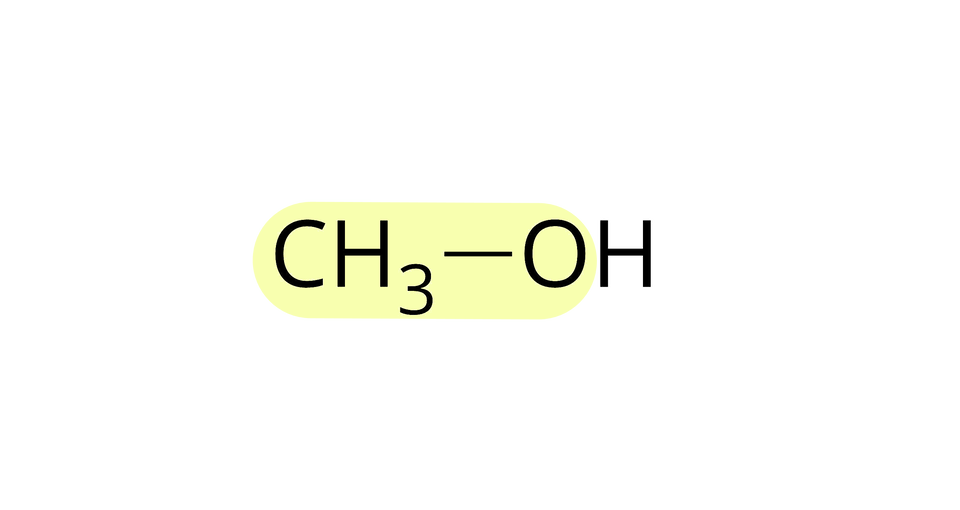 Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0. metanol |
Nazwy estrów kwasów karboksylowych pochodzą od nazw kwasów i alkoholi. Pierwszy człon nazwy estru pochodzi od kwasu karboksylowego, więc zmieniamy końcówkę na „–an” lub „–ian”, np. metanian, etanian, propanian czy butanian. Drugi człon nazwy estru pochodzi od alkoholu – wówczas zmieniamy końcówkę na „–ylu”, np. metylu, etylu, propylu czy butylu.
Ogólny schemat otrzymywania estrów kwasów karboksylowych w wyniku reakcji kwasów karboksylowych z alkoholami można zapisać następująco:
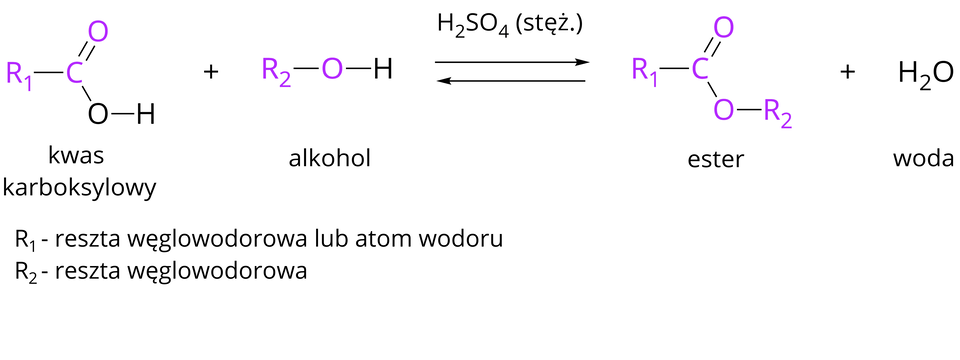
Jest to reakcja estryfikacji. Reakcja ta zachodzi pod wpływem stężonego kwasu siarkowego(), który znacząco ją przyspiesza. Jest to zatem katalizator reakcji estryfikacji.
Zatem równanie reakcji otrzymywania dla przykładu propanianu etylu zapisujemy w następujący sposób:
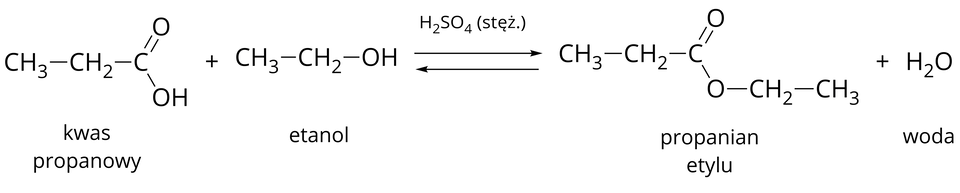
Zapisz równanie reakcji otrzymywania etanianu metylu.
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym, polegające na zbadaniu wybranych właściwości fizykochemicznych estrów kwasów karboksylowych na przykładzie etanianu etylu. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DLQUeisbT
Zapoznaj się z zamieszczonym poniżej opisem doświadczenia, a następnie wykonaj polecenia.
Hipoteza:
Etanian etylu to ciecz o charakterystycznym zapachu. Nie rozpuszcza się w wodzie. Rozpuszcza się w rozpuszczalnikach organicznych – etanolu i benzynie. Jest łatwopalny.
Sprzęt laboratoryjny:
probówki;
pipety Pasteura;
łyżka do spalań;
palnik gazowy;
pręciki szklane;
zapałki.
Odczynniki chemiczne:
etanian etylu;
etanol;
woda destylowana;
benzyna;
uniwersalne papierki wskaźnikowe.
Przebieg eksperymentu:
Za pomocą pipety wlano do trzech probówek po około etanianu etylu.
Do pierwszej probówki wlano około wody destylowanej. Sprawdzono odczyn roztworu estru za pomocą uniwersalnego papierka wskaźnikowego poprzez zanurzenie pręcika szklanego w probówce, a następnie umieszczenie kilku kropli cieczy na uniwersalnym papierku wskaźnikowym.
Do drugiej probówki wlano około etanolu, a do trzeciej około benzyny i intensywnie zamieszano zawartości probówek za pomocą pręcików szklanych.
Za pomocą pipety wlano niewielką ilość etanianu etylu na łyżkę do spalań, a następnie umieszczono ją nad zapalonym palnikiem gazowym.
Obserwacje:
W probówce, w której jest bezbarwna ciecz, wyczuwalny jest charakterystyczny, przyjemny zapach.
W pierwszej probówce powstały dwie warstwy bezbarwnych cieczy. Dolna warstwa zajmuje objętość równą , a górna . Uniwersalny papierek wskaźnikowy nie zmienił swojego zabarwienia pod wpływem cieczy.
W drugiej i trzeciej probówce powstały klarowne, bezbarwne roztwory.
Ciecz umieszczona na łyżce do spalań, zaczęła spalać się żółto–pomarańczowym płomieniem.
Wyniki:
Etanian etylu to bezbarwna ciecz o przyjemnym zapachu. Rozpuszcza się w etanolu i benzynie, ale nie w wodzie. Ma gęstość mniejszą od gęstości wody. Etanian etylu nie ulega dysocjacji, więc odczyn jego mieszaniny z wodą jest obojętny.
Etanian etylu jest substancją łatwopalną. Równanie reakcji spalania można przedstawić na przykładowy sposób:
W wyniku spalania zamiast tlenku węgla() może powstać tlenek węgla() lub węgiel. Produkty spalania zależą od dostępnej ilości tlenu w powietrzu.
Wnioski:
Hipoteza została potwierdzona.
Ze zbadanych właściwości etanianu etylu, wybierz i wpisz w odpowiednie miejsca te, które stanowią właściwości fizyczne oraz te stanowiące właściwości chemiczne.
węgla(cztery) lub niecałkowitemu do tlenku węgla(dwa) albo węgla. Od czego zależą produkty spalania? Zaznacz poprawną odpowiedź.
Przyporządkuj nazwę substancji do odpowiedniego miejsca w probówce.
Przeprowadź doświadczenie w wirtualnym laboratorium chemicznym, które polega na otrzymaniu czterech estrów kwasów karboksylowych. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz obserwacje, a następnie sformułuj wnioski.
Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DLQUeisbT
Zapoznaj się z zamieszczonym poniżej opisem doświadczenia, a następnie wykonaj polecenia.
Hipoteza:
Estry można otrzymać w wyniku reakcji kwasów karboksylowych z alkoholami.
Sprzęt laboratoryjny:
statyw z probówkami;
pipety;
zlewka;
palnik gazowy;
zapałki.
Odczynniki chemiczne:
etanol;
pentan––ol;
roztwór kwasu etanowego;
roztwór kwasu butanowego;
stężony roztwór kwasu siarkowego();
woda destylowana.
Przebieg eksperymentu:
Za pomocą pipety wlano do probówki około roztworu kwasu etanowego i około pentan––olu oraz kilka kropli stężonego roztworu kwasu siarkowego(). Następnie przeniesiono probówkę do zlewki wypełnionej gorącą wodą i ogrzewano nad płomieniem palnika.
Za pomocą pipety wlano do probówki około roztworu kwasu etanowego i około etanolu oraz kilka kropli stężonego roztworu kwasu siarkowego(). Następnie przeniesiono probówkę do zlewki wypełnionej gorącą wodą i ogrzewano nad płomieniem palnika.
Za pomocą pipety wlano do probówki około roztworu kwasu butanowego i około pentan––olu oraz kilka kropli stężonego roztworu kwasu siarkowego(). Następnie przeniesiono probówkę do zlewki wypełnionej gorącą wodą i ogrzewano nad płomieniem palnika.
Za pomocą pipety wlano do probówki około roztworu kwasu butanowego i około etanolu oraz kilka kropli stężonego roztworu kwasu siarkowego(). Następnie przeniesiono probówkę do zlewki wypełnionej gorącą wodą i ogrzewano nad płomieniem palnika.
Obserwacje:
W pierwszej probówce powstał klarowny, bezbarwny roztwór i wyczuwalny jest zapach bananów.
W drugiej probówce powstał klarowny, bezbarwny roztwór i wyczuwalny jest przyjemny, owocowy zapach.
W trzeciej probówce powstał klarowny, bezbarwny roztwór i wyczuwalny jest zapach gruszek.
W czwartej probówce powstał klarowny, bezbarwny roztwór i wyczuwalny jest zapach ananasów.
Wyniki:
Estry można otrzymać w wyniku reakcji kwasów karboksylowych z alkoholami. Katalizatorem reakcji estryfikacji jest kwas siarkowy().
Wnioski:
Hipoteza została potwierdzona.
Reakcja, która zachodzi pomiędzy kwasami karboksylowymi a alkoholami, nazywana jest reakcją:
Dopasuj równania reakcji do odpowiedniej probówki.
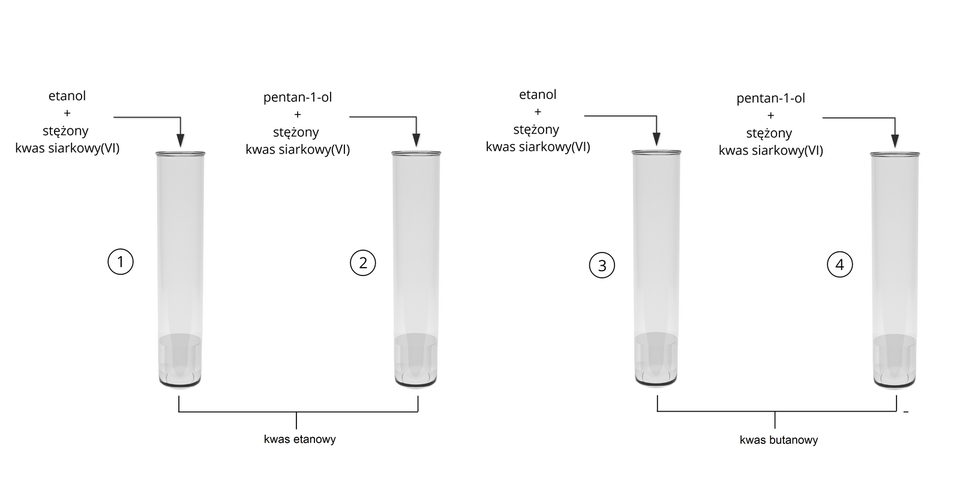
Przeprowadzono cztery reakcje chemiczne. W pierwszej i drugiej probówce znajdował się kwas etanowy, natomiast w trzeciej i czwartej kwas butanowy. Do probówek nr i dodano porcje etanolu oraz kwasu siarkowego(), natomiast do probówek nr i dodano porcje pentan––olu oraz kwasu siarkowego(). Dopasuj odpowiednie równania reakcji do numerów probówek podanych poniżej.
Probówka 2: 1. , 2. , 3. , 4.
Probówka 3: 1. , 2. , 3. , 4.
Probówka 4: 1. , 2. , 3. , 4.
Słownik
związki chemiczne zawierające grupę estrową ; powstają w wyniku reakcji estryfikacji
reakcja kwasów między innymi karboksylowych z alkoholami, zachodząca w obecności kwasu siarkowego(); w jej wyniku otrzymujemy estry
substancja, która przyspiesza reakcję chemiczną, np. stężony kwas siarkowy() w reakcji estryfikacji
Ćwiczenia
Poniżej przedstawiono model kulkowy pewnego estru. Atomy węgla oznaczono kolorem czarnym, atomy tlenu kolorem czerwonym, a atomy wodoru kolorem białym.
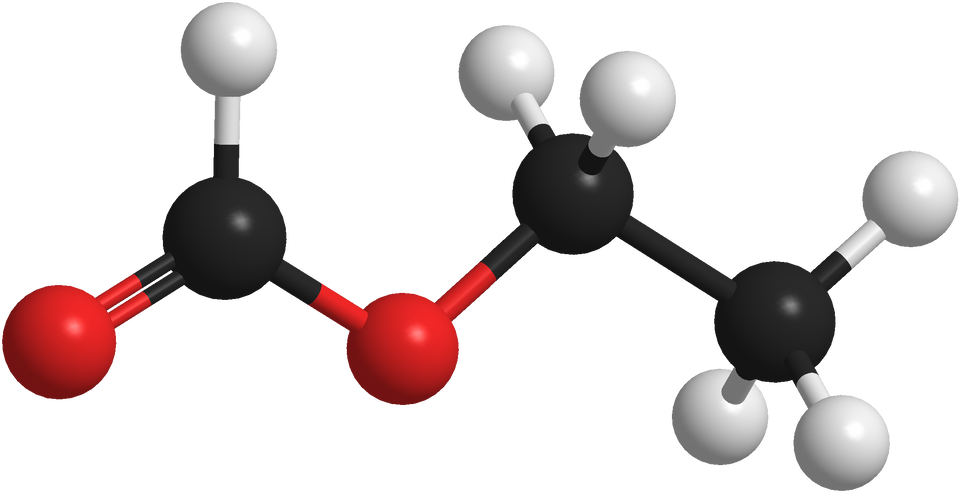
Podaj nazwę systematyczną tego estru.
Przyporządkuj wzór sumaryczny kwasu karboksylowego oraz nazwę systematyczną alkoholu do estru, którego wzór półstrukturalny przedstawiono poniżej.
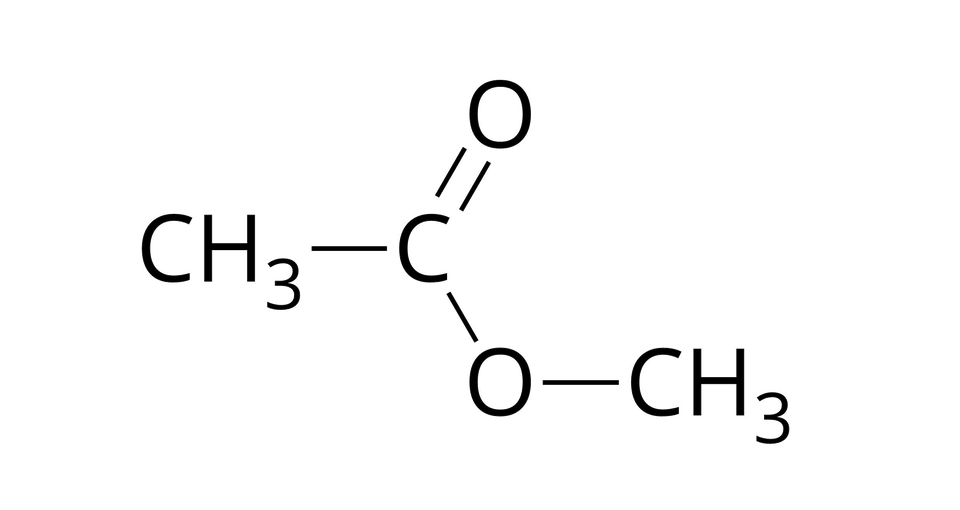
Zapisz równanie reakcji otrzymywania metanianu propylu z propan‑1-olu.
Bibliografia
Danikiewicz W., Podręcznik do kształcenia rozszerzonego w liceach, Część III. Chemia organiczna, Warszawa 2009.
Kulawik J., Kulawik T., Litwin M., Podręcznik do chemii dla klasy ósmej szkoły podstawowej, Warszawa 2020.
Łasiński D., Sporny Ł., Strutyńska D., Wróblewski P., Podręcznik dla klasy ósmej szkoły podstawowej, Mac Edukacja 2020.