Co to takiego stała dysocjacji?
Wiele reakcji chemicznych nie przebiega do końca, lecz po pewnym czasie osiąga stan, w którym w roztworze jednocześnie obecne są zarówno substraty, jak i produkty reakcji. Oznacza to, że tylko część indywiduów ulega przemianie, a pozostałe pozostają w postaci niezmienionej.
Taki stan nazywamy stanem równowagi chemicznej. W stanie tym skład roztworu nie zmienia się już w czasie, mimo że reakcja wciąż może zachodzić w obu kierunkach.
Jak definiuje się stałą dysocjacji?
Dlaczego kwasu chlorowodorowego (solnego) () jest niższe niż kwasu azotowego(III) (HNOIndeks dolny 22) o tym samym stężeniu? Który kwas jest kwasem słabym, a który mocnym? Z czego to wynika?
W stanie równowagi, w wodnym roztworze słabego kwasu, stężenie jonów nie jest równe stężeniu kwasu, jak w przypadku mocnego kwasu. Wynika to z faktu, że kwas ulega częściowej dysocjacji w wodzie.

Procesy równowagowe opisywane są za pomocą stałych równowagi reakcji. W stanie równowagi chemicznej stosunek iloczynu stężeń produktów do iloczynu stężeń substratów jest wielkością stałą, charakterystyczną dla danej reakcji (w danej temperaturze) i nosi nazwę stałej równowagi.
Stałą równowagi reakcji opisującej proces dysocjacji oznaczamy literą . Dla reakcji odwracalnej:
wyrażenie na stałą równowagi reakcji dysocjacji ma postać:
Gdzie:
– stała równowagi reakcji dysocjacji;
, , – równowagowe stężenia molowe.
Wielkość oznacza, że (w określonej temperaturze) w stanie równowagi stosunek iloczynu stężeń jonów oraz , powstałych w wyniku dysocjacji elektrolitycznej, do stężenia cząsteczek niezdysocjowanych jest wielkością stałą.
W przypadku dysocjacji w środowisku wodnym uwzględnia się również we wzorze wodę, której stężenie zapisuje się w mianowniku:
Stężenie wody w roztworach rozcieńczonych jest praktycznie wielkością stałą, dlatego można pomnożyć obie strony powyższego równania przez tę wartość, w wyniku czego otrzymuje się nową stałą – stałą dysocjacjistałą dysocjacji (również zapisywaną jako , w tej sekcji dla odróżnienia od stałej równowagi zapisywana będzie jako ):
Dla stałej dysocjacji kwasówkwasów w indeksie dolnym przy zapisujemy „a” – skrót pochodzi od angielskiego słowa acid, po polsku kwas – . Stałą dysocjacji zasad zapisujemy jako , gdzie „b” jest to skrót od angielskiego słowa base – zasadazasada.
W czasie dysocjacji słabych elektrolitów, np. słabych kwasów, nie wszystkie cząsteczki ulegają przemianom w jony. Ustala się zatem równowaga, którą dla słabych kwasów jednoprotonowych możemy zapisać w następujący sposób:
Gdzie:
– stała dysocjacji słabego kwasu;
, , , – równowagowe stężenia molowe.
Również amoniak rozpuszczony w wodzie nie ulega całkowitej, a tylko częściowej dysocjacji. Pomiędzy jonami powstałymi w czasie dysocjacji a cząsteczkami niezdysocjowanymi ustala się równowaga:
Gdzie:
– stała dysocjacji słabej zasady;
, , , – równowagowe stężenia molowe.
Stała dysocjacji jest wielkością bezwymiarową i dlatego wartości i w obliczeniach podaje się bez jednostki. Należy jednak pamiętać, że wartości stałych dysocjacji obliczane są w odniesieniu do stężeń molowych.
Stała dysocjacji a temperatura
Co istotne, wartość stałej dysocjacji zależy tylko od temperatury, a nie od stężenia elektrolituelektrolitu. Wraz ze wzrostem temperatury (reakcja endotermiczna), dysocjacja staje się łatwiejsza, a więc większe jest stężenie produktów dysocjacji. Tym samym rośnie wartość stałej dysocjacji. Zależność stałej dysocjacji od temperatury określa równanie:
gdzie:
– stała dysocjacji;
– stała charakterystyczna dla danej reakcji;
– ciepło reakcji ;
– stała gazowa, odpowiadająca wartości ;
– temperatura .
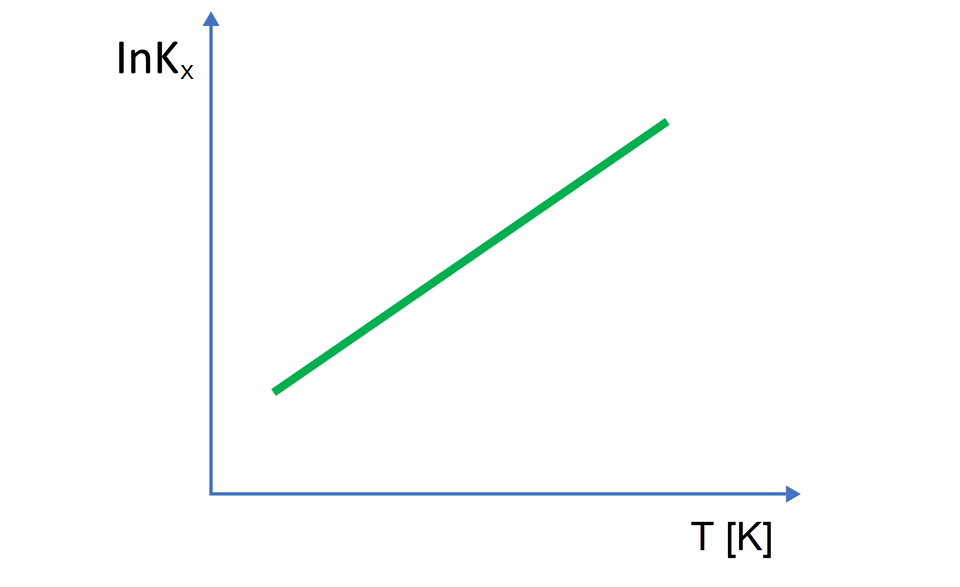
Można zatem zauważyć, że pobieranie ciepła do układu, w którym przebiega reakcja dysocjacji, oznacza jego przyrost, a tym samym rośnie temperatura. W tym wypadku wartość przyjmuje wartości dodatnie. Po podstawieniu dodatniej wartości do przedstawionego powyżej równania, zaobserwujemy wzrost wartości wraz ze wzrostem temperatury. Zależność taką prezentuje poniższy wykres.
Stała dysocjacji kwasów wieloprotonowych
Dla kwasów wieloprotonowych – dysocjujących wieloetapowo – można zauważyć, że stała dysocjacji pierwszego etapu () jest największa, a wartości kolejnych stałych dysocjacji się zmniejszają. Można to tłumaczyć tym, że w pierwszym etapie jon wodorowy odłącza się od cząsteczki elektrycznie obojętnej, natomiast w drugim etapie i każdym kolejnym musi oddysocjować od jonów naładowanych ujemnie, co jest znacznie trudniejsze. Tym samym widać wyraźnie, że w etapie pierwszym kwas dysocjuje w dużo większym stopniu niż w etapie drugim jon. W takim razie najbardziej intensywny jest etap dysocjacji, a każdy kolejny zachodzi coraz słabiej.
etap:
etap:
etap:
Jak wynika z powyższych zapisów, poszczególne etapy dysocjacji charakteryzują kolejne stałe dysocjacji, przy czym:
Dodatkowo ilości jonów z poszczególnych etapów dysocjacji są różne, przy czym najmniej jonów pochodzi z ostatniego etapu dysocjacji.
Stała dysocjacji a moc elektrolitu
Im większa wartość stałej dysocjacji, tym mocniejszy kwas lub zasada. Aby porównać moc kwasu, w przypadku kwasów wieloprotonowych, wybieramy pierwszą stałą dysocjacji (), przyjmując, że większość jonów pochodzi z pierwszego etapu dysocjacji. Dla przykładu, porównując wartości odpowiednich stałych dysocjacji, można stwierdzić, że azotowy() jest kwasem mocniejszym od kwasu węglowego , ale słabszym od kwasu chlorowego() .
Kwas nieorganiczny | Stała dysocjacji lub |
|---|---|
Zasada | Stała dysocjacji |
|---|---|
Indeks górny Źródło: Ł. Banasiak, J. Filipska, A. Grabowska, T. Ishikawa, M. Mroczek Wybrane wzory i stałe fizykochemiczne na egzamin maturalny z biologii, chemii i fizyki, Warszawa 2022. Wybrane wzory i stałe fizykochemiczne na egzamin maturalny z biologii, chemii i fizyki, Warszawa 2015. Indeks górny koniecŹródło: Ł. Banasiak, J. Filipska, A. Grabowska, T. Ishikawa, M. Mroczek Wybrane wzory i stałe fizykochemiczne na egzamin maturalny z biologii, chemii i fizyki, Warszawa 2022. Wybrane wzory i stałe fizykochemiczne na egzamin maturalny z biologii, chemii i fizyki, Warszawa 2015.
Częściej w tablicach pojawia się informacja o wartości stałej . Wówczas stałą , dla sprzężonej pary kwas‑zasada, można obliczyć, korzystając z zależności:
Powyższe równanie można także zapisać, stosując ujemne logarytmy. Wtedy otrzymujemy:
oraz
Otrzymujemy równanie:
Wykonaj kilka ćwiczeń
Zdefiniuj pojęcie stałej dysocjacji elektrolitycznej.
Czy wiesz, jakie pH mają substancje, z którymi masz styczność na co dzień? Przeanalizuj grafiki interaktywne, a następnie rozwiąż zadania.
Czy wiesz, jakie pH mają substancje, z którymi masz styczność na co dzień? Zapoznaj się z opisami grafik interaktywnych, a następnie rozwiąż zadania.
Roztwór A ma , a roztwór B ma . Określ pOH dla roztworu A, dla roztworu B pH oraz podaj stosunek stężeń do w obu roztworach.
Roztwór A ma , a roztwór B ma . Określ pOH dla roztworu A, dla roztworu B pH oraz podaj stosunek stężeń do w obu roztworach.