Denaturacja i wysalanie białek
Denaturacja
W trakcie smażenia jajka na patelni łatwo zaobserwować zmianę jego zabarwienia i struktury. Pod wpływem wysokiej temperatury pojawia się nowy twór, który właściwościami fizycznymi nie przypomina materii sprzed kilku minut. Sprawcą całego zdarzenia jest denaturacja.
Proces ten polega na utracie aktywności biologicznej oraz zniszczeniu struktur białek: drugo-, trzecio- i czwartorzędowych. Nie zostaje zmieniona jedynie struktura pierwszorzędowa, ponieważ wiązania peptydowe są wystarczająco silne, żeby pozostać nierozerwane. Podczas denaturacji zostają jednak zerwane wiązania stabilizujące pozostałe struktury białka, przez co dochodzi do zmian we właściwościach fizycznych i chemicznych protein. Ogólny schemat denaturacji przedstawiono poniżej.

Czynniki wpływające na denaturację białek
Białka mogą ulegać denaturacji pod wpływem wielu różnych czynników, które ogólnie podzielono na dwie grupy – czynniki fizyczne i chemiczne – co zostało przedstawione na poniższej mapie myśli.
- Nazwa kategorii: Czynniki denaturujące
- Nazwa kategorii: Fizyczne
- Nazwa kategorii: Temperatura
- Nazwa kategorii: Ciśnienie
- Nazwa kategorii: Wytrząsanie
- Nazwa kategorii: Promieniowanie UV i RTG
- Nazwa kategorii: Promieniowanie jonizujące
- Nazwa kategorii: Ultradźwięki Koniec elementów należących do kategorii Fizyczne
- Nazwa kategorii: Chemiczne
- Nazwa kategorii: Sole metali ciężkich
- Nazwa kategorii: Mocne kwasy i zasady
- Nazwa kategorii: Etanol
- Nazwa kategorii: Detergenty
- Nazwa kategorii: Niektóre kwasy organiczne
- Nazwa kategorii: Sole amonowe Koniec elementów należących do kategorii Chemiczne
- Elementy należące do kategorii Czynniki denaturujące
- Elementy należące do kategorii Fizyczne
- Elementy należące do kategorii Chemiczne
Temperatura
Wysoka temperatura (dla niektórych białek wystarczy ) powoduje rozerwanie wiązań wodorowych i oddziaływań hydrofobowych. Dzieje się tak, ponieważ podwyższając temperaturę, dostarczamy do układu dodatkową energię, która zwiększa energię kinetycznąenergię kinetyczną układu. Powoduje to zwiększony ruch cząsteczek. W ten sposób dochodzi do zerwania wiązań. W życiu codziennym takie zjawisko zachodzi podczas gotowania produktów żywnościowych. Zdenaturowane białka są bardziej podatne na działanie licznych enzymów, co ułatwia nam trawienie pożywienia i wchłanianie potrzebnych substancji odżywczych. Również podczas sterylizacjisterylizacji narzędzi czy opatrunków medycznych zwiększa się temperaturę. Tak niszczone są białka, które występują w patogenach, a tym samym zostają unieszkodliwione potencjalne mikroorganizmy, wywołujące choroby.
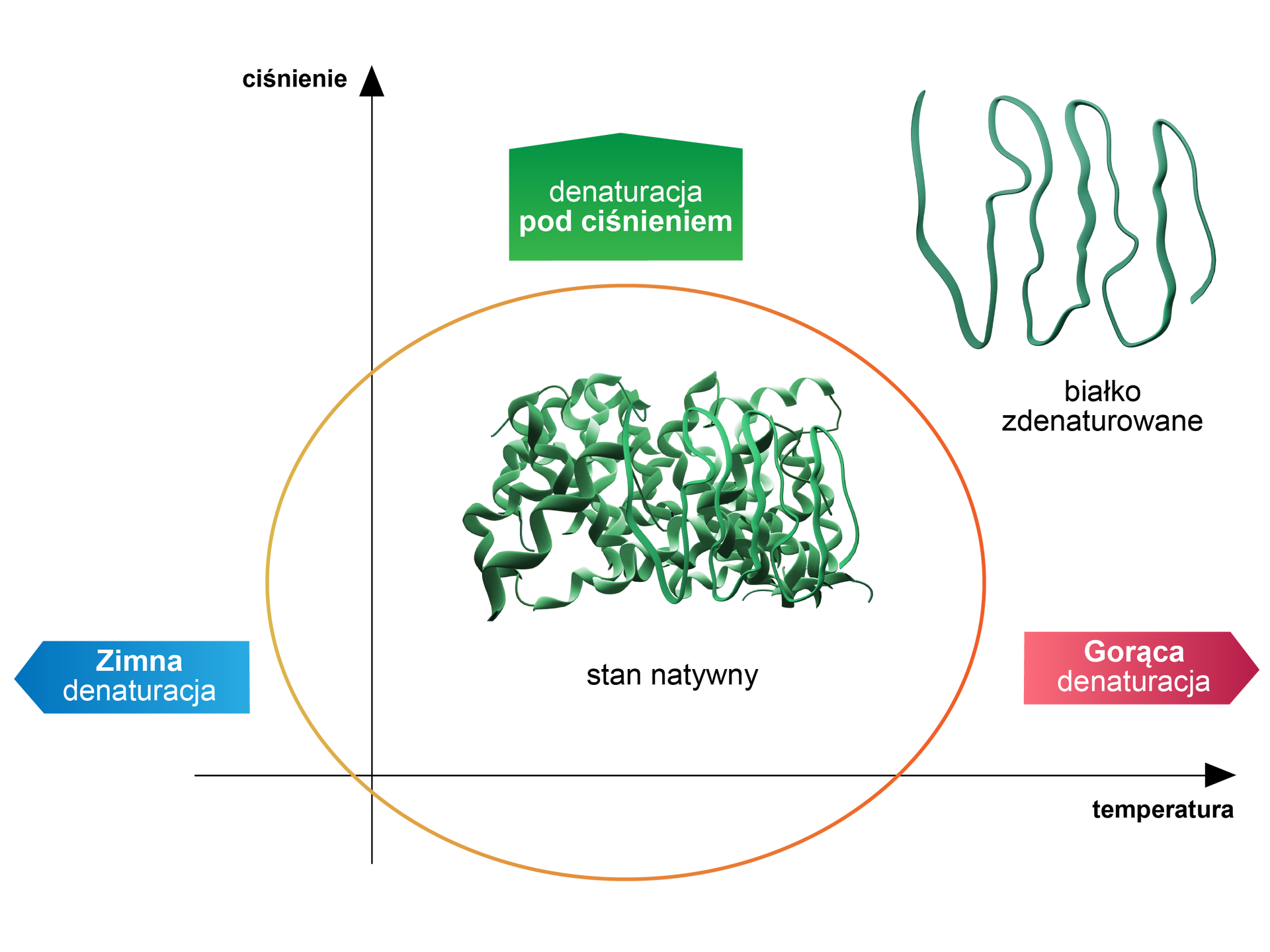
Może także dojść do tzw. zimnej denaturacji, z którą mamy do czynienia przy niskiej temperaturze i wysokim ciśnieniu (powyżej ). Takie warunki sprzyjają zmniejszeniu oddziaływań hydrofobowych, wówczas struktura białka ulega rozwinięciu. Na poniższym wykresie zaprezentowano rodzaje denaturacji i jej zależność od temperatury i ciśnienia.
Promieniowanie UV
Promieniowanie UV, nazywane również promieniowaniem nadfioletowym, to promieniowanie elektromagnetyczne o długości około – . W zależności od długości fali, wyróżnia się promieniowanie UVA, UVB i UVC. Słońce emituje fale we wszystkich trzech zakresach, natomiast na Ziemię dociera tylko część promieniowania UVB i całe UVA, które jest mniej szkodliwe dla człowieka niż pozostałe rodzaje. Promieniowanie UV w dużych dawkach powoduje rozerwanie wiązań wodorowych w białkach, co prowadzi do zniszczenia struktur drugo-, trzecio-, i czwartorzędowych. Dlatego długotrwałe narażanie się na promienie słoneczne nie jest wskazane ze względu na zwiększenie ryzyka zachorowań na nowotwory skóry. Jednak minimalna dawka promieniowania jest potrzebna dla organizmu do produkcji witaminy .
Wytrząsanie
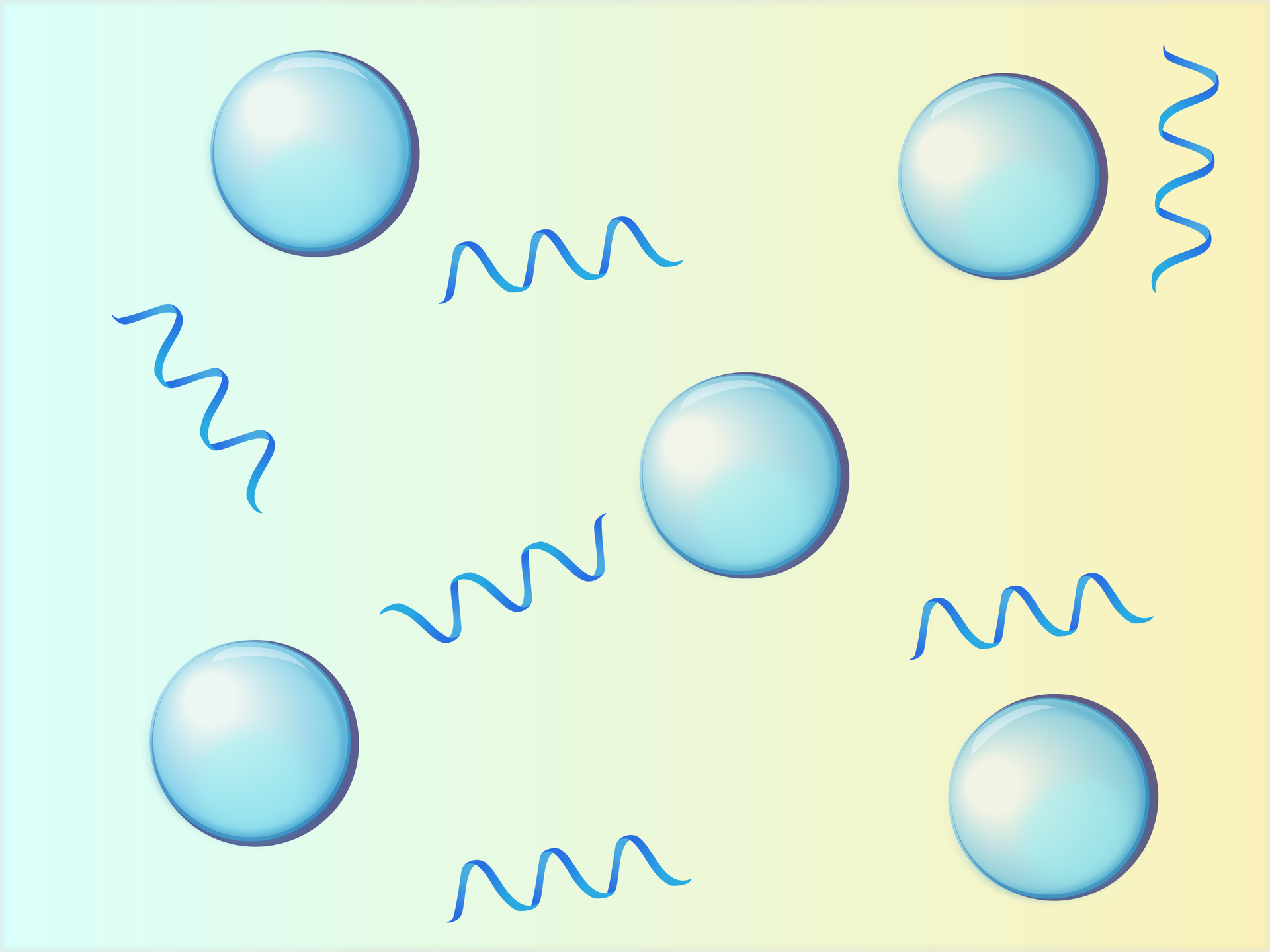
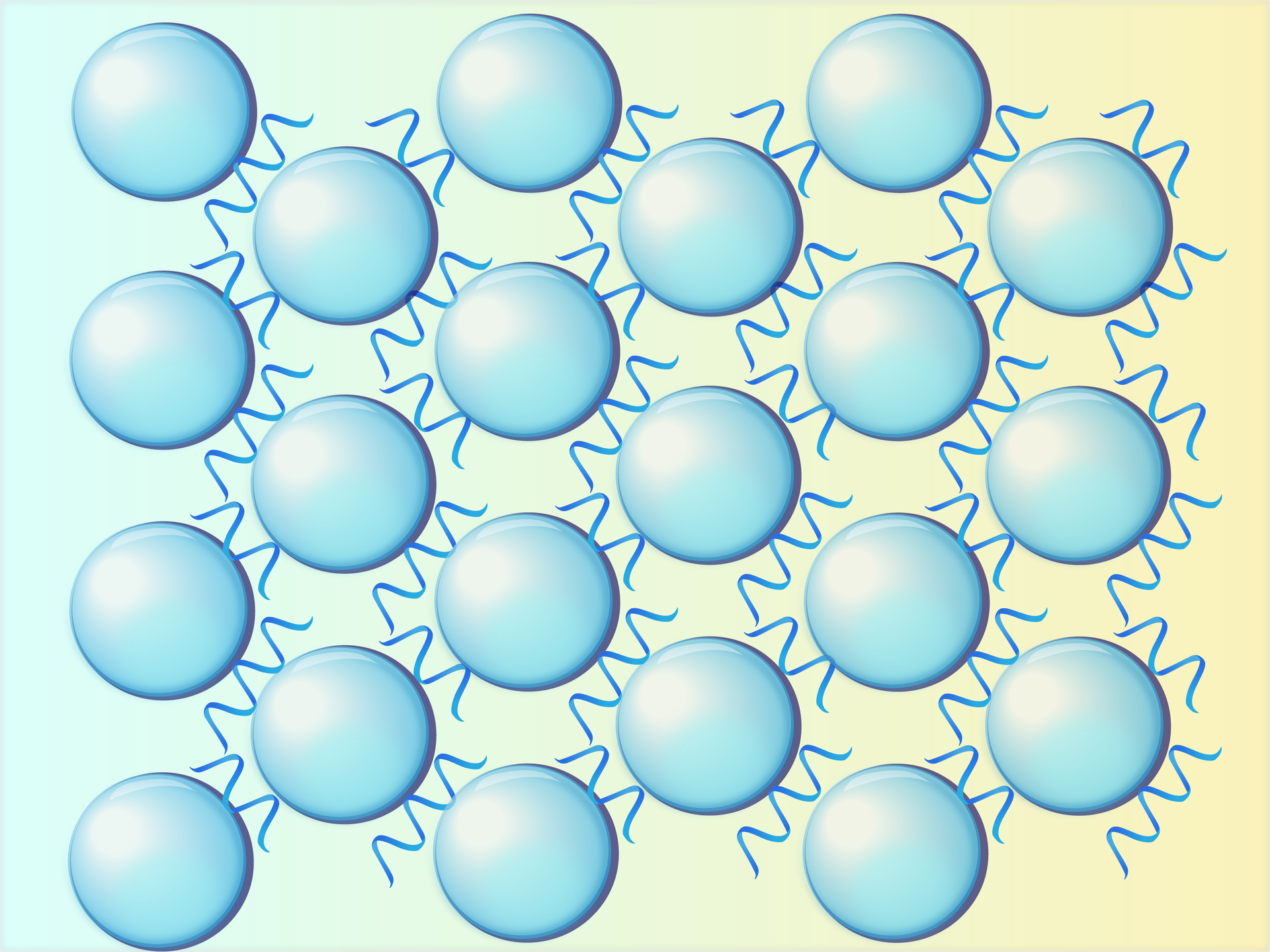
Gwałtowne mieszanie czy ubijanie białka powoduje zerwanie wiązań wodorowych. To właśnie dzieje się w momencie ubijania piany z białek. Dochodzi wtedy do zerwania wiązań i wprowadzenia pęcherzyków gazów do układu. Następnie cząsteczki białek tworzą nowe wiązania, które oplatają cząsteczki gazów, tworząc tym samym strukturę piany. Schemat reakcji zamieszczono poniżej. Proces tworzenia nowych wiązań w białku nosi nazwę koagulacjikoagulacji.
niebieskie tło to cząsteczki wody;
zwinięte kłębki to białko;
fale to zdenaturowane białka;
białe okręgi w środku to pęcherzyki powietrza.
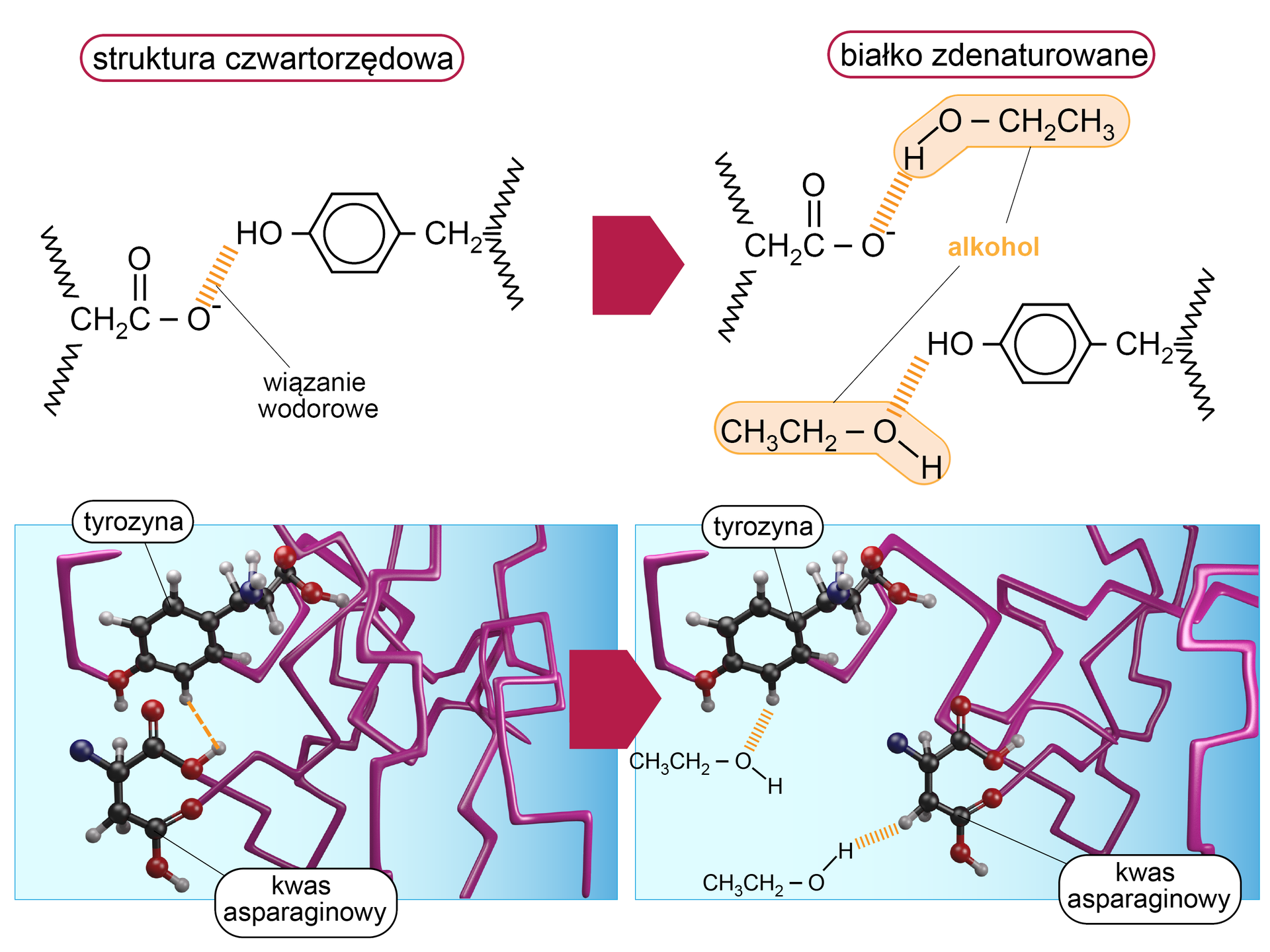
Etanol
Ten związek chemiczny zrywa wiązania wodorowe w białkach i wiążę się z grupami chemicznymi białek. Dla przykładu: etanol ma zdolność do przenikania przez ściany komórkowe bakterii i denaturacji obecnych w mikroorganizmach białek i enzymów, co prowadzi do śmierci komórki. Taka właściwość alkoholu, nazywana bakteriobójczą, jest wykorzystywana do dezynfekcji. Spożywanie etanolu sprawia, że białka, które budują nasz organizm, ulegają denaturacji i przez to nie mogą pełnić swoich funkcji. Etanol znajduje się w piwie, winie czy innych wyrobach alkoholowych.
Sole metali ciężkich
Sole metali ciężkich to związki chemiczne zawierające jony: , , , , i jony innych metali o gęstości większej niż . Niszczą one wiązania jonowewiązania jonowe w białku i prowadzą do zniszczenia mostków solnychmostków solnych i mostków disiarczkowychmostków disiarczkowych. Produktem takiej reakcji jest sól białka i metalu ciężkiego. Taką właściwość wykorzystuje się w przypadku zatrucia organizmu związkami metali ciężkich. Pacjentowi podaje się białko, które wytrąca sól, a następnie wywołuje się wymioty, usuwające z organizmu toksyny. Na przykład osobie zatrutej solami rtęci należy podać do wypicia mleko z białkiem kurzym, by doprowadzić do mdłości. W tym przypadku białka, zawarte w mleku i białku kurzym, wychwytują jony rtęci i są usuwane z organizmu.
Mocne kwasy i zasady
Mocne kwasy i zasady ulegają dysocjacji elektrolitycznejdysocjacji elektrolitycznej w roztworze rozpuszczalnika. Zaburzają one wiązania jonowe w mostkach solnychmostkach solnych w białku, niszcząc jego strukturę natywnąstrukturę natywną.
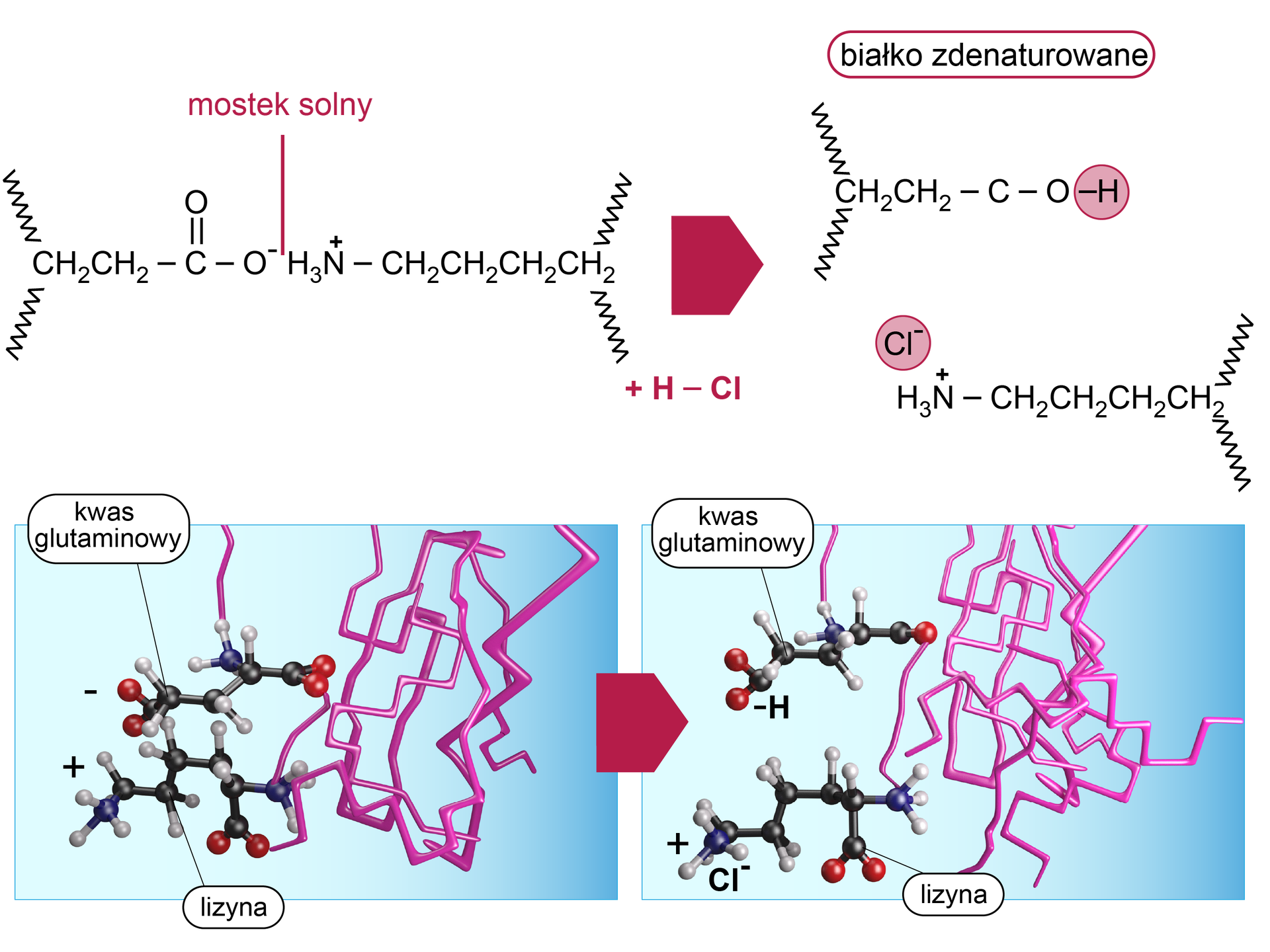
Zaprezentowane powyżej przykłady denaturacji nie są wszystkimi możliwymi reakcjami. Wśród związków chemicznych, które powodują zniszczenie struktury natywnej białka, znajdują się m.in.: mocznik, guanidyna, SDS (sól sodowa siarczanu() dodecylu).
Denaturacja jako proces nieodwaracalny
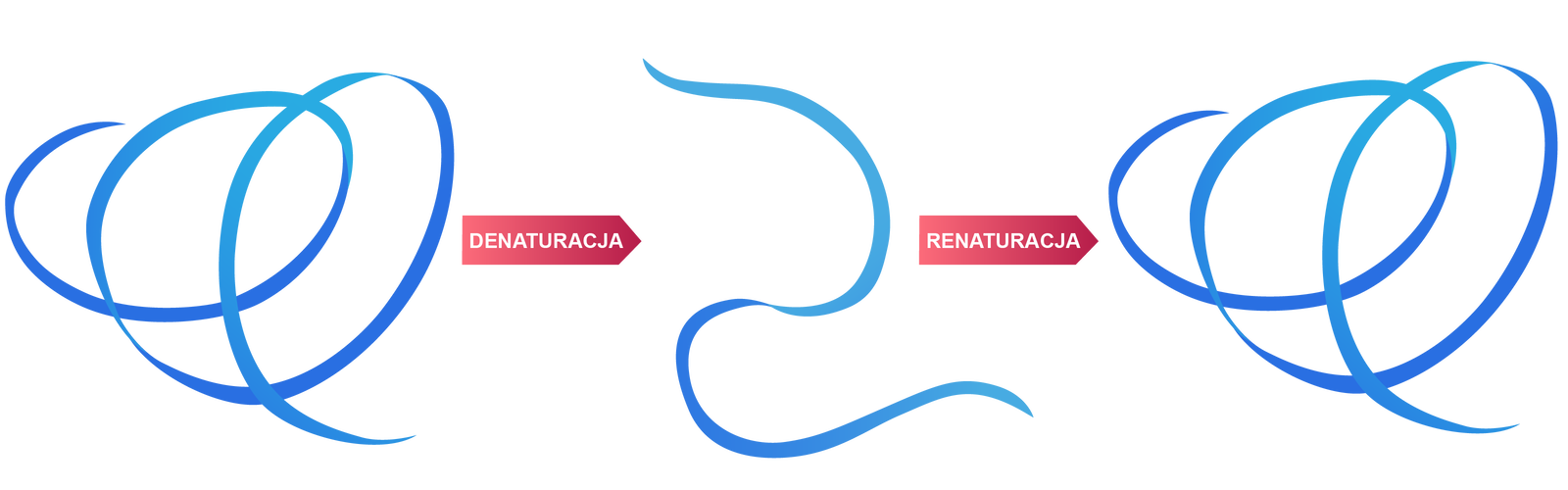
Denaturacja nie jest procesem nieodwracalnym. W początkowym jego etapie, po usunięciu czynnika denaturującego, może dojść do odtworzenia struktury natywnej białka. Takie zjawisko nazywa się renaturacją. Schemat został przedstawiony poniżej. Przykładem denaturacji odwracalnej jest zastosowanie soli amonowych, których użycie prowadzi do usunięcia płaszcza wodnego białka i zmiany jego struktury przestrzennej. Po dodaniu wody, białko wraca do struktury wyjściowej. Do czynników fizycznych, przyczyniających się do denaturacji nieodwracalnej, zaliczamy: ogrzewanie, silnie mieszanie, wytrząsanie, naświetlanie promieniowaniem nadfioletowym, rentgenowskimi i jonizującym lub działanie ultradźwiękami. Natomiast denaturacja chemiczna zachodzi w obecności mocznika, chlorku guanidyny, na skutek działania kwasów i zasad, soli metali ciężkich, alkoholi. Wszystkie te czynniki powodują rozerwanie wiązań wodorowych, jonowych, mostków disiarczkowych, czyli niszczą wiązania, które stabilizują strukturę łańcuchów polipeptydowych.
Sprawdź w poniższych laboratoriach, jakie czynniki powodują denaturację białek.
Przeprowadź doświadczenie w laboratorium chemicznym. Rozwiąż problem badawczy i zweryfikuj hipotezę. W formularzu zapisz swoje obserwacje i wyniki, a następnie sformułuj wnioski.
Szafa laboratoryjna
Zapoznaj się z opisem doświadczenia, a następnie rozwiąż zadania.
Analiza doświadczenia: Badanie wpływu wybranych czynników fizycznych i chemicznych na struktury białkowe.
Problem badawczy: Jakie czynniki wpływają na denaturację struktur białkowych?
Hipoteza: Zastosowanie detergentu, roztworu kwasu octowego oraz roztworu wodorotlenku sodu powoduje denaturację białka jaja kurzego.
Sprzęt laboratoryjny:
probówki – podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipeta – wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
lampa UV – sprzęt służący do naświetlania.
Odczynniki:
detergent,
roztwór kwasu octowego,
roztwór wodorotlenku sodu,
białko jaja kurzego.
Przebieg doświadczenia:
Rozlano białko jaja kurzego do czterech probówek – podłużnych naczyń szklanych do przeprowadzania prostych reakcji chemicznych.
Do pierwszej probówki wlano detergentu.
Do drugiej probówki wlano stężonego kwasu octowego.
Do trzeciej probówki wlano roztworu wodorotlenku sodu.
Czwartą probówkę naświetlano lampą UV przez minut (ustaw promieniowanie lampy na wylot probówki, gdyż szkło absorbuje część promieniowania UV).
Obserwacje:
Eksperyment z użyciem detergentu: Po wymieszaniu białka z detergentem w probówce wytrąca się biały, nitkowaty osad.Po wymieszaniu białka z detergentem w probówce wytrąca się biały, nitkowaty osad.
Eksperyment z użyciem stężonego kwasu octowego: Po wymieszaniu białka z detergentem w probówce wytrąca się biały, nitkowaty osad.
Eksperyment z użyciem roztworu wodorotlenku sodu: Po wymieszaniu białka z detergentem w probówce wytrąca się biały, nitkowaty osad.
Eksperyment z naświetlaniem lampą UV: Po czasie wytrąca się biały, nitkowaty osad.
Wyniki: Działanie czynników chemicznych i fizycznych spowodowało denaturacje białek.
Wnioski: Denaturację wywołują czynniki fizyczne, np. promieniowanie ultrafioletowe oraz czynniki chemiczne, np.: kwasy, zasady, detergenty.
Przeprowadź eksperyment w laboratorium chemicznym. Sformułuj problem badawczy i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.
Badanie wpływu soli metali ciężkich, alkoholu, kwasu i temperatury na roztwór białka.
Szafa laboratoryjna
Przeprowadzono doświadczenie, które miało na celu zbadanie oddziaływania białka z różnymi czynnikami. Zapoznaj się z opisem doświadczenia, a następnie wykonaj zadania.
Analiza eksperymentu: Badanie działania różnych czynników na roztwór białka.
Problem badawczy: Jak białko reaguje na obecność etanolu, siarczanu() miedzi(), kwasu chlorowodorowego i wrzącej wody destylowanej?
Hipoteza: Białko ulega denaturacji pod wpływem alkoholu etylowego, kwasu chlorowodorowego, roztworu siarczanu() miedzi() i wysokiej temperatury.
Sprzęt laboratoryjny:
pipety Pasteura – wąskie rurki do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
cztery probówki – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
czajnik – urządzenie elektryczne, służące do zagotowania wody.
Odczynniki chemiczne:
białko jaja kurzego
alkohol etylowy ;
roztwór siarczanu( ) miedzi( ) ;
roztwór kwasu chlorowodorowego ;
woda destylowana (wrząca).
Przebieg eksperymentu:
Rozlano białko jaja kurzego do czterech probówek.
a) Do pierwszej probówki wlano etanolu.
b) Do drugiej probówki wlano roztworu siarczanu() miedzi().
c) Do trzeciej probówki wlano roztworu kwasu chlorowodorowego.
d) Do czwartej probówki wlano wrzącej wody destylowanej.Wstrząśnięto probówkami i obserwowano zmiany.
Obserwacje:
We wszystkich probówkach białko uległo koagulacji wytrącając biały, nitkowaty osad.
Wyniki:
Alkohol etylowy, siarczan() miedzi(), stężony kwas chlorowodorowy oraz wrząca woda destylowana powodują denaturację białek.
Wnioski:
Obserwowany proces nieodwracalnego ścinania białka to denaturacja. W trakcie denaturacji, białko zmienia swoją strukturę i pierwotne właściwości. Czynnikami powodującymi denaturację białka są:
wysoka temperatura;
sole metali ciężkich;
kwasy;
alkohole.
Wysalanie białek
Pamiętasz z pewnością, że roztwory dzielą się na trzy główne typy: roztwory właściwe, koloidalne oraz zawiesiny. To, co je od siebie odróżnia, to średnica cząstek fazy rozproszonej (składnik, który chcemy rozpuścić) w fazie rozpraszającej, czyli w rozpuszczalniku. W tym rozdziale zajmiemy się koloidami, a właściwie jednym szczególnym, z punktu widzenia nauki w szkole średniej, typem roztworu koloidalnego, czyli wodnym roztworem białek.
Koloidy należą do mieszanin niejednorodnych, heterogenicznych, w których średnica cząstek fazy rozproszonej mieści się w przedziale od do (czyli od do ). W roztworze wodnym białka fazą rozproszoną jest np. białko jaja kurzego, a fazą rozpraszającą (rozpuszczalnikiem) woda.
Białka to makrocząsteczki, które występują w każdym żywym organizmie. Musimy pamiętać, że istnieje wiele typów białek, a funkcje, jakie spełniają są bardzo różnorodne. Jednak wszystkie białka łączy to, że są zbudowane z dużej liczby reszt jednostek aminokwasowych połączonych w długi łańcuch. Istotne jest również to, że łańcuchy te zawierają wiele hydrofilowych (polarnych) elementów strukturalnych. A ta cecha z kolei jest kluczowa w tym rozdziale.
Badanie rozpuszczalności białka w wodzie
Wyobraź sobie, że rozpuszczamy białko jaja kurzego w wodzie.
Obserwujemy wówczas, że białko „wisi” w wodzie, a po dokładnym wymieszaniu, tworzy się emulsja. Otrzymaliśmy typowy roztwór koloidalny.
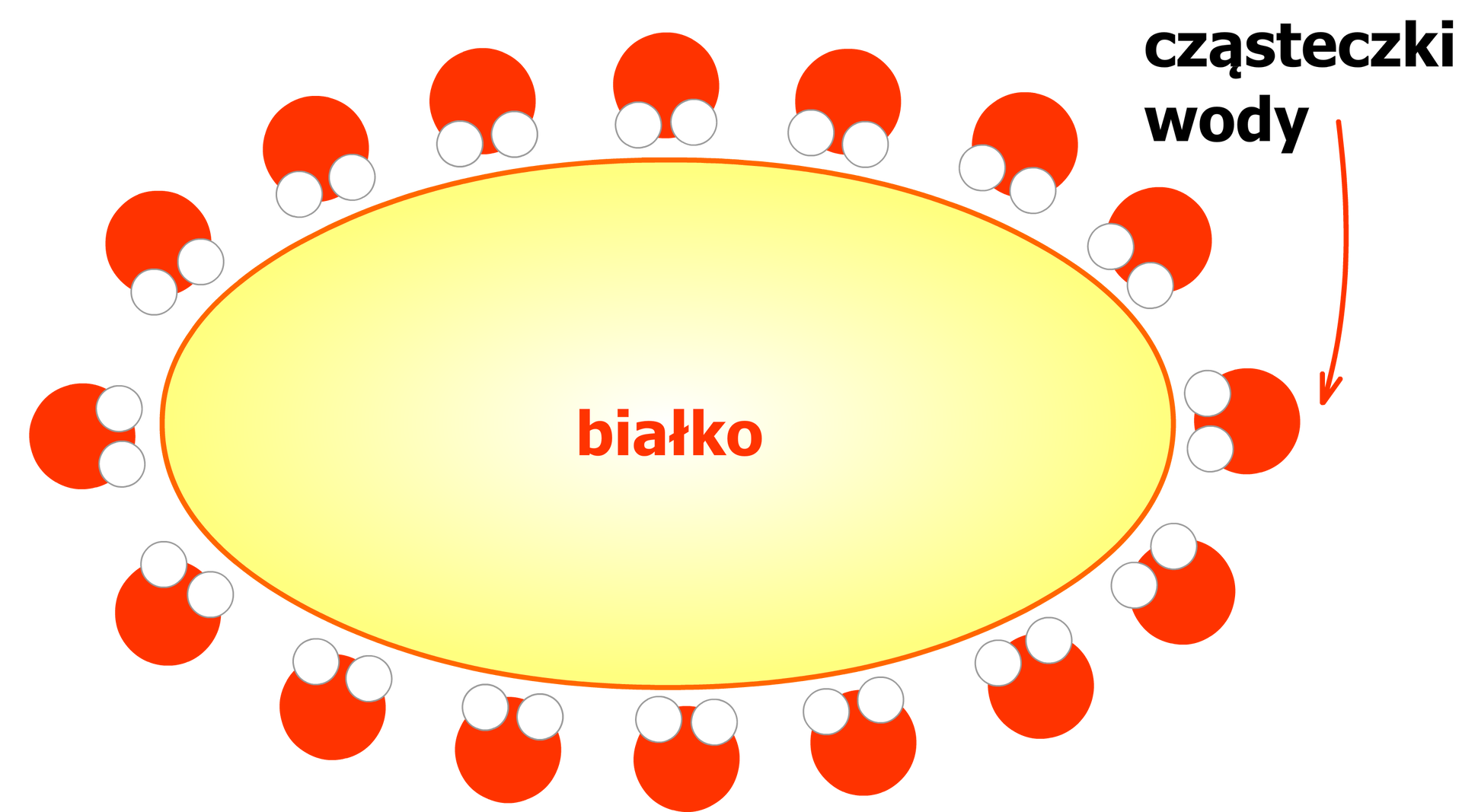
Przyczyną powstawania koloidu jest duży rozmiar cząsteczek białka. Oddziałują one solwatacyjnie z cząsteczkami wody. Innymi słowy są przez wodę hydratowane. A hydratacja to proces otaczania cząsteczek rozpuszczanego związku chemicznego przez wodę. To zjawisko jest możliwe dzięki własnościom polarnym wody oraz obecności w łańcuchach aminokwasowych białek grup polarnych, takich jak np.:
(grupa karboksylowa),
(grupa aminowa),
które oddziałują z wodą za pomocą wiązań wodorowych.
Sprawdź,w poniższym laboratorium, czy wysalanie jest procesem odwracalnym.
Rozpuszczalne białka, pomimo dużych cząsteczek, utrzymują się w roztworze z uwagi na fakt otaczania się dipolami wody. Jednak po dodaniu do takich roztworów białek soli dobrze rozpuszczalnych w wodzie, następuje odciągnięcie cząsteczek wody z powierzchni tych makromolekuł i w konsekwencji białka wytrącają się z roztworu. Zachodzi zjawisko wysalania. Czy to prawda, że zjawisko to, podobnie jak zjawisko denaturacji, jest procesem nieodwracalnym?
Zaprojektuj doświadczenie, za pomocą którego zweryfikujesz przedstawioną hipotezę badawczą. Zapisz w formularzu obserwacje, wyniki oraz wnioski. Spróbuj wykonać doświadczenie samodzielnie. Jeśli jednak będziesz mieć problemy, możesz skorzystać z instrukcji, która znajduje się pod ikoną notatnika w lewym górnym rogu.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D5VMUAGP6
Analiza doświadczenia: Badanie procesu wysalania białek.
Problem badawczy: Czy to prawda, że zjawisko wysalania, podobnie jak zjawisko denaturacji białek, jest procesem nieodwracalnym?
Hipoteza: Zjawisko wysalania białka jest procesem odwracalnym.
Sprzęt laboratoryjny:
5 probówek – podłużne naczynia szklane do przeprowadzania prostych reakcji chemicznych;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;
cylinder miarowy – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości; służy do odmierzania cieczy;
tryskawka z wodą destylowaną – naczynie z tworzywa sztucznego zamknięte nakrętką z długą końcówką – rurką sięgającą dna naczynia i wyprowadzoną na zewnątrz, gdzie się ona zwęża; tryskawka wypełniona jest wodą, która pod wpływem nacisku na plastikowe naczynie, uwalnia wodę na zewnątrz przez długą końcówkę;
pipety Pasteura – wąska rurka do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
korki do probówek – niewielki element wykonany z korka, służący do szczelnego zamykania probówek.
Odczynniki:
białko jaja kurzego, woda destylowana, wodne roztwory: siarczanu() amonu, chlorku sodu, siarczanu() sodu, siarczanu() magnezu, siarczanu() miedzi.
Przebieg doświadczenia:
Do pięciu probówek dodano jednakową objętość białka jaja kurzego.
Następnie dodano do nich roztwory soli: do pierwszej probówki siarczan() amonu, do drugiej chlorek sodu, do trzeciej siarczan() sodu, do czwartej siarczan() magnezu, do piątej siarczan() miedzi.
Wszystkie probówki zatkano korkami i wstrząśnięto.
Obserwowano zachodzące zmiany.
Następnie do każdej z nich dodano wody destylowanej, odmierzonej za pomocą cylindra miarowego.
Wszystkie probówki ponownie wstrząśnięto i obserwowano zachodzące zmiany.
Obserwacje:
Po dodaniu do roztworu białka dostępnych w laboratorium soli, strącił się biały osad. Po dolaniu wody i wstrząśnięciu, osad zniknął w czterech pierwszych probówkach. Pozostał tylko w probówce, gdzie dodany był siarczan() miedzi().
Wyniki:
W probówkach, gdzie dodano siarczan() amonu, chlorek sodu, siarczan() sodu, siarczan() magnezu, zachodzi odwracalny proces, natomiast siarczan() miedzi() powoduje nieodwracalną zmianę.
Wnioski:
W probówkach, gdzie dodano siarczan() amonu, chlorek sodu, siarczan() sodu, siarczan() magnezu, zachodzi proces wysalania białka – jest to proces odwracalny. Sole metali ciężkich (np. siarczan() miedzi()) powodują nieodwracalną denaturację białka. Hipoteza została potwierdzona.
Który z przedstawionych poniżej rysunków obrazuje doświadczalny proces wysalania białka, a który denaturacji?
Który z opisanych rysunków przedstawia doświadczalny proces wysalania białka, a który denaturacji?
Kiedy mamy już przygotowany roztwór białka w wodzie, to wyobraźmy sobie, że dodajemy do niego nasycony roztwór soli kuchennej (). Obserwujemy wówczas zmianę konsystencji. Roztwór białka robi się gęstszy i powstają w nim białe grudki. Natomiast kiedy dodamy do roztworu wodę, to zaobserwujemy ponowne utworzenie roztworu koloidalnego.

Po dodaniu soli metalu lekkiego, otoczka solwatacyjna tworzona przez wodę zostaje zniszczona. Jony mocnego elektrolitu są silniej solwatowane niż białko. Następuje wówczas wytrącenie białka z roztworu w postaci charakterystycznego osadu – żelu. Jest to proces koagulacji odwracalnej, czyli wysalania. Po dodaniu wody, białko przyjmuje pierwotną postać, ponieważ nadmiar wody odbudowuje otoczkę hydratacyjną. Takie ponowne przejście żelu w zol nazywane jest peptyzacją.

Należy pamiętać, że proces wysalania nie niszczy struktur białka, co wiąże się z zachowaniem przez białko swojej biochemicznej funkcjonalności. Koagulację odwracalną powodują tylko nasycone roztwory soli metali lekkich oraz amonowych.