Dysocjacja elektrolityczna
Dysocjacja elektrolityczna kwasów
Zbadaj przewodzenie prądu elektrycznego przez wodę i roztwory wodne , i . Wstaw końcówki elektrod do przygotowanych roztworów, zamykając w ten sposób obwód elektryczny. Obserwuj, w których roztworach zaświeci się dioda LED.
Podsumowanie doświadczenia (symulacji)
Woda destylowana nie przewodzi prądu. Przez pozostałe roztwory przepływa prąd elektryczny, o czym świadczy świecenie diody LED. Roztwory wodne kwasów przewodzą prąd elektryczny – znajdują się w nich jony, które są nośnikami ładunku elektrycznego.
Cząsteczki wody są zdysocjowane w znikomej ilości, przez co możemy traktować wodę jako nieelektrolit. Kwasy przedstawione w symulacji są elektrolitami i przewodzą prąd elektryczny.
Dysocjacja elektrolityczna chlorowodoru
W jaki sposób przebiega dysocjacja elektrolityczna chlorowodoru? Obejrzyj poniższy film.

Film dostępny pod adresem /preview/resource/R5X1cEGlbJ8XS
Film pod tytułem Dysocjacja chlorowodoru
Niektóre cząsteczki, takie jak chlorowodór, ulegają w wodzie praktycznie całkowitej dysocjacji elektrolitycznej. Oznacza to, że w utworzonym roztworze kwasu chlorowodorowego nie występują cząsteczki , lecz jedynie jony. Takie elektrolity nazywamy mocnymi. Strzałka wskazuje na to, że proces dysocjacji przebiega jednokierunkowo. Należy przy tym pamiętać, że jon (kation wodoru) nie występuje samodzielnie w roztworze wodnym. W obecności cząsteczek , łączy się z nimi, tworząc jon hydroniowy (najprostszy jon oksoniowy) o wzorze . Dlatego równanie reakcji dysocjacji elektrolitycznej chlorowodoru ma następującą postać:
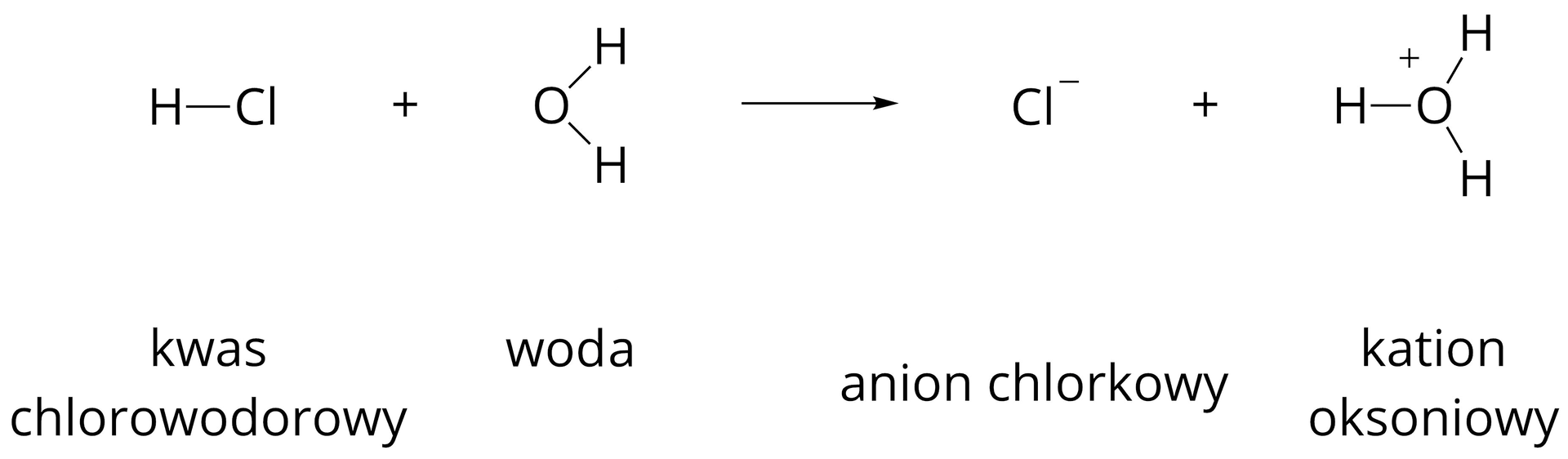
Często stosuje się jednak zapis uproszczony, w którym powstają kationy wodoru i aniony chlorkowe, zgodnie z następującym równaniem:
Dysocjacja elektrolityczna siarkowodoru
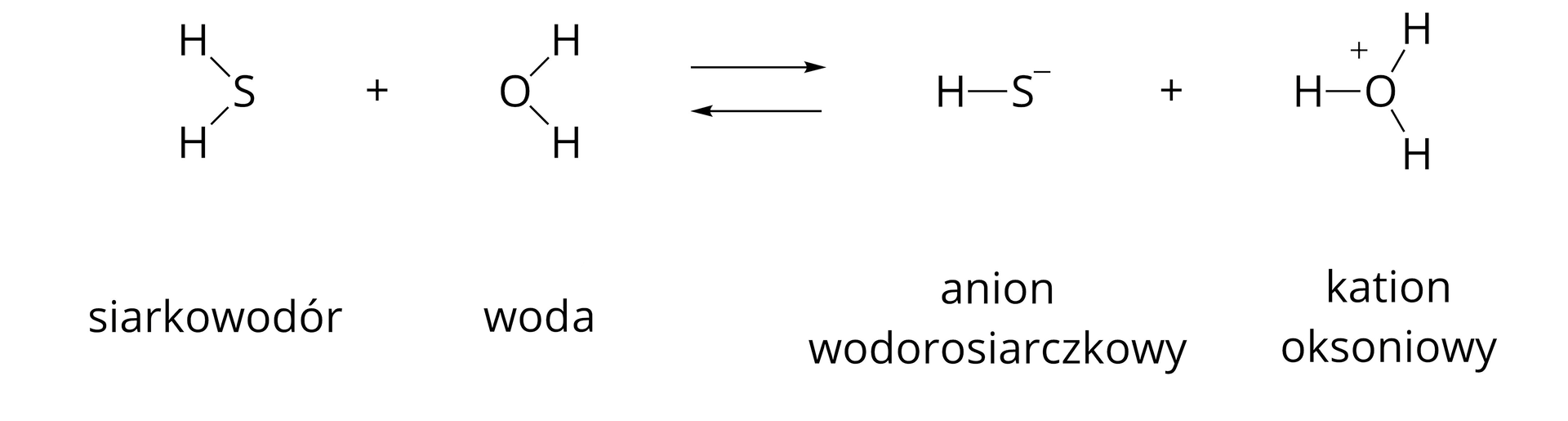
Cząsteczka siarkowodoru należy do słabych elektrolitów. Oznacza to, że w wodnym roztworze, obok jonów, występują również niezdysocjowane cząsteczki . W przypadku słabych wieloprotonowych elektrolitów, dochodzi do wielostopniowej dysocjacji elektrolitycznej.
W pierwszym etapie dysocjacji następuje oderwanie kationu wodoru od cząsteczki siarkowodoru. Powstaje zatem anion wodorosiarczkowy o wzorze . Jednocześnie kation wodoru łączy się z cząsteczką wody, tworząc kation oksoniowy (kation hydroniowy).
W drugim etapie dysocjacji następuje oderwanie kationu wodoru od anionu wodorosiarczkowego. Powstaje zatem anion siarczkowy o wzorze . Jednocześnie kation wodoru łączy się z cząsteczką wody tworząc jon oksoniowy (kation hydroniowy).
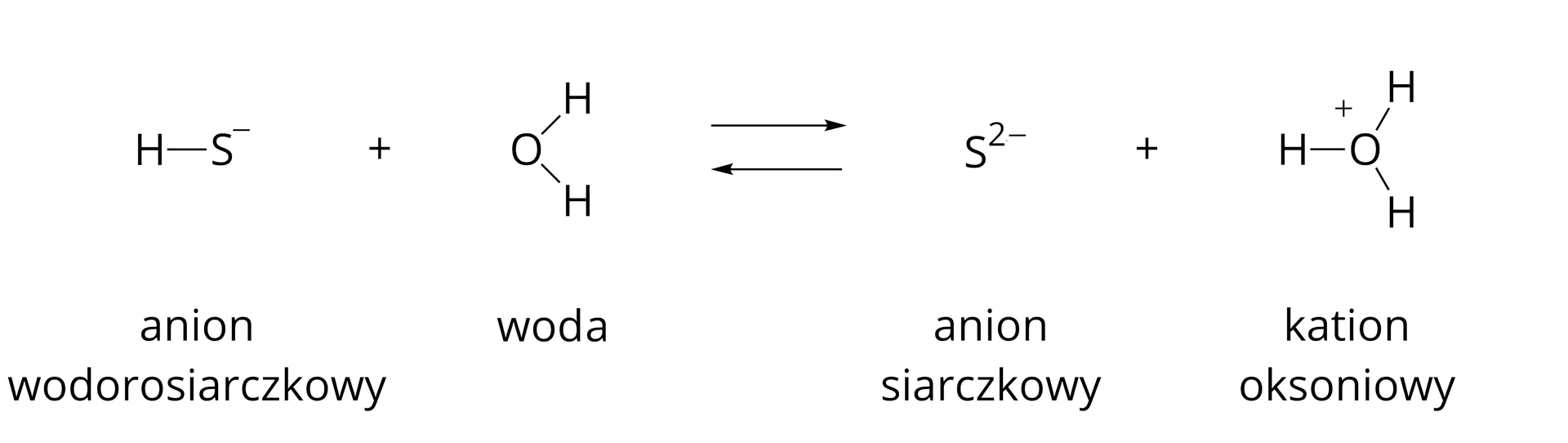
Dysocjacja elektrolityczna słabych elektrolitów jest procesem odwracalnym – cząsteczki rozpadają się na jony, które mogą się ponownie łączyć, tworząc cząsteczki. W roztworze wodnym powstałym poprzez rozpuszczenie w wodzie siarkowodoru występują więc jony , , , a także niezdysocjowane cząsteczki
(i ).
W przypadku takich kwasów, w równaniach reakcji dysocjacji elektrolitycznej stosuje się dwie strzałki skierowane w przeciwne strony.
Możemy również spotkać się z uproszczonym zapisem powyższych równań reakcji, w którym uwzględnia się kationy wodoru.
Pierwszy etap dysocjacji elektrolitycznej:
Drugi etap dysocjacji elektrolitycznej:
Podział kwasów ze względu na moc
Kwasy beztlenowe | |
|---|---|
Mocne | Słabe |
Do porównywania mocy kwasów często stosuje się wielkość nazywaną stałą dysocjacji. Wielkość ta określana jest dla każdego etapu dysocjacji. Im większa jest jej wartość, tym mocniejszy jest kwas, a co za tym idzie w roztworze wodnym więcej jest jonów powstałych z jego dysocjacji. W poniższej tabeli uszeregowano wybrane kwasy tlenowe według malejącej mocy i podzielono je na kwasy mocne i słabe.
Podział kwasów ze względu na moc | |
|---|---|
Wzór sumaryczny kwasu | Stała dysocjacji kwasu () |
Kwasy mocne | |
| |
Kwasy słabe | |
| |
| |
| |
Jak możesz zauważyć, kwasy mocne, to takie których stała dysocjacji jest wyższa niż .
Dysocjacja elektrolityczna wodorotlenków
Przez które z poniższych roztworów (woda destylowana, wodny roztwór wodorotlenku sodu, wodny roztwór wodorotlenku potasu, wodny roztwór wodorotlenku wapnia) przepływa prąd? Sprawdź to, wykonując krótką symulację.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D9Z43XPDZ
Zaznacz prawidłową odpowiedź.
Dysocjacja elektrolityczna wodorotlenków potasu i wapnia
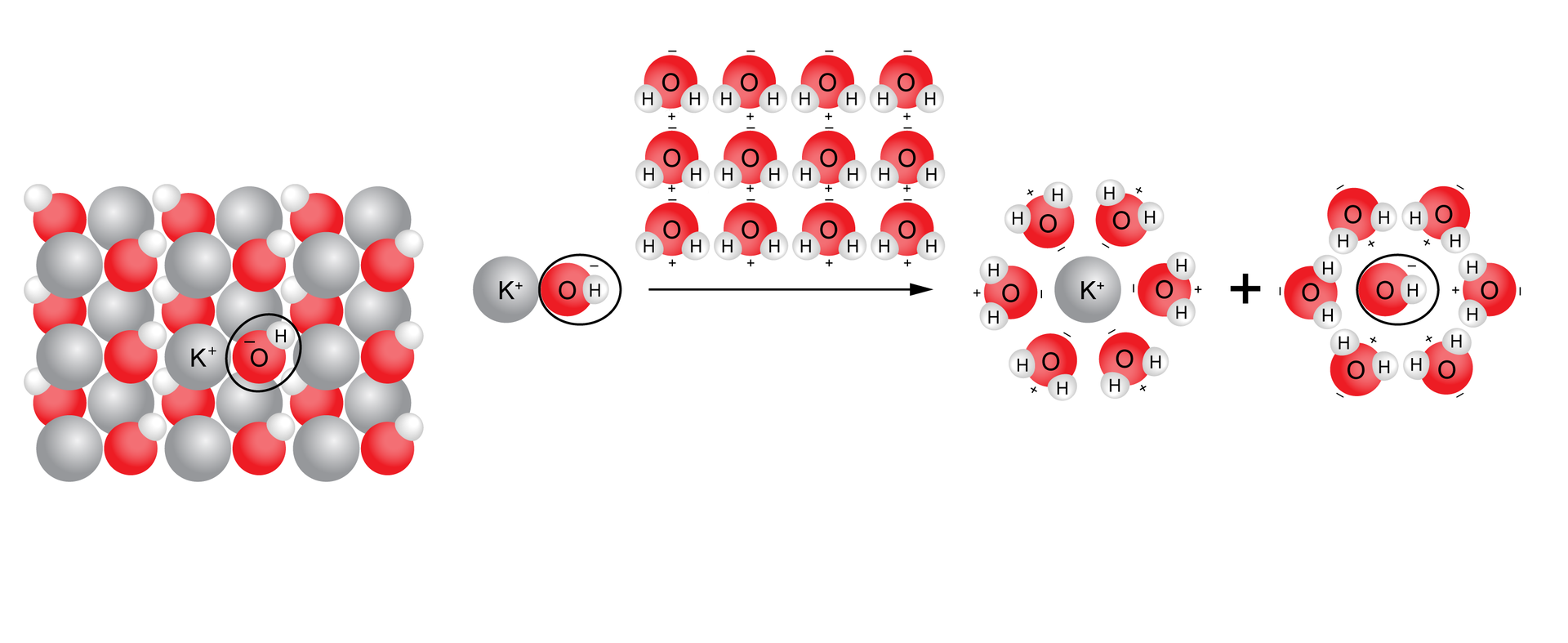

Wodorotlenek potasu dysocjuje, czyli rozpada się pod wpływem wody na jednododatni kation potasu i jednoujemny anion wodorotlenkowy. Zarówno kation potasu, jak i anion wodorotlenkowy są w roztworze wodnym otoczone cząsteczkami wody (solwatacja).


Wodorotlenek wapnia dysocjuje na dwudodatni kation wapnia i dwa jednoujemne aniony wodorotlenkowe.
Liczba powstających w wyniku dysocjacji ładunków dodatnich jest równa liczbie powstających ładunków ujemnych.

Teorię rozpadu substancji na jony opracował Svante Arrhenius (czyt. sfante arenius)Svante Arrhenius (czyt. sfante arenius). Zgodnie z nią, zasadami nazywamy związki chemiczne, które dysocjują na kationy metalu i aniony wodorotlenkowe:
Dysocjacja elektrolityczna soli
Rozpuszczalne w wodzie sole są elektrolitami, ponieważ ich roztwory wodne przewodzą prąd elektryczny. Pod wpływem wody kryształy soli ulegają rozpadowi na jony, z których są zbudowane. Uwalniane są wówczas kationy metali i aniony reszty kwasowej. Proces ten nazywa się dysocjacją elektrolityczną.
Obejrzyj film, w którym przedstawiono proces rozpuszczania i dysocjacji elektrolitycznej chlorku sodu, a następnie rozwiąż ćwiczenie.

Film dostępny pod adresem /preview/resource/RJyjH9THegEm7
Na filmie ukazano jak przebiega proces rozpuszczania i dysocjacji elektrolitycznej chlorku sodu.
Chlorek sodu ulega zatem procesowi dysocjacji elektrolitycznej. W jego wyniku z sieci krystalicznej uwalniane są jony, z których zbudowane są kryształy chlorku sodu.
Chlorek sodu, o wzorze , jest zbudowany z kationów sodu () i anionów chlorkowych (), dlatego proces dysocjacji elektrolitycznej zapisujemy następująco:
W jaki sposób zapisać równanie dysocjacji elektrolitycznej azotanu żelaza o wzorze ?
Azotan żelaza zbudowany jest z kationów żelaza () oraz anionów azotanowych (). W krysztale na jeden kation przypadają trzy aniony . Dlatego równanie procesu dysocjacji elektrolitycznej zapisujemy następująco:
Pamiętaj, że suma ładunków dodatnich musi się równać sumie ładunków ujemnych po lewej i prawej stronie równania. Przeanalizuj poniższą tabelę, w której zamieszczono równania procesów dysocjacji elektrolitycznej niektórych soli, a następnie wykonaj ćwiczenie.
Nazwa soli | Wzór sumaryczny soli | Dysocjacja soli |
azotan potasu | ||
siarczan miedzi | ||
fosforan potasu | ||
azotan ołowiu | ||
siarczan żelaza |
Zapisz równanie procesu dysocjacji elektrolitycznej azotanu glinu o wzorze .