Film samouczek
Polecenie 1
Zapoznaj się z poniższy filmem samouczkiem, a następnie wykonaj ćwiczenia.
Film samouczek pt. Jak zmienia się entropia w reakcjach chemicznych?
Źródło: GroMar Sp. z o.o., Piotr Dzwoniarek, licencja: CC BY-SA 3.0.
Film dostępny pod adresem /preview/resource/RVg6qAQlI7Tqu
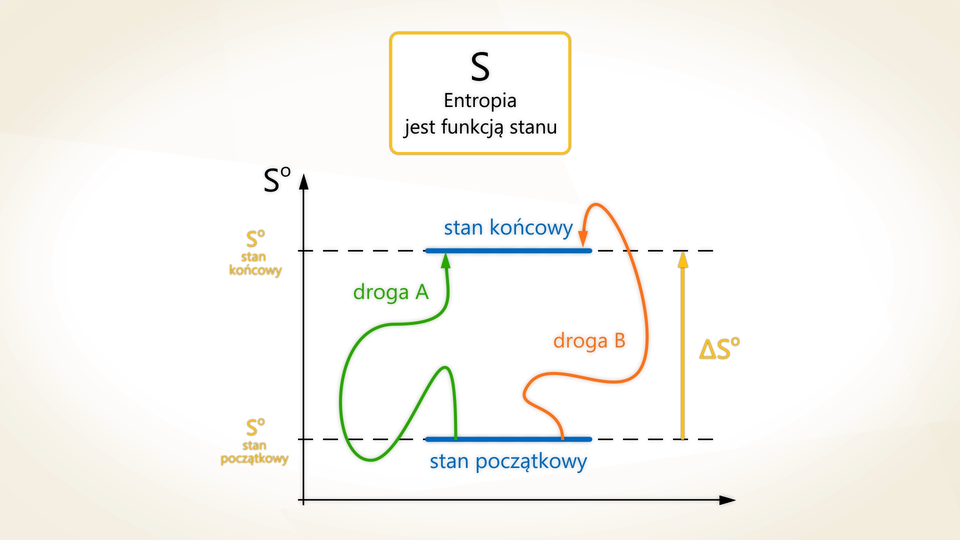
Film samouczek pt. Jak zmienia się entropia w reakcjach chemicznych?
Źródło: GroMar Sp. z o.o., Piotr Dzwoniarek, licencja: CC BY-SA 3.0.
Film nawiązujący do treści materiału dotyczącej zmiany entropii w reakcjach chemicznych.
Ćwiczenie 1
Napisz równanie reakcji chemicznej, powstałej z sumowania poniższych reakcji chemicznych:
Ćwiczenie 2
Korzystając z molowych entropii standardowych, uzupełnij poniższe równanie, aby obliczyć zmianę entropii poniżej zamieszczonej reakcji.