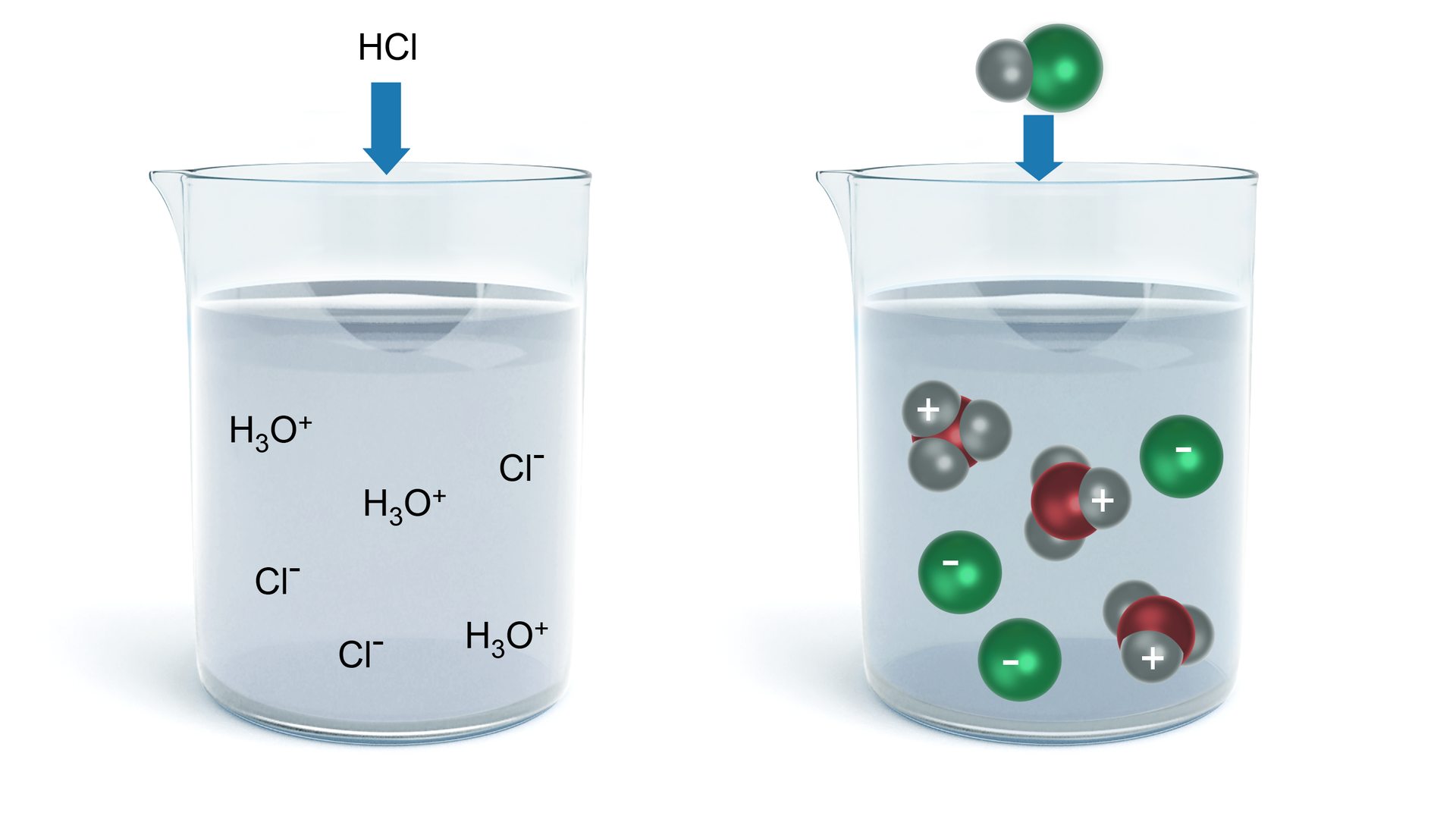
Jak rodzaj wiązania wpływa na właściwości cząsteczki?
Substancje o wiązaniach jonowych
Substancje te można podzielić na kilka grup związków, w zależności od budowy chemicznej. Jak wynika ze schematu poniżej, związki jonowe to nie tylko sole. W przypadku tlenków i wodorotlenków im większy jest udział wiązania jonowego w tych związkach, tym ich charakter jest bardziej zasadowy.

Okazuje się, że na siłę wiązania jonowego wpływa zarówno wielkość ładunku, jak i wielkość jonu. Wraz ze wzrostem wielkości ładunku siła wiązania rośnie. Wiązanie jonowe staje się tym silniejsze, im średnica jonu jest mniejsza. Jako miarę trwałości kryształu przyjęto energię sieci krystalicznej, definiowaną jako energię konieczną do zerwania wiązania jonowego. Niektóre energie sieci podano w tabeli poniżej.
Substancja | Teoretyczna energia sieciowa |
1034 | |
840,1 | |
914,2 | |
770,3 | |
728,4 | |
680,7 |
Warto zatem prześledzić właściwości związków posiadających wiązanie jonowe.
Zdolność do tworzenia kryształów jonowych
Tendencję do tworzenia kryształów jonowych mają związki o charakterze jonowym, do których zaliczyć można zwłaszcza tlenki, halogenki i siarczki pierwszej i drugiej grupy układu okresowego.
Jak wspomniano wcześniej, związki o wiązaniach jonowych są zbudowane z jonów dodatnich i ujemnych, przyciąganych wzajemnie siłami elektrostatycznymi. Jony te układają się w regularne formy krystaliczne, dążąc przy tym do takiego ułożenia, by energia układu była jak najmniejsza. W krysztale jonowym nie istnieje już zatem pojęcie cząsteczki. Pojedyncze cząsteczki jonowe mogą istnieć wyłącznie w fazie gazowej, a więc w bardzo wysokich temperaturach. W krysztale jonowym każdy jon dąży do otoczenia się jak największą liczbą jonów znaku przeciwnego, a więc osiągnięcia jak największej liczby koordynacyjnej.
Ponieważ wiązanie jonowe nie ma charakteru kierunkowego, jony zajmują pozycje zgodnie z zasadą najgęstszego upakowania. O strukturze kryształu zwykle jednak decyduje rozmiar anionu, ponieważ zazwyczaj jest on większy niż kation. Kation zajmuje luki sieci krystalicznej pozostawione przez aniony. W zależności od stosunku promienia kationu do anionu możliwe jest tworzenie przez związki o charakterze jonowym różnego typu sieci przestrzennych.
Wysokie temperatury topnienia i wrzenia
Związki jonowe często topią się, a po stopieniu gotują w znacznie wyższych temperaturach niż inne materiały. Na przykład chlorek sodu topi się w 801°C i wrze w 1413°C. Dla porównania, woda topi się w temperaturze 0°C i wrze w temperaturze 100°C. Z czego to wynika? Aby związki jonowe mogły ulec stopieniu, należy dostarczyć ogromną ilość energii, dzięki której kationy i aniony oddalą się od siebie. Silne oddziaływanie pomiędzy jonami powoduje, że do rozłączenia jonów potrzeba wysokiej energii, a co za tym idzie – dostarczenia dużej ilości ciepła. Kiedy temperatura rośnie, jony krążą wokół ich miejsca w sieci. Dopiero po oddaniu odpowiedniej dawki energii (w temperaturze topnienia) jony opuszczają swoje miejsca sieciowe i siła ich wzajemnego oddziaływania maleje. Z tego względu związki jonowe mają bardzo wysokie temperatury topnienia i wrzenia. Na wartość temperatur topnienia ma wpływ wielkość i ładunek zaangażowanych jonów. Przykładowo: tlenki (zawierające anion ), ze względu na podwójny ładunek anionu tlenu, wykazują szczególnie wysokie temperatury topnienia.
Dla związków (fluorek sodu) oraz (tlenek wapnia) rozmiary jonów są w przybliżeniu takie same: (102 pm) w porównaniu z (100 pm) i (133 pm) kontra (140 pm). Napisz, z czego wynika różnica w temperaturach topnienia tych związków?
Duża wytrzymałość mechaniczna i średnia twardość
Jedną z cech charakterystycznych ciał stałych jest twardość, czyli odporność na odkształcenia powierzchni. Do określenia twardości minerałów służy skala twardości Mohsa. Związki mające wiązanie jonowe są niezwykle twarde, ponieważ trudno poruszyć jony w krysztale. Nawet zastosowanie dużej siły na kryształ niekiedy nie jest wystarczające, aby rozbić związek jonowy. Dzieje się tak ze względu na dużą siłę przyciągania pomiędzy kationami a anionami, utrzymującą kryształ razem. Szczególnie twarde są kryształy jonowe zbudowane z kationów i anionów o tych samych rozmiarach.
Twarde to nie to samo, co kruche
Jeśli do kryształu zostanie przyłożona siła, warstwy jonowe poruszają się nieznacznie, co powoduje, że ładunki stykają się ze sobą i wzajemnie odpychają. Wtedy kryształ pęka. Mówi się o kruchości kryształu, ponieważ pęka pod wpływem naprężeń. Należy przy tym pamiętać, że twarde kryształy również mogą być kruche.
Co zrobić, jeśli związek jonowy jest naprawdę twardy?
W takim wypadku należy zastosować odpowiedni rodzaj siły. Okazuje się, że istnieją obszary, których naruszenie nawet małą siłą pozwoli rozłamać kryształ. Po uderzeniu w takie miejsce kryształ pęka wzdłuż płaszczyzn łupliwości.
Przewodnictwo elektryczne
W stanie stałym związki jonowe są dobrymi izolatorami (nie przewodzą prądu) ze względu na silne upakowanie jonów dodatnich i ujemnych. Po rozpuszczeniu w wodzie związki jonowe ulegają dysocjacji. Powstające jony dodatnie i ujemne łatwo mogą się przemieszczać i mają zdolność do przewodzenia ładunku elektrycznego przez roztwór. Dlatego właśnie w roztworze wodnym związki jonowe są bardzo dobrymi przewodnikami elektryczności. Podobnie sytuacja wygląda dla substancji w formie stopionej, gdzie jony mogą swobodnie przemieszczać się przez stopioną ciecz jonową. Elektrolizie ulegają stopione sole i wodorotlenki, a sama metoda została wykorzystana do otrzymywania aktywnych metali.
Rozpuszczalność
Większość związków o charakterze jonowym jest dobrze rozpuszczalna w wodzie i rozpuszczalnikach polarnych. Istnieje jednak pewna zależność, która reguluje rozpuszczalność. Związki jonowe rozpuszczają się w wodzie, jeśli energia, wydzielana podczas oddziaływania jonów z cząsteczkami wody, kompensuje energię potrzebną do rozbicia wiązań jonowych w ciele stałym i energię potrzebną do oddzielenia cząsteczek wody, aby jony mogły zostać wprowadzone do roztworu.
Dyskusje o równowagach rozpuszczalności opierają się na następującym założeniu: gdy ciała stałe rozpuszczają się w wodzie, dysocjują dając jony, z których są utworzone, np.

Kwasy również rozpuszczają się w wodzie i ulegają dysocjacji. Pamiętajmy jednak, że w cząsteczkach kwasów występują wiązania kowalencyjne.
Dla soli oraz niektórych wodorotlenków dane uzyskane z pomiaru rozpuszczalności są różne. Wzorce te stanowią podstawę zasad przedstawionych w tabeli rozpuszczalności, która może wskazywać, czy dana sól rozpuszcza się w wodzie. Zasady te opierają się na następujących definicjach terminów: rozpuszczalny, nierozpuszczalny i słabo rozpuszczalny.

Zapoznaj się z nagraniem na temat właściwości substancji o wiązaniach jonowych. Następnie wykonaj polecenia i odpowiedz na pytania.
Jakie właściwości mają substancje o wiązaniach jonowych?
Związki o wiązaniach jonowych to między innymi sole oraz niektóre wodorotlenki, tlenki, azotki, wodorki, a także węgliki. Możemy je znaleźć nie tylko w laboratorium chemicznym. Na przykład chlorek sodu, czyli sól kuchenną, spotykamy na co dzień w naszej kuchni. Fluorek sodu jest dodawany do pasty do zębów, aby wzmocnić szkliwo. Z kolei węglik wapnia znalazł zastosowanie jako podgrzewacz żywności w wojskowej kuchni.
Chociaż zastosowania wymienionych związków w życiu codziennym są odmienne, to substancje te mają wiele wspólnych cech.
Na podstawie uporządkowanego rozmieszczenia cząstek, ciała stałe można podzielić na krystaliczne i bezpostaciowe. Ciała stałe o regularnym rozmieszczeniu cząstek składowych nazywane są krystalicznymi ciałami stałymi. Składają się one z jednostek (tak zwanych komórek elementarnych), które powtarzają się we wszystkich trzech kierunkach i tworzą sieć krystaliczną. Okazuje się, że związki o wiązaniu jonowym z łatwością tworzą kryształy jonowe.
W strukturze sieci krystalicznej kryształów jonowych istnieją silne oddziaływania elektrostatyczne między ułożonymi naprzemiennie jonami dodatnimi i ujemnymi. Powoduje to, że do zerwania wiązań jonowych i naruszenia sieci krystalicznej potrzeba dużo energii, a co za tym idzie, wysokiej temperatury. Z tego względu kryształy jonowe mają wysoką temperaturę topnienia i wrzenia, a ponadto zwykle występują w postaci stałej, a nie w stanie ciekłym lub gazowym.
Kryształy jonowe są niezwykle twarde. Dzieje się tak, ponieważ pomiędzy kationami a anionami jest duża siła przyciągania. Szczególnie twarde są kryształy jonowe zbudowane z kationów i anionów o tych samych rozmiarach. Jako miarę trwałości kryształu przyjęto energię sieci krystalicznej, definiowaną jako energię konieczną do zerwania wiązania jonowego
Na wartość energii sieci krystalicznej wpływa wartość ładunku jonu oraz rozmiar promienia jonowego. Wiązanie jest silniejsze, a co za tym idzie energia sieci krystalicznej jest większa, gdy ładunek jonów wzrasta. Zatem siła wiązania między kationem +1 a anionem -1 nie jest tak silna, jak siła między kationem o wartości +3 a anionem o wartości -2. Jeśli rozważymy rozmiar promienia jonowego to siła wiązania między kationami a anionami tworzącymi sieć krystaliczną jest największa, gdy średnica jonów jest mała. Dla przykładu większą energię sieci krystalicznej posiada NaCl niż NaBr. W obu przypadkach promienie kationów są takie same, jednak promień anionu chlorkowego jest mniejszy niż anionu bromkowego. A zatem kation sodu będzie silniej przyciągał mniejszy anion, a więc anion chlorkowy
Wyobraź sobie budowę kryształu jonowego. Spróbuj odtworzyć jego model. W jaki sposób można zerwać wiązania jonowe w takim krysztale?
Po przyłożeniu siły mechanicznej na kryształ jonowy zostaje zaburzony regularny, powtarzający się wzór przeciwnie naładowanych jonów, przez co jony z podobnymi ładunkami zbliżają się do siebie. Wynikające z tego odpychanie powoduje rozpad sieci krystalicznej. To sprawia, że związki jonowe są uznawane za stosunkowo kruche.
Czy wiesz, co się dzieje, gdy związek jonowy rozpuszcza się w wodzie?
Po zanurzeniu związku jonowego w wodzie jony są przyciągane do cząsteczek wody, z których każda posiada ładunek polarny. Jeśli przyciąganie między jonami a cząsteczkami wody jest wystarczająco duże, aby rozerwać wiązania utrzymujące jony razem, związek rozpuszcza się. Większość związków jonowych jest rozpuszczalna w wodzie i rozpuszczalnikach polarnych, gdzie ulega dysocjacji, czyli rozpada się na jony. Związki jonowe są nierozpuszczalne w niepolarnych rozpuszczalnikach, takich jak na przykład benzen.
Reakcje związków jonowych są bardzo szybkie w porównaniu z reakcjami związków kowalencyjnych. Wynika to z faktu, że związki kowalencyjne posiadają wiązania, których rozerwanie wymaga dostarczenia sporej ilości energii. Związki te mogą tworzyć kryształy kowalencyjne, gdzie atomy połączone czystym wiązaniem kowalencyjnym tworzą jedną gigantyczną molekułę, albo kryształy molekularne, których elementem sieci przestrzennej są odrębne cząsteczki.
Jeśli rozpuścimy w wodzie kryształ jonowy, na przykład chlorek sodu, to bardzo szybko rozpadnie się on na kation sodu i anion chlorkowy. Powstałe jony ulegną rozproszeniu w roztworze, a każdy jon będzie solwatowany, czyli otoczony przez cząsteczkę wody, co uniemożliwi ponowne połączenie jonów. Po przyłączeniu wszystkich cząsteczek wody do jonów, w uzyskanym roztworze nie da się rozpuścić więcej substancji i staje się on nasycony. Powstały roztwór, w którym poruszają się zdysocjowane jony, nazywa się elektrolitem. Oznacza to, że może on przewodzić elektryczność. Dzieje się tak dzięki obecności w roztworze ruchliwych jonów mających zdolność przewodzenia ładunku elektrycznego.
Czy już wiesz, dlaczego piasek nie rozpuszcza się w wodzie?
Dobrą przewodność elektryczną wykazują również stopione związki jonowe. Na skutek działania wysokiej temperatury związek jonowy rozpada się na jony, które swobodnie poruszają się w cieczy jonowej i mają zdolność przewodzenia ładunku elektrycznego. Bez wątpienia związki jonowe w stanie stałym nie wykazują tych właściwości, ponieważ jony nie mogą się swobodnie poruszać. Dlatego związki jonowe w stanie stałym nie mogą przewodzić elektryczności.
Substancje o budowie kowalencyjnej
Przewodnictwo elektryczne
Aby substancja przewodziła prąd elektryczny, niezbędne są swobodne nośniki prądu (jony, elektrony). Na ogół substancje kowalencyjne nie przewodzą prądu elektrycznego w stanie stałym ani po rozpuszczeniu w wodzie. Wyjątkiem jest grafit, który w stanie stałym jest dobrym przewodnikiem elektronowym. ZdelokalizowaneZdelokalizowane wiązania pomiędzy atomami węgla umożliwiają swobodny ruch elektronów i przewodzenie prądu.
Temperatury topnienia i wrzenia
Temperatura topnienia i wrzenia związków kowalencyjnych jest ogólnie niższa niż w przypadku związków jonowych. Cząsteczki gazów szlachetnych (tworzące kryształy molekularne) mają dość niskie temperatury wrzenia i topnienia, co jest spowodowane tym, że oddziaływania międzycząsteczkowe są słabe (tabela poniżej).
Tabela 1. Temperatury topnienia i wrzenia helowców na podstawie pl.wikipedia.org.
Helowiec | Temperatura topnienia | Temperatura wrzenia |
|---|---|---|
Hel, | ||
Neon, | ||
Argon, | ||
Krypton, | ||
Ksenon, | ||
Radon, |
*Pod ciśnieniem normalnym;
**Hel pod normalnym ciśnieniem nie przechodzi w stan stały, nawet w najniższej osiągalnej temperaturze.
Z kolei kryształy kowalencyjne cechują się wysokimi temperaturami topnienia, co wynika z dużej energii wiązań kowalencyjnych.
Twardość
Kryształy kowalencyjne są twarde (jak diament), ponieważ ich atomy są silnie związane w sieci krystalicznej, w przeciwieństwie do kryształów molekularnych, których cząsteczki są w stanie do pewnego stopnia poruszać się i czasami mogą to robić także względem siebie. Warstwowa budowa grafitu decyduje o jego łupliwości, dlatego jest tak miękki.

Cząsteczka polarnaCząsteczka polarna a cząsteczka niepolarna
W substancjach kowalencyjnych występują wiązania kowalencyjne niespolaryzowanewiązania kowalencyjne niespolaryzowane (atomowe) albo kowalencyjne spolaryzowanekowalencyjne spolaryzowane.
Wśród chemików rozpowszechniony jest pogląd, że „podobne rozpuszcza się w podobnym”. Przeanalizujmy zatem rozpuszczalność obu grup substancji i sprawdźmy, czy ta myśl jest słuszna.
1. Związki, które zawierają wiązania kowalencyjne niespolaryzowane, nie rozpuszczają się w rozpuszczalnikach polarnych, jak np. wodzie. Jej cząsteczki posiadają niewielki ładunek ujemny na atomie tlenu i niewielki ładunek dodatni na atomie wodoru, co oznacza, że są to cząsteczki polarne. Jednak wiemy przy tym również, że związki kowalencyjne z wiązaniem niepolarnym składają się z obojętnych cząsteczek lub cząsteczek o niewielkich ładunkach. Z tego powodu związki te nie są silnie przyciągane do cząsteczek wody.
Substancje kowalencyjne z wiązaniem kowalencyjnym niespolaryzowanym rozpuszczają się w rozpuszczalnikach niepolarnych (np. benzyna, olej), zgodnie z zasadą „podobne rozpuszcza podobne”.
2. Substancje o wiązaniach silnie spolaryzowanych rozpuszczają się w wodzie i dysocjują na jony, co jest konsekwencją oddziaływań międzycząsteczkowych. Przykładem są wodorki fluorowców i mocne kwasy tlenowe.
Czy wiesz, jakie właściwości mają substancje o wiązaniach kowalencyjnych? Czy różnią się właściwościami między sobą? Zapoznaj się z poniższym nagraniem, a następnie wykonaj zadania.
Jakie właściwości mają substancje o wiązaniach kowalencyjnych?
Wszędzie dookoła nas mamy do czynienia ze związkami chemicznymi – powietrze, którym oddychamy, woda, którą pijemy, ziemia, po której chodzimy. Wszystkie przedmioty zbudowane są z różnych pierwiastków chemicznych lub ich związków. W powietrzu możemy znaleźć azot, którego zawartość wynosi około 78% objętościowych, tlen, zawartość w przybliżeniu to 21% oraz inne gazy, jak chociażby gaz szlachetny argon, stanowiące razem około 1%. Woda to z kolei nic innego jak tlenek wodoru, obecna również w postaci pary wodnej w powietrzu, zaś w skład litosfery wchodzi między innymi tlenek krzemu(IV).
W jaki sposób zbudowane są te związki? W przypadku azotu i tlenu mamy do czynienia z dwuatomowymi cząsteczkami, a ich atomy połączone są wiązaniem kowalencyjnym niespolaryzowanym. Jest to wiązanie chemiczne tworzone między atomami pierwiastków, dla których różnica elektroujemności wynosi poniżej 0,4. Argon nie tworzy cząsteczek - występuje w postaci pojedynczych atomów. W przypadku gazów szlachetnych, często mówi się o ich jednoatomowych cząsteczkach. Z drugiej strony, jeżeli chodzi o wodę i tlenek krzemu(IV), to w ich cząsteczkach występuje już inny rodzaj wiązania kowalencyjnego – kowalencyjne spolaryzowane. Tworzy się ono między atomami charakteryzującymi się dużą różnicą elektroujemności – większą niż 0,4, ale mniejszą niż 1,7. Tylko pamiętaj przy tym, że te wartości mają charakter umowny.
Związki o wiązaniach kowalencyjnych różnią się między sobą właściwościami chemicznymi i fizycznymi. Wynika to przede wszystkim z różnicy polarności ich cząsteczek, co przekłada się na ich inną rozpuszczalność. Związki o wiązaniach atomowych niespolaryzowanych niechętnie rozpuszczają się w rozpuszczalnikach polarnych, takich jak na przykład woda, a mimo to często wchodzą z nią w reakcje chemiczne. Z kolei związki o wiązaniach kowalencyjnych spolaryzowanych rozpuszczają się chętnie w rozpuszczalnikach polarnych i nie rozpuszczają się w rozpuszczalnikach niepolarnych, jak na przykład tetrachlorometan, dichlorometan lub heksan.
Porównując ze sobą związki kowalencyjne należące do jednej grupy, np. fluorowców, zauważymy, że posiadają one odmienne temperatury topnienia i wrzenia, ponieważ rosną wraz ze wzrostem liczby atomowej. Ma to również związek z promieniami atomów fluorowców tworzących te cząsteczki. Promień atomowy rośnie wraz ze wzrostem liczby atomowej w danej grupie, a im większy promień, tym silniejsze są siły Van der Waalsa pomiędzy cząsteczkami fluorowca. Właśnie dlatego temperatury topnienia i wrzenia rosną wraz ze wzrostem siły tych oddziaływań.
W przypadku związków, których cząsteczki zbudowane są z atomów różnych pierwiastków, często w ich cząsteczkach występują wiązania kowalencyjne spolaryzowane. Na tej podstawie można zauważyć, że polarność tych cząsteczek ma wpływ także na temperatury topnienia i wrzenia. Związki organiczne mogą posiadać grupy funkcyjne kilku rodzajów, jak na przykład hydroksylowa, aminowa, karboksylowa czy nitrowa, co ich zwiększa polarność.
Wyobraźmy sobie trzy cząsteczki, etan, etanol oraz etano-1,2-diol. Etan nie posiada grup funkcyjnych, ale ma najniższą temperaturę wrzenia. Etanol posiada jedną grupę hydroksylową oraz znacznie wyższą temperaturę wrzenia od etanu, a z kolei etano-1,2-diol posiada dwie grupy hydroksylowe i ma najwyższą temperaturę wrzenia. Jest to spowodowane obecnością oddziaływań dipol-dipol pomiędzy cząsteczkami etanolu lub etano-1,2-diolu, których oddziaływań brakuje w przypadku niepolarnej cząsteczki etanu. Dodatkowo w tym przypadku grupa hydroksylowa, poza zwiększeniem polarności łańcucha węglowego, umożliwia wytworzenie wiązania wodorowego – słabego wiązania, które tworzy się między atomem wodoru danej cząsteczki a silnie elektroujemnym atomem tlenu innej cząsteczki tego związku.
Jak można zauważyć, związki kowalencyjne są niejednakowe. Poza wymienionymi różnicami istnieje jeszcze wiele innych, jak choćby ich barwa, ale nie mają one już tak istotnego znaczenia jak rozpuszczalność czy różnice w temperaturach topnienia i wrzenia. Warto zapamiętać, jak kluczowa jest elektroujemność atomów budujących daną cząsteczkę, polarność, czy występowanie lub brak oddziaływań międzycząsteczkowych na zmianę tych właściwości.
Wiązanie ukryte w monecie
Na poniższych ilustracjach przedstawiono monety, wykonane z różnych metali, m.in. z miedzi. Wiek monet wskazuje na to, że materiał, z którego zostały zrobione, cechuje się wyjątkową trwałością. Z czego to wynika?
Co by się stało, gdybyśmy zdecydowali, że chlorek miedzi() jest równie dobrym materiałem do wykonania monet? Czy łatwo byłoby ukształtować monetę z ? Spróbuj odpowiedzieć na to pytanie.
Unikalne właściwości metali oraz ich stopów
Metale oraz ich stopy mają wszechstronne zastosowania. Wynikają one z właściwości substancji, które są powiązane z budową chemiczną i faktem, że w metalach występuje wiązanie metaliczne. Poniższa oś przedstawia właściwości typowe dla różnych metali.
Wiązania metaliczne pozwalają wyjaśnić, dlaczego metale mogą na przykład przewodzić prąd lub zginać się bez zerwania. Należy pamiętać, że właściwości substancji o wiązaniu metalicznym bywają odmienne. Sód jest metalem miękkim, a żelazo twardym. Jedyne, co łączy oba metale, to fakt istnienia wiązania metalicznego.
Warto również nie zapomnieć, że poznanie charakterystycznych cech metali wymaga wykonania wielu doświadczeń i niekiedy długotrwałych obserwacji. Dlatego należy być ostrożnym przy dokonywaniu identyfikacji metali i ich stopów.
Zapoznaj się z treścią audiobooka i rozwiąż ćwiczenia.
Jest rok 1812. Napoleon ze swoją sześćset tysięczną armią francuską wyrusza na wojnę z Rosją. Mijają miesiące ciężkiej walki. Armia Napoleona rozpierzchła się po ogromnym obszarze. Nacierają co sił w stronę Moskwy, ale z dnia na dzień liczba rannych rośnie. Wzmaga się strach i panika wśród żołnierzy. Czy uda się pokonać wroga? Takie pytania padają bezustannie. Czy wygra armia lepiej zaopatrzona i wymusztrowana?
16 października 1813 r.
VII korpus Napoleona stacjonuje pod Lipskiem. Walki nie ustają. Pod wodzą Napoleona stoi około 160 tysięcy osób. Wieczorem wojska rozbijają pod gołym niebem swoje namioty, by choć na chwilę uciszyć skołatane myśli.
- Nie wytrzymamy tu w tym mrozie – powiedział jeden z żołnierzy, rozcierając dłonie nad rozpalonym ogniskiem. Miał całe porozdzierane spodnie, z których wystawały jedynie fragmenty lnianych nici. Jego szynel nie miał guzików, a na mankiecie widoczny był jedynie szary proszek.
- Czy to cyna? – zapytał jego kompan.
- Tak – odpowiedział. – Zgubiłem już wszystkie cynowe guziki – dodał.
Popatrzył na mundur swojego towarzysza i zauważył, że mankiety jego płaszcza również były wybrakowane.
W układzie okresowym, który zawiera ponad sto różnych pierwiastków, nie odnajdziemy drugiego takiego metalu jak cyna, który może występować w kilku postaciach.
Trudno uwierzyć, że ta miękka, plastyczna i krucha zarazem bryłka metalu, z której wykonano guziki w mundurach żołnierzy oraz szary proszek na ich mankietach mają ten sam wzór chemiczny, Sn. Jak to możliwe? Doświadczalnie udowodnił to Dymitr Mendelejew, a w wyjaśnieniu tego zjawiska pomogło pojęcie alotropii. Czy wiesz czym jest alotropia?
Każda z odmian alotropowych cyny różni się między sobą właściwościami chemicznymi i fizycznymi, co jest spowodowane zazwyczaj odmienną postacią krystaliczną, zależną od temperatury i ciśnienia. Odmiany alotropowe cyny oznacza się literami greckimi β (beta), γ (gamma), α (alfa).
W jaki sposób zapobiegać przechodzeniu jednej odmiany w drugą?
Okazuje się, że już niewielki dodatek takich metali jak As, Ge , In, Pb, Sb i Bi zapobiega przechodzeniu metalicznej cyny w proszek.
Z kolei domieszki metali metali jak Al, Co, Mg, Mn, Zn przyspieszają ten proces.
Co istotne, proces przechodzenia odmiany metalicznej w sproszkowaną odbywa się na zasadzie kontaktu z przedmiotem, który takiej przemianie podlega.
Czy podczas trwającej bitwy wszystkie przedmioty metaliczne posiadały tę samą właściwość jak cyna i zamieniały się w proszek?
Nagle żołnierze usłyszeli czyjeś kroki. Ten charakterystyczny dźwięk mogły wydawać tylko buty na skórzanej podeszwie, podkute metalowymi ćwiekami. Zbliżał się dowódca.
Żołnierze zerwali się na równe nogi, poprawili swoje mundury i czapki. Stanęli na rozkaz.
- Spocznij! – powiedział dowódca. – Jak wygląda u was sytuacja?
- Brakuje żywności – odpowiedział dość nieśmiało młody żołnierz. Nie przenosząc wzroku z ramion dowódcy dodał po chwili – Musimy zawracać z frontu. – i zaprowadził go do polowej kuchni pod namiotem.
- Proszę spojrzeć – wskazał na puste żelazne kociołki i kubki – kuchnia świeci pustkami. Zostały nam tylko sztućce i menażki. Są piękne i błyszczące, ale nimi nie nakarmimy całej armii.
Napoleon zmarszczył brwi, posmutniał, po czym odwrócił wzrok w stronę frontu. W wyobraźni analizował przebieg bitwy ciągle mając nadzieję, że zła passa w końcu minie. W głowie kalkulował czas, próbując przewidzieć ruchy obu wojsk.
Nagle rozległ się huk. Armata wystrzeliła pocisk w stronę wroga. Ten jednak odpowiedział całą serią strzałów. Francuzi byli coraz słabsi. Ich spiż armatni był nieustannie napełniany prochem. Działa były co chwilę gotowe do nabicia. Spiż czyli stop miedzi z cyną i ołowiem z uwagi na swoją twardość i odporność na ścieranie był stosowany w tamtych czasach nie tylko do produkcji armat.
Jaką bronią posługiwała się armia Napoleona ?
Prawie sto kul żeliwnych małego kalibru umieszczonych w blaszanej puszcze, wystrzeliwano nieustannie w stronę wroga. Mimo to nie dawały rady zdławić oporu. W tle ciągle rozlegał się krzyk żołnierzy armii francuskiej i koalicji antyfrancuskiej. Wielka Armia Napoleona liczy już jedynie sto tysięcy żołnierzy. Każda godzina ciągnie do okopów kolejnych rannych.
- Czy to już koniec? – słychać ze wszystkich stron to jedno, zmęczone pytanie.
- Nie! – stanowczo odpowiada Napoleon – rozpoczynamy Wielką Bitwę – dodaje, przekonany o jej strategicznym znaczeniu.
19 października 1813 r.
Był środek nocy. Siarczyste mrozy dawały się we znaki. Napoleon obserwował sytuację na froncie i analizował kolejną przeprawę. Jednak armia malała w oczach i chociaż obie strony poniosły ciężkie straty, to przewaga wciąż leżała po stronie przeciwnika.
- VIII korpus! Gdzie wasz dowódca? – zapytał zmartwiony Bonaparte.
- Nie żyje. – odpowiedział jeden z żołnierzy. Ciało Marszałka Poniatowskiego znaleziono nad rzeką. Została tylko szabla z mosiężną wypolerowaną rękojeścią i ordery. Mnożą się następni ranni.
- Odwrót! – krzyknął Napoleon –Wracamy.
W. Knap, Lipsk. Bitwa Narodów , "Dziennik Polski" 2013.
M. Dworniczak, Napoleona pod Moskwą pokonała zaraza cynowa? , "Gazeta Wyborcza" 2014.
Bóg wojny – bitwy epoki napoleońskiej , "Mówią wieki. Historia w sieci" [dostęp online: 23.10.2019].
S. Sękowski, Chemiczny kameleon , "Chemia praktyczna" 2006.
Na rysunku poniżej przedstawiono dwie odmiany alotropowe cyny.
Zapoznaj się z opisem zdjęcia, na którym przedstawiono dwie odmiany alotropowe cyny.

Odpowiedz na poniższe pytania.