Jakie wiązania występują pomiędzy metalami?
Dlaczego uderzając młotkiem w kawałek szkła, rozbijasz je na tysiąc kawałków, a uderzając w kawałek metalu, możesz go po prostu spłaszczyć i uformować?Dlaczego metalowa łyżeczka włożona do gorącej herbaty niemal natychmiast parzy w palce, podczas gdy plastikowa pozostaje chłodna? Dlaczego kabel do ładowarki jest z miedzi, a nie z plastiku? Co sprawia, że metale tak pięknie błyszczą, a inne materiały są bardzo często matowe?
Odpowiedź na te pytania kryje się w unikalnym sposobie, w jaki atomy metali „trzymają się razem” – w wiązaniu metalicznym.
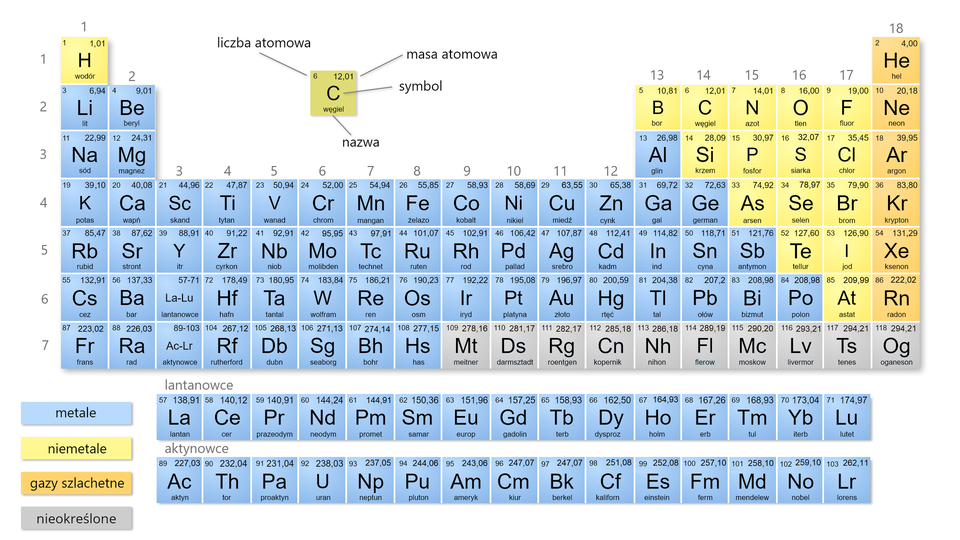
Przeanalizuj poniższy układ okresowy pierwiastków i zakreśl kolorem czerwonym pola, które zajmują metale.
Łącznie w układzie okresowym występuje 86 pierwiastków metalicznych, w których wiązaniem chemicznym odpowiadającym za szereg właściwości tych metali jest wiązanie metaliczne. Oznacza to, że zarówno w czystej próbce miedzi, jak i próbce glinu jedynym wiązaniem jest wiązanie metaliczne. Warto nadmienić, że pojęcie wiązania metalicznego stosowane jest dla scharakteryzowania wiązania chemicznego, obecnego w stopach metali (np. brązie, mosiądzu). Poniżej przedstawiono przykłady obecności sieci metalicznej w różnych przedmiotach.
Zapoznaj się z animacją, w której opisany został elektronowy model wiązania metalicznego. Następnie przystąp do rozwiązania ćwiczeń zamieszczonych poniżej.

Film dostępny pod adresem /preview/resource/RPKrKuAjfsdtO
Film nawiązujący do treści materiału - opisuje wiązanie metaliczne.
Wyjaśnij, czym jest gaz elektronowy.