Jak zmierzyć pH?
Dodając cytrynę do esencji herbacianej, sprawisz, że zblednie lub zmieni swoją barwę na żółtą. Z kolei inny będzie mieć kolor, jeśli dodasz ją do soku z buraka lub naparu z hibiskusa. Jeszcze inny, jeśli użyjesz sody oczyszczonej. W chemii odczyn roztworu określa się za pomocą wskaźników kwasowo‑zasadowych, zwanych także indykatoramiindykatorami. Są to substancje, które pod wpływem przemian odczynu środowiska zmieniają swoją barwę. Ale czy potrafisz powiedzieć, dlaczego tak się dzieje?
Czym są wskaźniki pH?
Do określenia pH najczęściej używane są indykatoryindykatory (wskaźniki) pH. Głównie to słabe kwasy lub słabe zasady organiczne, które w wyniku zmiany stężeń jonów i zmieniają swoją formę, co w konsekwencji skutkuje zmianą zabarwienia roztworu. Przykładowo, w przypadku wskaźnika pH, będącego słabym kwasem organicznym, może ustalać się następująca równowaga:
Gdzie:
– wskaźnik w postaci kwasu;
– sprzężona z nim zasada.
Forma nadaje inną barwę roztworowi niż forma . Stąd, w wyniku zajścia przedstawionej reakcji, zmienia się barwa roztworu.
Jak działają wskaźniki?
Czy wiesz, jak działają wskaźniki kwasowo‑zasadowe? Aby poznać odpowiedź na to pytanie, zapoznaj się z poniższym filmem edukacyjnym.
W filmie zastosowano skrót Ind. – ang. Indicator "wskaźnik"

Film dostępny pod adresem /preview/resource/R1HOX64ZGPPNM
W filmie zastosowano skrót Ind. – ang. Indicator "wskaźnik"
Film nawiązujący do działania wskaźników kwasowo‑zasadowych.
Jakie są najpopularniejsze wskaźniki?
Wskaźnik uniwersalny jest to mieszanina różnych wskaźników, która zmienia barwę w skali pH od do . Nasączone wskaźnikiem uniwersalnym papierki nazywane są uniwersalnymi papierkami wskaźnikowymi.

Fenoloftaleina jest jednym z najczęściej stosowanych wskaźników pH. Powszechnie wiadomo, że w środowisku zasadowym zmienia barwę z bezbarwnej na malinową (różowo‑czerwoną). Jednak fenoloftaleina posiada bogatszą paletę barw.

Przyjmuje intensywne zabarwienie koloru malinowego w roztworach zasadowych w pH od do . Powyżej tego pH jej malinowe zabarwienie stopniowo zanika. W środowisku kwasowym lub obojętnym jest bezbarwna. W przypadku bardzo niskiego pH (poniżej ) przyjmuje pomarańczowe zabarwienie.
Oranż metylowy jest to wskaźnik dla roztworów o odczynie mocno kwasowym.

Naturalne wskaźniki pH
Wskaźnikami pochodzenia naturalnego są np.: sok z czerwonej kapusty, wywar z buraka, borówki, napar z czarnej herbaty czy kwiat kalafioru fioletowego. Nie są one jednak powszechnie używane, ze względu na swoją krótką trwałość.
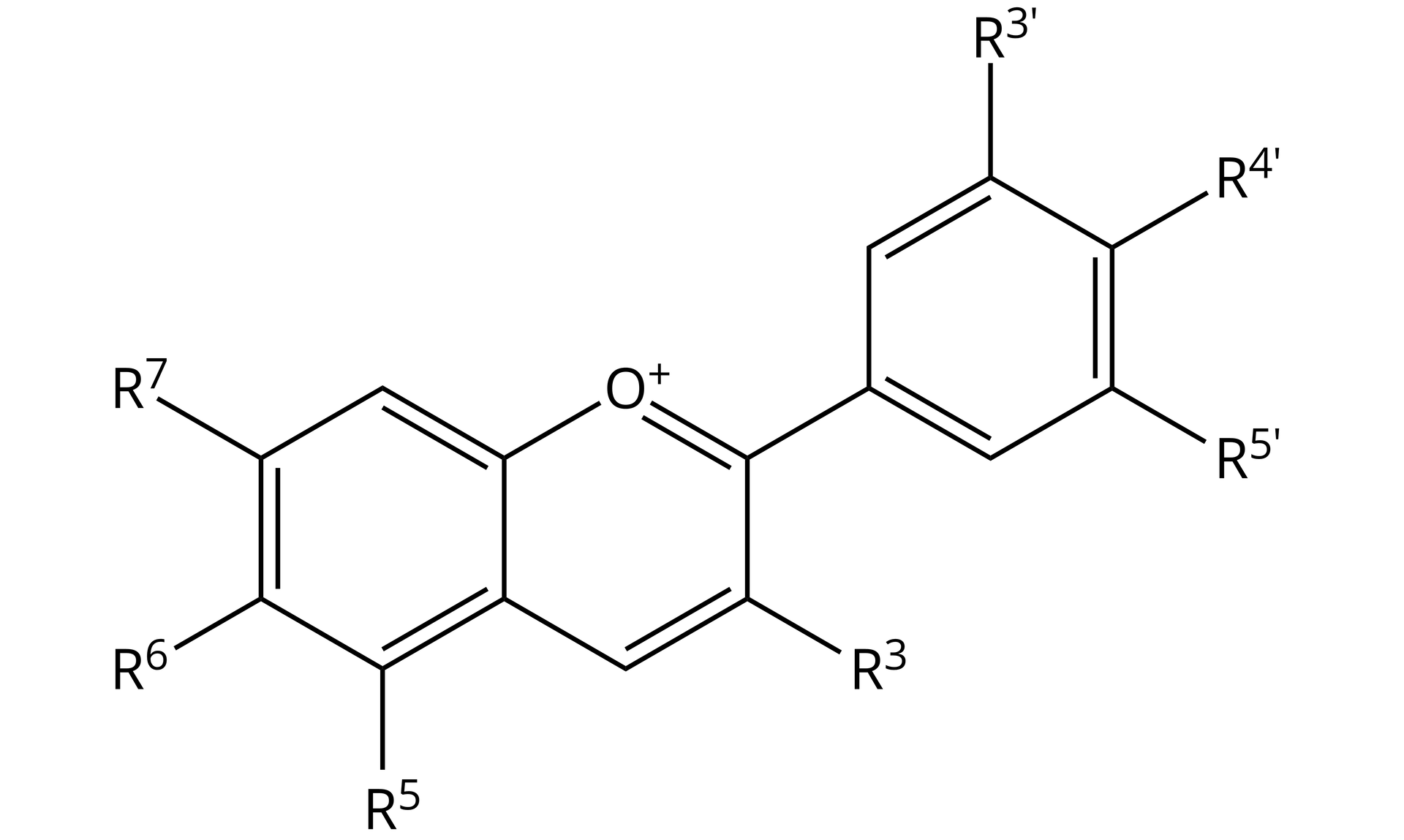
Za zmianę barwy wywaru z czerwonej kapusty odpowiadają antocyjany. Są to związki organiczne o złożonej budowie.
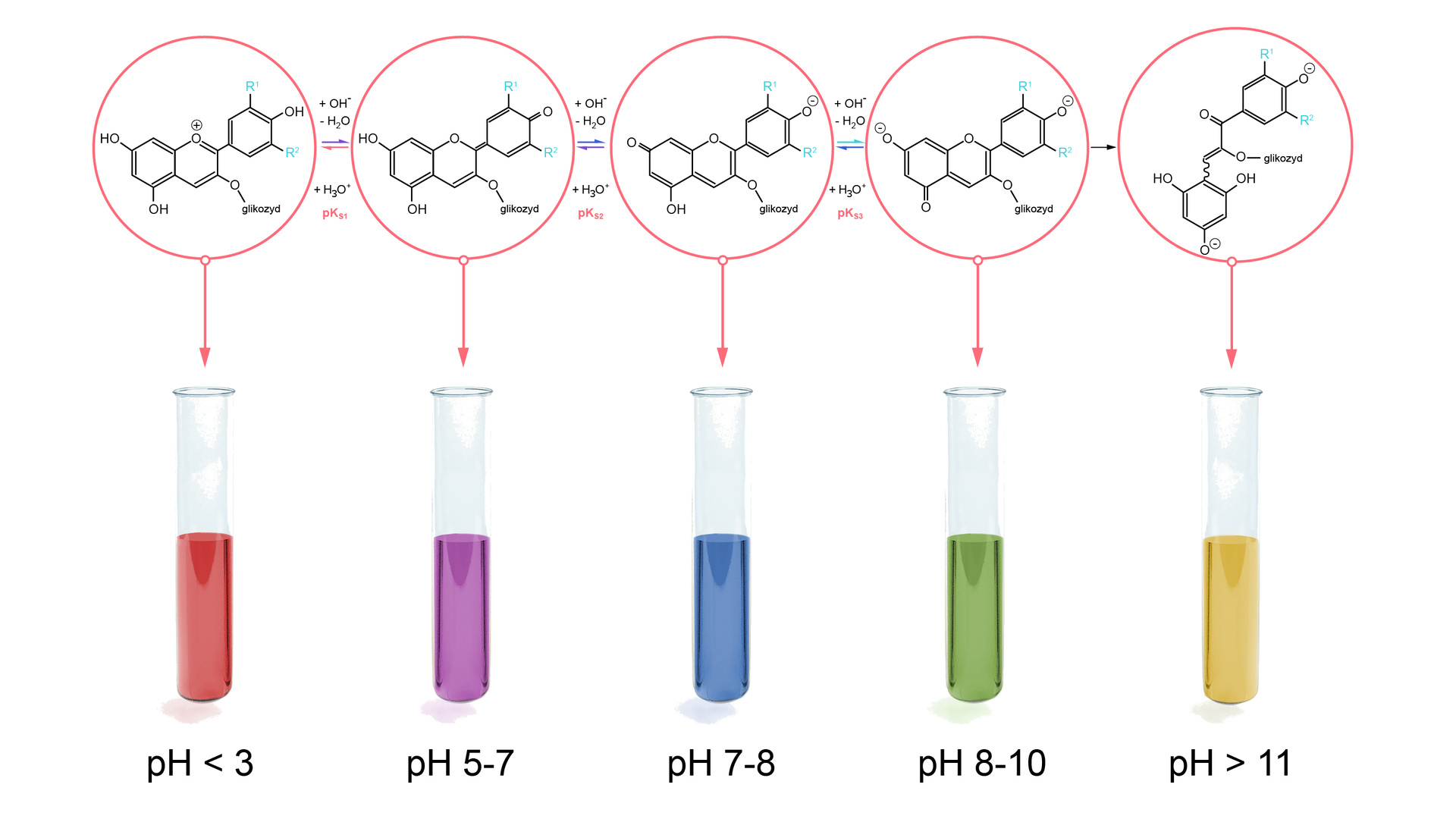
W trakcie zmiany pH, w antocyjanach zachodzą złożone reakcje chemiczne. Ze względu na złożoną budowę cząsteczek antocyjanów, wywar z czerwonej kapusty jest wskaźnikiem działającym w szerokim zakresie pH. Jednakże powyżej pewnej wartości zachodzi reakcja, która dezaktywuje wskaźnik i nie pozwala na jego dalsze działanie.
Inne metody oznaczania pH
Powyższe wskaźniki nie są dostatecznie precyzyjne, aby określić pH z dużą dokładnością. W celu określenia pH z dużą dokładnością, używa się pH‑metru lub metod analitycznych. Urządzenie, jakim jest pH‑metrpH‑metr, pozwala na precyzyjne określenie pH roztworu. Składa się on z elektrody oraz miernika. W rzeczywistości jest to pomiar tak zwanej siły elektromotorycznej (SEM), na podstawie której określany jest potencjał elektrochemiczny. Metody elektrochemiczne należą do jednych z najbardziej precyzyjnych metod pomiarowych. W trakcie pomiaru układ musi być termostatowanytermostatowany. Oznacza to, że temperatura podczas pomiaru jest stała. Miernik sam przelicza SEM na pH.
Pomiar pH za pomocą wskaźników
Czy wiesz, jak zbadać pH roztworów wodnych nieznanych substancji? Zbadaj pH i określ odczyn niewiadomych próbek wodnych roztworów. Do dyspozycji masz 10 wskaźników pH. Instrukcja do gry znajduje się w lewym górnym rogu ekranu.
Uwaga! Wybieraj wskaźniki uważnie. Maksymalna ilość punktów, możliwych do zdobycia za każdą z prób, to 3 punkty (przy zastosowaniu dwóch wskaźników pH). Im więcej wskaźników użyjesz, tym mniejszą ilość punktów zdobędziesz po udzieleniu poprawnej odpowiedzi. Jeśli uda Ci się określić pH przy użyciu trzech wskaźników, to zdobędziesz 2 punkty, przy użyciu czterech – 1 punkt.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D8NCNZG65
Wybierz poprawne odpowiedzi.
Roztwór tymoloftaleiny barwi się na niebiesko przy wartościach pH: Możliwe odpowiedzi: 1. powyżej dziewięć., 2. powyżej trzynaście., 3. poniżej dziewięć., 4. poniżej siedem.
Pomiar pH za pomocą pH‑metru
Przygotowanie aparatu do pomiaru
Pierwszym krokiem potrzebnym do wykonania pomiaru pH jest kalibracja pH‑metru. Wykonywana jest ona w celu zapewnienia dokładności pomiaru, ponieważ aktywność jonów oksoniowych zależy od temperatury. Większość nowoczesnych pH‑metrów ma dodatkową opcję kompensacji temperatury, dzięki czemu wpływ temperatury jest niwelowany. Aby wykalibrować pH‑metr są nam potrzebne roztwory wzorcowe, które możemy zakupić w sklepie chemicznym lub przygotować w laboratorium roztwory buforowe Britton’a–Robinson’a.
Elektroda jest elementem delikatnym, dlatego trzeba postępować bardzo ostrożnie.
Aby wykonać kalibrację postępuj zgodnie z instrukcją dołączoną do pH‑metru. Zwykle procedura kalibracji przebiega w następujacy sposób:
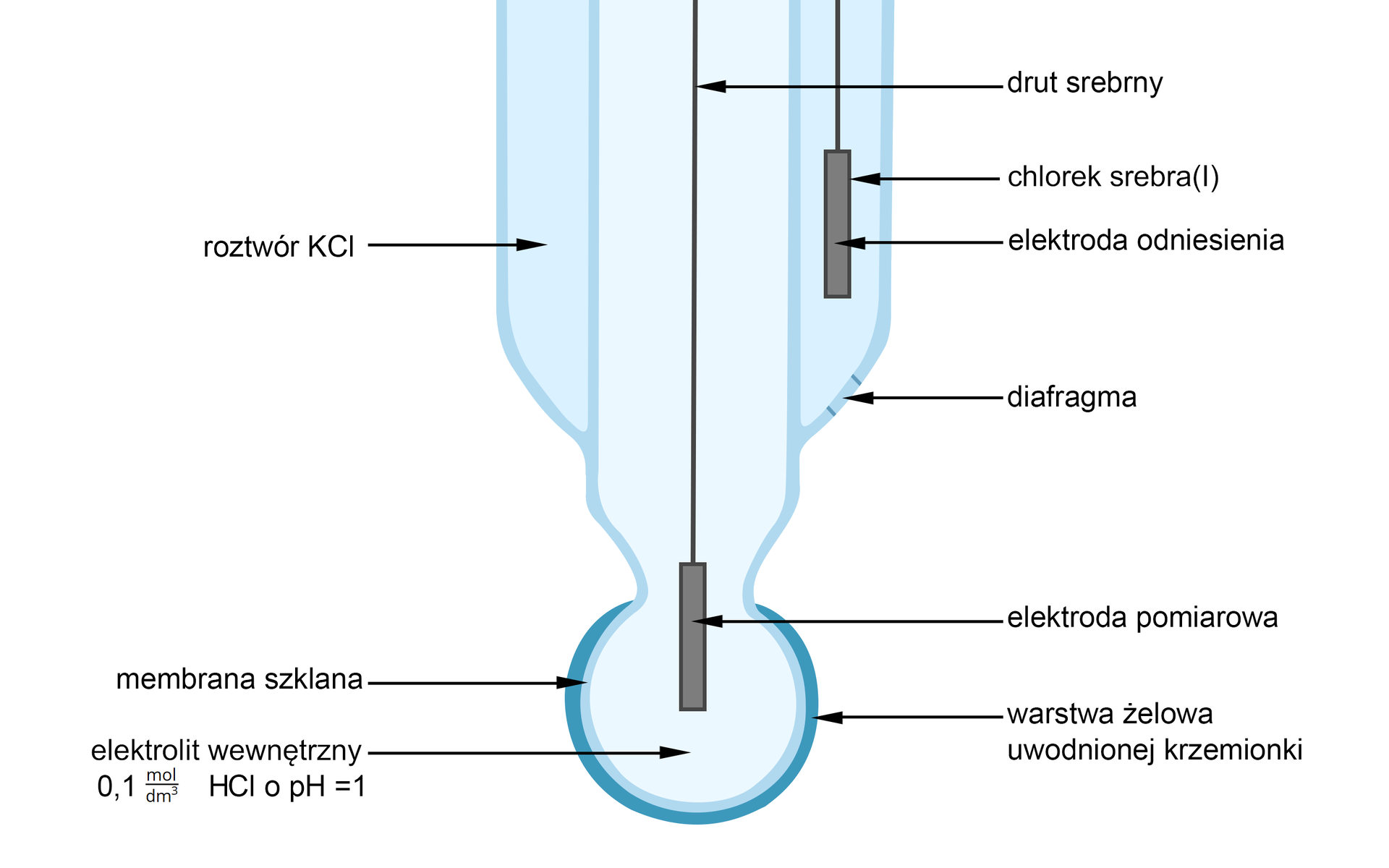
Wyciągnij elektrodę z naczynia z wodnym roztworem chlorku potasu, w którym jest ona zanurzona, a następnie przepłucz ją wodą destylowaną. Pozostałą na szklanej bańce wodę zbierz za pomocą bibuły.
Umieść elektrodę w roztworze buforowym, tak, aby w roztworze znalazł się punkt elektrody oznaczony na rysunku jako „diafragma”.
Naciśnij przycisk kalibracji i odczekaj do momentu, aż urządzenie poinformuje cię o zakończeniu pomiaru.
W zależności od rodzaju pH‑metru możemy kalibrować go na kilka roztworów buforowych, a im więcej użytych roztworów tym dokładniejsze wyniki pomiarów. Trzeba pamiętać o tym, aby przed każdym pomiarem przepłukać elektrodę wodą destylowaną i dokładnie osuszyć.
W celu prawidłowego działania pH‑metru kalibrację należy wykonać ściśle przestrzegając instrukcji dołączonej przez producenta.
Wykonanie pomiaru
Po wykonaniu kalibracji możesz przystąpić do pomiaru.
Pamiętaj, że każdy pomiar powinien być poprzedzony przemyciem elektrody i osuszeniem zgodnie z instrukcją opisaną w czasie kalibracji. Elektrodę należy oczyścić również po jej ostatnim użyciu, a przed ponownym jej umieszczeniem w roztworze .
Sam pomiar polega również na zanurzeniu elektrody w analizowanym roztworze (pamiętaj o konieczności zanurzenia diafragmy). Niektóre pH‑metry wymagają dodatkowo wciśnięcia odpowiedniego przycisku rozpoczynającego pomiar.
Wiesz, jak działa pH‑metr? Zapoznaj się z poniższą symulacją. Zmierz pH przygotowanych roztworów. Pamiętaj o prawidłowym wykonaniu pomiaru oraz o tym, aby na początku przemyć sondy (elektrody) wodą destylowaną. Następnie rozwiąż poniższe zadania.
Wiesz, jak działa pH‑metr? Zapoznaj się z opisem symulacji. Następnie rozwiąż poniższe zadania.
- Do zlewki wlano niewielką ilość wybranego roztworu.
- Wyjęto elektrodę z roztworu, w którym jest przechowywana, a następnie przemyto wodą destylowaną.
- Do wybranego uprzednio roztworu włożono elektrodę.
- Sprawdzono wartość pH.
- dla roztworu chlorowodoru o stężeniu 0,1 pH jest równe 1;
- dla roztworu chlorowodoru o stężeniu 0,15 pH jest równe 0,82;
- dla roztworu chlorowodoru o stężeniu 0,2 pH wynosi 0,7;
- dla roztworu chlorowodoru o stężeniu 0,25 pH jest równe 0,6;
- dla roztworu chlorowodoru o stężeniu pH jest równe 0,26;
- dla roztworu chlorowodoru o stężeniu 0,01 pH jest równe 1,91;
- dla roztworu chlorowodoru o stężeniu 0,001 pH jest równe 3;
- dla roztworu chlorowodoru o stężeniu 0,002 jest równe 2,67;
- dla roztworu wodorotlenku sodu o stężeniu 1 pH wynosi 14;
- dla roztworu wodorotlenku sodu o stężeniu 0,1 pH jest równe 13;
- dla roztworu wodorotlenku sodu o stężeniu 0,01 pH jest równe 12;
- dla roztworu wodorotlenku sodu o stężeniu 0,005 pH wynosi 11,7;
- dla roztworu wodorotlenku sodu o stężeniu 0,001 pH jest równe 11

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D8NCNZG65
Wyjaśnij, dlaczego przed każdym pomiarem musimy przepłukiwać elektrodę.
W laboratorium chemicznym wykonywano analizę pewnej substancji. W tym celu przygotowano zestaw do analizy, składający się z: biurety, pipety jednomiarowej, naciągarki oraz kilku kolb Erlenmeyera. Po zakończeniu oznaczania na stole laboratoryjnym pozostały trzy nieopisane kolby z bezbarwnymi roztworami, a po wskaźniku uniwersalnym pusta butelka. Do dyspozycji uczniowie mieli: pH‑metr, alkoholowy roztwór fenoloftaleiny oraz wodny roztwór oranżu metylowego, statyw oraz probówki.
Z każdej kolby pobrano po znajdującego się w nich roztworu, a każdy z pobranych roztworów umieszczono w osobnych probówkach. Do każdej z nich dodano po kilka kropel alkoholowego roztworu fenoloftaleiny oraz zapisano obserwacje. Powtórzono procedurę dla wodnego roztworu oranżu metylowego. Następnie zawartość każdej kolby została zbadana przy pomocy pH‑metru. Wyniki eksperymentu zanotowano.
Na podstawie wyników pomiarów postaraj się określić zawartość poszczególnych kolb.
Kolba | Fenoloftaleina | Oranż metylowy | pH‑metr |
brak zmian | brak zmian | ||
kolor zmienia się na | brak zmian | ||
brak zmian | kolor zmienia się na |