Jakie właściwości i zastosowanie wykazują kwasy?
Klasyfikacja kwasów ze względu na ich moc
Jednym ze sposobów klasyfikacji kwasów jest ich podział. Wyróżniamy kwasy mocne oraz słabe. Podstawą do określenia mocy kwasu jest przebieg jego dysocjacji jonowej, a w związku z tym wartość stałej dysocjacji . Wszystkie rozpuszczalne w wodzie kwasy ulegają dysocjacji jonowej. Jeżeli proces ten przebiega praktycznie w 100%, można je wówczas uznać za mocne kwasy. Jeżeli natomiast dysocjacja zachodzi w niewielkim stopniu, to mamy doczynienia z kwasem słabym.
Mocne kwasy
Mocne kwasy to elektrolity, które w roztworze wodnym są całkowicie lub prawie całkowicie zdysocjowane. Dzieli się je na tlenowe oraz beztlenowe.

Słabe kwasy
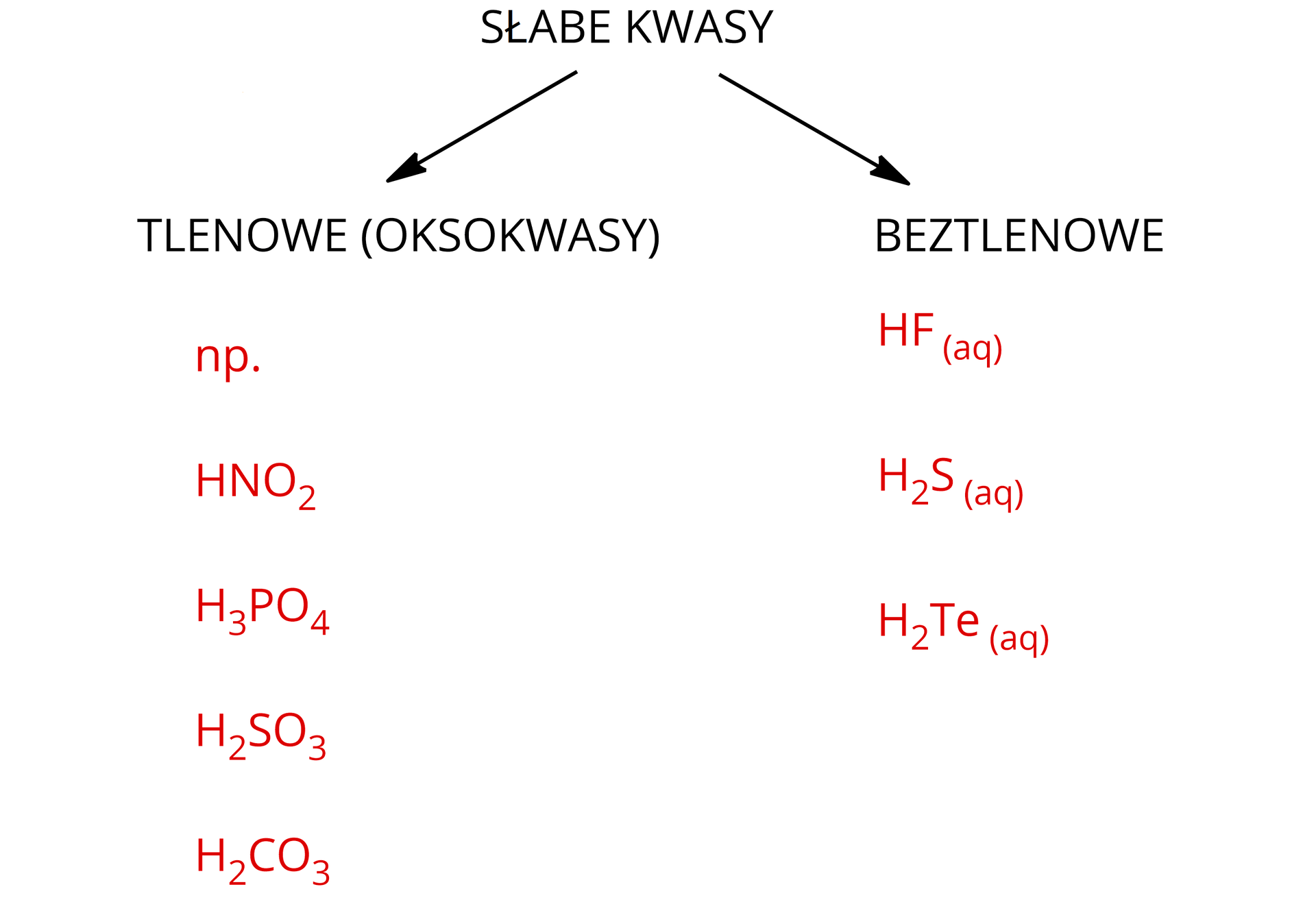
Moc kwasów beztlenowych i tlenowych
- wzrasta wraz ze wzrostem liczby atomowej atomu centralnego (wraz ze zmniejszaniem się elektroujemności niemetalu)
- wzrasta wraz ze wzrostem elektroujemności atomu centralnego reszty kwasowej
- wzrasta ze wzrostem liczby atomów tlenu
Jak dzielimy kwasy ze względu na ich moc? Czy kwas siarkowy() jest reprezentantem kwasów mocnych czy słabych? Które kwasy dysocjują całkowicie? Zapoznaj się z mapą myśli na temat mocy kwasów, a następnie wykonaj ćwiczenia.
- Nazwa kategorii: Kwasy
- Nazwa kategorii: mocne (dysocjują całkowicie, posiadają wysokie wartości stałej i stopnia dysocjacji)
- Nazwa kategorii: tlenowe
- Nazwa kategorii: H N O indeks dolny, trzy, koniec indeksu dolnego
- Nazwa kategorii: H indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, cztery, koniec indeksu dolnego
- Nazwa kategorii: H C l O indeks dolny, cztery, koniec indeksu dolnego
- Nazwa kategorii: H C l O indeks dolny, trzy, koniec indeksu dolnego Koniec elementów należących do kategorii tlenowe
- Nazwa kategorii: beztlenowe
- Nazwa kategorii: H C l indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego
- Nazwa kategorii: H B r indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego
- Nazwa kategorii: H I indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego Koniec elementów należących do kategorii beztlenowe
- Nazwa kategorii: słabe (dysocjują w małym stopniu, posiadają niskie wartości stałej i stopnia dysocjacji)
- Nazwa kategorii: tlenowe
- Nazwa kategorii: nieorganiczne
- Nazwa kategorii: H indeks dolny, dwa, koniec indeksu dolnego, S O indeks dolny, trzy, koniec indeksu dolnego
- Nazwa kategorii: H indeks dolny, dwa, koniec indeksu dolnego, C O indeks dolny, trzy, koniec indeksu dolnego
- Nazwa kategorii: H indeks dolny, trzy, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego
- Nazwa kategorii: H indeks dolny, trzy, koniec indeksu dolnego, P O indeks dolny, cztery, koniec indeksu dolnego
- Nazwa kategorii: H C l O
- Nazwa kategorii: H indeks dolny, dwa, koniec indeksu dolnego, S i O indeks dolny, trzy, koniec indeksu dolnego Koniec elementów należących do kategorii nieorganiczne
- Nazwa kategorii: organiczne
- Nazwa kategorii: C H indeks dolny, trzy, koniec indeksu dolnego, C O O H
- Nazwa kategorii: H C O O H
- Nazwa kategorii: C indeks dolny, dwa, koniec indeksu dolnego, H indeks dolny, pięć, koniec indeksu dolnego, C O O H Koniec elementów należących do kategorii organiczne
- Nazwa kategorii: beztlenowe
- Nazwa kategorii:H F indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego
- Nazwa kategorii: H C N indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego
- Nazwa kategorii: H indeks dolny, dwa, koniec indeksu dolnego, S indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego
- Nazwa kategorii: H indeks dolny, dwa, koniec indeksu dolnego, T e indeks dolny, nawias, aq, zamknięcie nawiasu, koniec indeksu dolnego Koniec elementów należących do kategorii beztlenowe
- Elementy należące do kategorii Kwasy
- Elementy należące do kategorii mocne (dysocjują całkowicie, posiadają wysokie wartości stałej i stopnia dysocjacji)
- Elementy należące do kategorii tlenowe
- Elementy należące do kategorii beztlenowe
- Elementy należące do kategorii słabe (dysocjują w małym stopniu, posiadają niskie wartości stałej i stopnia dysocjacji)
- Elementy należące do kategorii tlenowe
- Elementy należące do kategorii nieorganiczne
- Elementy należące do kategorii organiczne
- Elementy należące do kategorii beztlenowe
Reakcje wybranych kwasów nieorganicznych z materiałami z życia codzienniego
Czy wiesz, jakie działanie wykazują kwasy w kontakcie z tkaniną, papierem czy drewnem? Zaplanuj i przeprowadź eksperymenty. Zapoznaj się z problemem badawczym i zweryfikuj własną hipotezę. W formularzu zanotuj swoje obserwacje i wyniki, a następnie zapisz wnioski.
Po przeprowadzeniu eksperymentu z pierwszym kwasem, kliknij na ikonę domu znajdującą się w prawym górnym rogu ekranu, która przeniesie Cię do wyboru następnego eksperymentu z kolejnym kwasem.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DCZJG8RH3
Czy wiesz, jakie działanie wykazują kwasy w kontakcie z tkaniną, papierem czy drewnem? Zapoznaj się z problemem badawczym i postawioną hipotezą, zanotowanymi obserwacjami i wynikami oraz wnioskami.
Eksperyment
Analiza eksperymentu:
Reaktywność kwasu siarkowego() w kontakcie z materiałami spotykanymi w życiu codziennym.
Problem badawczy:
Jakie działanie wykazuje kwas siarkowy() w kontakcie z tkaniną, papierem, drewnem i cukrem?
Hipoteza:
Kwas siarkowy() prowadzi do zwęglenia materiałów pochodzenia organicznego.
Sprzęt laboratoryjny:
szkiełka zegarowe – szklane naczynia o zaokrąglonym kształcie podstawy, służące np. do odważania niewielkich ilości substancji chemicznych;
zlewka – naczynie szklane o kształcie cylindrycznym, stosowane do przeprowadzania prostych reakcji chemicznych;;
pipety Pasteura – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
łyżeczka – długi trzonek wykonany ze szkła, porcelany lub metalu, zakończony z jednej strony łyżeczką;
cylinder – podłużne szklane naczynie laboratoryjne w kształcie walca z umieszczoną na ściance podziałką objętości, służące do odmierzania cieczy.
Odczynniki chemiczne:
dziewięćdziesięciosześcioprocentowy kwas siarkowy(); skrawek tkaniny; papier; drewno; cukier.
Przebieg eksperymentu:
Na przygotowane na szkiełkach zegarowych materiały: skrawek tkaniny, papier i drewno, naniesiono kilka kropli stężonego kwasu siarkowego().
Zaobserwowano zmiany zachodzące na materiałach.
Do wysokiej zlewki dodano cukier (do trzech czwartych wysokości).
Następnie dodano około centymetrów sześciennych dziewięćdziesięciosześcioprocentowego kwasu siarkowego().
Ponownie zaobserwowano zachodzące zmiany.
Obserwacje:
Po naniesieniu kilku kropli kwasu siarkowego() na skrawek tkaniny, papier oraz drewno nastąpiło szybkie zniszczenie materiałów i pojawienie się na nich czarnych plam przypominających zwęglenie. Dodanie dziewięćdziesięciosześcioprocentowego kwasu siarkowego() do zlewki z cukrem doprowadziło do zmiany barwy cukru miejscowo na kolor żółty, potem na brązowy, a ostatecznie na całej objętości cukru na kolor czarny oraz do znacznego wzrostu objętości.
Wyniki:
W wyniku działania stężonego kwasu siarkowego() doszło do zwęglenia każdego z badanych materiałów.
Wnioski:
Stężony kwas siarkowy() reaguje z materią organiczną, prowadząc do jej zniszczenia. Jednym z produktów tej reakcji jest węgiel pierwiastkowy, który odpowiada za czarną barwę pojawiającą się w miejscach oddziaływania kwasu siarkowego() z badanymi materiałami.
Eksperyment
Analiza eksperymentu:
Reaktywność kwasu azotowego() w kontakcie z materiałami spotykanymi w życiu codziennym.
Problem badawczy:
Jakie działanie wykazuje kwas azotowy() w kontakcie z białym serem, wełną owczą, ptasim piórem i blaszką miedzianą?
Hipoteza:
W wyniku kontaktu białego sera, owczej wełny oraz ptasiego pióra ze stężonym kwasem azotowym() dochodzi do reakcji ksantoproteinowej, a miedź reaguje z kwasem azotowym(), czego produktem jest azotan() miedzi().
Sprzęt laboratoryjny:
probówka – podłużne U–kształtne naczynie szklane do przeprowadzania prostych reakcji chemicznych;
pipety Pasteura – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
3 szkiełka zegarowe – szklane naczynia o zaokrąglonym kształcie podstawy, służące np. do odważania niewielkich ilości substancji chemicznych szklane;
pęseta (szczypce) – z reguły metalowe narzędzie o sprężystych ramionach, umożliwiające chwytanie niewielkich przedmiotów.
Odczynniki chemiczne:
sześćdziesięciopięcioprocentowy kwas azotowy(); biały ser; wełna owcza; ptasie pióro; blaszka miedziana.
Przebieg eksperymentu:
Na przygotowane na szkiełkach zegarowych materiały: biały ser, ptasie pióro i owczą wełnę, naniesiono kilka kropli sześćdziesięciopięcioprocentowego kwasu azotowego().
Zaobserwowano zmiany zachodzące na materiałach.
Do probówki dodano kwasu azotowego().
Następnie szczypcami umieszczono w niej kawałek blaszki miedzianej.
Ponownie zaobserwowano zmiany zachodzące w probówce.
Obserwacje:
Po naniesieniu kilku kropli kwasu azotowego() na biały ser, ptasie pióro i owczą wełnę zaobserwowano zmianę barwy badanych materiałów na żółty kolor. Zmiana zabarwienia z bezbarwnego roztworu na niebiesko‑zielony po dodaniu blaszki miedzianej, wydzielające się pęcherzyki gazu oraz brunatny gaz.
Wyniki:
Na białym serze, wełnie oraz piórze widoczne są skutki reakcji ksantoproteinowej w miejscach, gdzie doszło do kontaktu z kwasem azotowym(). W reakcji z metaliczną miedzią doszło do powstania niebieskozielonego roztworu azotanu() miedzi(), a innym produktem tej reakcji był tlenek azotu().
Wnioski:
Reakcja ksantoproteinowa jest wynikiem reakcji pomiędzy białkami (a dokładniej aminokwasami aromatycznymi) a kwasem azotowym(). Żółta barwa pochodzi od powstałych nitropochodnych aminokwasów aromatycznych. Miedź reaguje ze stężonym kwasem azotowym, bowiem jest to kwas utleniający. Zachodzi reakcja redoks, w której jon redukuje się, a atom miedzi utlenia. Dzięki temu powstaje sól – azotan() miedzi() oraz brunatny gaz – tlenek azotu().
Eksperyment
Analiza eksperymentu:
Reaktywność kwasu ortofosforowego() w kontakcie z materiałami spotykanymi w życiu codziennym.
Problem badawczy:
Jakie działanie wykazuje kwas ortofosforowy() w kontakcie z tkaniną, papierem i zardzewiałym gwoździem?
Hipoteza:
Kwas ortofosforowy() prowadzi do uszkodzenia papieru oraz odrdzewienia gwoździa. Nie widać z kolei objawów reakcji w kontakcie z tkaniną.
Sprzęt laboratoryjny:
2 szkiełka zegarkowe – szklane naczynia o zaokrąglonym kształcie podstawy, służące, np. do odważania niewielkich ilości substancji chemicznych;
statyw na probówki – prostokątny sprzęt laboratoryjny z rzędami otworów, w których umieszczane są probówki;
pipety Pasteura – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki;
probówka – podłużne U‑kształtne naczynie szklane do przeprowadzania prostych reakcji chemicznych.
Odczynniki chemiczne:
osiemdziesięciopięcioprocentowy kwas ortofosforowy(); skrawek tkaniny; papier; zardzewiały gwóźdź.
Przebieg eksperymentu:
Na kawałki tkaniny i papieru naniesiono kilka kropli roztworu kwasu ortofosforowego().
Zaobserwowano zmiany zachodzące na materiałach.
Następnie umieszczono zardzewiały gwóźdź w probówce z roztworem kwasu na kilka dni.
Ponownie zaobserwowano zmiany po kilku dniach.
Obserwacje:
Papier ulega zniszczeniu, natomiast tkanina nie. Po upływie kilku dni rdza na gwoździu ulega zmniejszeniu – roztwarza się.
Wyniki:
Stężony kwas ortofosforowy() doprowadził do zwęglenia papieru oraz usunął znaczną ilość rdzy z gwoździa. W kontakcie tkaniny z kwasem nie zaszły żadne zmiany.
Wnioski:
Stężony kwas ortofosforowy() jest słabszym kwasem od stężonego kwasu siarkowego(), dlatego efekt zwęglenia w kontakcie z materią organiczną jest słabszy niż dla kwasu siarkowego(). Z kolei efekt usuwania rdzy bierze się z reakcji zachodzącej między tlenkiem żelaza() a kwasem ortofosforowym(), w wyniku której powstaje fosforan() żelaza().
Eksperyment
Analiza eksperymentu:
Reaktywność kwasu chlorowodorowego w kontakcie z materiałami spotykanymi w życiu codziennym.
Problem badawczy:
Jakie działanie wykazuje kwas chlorowodorowy w kontakcie z tkaniną i papierem?
Hipoteza:
Kwas chlorowodorowy prowadzi do zwęglenia papieru oraz tkaniny.
Sprzęt laboratoryjny:
szkiełka zegarkowe – szklane naczynia o zaokrąglonym kształcie podstawy, służące np. do odważania niewielkich ilości substancji chemicznych;
pipety Pasteura – wąskie rurki służące do pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki.
Odczynniki chemiczne:
trzydziestopięcioprocentowy kwas chlorowodorowy; skrawek tkaniny; papier.
Przebieg eksperymentu:
Na przygotowane na szkiełkach zegarowych materiały: papier i tkaninę, naniesiono niewielką ilość kwasu chlorowodorowego.
Zaobserwowano zachodzące zmiany.
Obserwacje:
Papier oraz tkanina w kontakcie ze stężonym kwasem chlorowodorowym ulegają zniszczeniu i powstają czarne plamy.
Wyniki:
Wskutek kontaktu stężonego kwasu chlorowodorowego z papierem oraz tkaniną doszło do ich zwęglenia.
Wnioski:
Kwas chlorowodorowy, podobnie jak kwas siarkowy(), jest kwasem mocnym i prowadzi do zwęglenia materii organicznej, a czarne plamy są wynikiem powstawania pierwiastkowego węgla.
Jak kwasy reagują z metalami?
Zastanów się, co się dzieje, gdy żelazny gwóźdź włożymy w miąższ jabłka. Jednym ze składników miąższu jest kwas jabłkowy (nazwa systematyczna kwas 2‑hydroksybutano‑1,4‑diowy). Żelazo reaguje z tym kwasem, w wyniku tej reakcji powstają związki żelaza przyswajalne dla organizmów, co może zapobiegać anemii. Potwierdziły to badania na szczurach z 1982 r. Stalowe gwoździe wbite w jabłko na 24 godziny spowodowały wytworzenie związków żelaza przyswajalnych dla szczura. Jednak gwoździe nie są zbudowane tylko z atomów żelaza – zawierają też inne dodatki, które mogą być szkodliwe. A ponieważ w dzisiejszych czasach mamy rozwiniętą naukę i medycynę, możemy skorzystać ze skuteczniejszych metod zapobiegania anemii i podawania przebadanych suplementów diety zawierających dobrze przyswajalne związki żelaza. Dlatego dr Ciemięga stwierdza na swojej stronie: Będąc w ciąży i jedząc jabłka potencjalnie nafaszerowane szkodliwymi substancjami z gwoździ, to nie jest ani EKO ani Natural. To po prostu głupie
.
Wiesz już, że żelazo przereagowało z kwasem jabłkowym. Czy oznacza to, że każdy metal reaguje z każdym kwasem? I że reakcja przebiega według tego samego schematu?
Przeanalizuj ogólną mapę pojęć dotyczącą reakcji metali z kwasami oraz jej szczegółowe wersje poniżej.
Przeanalizuj opis ogólnej mapy pojęć dotyczącej reakcji metali z kwasami oraz ich szczegółowych wersji.
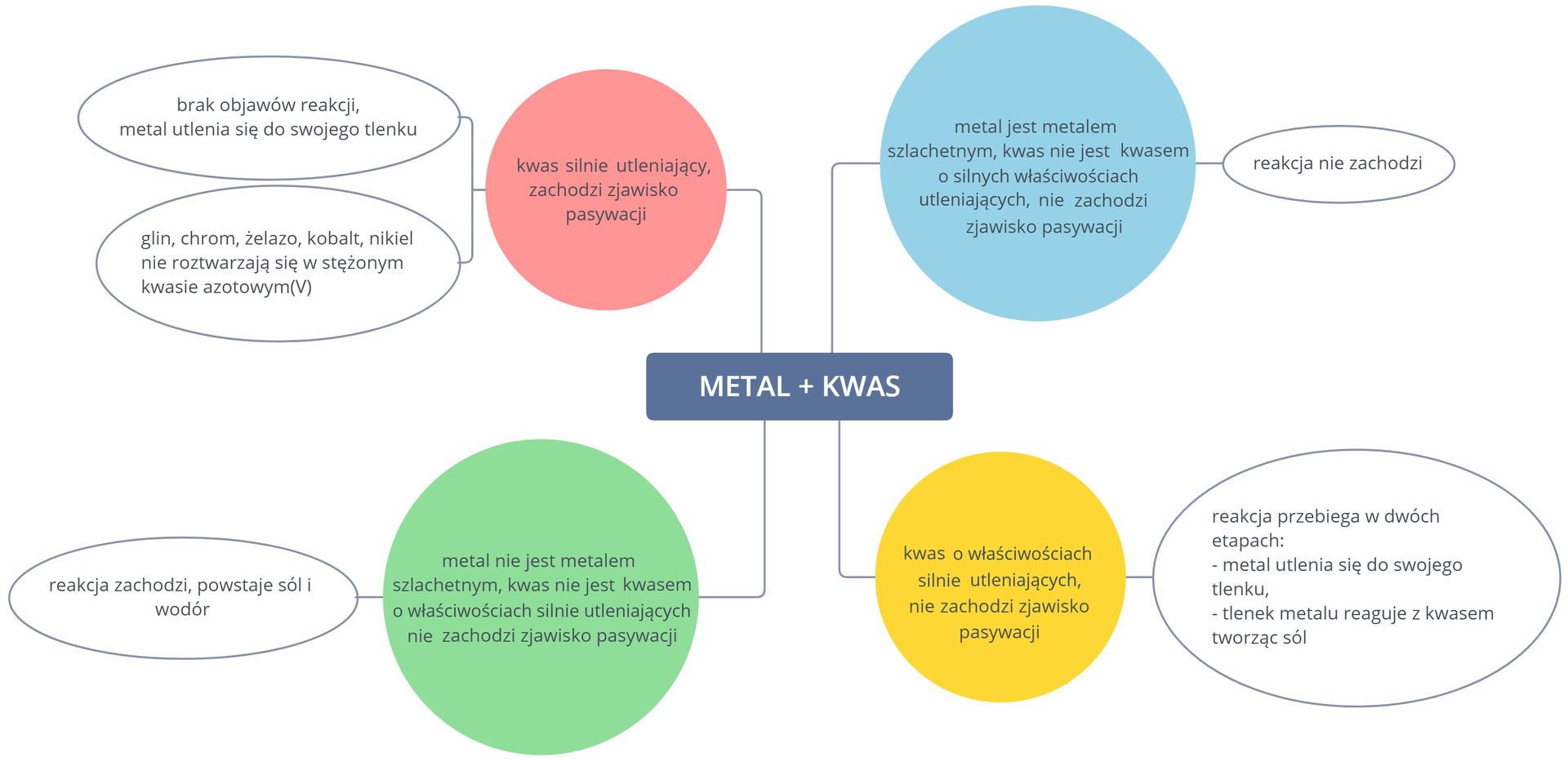
Reakcje metalu z kwasem, w wyniku których powstaje sól i wodór, są reakcjami wymiany pojedynczej i reakcjami redoks. W tych reakcjach atomy metalu oddają elektrony, a jon (pochodzący z dysocjacji kwasu) przyjmuje te elektrony. Symbolicznie można zapisać ten proces jako:
Dla reakcji ukazanych na mapie, w których powstaje sól i wodór, równania jonowe przyjmą postać:
Zwróć uwagę, że dla danego metalu skrócony jonowy zapis równania reakcji jest taki sam, niezależnie od kwasu biorącego udział w reakcji.
Wiesz już, że żelazne gwoździe reagują z kwasem jabłkowym, ale nie będziesz z tego korzystać, gdy zechcesz zapobiec anemii. Czy zatem wiedza o reakcjach kwasów z metalami przydaje się nam w codziennym życiu?
Wiesz już, że wybrane metale, które reagują wg schematu:
ulegają roztworzeniu w kwasie, czyli metale te poddane działaniu kwaśnych deszczy również ulegają roztworzeniu – dlatego musimy je zabezpieczać (np. poprzez pomalowanie ich powierzchni).
Dzięki temu, że glin ulega pasywacji, znalazł on zastosowanie do budowy cystern, w których jest przewożony stężony kwas azotowy(V), a także do budowy puszek do napoju typu cola (zawierającego kwas ortofosforowy(V)).
Przeprowadź eksperyment w wirtualnym laboratorium i sprawdź, jak zachowują się wybrane metale w reakcji z kwasami. Zapoznaj się z problem badawczym, sformułuj i zweryfikuj hipotezę. W formularzu zanotuj użyty sprzęt laboratoryjny i odczynniki chemiczne, swoje obserwacje oraz zapisz wyniki i wnioski.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/DCZJG8RH3
Zadanie: sprawdź, jak zachowują się wybrane metale w reakcji z kwasami.
Analiza eksperymentu: Reakcja wybranych metali z kwasami.
Problem badawczy: Czy przebieg reakcji kwasów utleniających i nieutleniających z metalami jest taki sam?.
Hipoteza: Przebieg reakcji kwasów utleniających i nieutleniających z metalami jest odmienny.
Sprzęt laboratoryjny: 12 probówek - podłużne naczynie szklane do przeprowadzania prostych reakcji chemicznych, pipety jednorazowe - wąska rurka pobierania i przenoszenia niewielkiej ilości cieczy przy pomocy ssawki; pipety jednorazowe; łyżeczki - długi trzonek wykonany ze szkła, porcelany lub metalu zakończony z jednej strony łyżeczką. Służy do nabierania sypkich substancji chemicznych.
Odczynniki chemiczne: 30% roztwór kwasu chlorowodorowego; 60% roztwór kwasu azotowego(V); 25% roztwór kwasu siarkowego(VI); magnez; żelazo; miedź; cynk.
Przebieg eksperymentu: Całe doświadczenie należy wykonać pod dygestorium z włączonym wyciągiem. Należy przygotować 12 probówek. Do czterech probówek za pomocą pipety jednorazowej należy wkroplić 3 centymetry sześcienne 60% roztwór kwasu azotowego(V). Tę samą czynność powtarza się dla następnych czterech probówek, wprowadzając do nich po 3 centymetry sześcienne 30% roztworu kwasu chlorowodorowego, a do pozostałych 3 centymetrów sześciennych 25% roztworu kwasu siarkowego(VI). Następnie trzeba umieścić w probówkach za pomocą łyżeczki próbki metali (po 1 gramie danego metalu do każdej z probówek).
Obserwacje: W przypadku kwasu azotowego(V) w probówce z magnezem i cynkiem wydziela się brunatny gaz. W probówce z żelazem brak objawów reakcji. W probówce z miedzią reakcja zachodzi wolno – po dłuższej chwili obserwujemy jasnoniebieskie zabarwienie roztworu oraz wydzielający się brunatny gaz. W przypadku kwasu solnego w probówkach z magnezem, cynkiem i żelazem wydzielają się pęcherzyki gazu. Dodatkowo w probówce z żelazem zauważalna jest zmiana zabarwienia roztworu na jasnozielony kolor. W probówce z miedzią brak objawów reakcji. W przypadku kwasu siarkowego(VI) w probówkach z magnezem, cynkiem i żelazem wydzielają się pęcherzyki gazu. W probówce z miedzią brak objawów reakcji.
Wyniki: Nie wszystkie metale reagują identycznie z kwasami utleniającymi (kwas azotowy(V)) i nieutleniającymi (kwas chlorowodorowy i kwas siarkowy(IV)).
Wnioski: W reakcjach kwasu chlorowodorowego i kwasu siarkowego(VI) z żelazem, cynkiem i magnezem ulatniający się gaz z probówki to wodór. W czasie reakcji metale te wypierają wodór z kwasu i zajmują jego miejsce. W reakcjach kwasu azotowego(V) z magnezem, cynkiem i miedzią wydziela się bezbarwny gaz, który szybko brunatnieją na powietrzu, tworząc tlenek azotu(IV). W reakcji z żelazem brak objawów reakcji, ponieważ zachodzi proces pasywacji. W reakcji kwas azotowy(V) reaguje z miedzią, tworząc jasnoniebieski roztwór pochodzący od kationów miedzi(II). Hipoteza została potwierdzona.
Kwasy nieorganiczne w roztworze wodnym reagują z wodorotlenkami
Reakcja tlenków z kwasami
Reakcja kwasu z solą innego kwasu
W roztworze wodnym kwas reaguje z solą innego kwasu. Gdy mocny kwas reaguje z solą słabszego kwasu, to następuje reakcja wymiany podwójnej:
np.:
