Mydło w walce o czystość
Dbanie o czystość nie byłoby trudne, gdyby wszystkie zabrudzenia i plamy rozpuszczały się w wodzie. Niestety, większość z nich jest odporna na działanie wody. Ludzie od najdawniejszych czasów poszukiwali skutecznych sposobów pozbywania się brudu podczas mycia i prania. Okazało się, że do tego celu doskonale nadają się mydła. Czym się charakteryzują i jaki jest mechanizm ich działania?
charakterystykę substancji polarnych i niepolarnych;
właściwości wody, jako rozpuszczalnika polarnego;
właściwości fizyczne i chemiczne tłuszczów;
właściwości fizykochemiczne wodorotlenków i charakterystykę ich wodnych roztworów.
opisywać właściwości mydeł;
klasyfikować mydła ze względu na stan skupienia, twardość, rozpuszczalność w wodzie i wymieniać przykłady mydeł;
wyjaśniać, na czym polega proces zmydlania tłuszczów;
omawiać, posługując się schematem (rysunkiem), mechanizm działania mydła na brud i zaznaczać fragmenty hydrofobowe i hydrofilowe we wzorach oraz modelach substancji powierzchniowo czynnych;
wyjaśniać, na czym polega proces usuwania brudu z użyciem mydła;
uzasadniać, w jaki sposób twardość wody wpływa na proces mycia oraz proponować sposoby zbadania wpływu twardości wody na powstawanie podczas mycia związków trudno rozpuszczalnych.
1. Właściwości mydeł i ich otrzymywanie
MydłaMydła mają zdolność pienienia się w wodzie i usuwania brudu. Te twarde, stosowane w gospodarstwie domowym, są mydłami sodowymi z dodatkiem substancji zapachowych i barwników. Natomiast składnikami innych produktów, np. kremów do golenia czy preparatów myjących w płynie, są zwykle mydła potasowe.
Mydła są solami wyższych kwasów karboksylowych (kwasów tłuszczowych) – najczęściej kwasu kwasu heksadekanowego (palmitynowego), oktadekanowego (stearynowego) oraz oktadek––enowego (oleinowego). Są to między innymi:
heksadekanian (palmitynian) sodu ;
oktadekanian (stearynian) potasu ;
oktadek––enian (oleinian) sodu .
Znane są takie rodzaje mydeł, które zamiast kationu metalu zawierają inne ugrupowania pierwiastków, jak chociażby kation amonowy. Mydła można podzielić ze względu na ich rozpuszczalność w wodzie:
mydła rozpuszczalne: sodowe, potasowe, amonowe;
mydła nierozpuszczalne: glinowe, żelazowe, wapniowe, magnezowe.
Mają wiele zastosowań. Najczęściej są stosowane jako środki myjące, ale używa się ich również jako dodatków do smarów (mydła litowe) i impregnatów tkanin w produkcji np. namiotów.

Doświadczenie przeprowadzono w rękawicach i okularach ochronnych. W czasie wykonywania doświadczenia użyto stężonego roztworu wodorotlenku, który ma silne właściwości żrące.
Problem badawczy:
Czy można otrzymać mydła w wyniku reakcji kwasów tłuszczowych z wodorotlenkami?
Hipoteza:
Podobnie jak wiele innych kwasów, wyższe kwasy tłuszczowe reagują z wodorotlenkami, tworząc sole. Jednym z produktów reakcji wyższego kwasu tłuszczowego z wodorotlenkiem sodu (lub potasu) będzie sól sodowa (bądź potasowa) tego kwasu, czyli mydło.
Co było potrzebne:
stężony roztwór wodorotlenku sodu;
kwas heksadekanowy (palmitynowy);
fenoloftaleina;
probówka;
szczypce drewniane;
palnik.
Przebieg doświadczenia:
Do probówki z małą ilością stężonego roztworu wodorotlenku sodu dodano kilka kropel fenoloftaleiny. Następnie małymi porcjami dodawano kwas heksadekanowy (palmitynowy), cały czas ogrzewając zawartość probówki w płomieniu palnika. Gdy roztwór zaczął się odbarwiać przerwano dodawanie kwasu i ogrzewanie. Po ostygnięciu probówki, wstrząśnięto jej zawartością, a następnie zbadano właściwości otrzymanego produktu.
Obserwacje:
Malinowy roztwór stopniowo ulega odbarwieniu. Po wstrząśnięciu roztwór spienił się.
Wnioski:
W trakcie reakcji, odczyn roztworu zmienia się z zasadowego na obojętny. Zużywany jest wodorotlenek sodu, co świadczy o tym, że zachodzi jego reakcja z kwasem heksadekanowym. Produkt jest mydłem, o czym świadczy pienienie się roztworu.
Jak myślisz, w jakim celu w doświadczeniu zastosowano fenoloftaleinę?
W wyniku reakcji kwasu heksadekanowego z wodorotlenkiem sodu powstaje sól – heksadekanian (palmitynian) sodu (mydło). Reakcja przebiega zgodnie z równaniem:


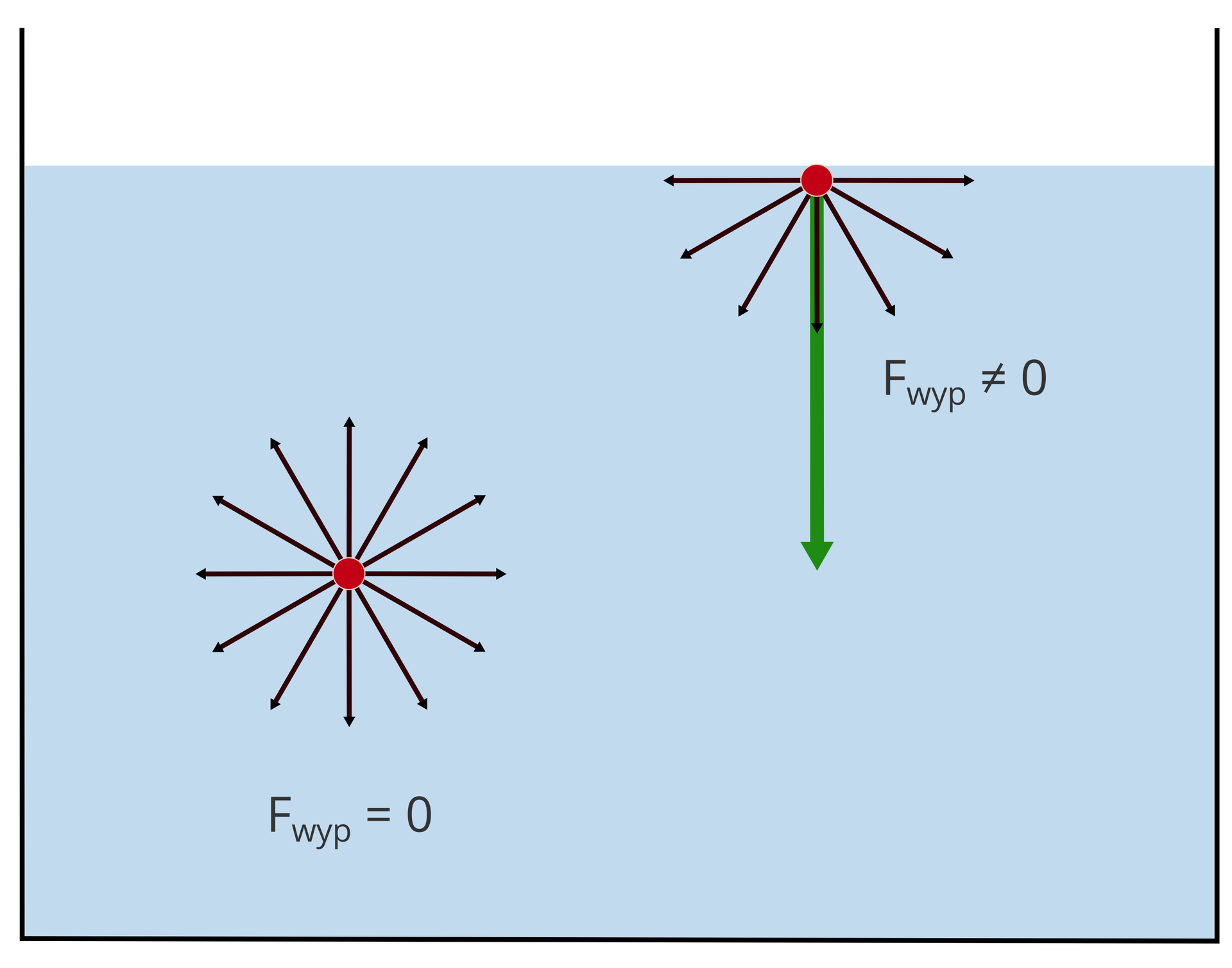
Mydło jest substancją powierzchniowo czynnąsubstancją powierzchniowo czynną. Jego działanie polega na obniżaniu napięcia powierzchniowegonapięcia powierzchniowego wody.

Najstarsze doniesienia o używaniu mydła pochodzą ze starożytnego Babilonu. Przepis na wytwarzanie mydła odczytano na babilońskiej glinianej tabliczce pochodzącej z około . Podobnie na egipskich papirusach pochodzących z — wg nich starożytni Egipcjanie regularnie korzystali z kąpiel, do których używali mydła wytwarzanego z tłuszczów zwierzęcych i roślinnych. Substancje alkaliczne (o właściwościach zasadowych), potrzebne do wyrobu mydła, uzyskiwano z popiołów roślinnych.
Jeszcze na początku mydło było wytwarzane w domach i pralniach, często ze względów ekonomicznych. Surowcem do jego produkcji był tłuszcz, który zbierano miesiącami jako odpadki gospodarstwa domowego i trzymano w specjalnie do tego celu przeznaczonych beczkach lub kadziach. Do nich dodawano jeszcze ług sodowy (wodorotlenek sodu). Trzeba je było chronić przed deszczem, a w momencie słonecznych dni – wystawiać na ekspozycję Słońca. Zawartość kadzi gotowano przeważnie jesienią przez kilka godzin, dodając w miarę potrzeby większą ilość ługu. Następnie próbkę uzyskanej mieszaniny sprawdzano – jeśli twardniała, kończono proces, jeśli nie, kontynuowano gotowanie lub poddawano dalszej obróbce.

Proces otrzymywania mydła z tłuszczu, zwany zmydlaniem tłuszczówzmydlaniem tłuszczów, można przedstawić w postaci schematu:
Przebieg reakcji otrzymywania mydła z tłuszczu przebiega zgodnie z równaniem:

Reakcję zmydlania tłuszczów wykorzystuje się na skalę przemysłową do produkcji mydła, głównie z tłuszczów nasyconych. Proces ten polega na długotrwałym gotowaniu tłuszczów ze stężonym roztworem wodorotlenku sodu. Powstającą obok mydeł glicerynę usuwa się z końcowego produktu lub czasem pozostawia, ponieważ ma ona działanie natłuszczające. Obecnie do produkcji mydła używa się kwasów tłuszczowych, otrzymywanych podczas przerobu ropy naftowej. Często, zamiast czystych kwasów tłuszczowych, stosuje się także naturalne oleje i tłuszcze bądź ich mieszaniny, z których – w procesie zmydlania – powstają bezpośrednio sole odpowiednich kwasów tłuszczowych.
Produkowane współcześnie mydła toaletowe, w celu podniesienia ich walorów służących pielęgnacji skóry oraz ich atrakcyjności dla użytkowników, wzbogaca się różnymi dodatkami – środkami nawilżającymi, substancjami zakwaszającymi, środkami bakteriobójczymi, olejkami zapachowymi, substancjami barwiącymi.

2. Mechanizm usuwania brudu
Woda, jako rozpuszczalnik polarny, znakomicie rozpuszcza inne substancje polarne, czyli substancje o wiązaniach jonowych. Jej cząsteczki łatwo otaczają inne cząsteczki polarne, ponieważ następuje oddziaływanie między ich ładunkami lub ładunkami cząstkowymi. Oleje mineralne czy tłuszcze nie mają w swojej strukturze naładowanych fragmentów i praktycznie nie rozpuszczają się w wodzie. Brud jest mieszaniną składników, np. potu, białek, tłuszczów lub sadzy. Ma charakter hydrofobowy, dlatego sama woda nie wystarcza do pozbycia się brudu. Aby go usunąć, potrzebne jest mydło.

Film dostępny pod adresem /preview/resource/R51ag3bgCHDfI
Film ukazuje, w jaki sposób mydło ułatwia usuwanie brudu podczas mycia.
Mieszanie substancji polarnej i niepolarnej.
Problem badawczy:
Czy dodanie mydła do mieszaniny wody i oleju wpływa na proces ich mieszania się?
Hipoteza:
Dodanie mydła do wody i oleju umożliwi zmieszanie się tych dwóch niemieszających się cieczy – nastąpi rozproszenie cząstek oleju w wodzie.
Co było potrzebne:
roztwór mydła;
olej;
woda;
dwie probówki.
Przebieg doświadczenia:
Do probówki z wodą dodano niewielką ilość oleju i wstrząśnięto jej zawartością. Do drugiej probówki, w której znajdował się roztwór mydła, dodano podobną ilość oleju, a następnie zawartością probówki wstrząśnięto i porównano efekty obu prób.
Obserwacje:
W pierwszej probówce olej i woda nie uległy zmieszaniu. Po wstrząśnięciu na chwilę powstała emulsja, która rozdzieliła się na dwie warstwy. W drugiej probówce powstała mieszanina jednorodna, nie obserwuje się rozdziału na dwie warstwy, jak to miało miejsce w pierwszej probówce.
Wnioski:
Mydło umożliwia zmieszanie substancji polarnej i niepolarnej.
Zapisz, jaką inną substancję można byłoby wykorzystać zamiast mydła, w celu zmieszania substancji polarnej i niepolarnej.
Zdarza się, że podczas mycia tworzy się w wodzie kłaczkowaty osad. Dzieje się tak, gdy woda używana do mycia jest twarda.
Woda twardaWoda twarda zawiera znaczne ilości rozpuszczonych w niej soli wapnia i magnezu.
Podczas mycia i prania w twardej wodzie z użyciem mydła tworzą się nierozpuszczalne sole wapnia i magnezu, które tworzą osad. Użyte mydło nie pieni się, a przecież wytwarzanie piany jest niezbędnym warunkiem usunięcia brudu.
Przykładowe równania zachodzących reakcji można zapisać następująco:

Rozróżniamy dwa rodzaje twardości wody – twardość wodorowęglanową (przemijającą), spowodowaną obecnością między innymi wodorowęglanów wapnia i magnezu, oraz twardość trwałą (nieprzemijającą), której przyczyną są rozpuszczone w wodzie inne sole wapnia i magnezu (chlorki, azotany(
Gdy woda zawierająca wodorowęglany wapnia i magnezu zostanie zagotowana, zachodzą reakcje, w wyniku których węglan wapnia, węglan magnezu oraz wodorotlenek magnezu osadzają się na ściankach naczynia (np. czajnika) w postaci ciała stałego, zwanego potocznie kamieniem kotłowym. Proces usuwania twardości przemijającej, wynikającej z obecności w wodzie jonów wapnia i magnezu, opisuje równanie:
Jony wapnia i magnezu, będące przyczyną twardości wody, zostają usunięte. Uzyskuje się efekt zmiękczania wody. Właśnie dlatego twardość wodorowęglanową nazywa się twardością przemijającą.
Twardość wody jest najczęściej wyrażana w stopniach niemieckich lub francuskich.
Stopień niemiecki
Stopień francuski
Twardość wody | |
|---|---|
woda bardzo miękka | |
woda miękka | |
woda średnio twarda | |
woda dość twarda | |
woda twarda | |
Powyżej | woda bardzo twarda |
Inną skalą oznaczania twardości wody są stopnie angielskie lub Clarka, oznaczane jako (
Producenci pralek i zmywarek często przestrzegają przed działaniem twardej wody na te urządzenia i zalecają – w celu ich ochrony przed osadzaniem się kamienia – stosowanie preparatów zmiękczających wodę. Informacja, czy woda, którą czerpiemy z kranu jest twarda, ważna jest także dla hodowców rybek akwariowych i użytkowników filtrów do wody. Obecnie w sprzedaży dostępne są produkty służące do przeprowadzenia badania twardości wody w warunkach domowych.
Obejrzyj poniższe ilustracje. Kliknij strzałkę w prawo, aby zobaczyć następną grafikę.
Podsumowanie
Mydła otrzymuje się w reakcjach kwasów tłuszczowych z wodorotlenkami metali oraz – na skalę przemysłową – w procesie zmydlania tłuszczów.
Mydła skutecznie usuwają brud, ponieważ są substancjami powierzchniowo czynnymi. Ich specyficzna budowa – obecność hydrofilowej głowy oraz hydrofobowego ogona – wpływa na zmniejszenie napięcia powierzchniowego wody i ułatwia usuwanie brudu.
Korzystając ze swojej wiedzy oraz dostępnych źródeł informacji, zapisz równania reakcji węglanu sodu z rozpuszczonymi w twardej wodzie chlorkiem wapnia oraz siarczanem(
Poniżej zapisano równania reakcji węglanu sodu z rozpuszczonymi w twardej wodzie chlorkiem wapnia oraz siarczanem(
Problem badawczy:
Jaki wpływ mają mydła na napięcie powierzchniowe wody?
Co było potrzebne:
woda;
dwie miseczki;
mydło;
dwie małe spinacze biurowe (lub igły).
Przebieg doświadczenia:
Do miseczki nalano wody. Do drugiej miseczki nalano wody i rozpuszczono w niej trochę mydła. W obu miseczkach na powierzchni wody położono spinacze (płasko). Spinacz utrzymał się na powierzchni wody w misce, w której nie dodano mydła. W misce z mydlinami spinacz zatonął.
Zapisz notatkę, w której na podstawie doświadczenia udzielisz odpowiedzi na postawione pytanie.
Zapisz, jaki wniosek można wyciągnąć z powyższego doświadczenia.
Słownik
sole wyższych kwasów karboksylowych (kwasów tłuszczowych)
zjawisko spowodowane siłami spójności występującymi w cieczach; dzięki niemu powierzchnia cieczy zachowuje się jak sprężysta błona;
substancja, która powoduje zmniejszenie napięcia powierzchniowego wody
woda, która zawiera znaczne ilość soli wapnia i magnezu (wodorowęglanów, chlorków, siarczanów(
proces otrzymywania mydła w reakcji tłuszczu z zasadą sodową lub potasową; drugim produktem tej reakcji jest glicerol
Ćwiczenia
Uzupełnij notatkę dotyczącą różnych rodzajów mydeł.
powierzchniowo czynnymi, kationu metalu, barwnymi, lotne, napięcia powierzchniowego, rozpuszczalne, kwasu stearynowego, trudnorozpuszczalne, anionu metalu, sił magnetycznych, o niezwykłej trwałości, kwasu masłowego, w kostkach, kwasu palmitynowego, twardymi
Mydła są solami wyższych kwasów tłuszczowych, np. ..................................................... Rozpuszczalność w wodzie i twardość mydła zależą od rodzaju .................................................... wchodzącego w jego skład. Mydła potasowe i sodowe są .................................................... w wodzie. Wykorzystuje się je do mycia i prania, ponieważ są związkami ..................................................... Ich działanie polega na zmniejszaniu ..................................................... Mydła sodowe są mydłami ..................................................... Produkuje się z nich najbardziej popularne mydła ..................................................... Mydła potasowe i sodowe reagują z jonami
Mydło jest substancją powierzchniowo czynną. We wzorze palmitynianu sodu, wskaż część hydrofobową i część hydrofilową. Jak zachowuje się mydło w wodzie? Uzupełnij zdania.

kwas oktadekanowy
tłuszcz
Uzupełnij proponowane zapisy procesów otrzymywania mydeł.
wodorotlenek potasu, stearynian sodu, kwas masłowy, wodorotlenek sodu, palmitynian potasu, woda, glicerol, parafina, wodorotlenek magnezu
1. Reakcja kwasu stearynowego wodorotlenkiem potasu
kwas stearynowy + ........................................ → stearynian potasu + ........................................
2. Schemat reakcji zmydlania tłuszczów
tłuszcz + ........................................ → mydło sodowe + ........................................
Uczeń przeprowadził doświadczenie, którego celem było badanie zachowania mydła w roztworach wodnych różnych substancji.
Na podstawie schematu ilustrującego przebieg eksperymentu, ustal, w której probówce/probówkach uczeń zaobserwował zanikanie piany.

Uczeń przeprowadził doświadczenie, którego celem było badanie zachowania mydła w roztworach wodnych różnych substancji:
Każdą z substancji uczeń umieścił w osobnych probówkach, a następnie do każdej z nich dodał roztwór mydła (pianę). Zaznacz, w której probówce/probówkach uczeń zaobserwował zanikanie piany.
Przeczytaj poniższy tekst, a następnie wykonaj polecenie. Skorzystaj ze słownika zamieszczonego pod zadaniem.
Micelles are spherical clusters of hydrocarbon molecules that act as emulsifying agents. A typical micelle in aqueous solution forms an aggregate with the hydrophilic „head” regions in contact with surrounding solvent, and the hydrophobic tail regions in the micelle centre. When surfactants are present above the critical micelle concentration, they can act as emulsifiers that will allow a compound that is normally insoluble to dissolve. The most common example of this phenomenon is detergents, which clean poorly soluble hydrophobic materials such as oils and waxes that cannot be removed by water alone.
Połącz w pary cyfrę na schemacie z odpowiednim podpisem.

Przeczytaj poniższy tekst, a następnie wykonaj polecenie. Skorzystaj ze słownika zamieszczonego pod zadaniem.
Micelles are spherical clusters of hydrocarbon molecules that act as emulsifying agents. A typical micelle in aqueous solution forms an aggregate with the hydrophilic „head” regions in contact with surrounding solvent, and the hydrophobic tail regions in the micelle centre. When surfactants are present above the critical micelle concentration, they can act as emulsifiers that will allow a compound that is normally insoluble to dissolve. The most common example of this phenomenon is detergents, which clean poorly soluble hydrophobic materials such as oils and waxes that cannot be removed by water alone.
Wymień elementy, z których składają się micele.
Bibliografia
McMurry J., Chemia organiczna, Warszawa 2000.