Niemetale
Substancje tworzące skorupę ziemską oraz występujące w powietrzu atmosferycznym są zbudowane z 88 pierwiastków chemicznych. Czy te same pierwiastki są składnikami ciała człowieka? Okazuje się, że około 96% masy naszego organizmu stanowią zaledwie cztery pierwiastki – niemetale: tlen, węgiel, wodór i azot. Są one składnikami wody, białek, tłuszczów, cukrów i soli. Czym są niemetale? Jakie są ich właściwości? Czy niemetale różnią się od metali?
jakie właściwości ma materia w różnych stanach skupienia;
co to są symbole pierwiastków chemicznych i jak się nimi posługiwać;
w jaki sposób określić i rozróżnić właściwości fizyczne od chemicznych;
według jakich kryteriów klasyfikuje się mieszaniny;
jakie zasady bezpieczeństwa należy zachować w szkolnej pracowni chemicznej.
jakie niemetale znajdują się w układzie okresowym pierwiastków;
jakie jest zastosowanie niemetali w życiu codziennym;
planować doświadczenia pozwalające zbadać właściwości niemetali;
odróżniać metale od niemetali na podstawie właściwości;
planować doświadczenia pozwalające porównać właściwości metali i niemetali;
przestrzegania zasad bezpieczeństwa podczas wykonywania eksperymentów chemicznych.
1. Z jakich pierwiastków (niemetali) jest zbudowany organizm człowieka?
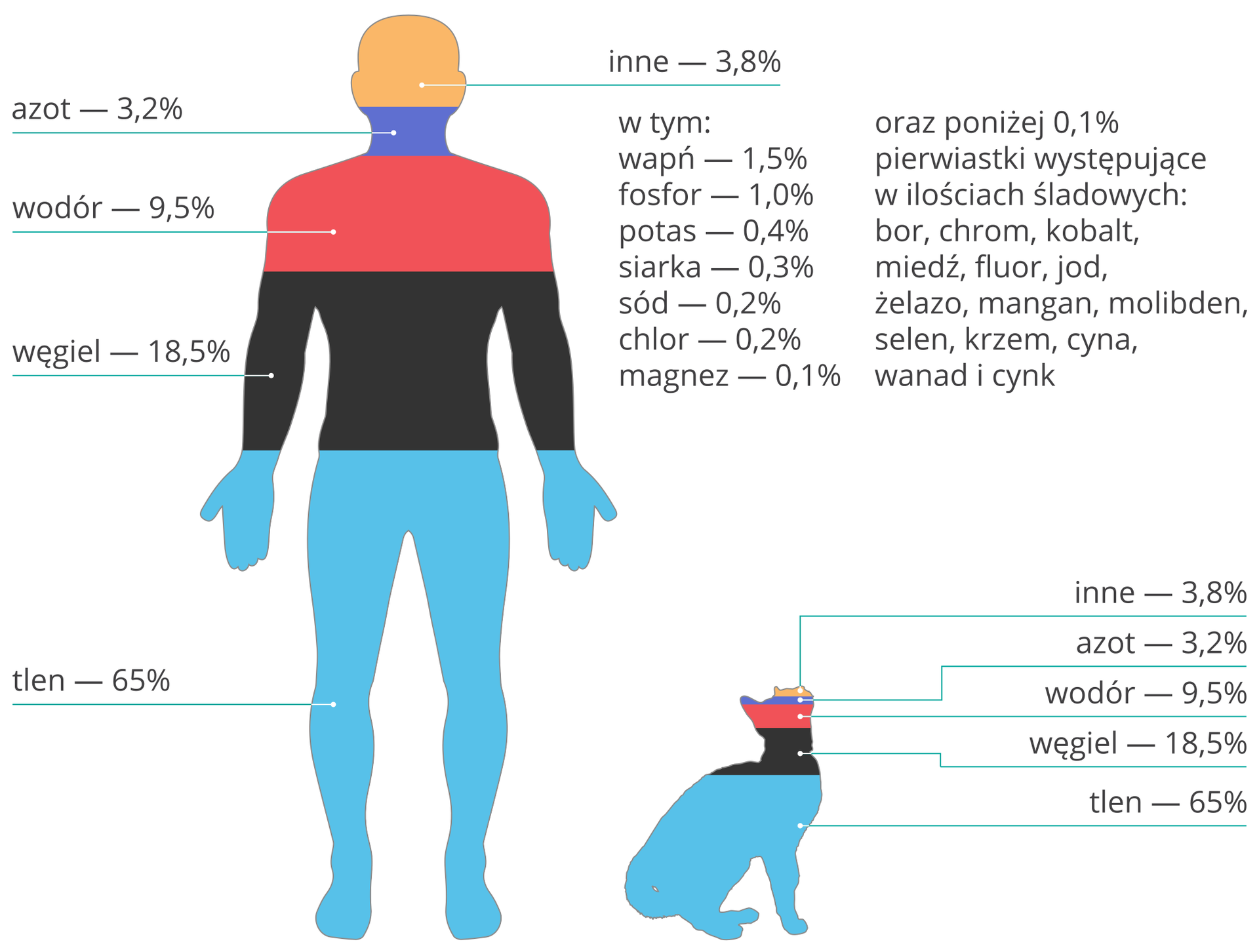
Organizmy żywe (w tym ciało ludzkie) są zbudowane w około 96% z czterech pierwiastków powszechnie występujących we Wszechświecie. Ich średnia masa u osoby ważącej 50 kg wynosi:
32,5 kg tlenu,
9,25 kg węgla,
4,75 kg wodoru,
1,6 kg azotu.
Średnia procentowa zawartość pierwiastków i wybrane funkcje, jakie pełnią w organizmie:
tlen (65%) – m.in. niezbędny do funkcjonowania mózgu, procesów oddychania i spalania w komórkach;
węgiel (18%) – budulec wszystkich żywych komórek;
wodór (10%) – wraz z tlenem tworzy wodę, która stanowi 60–80% masy organizmu, jest składnikiem m.in. białek, cukrów, tłuszczów;
azot (3%) – niezbędny w procesie budowy komórek, składnik białek;
fosfor (1%) – podobnie jak wapń (1,5%) jest składnikiem związków, z których zbudowane są zęby i kości;
w ilościach śladowych:
siarka – składnik paznokci i włosów;
jod – niezbędny do produkcji hormonów tarczycy.
Pierwiastek | Symbol | Zawartość w organizmie [%] |
tlen | 65,0 | |
węgiel | 18,0 | |
wodór | 10,0 | |
azot | 3,0 | |
wapń | 1,5 | |
fosfor | 1,0 | |
potas | 0,4 | |
siarka | 0,3 | |
sód | 0,2 | |
magnez | 0,1 |
2. Jakie jest położenie niemetali w układzie okresowym?
Obecnie znanych jest 118 pierwiastków chemicznych, spośród których oficjalnie uznano 114. Lewą stronę układu okresowego zajmują metale, natomiast prawą – niemetaleniemetale. Pierwiastki te tworzą ukośną granicę, z wyjątkiem wodoru usytuowanego w lewym górnym rogu. Podział na metale i niemetale był stosowany już w czasach starożytnych. Większość pierwiastków chemicznych stanowią metale, a tylko 22 z nich to niemetale. Najbardziej znane to: siarka, węgiel, tlen, azot, wodór, fosfor, jod i chlor. Niektóre pierwiastki mogą przyjmować różne postaci, np. węgiel, który występuje w kilku odmianach m.in. jako szaroczarny grafitu i bezbarwny diament.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D1Ai6WKHV
2.1. W jakim stanie skupienia występują niemetale?
Wyszukaj w układzie okresowym wymienione niżej pierwiastki chemiczne, zapoznaj się z ich charakterystyką i zapisz w zeszycie informacje na temat ich stanu skupienia.
tlen
węgiel
siarka
azot
brom
chlor
Wypisz z układu okresowego nazwy niemetali o:
najniższej i najwyższej temperaturze wrzenia,
największej i najmniejszej gęstości.
Odmiany alotropowe węgla
Niektóre niemetale występują w przyrodzie w kilku odmianach różniących się między sobą budową wewnętrzną. Odmiany takie nazywamy alotropowymi. W odmianach alotropowych występują również niektóre metale, np. cyna (cyna biała i cyna szara).
Znane są odmiany alotropowe węgla (np. diament, grafit, fulereny, grafen), siarki (rombowa i jednoskośna) i fosforu (biały, czerwony, fioletowy i czarny) oraz tlenu, różniące się liczbą atomów w cząsteczce (tlen , ozon , tlen czerwony ).

*Więcej na temat odmian alotropowych

Film dostępny na portalu epodreczniki.pl
Film rozpoczyna prezentacja czterech odmian alotropowych węgla przypominająca tę zamieszczoną na zdjęciu powyżej. Następuje zmiana ujęcia na obrazek przedstawiający grafit i schemat jego struktury cząsteczkowej. Zmiana ujęcia na zdjęcie skrawka grafenu i schematu jego płaskiej struktury cząsteczkowej. Zmiana ujęcia na zbliżenie sterty czarnych, połyskujących kryształów fulerenu. Obok prezentowany jest schemat kulistej cząsteczki składającej się z sześćdziesięciu atomów. Zmiana ujęcia na zdjęcie żółtawego diamentu i widok jego schematu budowy cząsteczkowej. Następuje zmiana ujęcia na prezentację barwnych odmian diamentów. Komentarzowi lektora towarzyszą pojawienia się kamieni o kolejno wymienianych barwach trzymanych w szczypcach. Zmiana ujęcia na zdjęcie kopalni odkrywkowej diamentów mającą postać ogromnej, lejkowatej dziury w ziemi, wzdłuż krawędzi której ciągną się drogi prowadzące w dół. Dziura jest naprawdę wielka, na jej krawędzi w oddali znajdują się maleńkie zabudowania miasteczka, osiedla lub zakładu. Następuje zmiana ujęcia na fotografię przedstawiającą maszyny wydobywcze, na pierwszym planie wielką kołową, nieco dalej mniejszą gąsienicową, a w tle stacjonarny dźwig. Zmiana ujęcia na zdjęcie dwóch mijających się ciężarówek jadących pochyłą drogą wzdłuż zbocza kopalni. W Pod górę jedzie pojazd załadowany wydobytymi skałami, a w dół zjeżdża taki sam pojazd pusty. Zmiana ujęcia na serię fotografii przedstawiających kolejne etapy obróbki urobku: mielenie, płukanie i sortowanie na pojedyncze ziarna na taśmociągu z rowkami. Zmiana ujęcia na zdjęcie mężczyzny wypłukującego diamenty w tradycyjny sposób z żółtej gliny. Zmiana na zdjęcie skały z widocznym w niej diamentem. Przy części skalnej znajduje się podpis 250 ton, a przy zatopionym w niej błyszczącym kamieniu - 0,2 grama. Zmiana ujęcia na rysunek mapy świata z zaznaczonymi złożami diamentów na wszystkich kontynentach. W miarę omawiania przez lektora ciemniejszym kolorem wyróżniane są określone państwa.

Film dostępny na portalu epodreczniki.pl
Zdjęcia prezentujące: siarkę, kompleks wulkanicznego Ijen w Indonezji, mapa złóż siarki w Polsce
3. Jakie właściwości mają niemetale?
Niemetale, w przeciwieństwie do metali, różnią się właściwościami. W warunkach normalnych występują w trzech stanach skupienia.
Najczęściej są gazami, np.:
tlen, azot i wodór (bezbarwnymi i bezwonnymi);
chlor i fluor (o zielonożółtej barwie i o ostrym zapachu);
hel, neon, argon (bezbarwnymi i bezwonnymi gazami szlachetnymi).
Rzadziej są ciałami stałymi, np.:
węgiel, siarka, fosfor, krzem, jod.
W postaci cieczy występuje jedynie brom (ciemnobrunatny o drażniącym zapachu).
Niemetale mają różne barwy. Te, które są ciałami stałymi, nie mają charakterystycznego połysku (z wyjątkiem jodu) i są kruche. Niemetale możemy opisywać, badając ich właściwości fizyczne i chemiczne oraz odczytując dane z układu okresowego pierwiastków lub tablic chemicznych.
Czy niemetale mają takie same właściwości?
Wybierz jedną z przedstawionych hipotez, a następnie zweryfikuj ją.
Niemetale różnią się właściwościami.
Niemetale mają podobne właściwości.
siarka,
węgiel w postaci grafitu,
fosfor czerwony,
chlor,
*fosfor biały,
*brom,
pęseta,
bibuła,
młotek,
okulary ochronne.
Określ stan skupienia i barwę substancji.
Połóż na bibule węgiel w postaci grafitu oraz kilka kryształów siarki, a następnie uderz w nie młotkiem.
Siarka to substancja krystaliczna o żółtej barwie. Jest krucha. Węgiel w postaci grafitu to kruche ciało stałe o ciemnoszarej barwie i metalicznym połysku. Fosfor czerwony to proszek ociemnoczerwonej barwie. *Fosfor biały stanowi miękką, białą masę. Ze względu na łatwość samozapłonu przechowuje się go w wodzie. Z tych samych powodów kroi się go również pod wodą. Brom to ciecz o barwie ciemnobrunatnej*. Chlor to gaz o barwie zielonożółtej.
Niemetale w temperaturze pokojowej występują w trzech stanach skupienia. Mają różne barwy.
Czy niemetale przewodzą prąd elektryczny?
Wybierz jedną z przedstawionych hipotez, a następnie zweryfikuj ją.
Niemetale przewodzą prąd elektryczny.
Niemetale nie przewodzą prądu elektrycznego.
bateria,
żarówka,
przewody elektryczne,
próbki niemetali, np. siarka, węgiel w postaci gafitu i diamentu.
W odpowiednio zmontowany obwód wstaw próbkę badanego niemetalu.
Obserwuj, co się dzieje z żarówką.
Zamknięcie obwodu elektrycznego prętem grafitowym powoduje świecenie żarówki. W przypadku siarki i diamentu żarówka się nie świeci. Niemetale nie przewodzą prądu elektrycznego.
Wyjątkami są grafit, grafen oraz fosfor czarny.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D1Ai6WKHV
Badane metale (żelazo, miedź i złoto) przewodzą prąd elektryczny (żarówka świeci się). Niemetale: węgiel w postaci grafitu oraz fosfor czarny przewodzą prąd elektryczny, siarka, fosfor czerwony i diament nie przewodzą prądu (żarówka nie świeci się).
Czy niemetale przewodzą ciepło?
Wybierz jedną z przedstawionych hipotez, a następnie zweryfikuj ją.
Niemetale przewodzą ciepło.
Niemetale nie przewodzą ciepła.
statyw laboratoryjny z łapą,
palnik,
termometr cyfrowy z sondą,
okulary ochronne,
próbki niemetali: siarki, węgla (grafitu), *diamentu.
Zmierz temperaturę próbki, np. pręta grafitowego, kryształu siarki lub diamentu za pomocą sondy termometru cyfrowego.
Ogrzewaj palnikiem jeden z końców pręta z grafitu, kryształu siarki lub diamentu przez około minutę, a następnie zmierz temperaturę na przeciwległym końcu.
R16XzKOw4c5sY1  Źródło: Tomorrow Sp.z o.o., licencja: CC BY 3.0.
Źródło: Tomorrow Sp.z o.o., licencja: CC BY 3.0.
Ogrzewanie jednego końca grafitowego pręta powoduje wzrost temperatury przeciwległego końca. Większość niemetali nie przewodzi ciepła. Wyjątki to grafit i diament, które są dobrymi przewodnikami ciepła.

Zasób interaktywny dostępny pod adresem https://zpe.gov.pl/a/D1Ai6WKHV
Niemetal (symbol) | Barwa | Stan skupienia | Połysk | Gęstość [kg/m³] | Temperatura topnienia [°C] | Temperatura wrzenia [°C] |
węgiel () (grafit) | szaroczarna | ciało stałe | brak | 2300 | 4000 (sublimacja) | – |
węgiel () (diament) | bezbarwna | ciało stałe | brak | 3500 | 4800 (sublimacja) | – |
siarka () | żółta | ciało stałe | brak | 2070 | 119 | 445 |
fosfor () (biały) | biała | ciało stałe | brak | 1820 | 44 | 280 |
krzem () | ciemnoszara | ciało stałe | metaliczny | 2330 | 1417 | 3280 |
chlor () | zielonożółta | gaz | brak | 3,2 | –101 | –34 |
brom () | ciemnobrunatna | ciecz | brak | 3119 | –7 | 59,5 |
jod () | szaroczarna | ciało stałe | metaliczny | 4940 | 114 | 185 |

Film dostępny na portalu epodreczniki.pl
Prezentowany jest pokaz slajdów przedstawiający poszczególne niemetale omawiane przez lektora. Kolejno pojawia się: diament, grafit, siarka, fosfor, jod, brom, chlor i fuor.
Grafen – materiał przyszłości
Opis teoretyczny grafenu powstał już w 1947 roku, zaś w 2010 roku przyznano za jego odkrycie Nagrodę Nobla w dziedzinie fizyki. Grafen to najbardziej wytrzymały materiał w przyrodzie – sto razy mocniejszy niż stal. Doskonale przewodzi ciepło i prąd elektryczny. Ma małą gęstość, jest cienki (złożony z jednej warstwy atomów węgla) i przezroczysty. Jednym gramem grafenu można pokryć powierzchnię kilku boisk futbolowych.
W Polsce badania nad otrzymaniem wysokiej jakości grafenu trwały od 2006 roku, ale dopiero w roku 2013 osiągnięto sukces komercyjny i rozpoczęto produkcję.
Gdyby udało się wytwarzać z grafenu przedmioty codziennego użytku, zrewolucjonizowałaby one nasze życie bardziej niż krzem. Mogłyby powstać rozciągliwe i przezroczyste tablety dające się zwinąć w rulonik i włożyć do kieszeni, procesory kilkaset razy szybsze od krzemowych albo sztuczne ścięgna do wszczepiania w stawy.


Film dostępny na portalu epodreczniki.pl
Zdjęcia przedstawiające: odkrywców grafenu, sposób odkrycia grafenu, strukturę grafenu, wizualizację wytrzymałości grafenu
4. Gdzie stosuje się niemetale?
Niemetale, dzięki różnorodnym właściwościom, znalazły wiele zastosowań. Są używane m.in. do produkcji nawozów sztucznych, barwników, leków, środków odkażających, materiałów wybuchowych, sztucznych ogni, a należące do nich gazy szlachetne – m.in. w technice oświetleniowej, do wypełniania neonów.
Niemetale, podobnie jak metale, odgrywają znaczącą rolę we właściwym funkcjonowaniu organizmu człowieka, np. fluor bierze udział w procesach tworzenia kości i zębów oraz zapobiega próchnicy.
Pierwiastek | Zastosowanie |
wodór | paliwo rakietowe (mieszanina ciekłego wodoru z ciekłym tlenem) |
paliwo w ogniwach paliwowych do samochodów | |
stosowany do utwardzania tłuszczów pochodzenia roślinnego | |
hel | ciekły – chłodziwo w reaktorach atomowych |
składnik mieszaniny, którą oddychają nurkowie głębinowi | |
gaz do wypełniania balonów, lamp jarzeniowych (podobnie jak inne gazy szlachetne) i niektórych termometrów | |
węgiel | diament – po oszlifowaniu ceniony kamień jubilerski (brylant), nasadki świdrów górniczych, składnik materiałów polerskich |
grafit – materiał do wyrobu elektrod, wkładów do ołówków, ognioodpornych tygli, składnik smarów | |
węgiel C‑14 – stosowany do datowania wieku przedmiotów w badaniach archeologicznych, pozwala ustalić wiek zabytku pochodzenia organicznego od 200 do 30 000 lat z dokładnością do 30 lat | |
azot | ciekły – chłodziwo do przechowywania materiału biologicznego, np. krwi, w medycynie do zamrażania kurzajek pochodzenia wirusowego |
stosowany jako gaz do pakowania produktów spożywczych | |
związki azotu – nawozy sztuczne, materiały wybuchowe, leki | |
tlen | proces uzdatniania wody (ozonowanie) |
butle z tlenem wykorzystywane m.in. w przemyśle (uzyskiwanie wysokich temperatur do cięcia i spawania trudno topliwych metali w procesach spalania np. acetylenu) | |
w medycynie | |
składnik paliwa pojazdów kosmicznych | |
fluor | związki fluoru – składnik pasty do zębów |
związki fluoru – teflon: patelnie, tostery, narty, protezy stawów | |
związki fluoru – odzież i buty | |
krzem | układy scalone w urządzeniach elektronicznych, m.in. komputerach, odtwarzaczach MP3 |
fotoogniwa w bateriach słonecznych | |
składnik stali transformatorowej | |
fosfor | draska na pudełkach zapałek |
dodatek w stopach – podwyższa ich twardość | |
związek fosforu – składnik napojów typu cola | |
siarka | proces wulkanizacji (dodawana do kauczuków w procesie produkcji gumy) |
związki siarki – składnik leków | |
związki siarki – składnik nawozów, barwników | |
chlor | związki chloru – środki dezynfekujące i wybielające, np. dezynfekcja wody w basenie |
związek chloru – składnik wykładzin PCW | |
związek chloru – fosgen gaz bojowy | |
związeki chloru – stosowane w fotografii | |
brom | związki bromu – składnik leków, barwników |
związki bromu – składnik niektórych tworzyw sztucznych | |
związki bromu – stosowane w fotografii | |
jod | alkoholowy roztwór jodu (jodyna) – środek dezynfekujący w medycynie |
leczenie i profilaktyka chorób tarczycy | |
jod i związki – stosowane w produkcji barwników oraz fotografii |
Gazy szlachetne
Gazy szlachetne: hel, neon, argon i ksenon występują w niewielkich ilościach w powietrzu. Wykorzystywane są m.in. do napełniania żarówek i neonów, w których podczas przepływu prądu po podgrzaniu świecą charakterystycznymi barwami.

Gazy szlachetne a Deklaracja niepodległości USA
Gazy szlachetne znajdują także zastosowanie do przechowywania i eksponowania wartościowych, zabytkowych dokumentów – zapobiegają niszczeniu materiałów pod wpływem składników powietrza, głównie tlenu. Oryginał konstytucji i Deklaracji niepodległości USA przechowuje się w gablocie wypełnionej helem.

Podsumowanie
Pierwiastki chemiczne dzielimy na metale i niemetale.
Niemetale tworzą prawą część układu okresowego, wyjątek stanowi wodór, który znajduje się w I grupie.
Niemetale:
występują we wszystkich stanach skupienia,
mają różne barwy,
mogą mieć charakterystyczne zapachy,
mają różny zakres temperatur wrzenia i topnienia,
zazwyczaj są złymi przewodnikami prądu elektrycznego oraz złymi przewodnikami ciepła. Węgiel w postaci grafitu i grafenu oraz fosfor czarny, mimo iż są niemetalami, przewodzą prąd elektryczny oraz ciepło. Diament przewodzi tylko ciepło,
w większości stanowią gazy w temperaturze pokojowej.
Przedstaw w formie tabeli porównanie właściwości metali i niemetali.
Sporządź notatkę na temat zastosowania niemetali w najbliższym otoczeniu.
Zdaj relację z wywiadu, np. z lekarzem lub dietetykiem, na temat niedoboru niemetali w organizmie.
Opisz zastosowania niemetali i zilustruj je, wykonując trzy zdjęcia.
Słowniczek
pierwiastki chemiczne, które w odróżnieniu od metali źle przewodzą prąd elektryczny (z wyjątkiem grafitu, grafenu i fosforu czarnego) i ciepło (z wyjątkiem diamentu, grafitu i fosforu czarnego); w stanie stałym są na ogół kruche, bez metalicznego połysku (z wyjątkiem jodu, krzemu, grafitu)
Zadania
Uzupełnij puste miejsca, wybierając brakujące elementy z listy w taki sposób, by całość tworzyła poprawne zdania.
srebrzystoszarą, siarki, siarki, srebrzystobiałą, diamentu, różną, krzemu, tlen, wodór, diamentu, jodu, jodu, grafitu, azot, taką samą, węgiel
Niemetale tworzą prawą części układu okresowego, wyjątek stanowi .................................. , który znajduje się w I grupie. Charakterystyka niemetali:
− w temperaturze pokojowej występują we wszystkich stanach skupienia,
– mają .................................. barwę,
– nie przewodzą ciepła (z wyjątkiem fosforu czarnego, grafitu i .................................. ),
– nie przewodzą prądu (z wyjątkiem .................................. i fosforu czarnego).
Określ cechy wymienionych niemetali, wybierając je z rozwijanej listy.
srebrzystoróżowa (łososiowa), S, srebrzystobiała, S, Cl, szaroczarna, ciemnobrunatna, granatowa, żółta, biała, szaroczarna, szaroczarna, pomarańczowożółta, żółta, granatowa, szaroczarna, Cl, szaroczarna, ciekły, ciekły, srebrzystobiała, pomarańczowożółta, Br, I, stały, granatowa, brązowa, srebrzystoróżowa (łososiowa), I, gazowy, Cl, granatowa, pomarańczowożółta, C, srebrzystoróżowa (łososiowa), S, srebrzystoróżowa (łososiowa), C, I, biała, srebrzystobiała, żółta, stały, brązowa, Cl, I, Br, pomarańczowożółta, ciekły, C, gazowy, pomarańczowożółta, Br, żółta, zielonożółta, srebrzystobiała, granatowa, Br, brązowa, I, C, biała, S, C, ciekły, srebrzystoróżowa (łososiowa), brązowa, Br, ciekły, S, gazowy, brązowa, żółta, stały, stały, stały, gazowy, gazowy, Cl, srebrzystobiała
węgiel (grafit) – stan skupienia .............................................................., barwa .............................................................., symbol ..............................................................
brom – stan skupienia .............................................................., barwa .............................................................., symbol ..............................................................
chlor – stan skupienia .............................................................., barwa .............................................................., symbol ..............................................................
siarka – stan skupienia .............................................................., barwa .............................................................., symbol ..............................................................
jod – stan skupienia .............................................................., barwa .............................................................., symbol ..............................................................
Zaznacz odpowiednie pola obok podanych zdań, wskazując, czy są one prawdziwe, czy fałszywe.
| Prawda | Fałsz | |
| Brom to jedyny niemetal, który w temperaturze pokojowej występuje w stanie ciekłym. | □ | □ |
| Do niemetali zaliczamy węgiel i siarkę. | □ | □ |
| Niemetale występują w warunkach normalnych tylko w dwóch stanach skupienia – jako ciała stałe lub gazy. | □ | □ |
| Niemetale nie przewodzą prądu elektrycznego. | □ | □ |











