Przeczytaj
Oksydacyjna deaminacja aminokwasów
DeaminacjaDeaminacja to reakcja chemiczna, która polega na odłączeniu od danego aminokwasu, najczęściej glutamininanu, grupy aminowej.
Podczas reakcji utleniania glutaminianu, nazywanej oksydacyjną deaminacją, grupa aminowa zostaje usunięta i zastąpiona grupą ketonową. Ta reakcja chemiczna jest katalizowana przez enzym – dehydrogenazędehydrogenazę glutaminianową. W reakcji deaminacji glutaminianu powstają amoniakamoniak (NHIndeks dolny 33) oraz ketokwas (alfa‑ketoglutaran z grupą ketonową –C=O), który podlega dalszym przemianom. Dehydrogenaza glutaminianowa może współdziałać ze związkami takimi jak NADIndeks górny ++NADIndeks górny ++ i NADPIndeks górny ++NADPIndeks górny ++, które są przenośnikami elektronów i protonów (HIndeks górny ++).
Uważa się, że deaminację aminokwasów może katalizować także inny enzym – oksydazaoksydaza. Oksydaza glutaminianowa współdziała z FADFAD i FMNFMN, które należą do nukleotydów flawinowych. W trakcie reakcji deaminacji z udziałem oksydazy powstają również ketokwas oraz amoniak, a także zredukowane formy tych nukleotydów, czyli FADHIndeks dolny 22 oraz FMNHIndeks dolny 22. Związki te zdolne są do przekazywania wodoru na tlen, w wyniku czego dochodzi do powstawania nadtlenku wodoru (HIndeks dolny 22OIndeks dolny 22). Jest on następnie rozkładany do tlenu i wody przez enzym – katalazękatalazę – występujący w dużych ilościach w wątrobie.
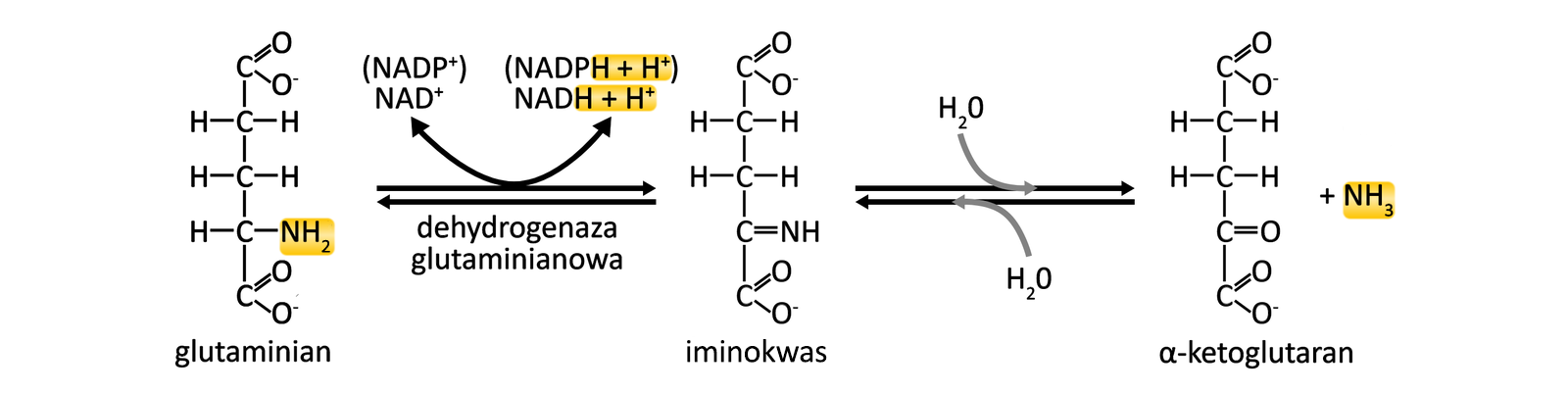
Deaminacja aminokwasów przez dehydratazy
Dehydrogenazy i oksydazy to nie wszystkie enzymy zdolne do przeprowadzania reakcji deaminacji aminokwasów. Enzym dehydratazadehydrataza serynowo‑treoninowa odpowiada za katalizowanie reakcji usuwania grup aminowych z aminokwasów – treoniny oraz seryny. W pierwszej fazie tej reakcji od związku organicznego odłączają się cząsteczki wody (dehydratacja). Następnie zachodzi reakcja główna, czyli odłączenie grupy aminowej w postaci amoniaku.
Szkodliwy dla organizmu amoniak wchodzi do cyklu mocznikowego przeprowadzanego w wątrobie. Ulega przekształceniu w nietoksyczny mocznikmocznik.
Związki pośrednie – ketokwasy
Usunięcie grupy aminowej z aminokwasu rozpoczyna katabolizm tego związku organicznego. Po usunięciu z aminokwasów atomów azotu z pozostałych szkieletów węglowodorowych powstają związki pośrednie, takie jak:
Alfa-ketoglutaran
powstaje w wyniku deaminacji glutaminianu. Jest też produktem przemian katabolicznych histydyny, ornityny i argininy. Ten ketokwas jest związkiem pośrednim w cyklu Krebsa.
Pirogronian
powstaje w wyniku przemian glicyny, alaniny, cysteiny oraz seryny. Ten związek organiczny przekształcany jest w mitochondriach do acetylo-CoA, który wchodzi do cyklu Krebsa.
Szczawiooctan
ketokwas, który powstaje w wyniku przemian aminokwasu asparaginy. Związek ten może wchodzić w reakcje glukoneogenezy – reakcje przekształcania niecukrowych prekursorów w glukozę. Jest również produktem wchodzącym w cykl Krebsa.
Powstawanie amin biogennych
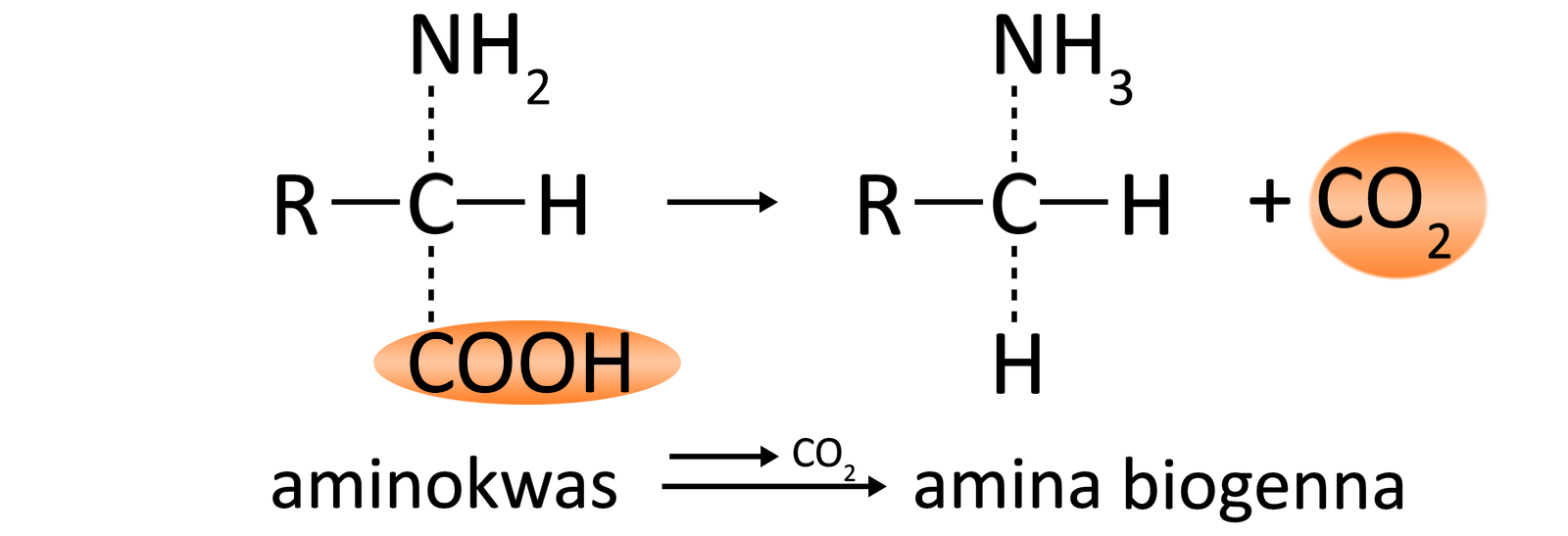
Aminy biogenneAminy biogenne tworzą się w wyniku dekarboksylacji aminokwasów, czyli usunięcia grupy karboksylowej z danego związku. Przykładem aminy biogennej jest histamina powstająca na drodze dekarboksylacji aminokwasu histydyny. Jest to związek biologicznie czynny, obniżający ciśnienie tętnicze, zwiększający przepuszczalność naczyń krwionośnych, a także biorący udział w reakcji alergicznej i stanie zapalnym. Inne aminy biogenne to przede wszystkim:
Serotonina
hormon tkankowy, produkt przemian aminokwasu tryptofanu. Pełni funkcję przekaźnika w ośrodkowym układzie nerwowym, reguluje sen, apetyt, temperaturę ciała i ciśnienie krwi. Występuje również w dużych ilościach w płytkach krwi (trombocytach).
Kwas gamma-aminomasłowy
w skrótcie GABA – to neuroprzekaźnik hamujący, który powstaje w wyniku dekarboksylacji kwasu glutaminowego. Reguluje przepływ jonów chlorkowych.
Etanoloamina
powstaje w wyniku dekarboksylacji aminokwasu seryny i wchodzi w skład glicerofosfolipidów. Wspomaga prawidłową pracę układu nerwowego.
Słownik
pierwszorzędowe aminy powstające we wszystkich organizmach w wyniku dekarboksylacji aminokwasów zasadowych (ornityny i lizyny)
NHIndeks dolny 33, związek nieorganiczny, bezbarwny gaz o charakterystycznym zapachu
cykl kwasu cytrynowego; kołowy, wieloetapowy ciąg reakcji enzymatycznych, katalizowanych głównie przez oksydoreduktazy. Przebiega w mitochondriach u organizmów eukariotycznych i w cytoplazmie u organizmów prokariotycznych. U większości organizmów stanowi podstawę oddychania tlenowego. Opisany w 1937 r. przez Hansa A. Krebsa
reakcja chemiczna eliminacji grupy aminowej (–NHIndeks dolny 22) z zasad azotowych i aminokwasów, najczęściej z wydzieleniem amoniaku
enzym katalizujący reakcję dehydratacji, inaczej odwodnienienia, w której jednym z produktów jest woda
grupa enzymów zdolna do odszczepienia atomów wodoru od związków organicznych
dinukleotyd flawinoadeninowy, grupa prostetyczna flawoprotein złożona z kwasu adenozynomonofosforowego i nukleotydu flawinowego
mononukleotyd flawinowy, koenzym flawinowy – ester ryboflawiny i kwasu fosforowego
gr. genesis – powstawanie, zachodzący w wątrobie i nerkach proces wytwarzania glukozy z substancji nie będących sacharydami
potoczna nazwa enzymów z klasy oksydoreduktaz, posiadających zdolność przyspieszania rozpadu nadtlenku wodoru według reakcji: 2HIndeks dolny 22OIndeks dolny 22 → 2HIndeks dolny 22O + OIndeks dolny 22
związek organiczny – końcowy produkt przemiany białek. Wydalany z organizmu głównie razem z moczem
dinukleotyd nikotynoamidoadeninowy, związek organiczny, który może występować w formie zredukowanej, jako NADH oraz w formie utlenionej, jako NADIndeks górny ++. Cząsteczka NADIndeks górny ++ jest dinukleootydem, który może związać jeden proton (HIndeks górny ++) oraz dwa elektrony, czyli może ulegać redukcji, w wyniku której powstaje NADH.
dinukleotyd nikotynoamidoadeninowy, organiczny związek chemiczny, który występuje w formie zredukowanej – NADPH i utlenionej – NADPIndeks górny ++, dzięki czemu bierze udział w reakcjach utleniania i redukcji
związki chemiczne wydzielane z zakończenia aksonu komórki presynaptycznej i oddziałujące w specyficzny sposób na receptory w błonie postsynaptycznej
enzym katalizujący oderwanie od różnych związków atomów wodoru lub elektronów i wiązanie ich z tlenem cząsteczkowym