Przeczytaj
Odkrywcą toluenu był polski chemik – Filip Neriusz Walter. Swoją pracę naukową poświęcił destylacji żywic i olejków roślinnych oraz ropie naftowej.
Doświadczenie 1
Czy reaguje z toluenem?
Przeprowadź doświadczenie, w którym sprawdzisz, czy manganian() potasu reaguje z toluenem.
Uwaga! Doświadczenie wykonuj pod działającym wyciągiem, przestrzegając przepisów BHP.
Do probówki dodaj 1 cm3 toluenu, pięć kropli 5% roztworu oraz cztery krople 10% . Podgrzej mieszaninę łaźni wodnej.
Wnioski:
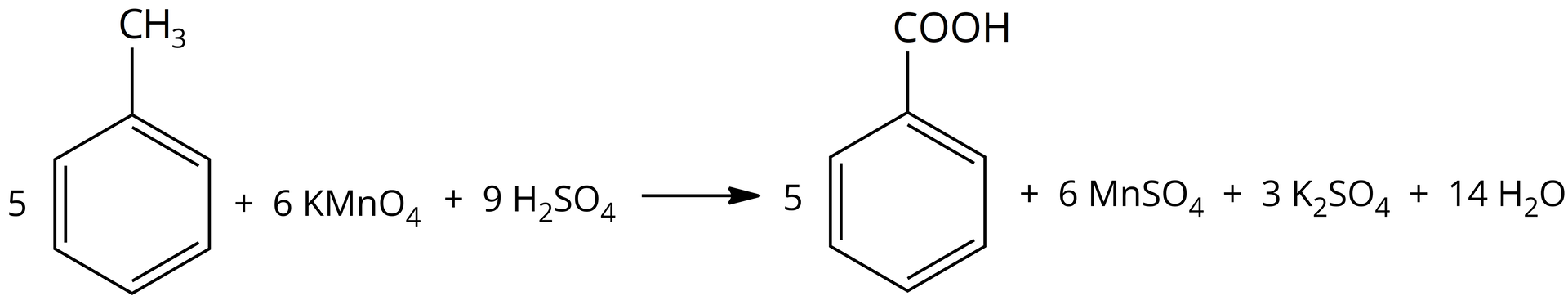
Równanie reakcji:
Przeprowadzono doświadczenie, w którym sprawdzono, czy manganian() potasu reaguje z toluenem. Doświadczenie wykonano pod działającym wyciągiem, przestrzegając przepisów BHP. Zapisz obserwacje, wnioski oraz równanie reakcji z opisanego doświadczenia.
Manganian() potasu jest silnym utleniaczemutleniaczem, co oznacza, że podczas reakcji chemicznej zwiększa stopień utlenienia substratu, a sam ulega redukcji. W wyniku reakcji oksydacyjno‑redukcyjnejreakcji oksydacyjno‑redukcyjnej, utlenia on łańcuch węglowodorowy do kwasu karboksylowego. Pierścień aromatyczny nie reaguje z manganianem() potasu.
W związkach organicznych atom węgla może występować w stopniu utlenienia od (np. dla cząsteczki metanu) do (np. dla cząsteczki mocznika).
Reakcji utlenienia ulega tylko grupa metylowa, przyłączona do pierścienia aromatycznego. Atom węgla grupy metylowej zmienia stopień utlenienia z na . W wyniku reakcji następuje rozerwanie wiązania i wytworzenie trzech nowych wiązań: oraz .
Węglowodory aromatyczne, które posiadają łańcuch alkilowy, ulegają reakcji utlenienia z utworzeniem kwasu benzoesowego, niezależnie od długości łańcucha alkilowego.
Mechanizm reakcji nie został jeszcze dokładnie poznany, jednak za pomocą doświadczeń wykazano, że reakcji utlenienia nie ulegają związki, które przy atomie węgla, który jest połączony pierścieniem aromatycznym, nie posiadają atomu wodoru.
Słownik
atom, jon lub cząsteczka, które w reakcji oksydacyjno‑redukcyjnej są akceptorem elektronu (elektronów)
substancja oddająca elektrony substancji redukowanej, a sama ulegająca utlenieniu
reakcja utleniania‑redukcji, reakcja redoks, reakcja, w której dochodzi do przeniesienia jednego lub więcej elektronów od atomu, jonu lub cząsteczki donora (czyli reduktora) do akceptora (czyli utleniacza)
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.