Przeczytaj
Berylowce
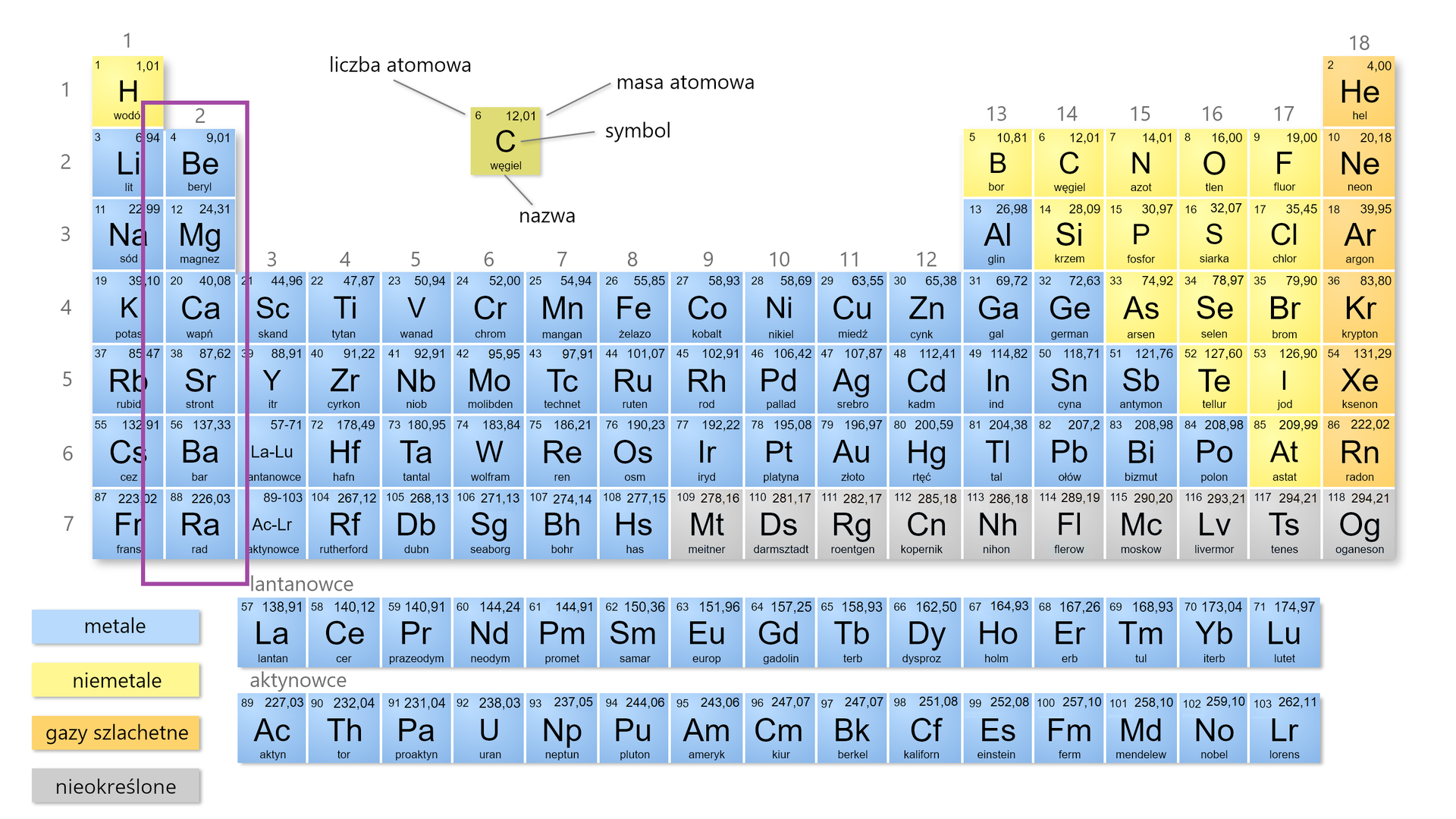
Berylowce (nazywane metalami ziem alkalicznych) znajdują się w drugiej grupie układu okresowego. Nazwa metale alkaliczne pochodzi od od arabskiego „al–qili”, co oznacza „popioły”, jako, że występowały w spalonych częściach niektórych roślin. Konfiguracja elektronowa powłoki walencyjnej tej grupy to . Ze względu na swoją wysoką reaktywność nie występują w przyrodzie w stanie wolnym, za to możemy je odnaleźć w postaci związanej (głównie jako dwudodatnie kationy gdzie to atom berylowca). Poza berylem (którego tlenkitlenki mają charakter amfoteryczny) berylowce tworzą stabilne tlenki, które w kontakcie z wodą tworzą wodorotlenki o charakterze alkalicznym (zasadowym).
Idąc w dół grupy możemy zauważyć, że maleje energia jonizacji, czyli energia potrzebna do oderwania elektronu. Jednocześnie wzrasta promień atomowy pierwiastków, ponieważ zwiększa się ilość powłok wokół jąder atomów. Powoduje to wzrost reaktywności pierwiastków w dół grupy. Zauważyć można również, że promień jonowy dwudodatnich kationów (od wapnia do radu) zwiększa się nieznacznie.

Wpływ berylowców na zdrowie
Słownik
związki kompleksowe, w których jon metalu łączy się z ligandem organicznym więcej niż jednym wiązaniem
atomy tego samego pierwiastka różniące się liczbą masową
rodzaj promieniowania jonizującego, wysyłanego przez promieniotwórcze jądra atomowe
reakcja jądrowa w której eliminowana jest cząstka
związki tlenu z innymi pierwiastkami
Bibliografia
Atkins P., Jones L., Laverman L., Chemical Principles, 7th Edition, New York .
Bielański A., Podstawy chemii nieorganicznej, t. , Warszawa .
Greenwood N. N., Earnshaw A., Chemistry of the Elements, Second Edition, Oksford .