Przeczytaj
Chemia organiczna
Historia chemii organicznej sięga połowy wieku, bowiem w roku szwedzki chemik Torbern Bergman zauważył różnice między substancjami otrzymywanymi z minerałów i substancjami pochodzącymi z organizmów żywych. Związki powstałe z organizmów żywych były trudne do wydzielenia, a także oczyszczenia. Bardzo szybko dochodziło także do ich rozpadu.
W tamtym czasie wielu chemików było zwolennikami teorii witalistycznej. Przyczyną różnic między substancjami nieorganicznymi a organicznymi uważano niematerialne indywidua zwane „siłami życiowymi”. Dlatego twierdzono, że związków organicznych nie można syntezować w laboratorium. Jednak w roku teoria witalistyczna została podważona przez Friedricha Wöhlera. Odkrył on, że możliwe jest przekształcenie cyjanianu amonu (nieorganicznej soli) w mocznik (związek organiczny).
Dzisiejsza chemia organiczna jest nauką o ściśle określonych regułach. Związki organiczne wyróżniają się tym, że każdy z nich zawiera atom węgla, ale mogą zawierać także atomy innych pierwiastków: azotu, tlenu, fosforu, chloru, siarki itd.
Związki organiczne
Termin „związki organiczne” obejmuje wszystkie związki węgla, oprócz tlenków oraz związków zawierających aniony węglanowe lub cyjankowe oraz ich analogi. Związki organiczne są wyróżniane ze względu na ich znaczną liczbę, wielokrotnie przekraczającą liczbę związków nieorganicznych, a także z powodu ich charakterystycznych cech budowy i właściwości.
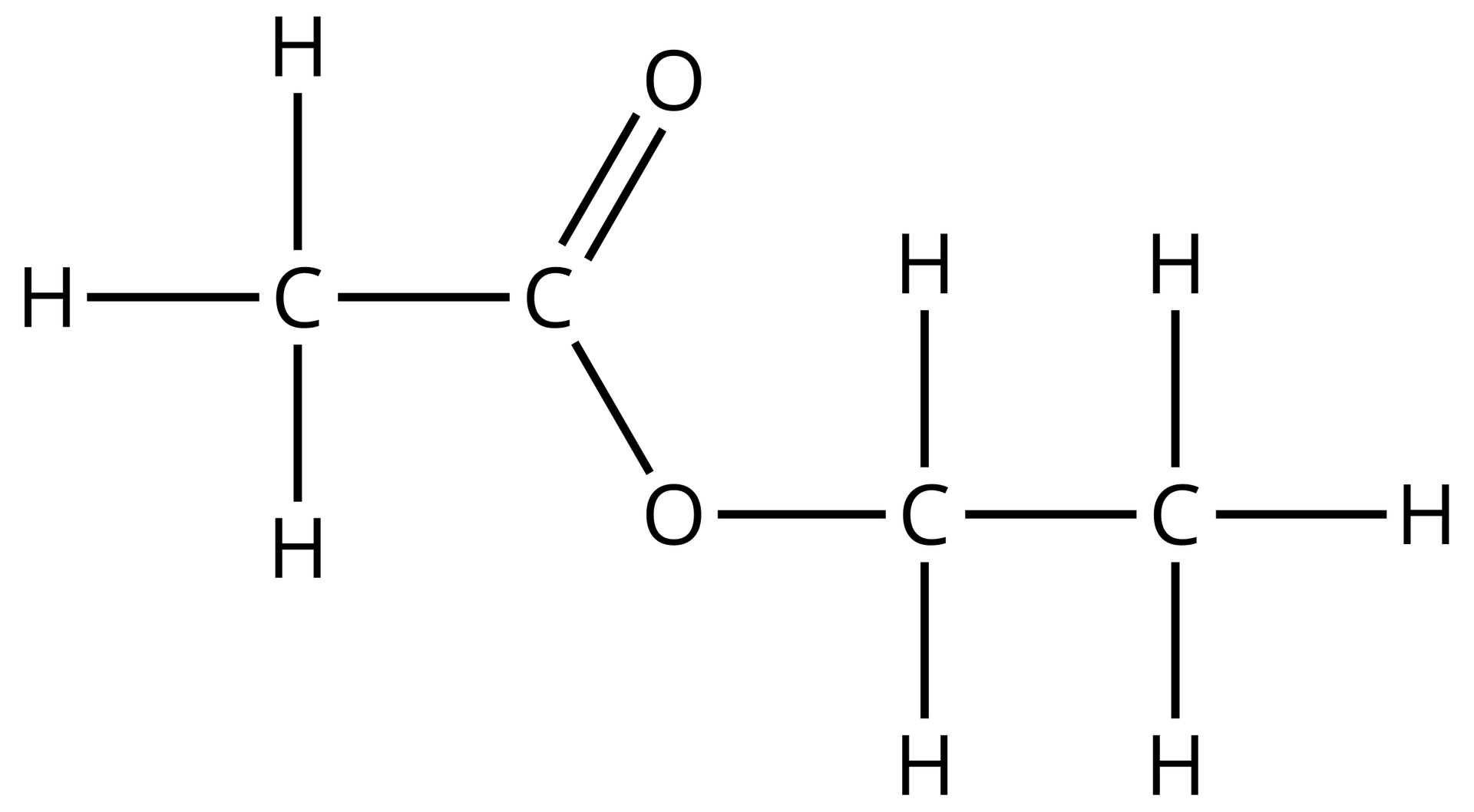
Atomy węgla posiadają unikalną zdolność katenacjikatenacji, czyli łączenia się ze sobą i tworzenia łańcuchów oraz pierścieni o praktycznie nieograniczonym stopniu komplikacji i liczbie atomów węgla. Zagadnienia te ujmuje teoria strukturalna, a poniżej przedstawiono jej podstawowe założenia:
W związkach chemicznych atomy węgla są czterowiązalne (tworzą cztery wiązania chemiczne – cztery wspólne pary elektronowe z innymi atomami). Trwałe związki organiczne nie posiadają wolnych par elektronowych na atomach węgla.
Każdemu z atomów węgla w cząsteczce związku organicznego można przypisać jeden z trzech typów hybrydyzacji orbitali walencyjnych:
Kliknij na poniższe kafelki, aby dowiedzieć się więcej.
Atomy węgla mogą łączyć się z innymi atomami węgla, wodoru, tlenu, azotu lub innych niemetali, za pomocą wiązań kowalencyjnych lub kowalencyjnych spolaryzowanych (mogą to być wiązania pojedyncze, podwójne lub potrójne).
Atomy węgla mogą się łączyć ze sobą, tworząc łańcuchy o różnej długości (proste lub rozgałęzione), pierścienie lub połączenie łańcucha z pierścieniem.
Słownik
tworzenie wiązań pomiędzy atomami tego samego pierwiastka; prowadzi do powstania łańcuchowych związków chemicznych
Bibliografia
Morrison R. T., Boyd R. N., Chemia organiczna, Warszawa 1985.