Przeczytaj
KwasyKwasy, zarówno organiczne, jak i nieorganiczne, można otrzymywać na kilka sposobów. Jedną z metod, którą można otrzymać wybrane kwasy, jest reakcja wymiany podwójnej. W tym przypadku, do soli słabego kwasu bądź jej wodnego roztworu dodajemy kwasu mocnego. W wyniku takiej reakcji chemicznej otrzymamy sól oraz słaby kwas, który zostaje wyparty ze swojej soli.
sól słabego kwasu + mocny kwas → słaby kwas + sól mocnego kwasu
Moc kwasu
Kwasy charakteryzują się swoją indywidualną stałą dysocjacji kwasowej, która decyduje o mocy kwasu. Stała ta nie zależy od stężenia elektrolitu, lecz od rodzaju rozpuszczalnika i temperatury (ze wzrostem temperatury wartość stałej dysocjacji kwasowej rośnie). Wraz ze wzrostem wartości stałej dysocjacji kwasowej, dysocjacja zachodzi w większym stopniu, więc moc kwasu także rośnie.
Porównajmy dwa kwasy: kwas octowy oraz kwas chlorowodorowy.
Proces dysocjacji obu kwasów możemy zilustrować następującymi równaniami:
dla kwasu octowego
dla kwasu chlorowodorowego
Zauważasz różnicę w zapisie tych procesów?
Wyrażenia na stałe dysocjacji dla tych kwasów wyglądają następująco:
Jak widzisz, stała dysocjacji kwasu chlorowodorowego jest znacząco wyższa od stałej dysocjacji kwasu octowego. Oznacza to, że w kwasie chlorowodorowym występują tak naprawdę tylko jony, a kwas ten dysocjuje w 100%, stąd zapis reakcji dysocjacji ze strzałką w jedną stronę. W roztworze kwasu octowego stała dysocjacji jest mała – obecne są zdysocjowane jony oraz cząsteczki kwasu, które są w równowadze, dlatego zapisujemy równanie reakcji ze strzałkami w dwie strony.
Stałe dysocjacji wybranych kwasów nieorganicznych w roztworach wodnych w temperaturze 25°C | |
|---|---|
Kwas nieorganiczny | Stała dysocjacji lub KIndeks dolny a1a1 |
6,3 · 10Indeks górny -4-4 | |
1,0 · 10Indeks górny 77 | |
3,0 · 10Indeks górny 99 | |
1,0 · 10Indeks górny 1010 | |
1,0 · 10Indeks górny -7-7 | |
1,9 · 10Indeks górny -4-4 | |
2,5 · 10Indeks górny -3-3 | |
5,0 · 10Indeks górny -8-8 | |
1,1 · 10Indeks górny -2-2 | |
5,0 · 10Indeks górny 22 | |
5,1 · 10Indeks górny -4-4 | |
27,5 | |
1,5 ·10Indeks górny -2-2 | |
5,8 · 10Indeks górny -10-10 | |
5,9 · 10Indeks górny -10-10 | |
6,5 · 10Indeks górny -4-4 | |
6,9 · 10Indeks górny -3-3 | |
3,2 · 10Indeks górny -10-10 | |
4,5 · 10Indeks górny -7-7 | |
Stałe dysocjacji wybranych kwasów organicznych w roztworach wodnych w temperaturze 25°C (jeśli w tabeli nie zaznaczono inaczej) | |
|---|---|
Kwas organiczny | Stała dysocjacji |
1,8 · 10Indeks górny -4-4 (T = 20°C) | |
1,8 · 10Indeks górny -5-5 | |
1,4 · 10Indeks górny -5-5 | |
6,5 · 10Indeks górny -5-5 | |
1,3 · 10Indeks górny -10-10 (T = 20°C) | |
Stałe dysocjacji wybranych zasad w roztworach wodnych w temperaturze 25°C | |
|---|---|
Zasada | Stała dysocjacji KIndeks dolny bb |
1,8 · 10Indeks górny -5-5 | |
4,3 · 10Indeks górny -4-4 | |
5,0 · 10Indeks górny -4-4 | |
4,0 · 10Indeks górny -4-4 | |
7,4 · 10Indeks górny -4-4 | |
7,4 · 10Indeks górny -5-5 | |
4,3 · 10Indeks górny -10-10 | |
Indeks górny Źródło: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
J. Sawicka, A. Janich‑Kilian, W. Cejner‑Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2001. Indeks górny koniecŹródło: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2010.
J. Sawicka, A. Janich‑Kilian, W. Cejner‑Mania, G. Urbańczyk, Tablice chemiczne, Gdańsk 2001.
Moc kwasów beztlenowych (, gdzie to niemetal) można określić za pomocą porównania elektroujemności atomu niemetalu. Wraz ze wzrostem elektroujemności atomu niemetalu w okresie, moc kwasów się zwiększa. Czym większa jest różnica elektroujemności pomiędzy pierwiastkami i w wiązaniu, tym wiązanie jest bardziej spolaryzowane. Większe spolaryzowanie wiązania sprzyja rozpadowi substancji chemicznej na jony. Moc kwasów beztlenowych w grupie zwiększa się wraz ze zmniejszeniem się wartości elektroujemności w atomie .
Powyżej opisana tendencja ma jednak charakter orientacyjny. W przypadku kwasów beztlenowych czynnikiem decydującym o mocy kwasu jest wielkość promienia atomowego – im większy promień atomowy niemetalu, połączonego z atomem wodoru, tym moc kwasu będzie równie większa.
Przeanalizujmy teraz kwasy z pierwiastkami z grupy 17. układu okresowego pierwiastków.
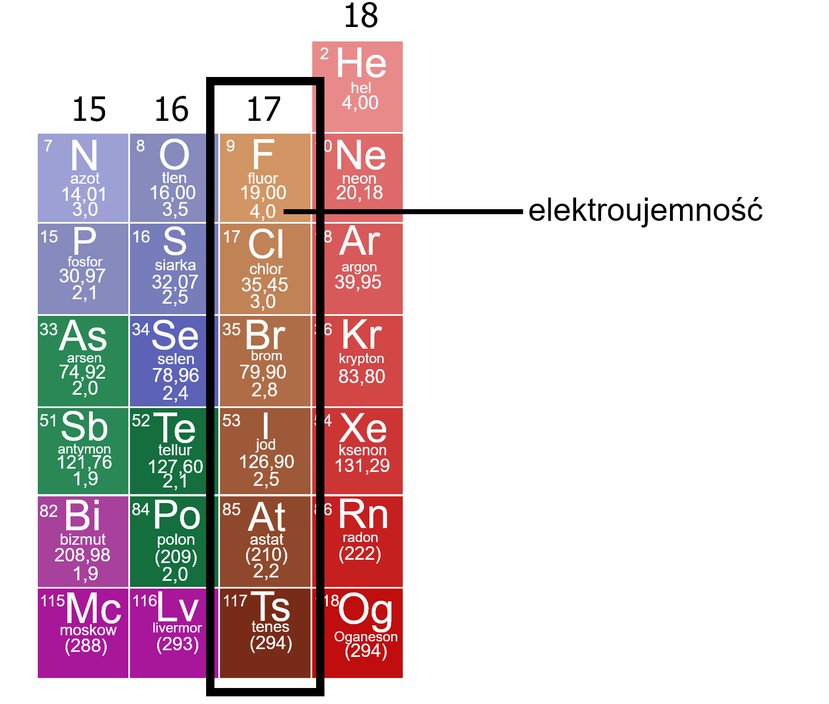
Porównując wartości elektroujemności niemetali 17. grupy układu okresowego pierwiastków, można stwierdzić, że jest kwasem najsłabszym, ponieważ fluor wykazuje największą wartość elektroujemności, a co za tym idzie – promień atomowy fluoru jest najmniejszy. Najmocniejszym kwasem z tej grupy jest natomiast , ponieważ jod ma najniższą wartość elektroujemności, a więc jego promień atomowy jest największy.
Korzystając z powyższego fragmentu układu okresowego pierwiastków, odczytaj wartości elektroujemności fluorowców oraz postaraj się ustalić, który z tych niemetali tworzy kwasy najmocniejsze.
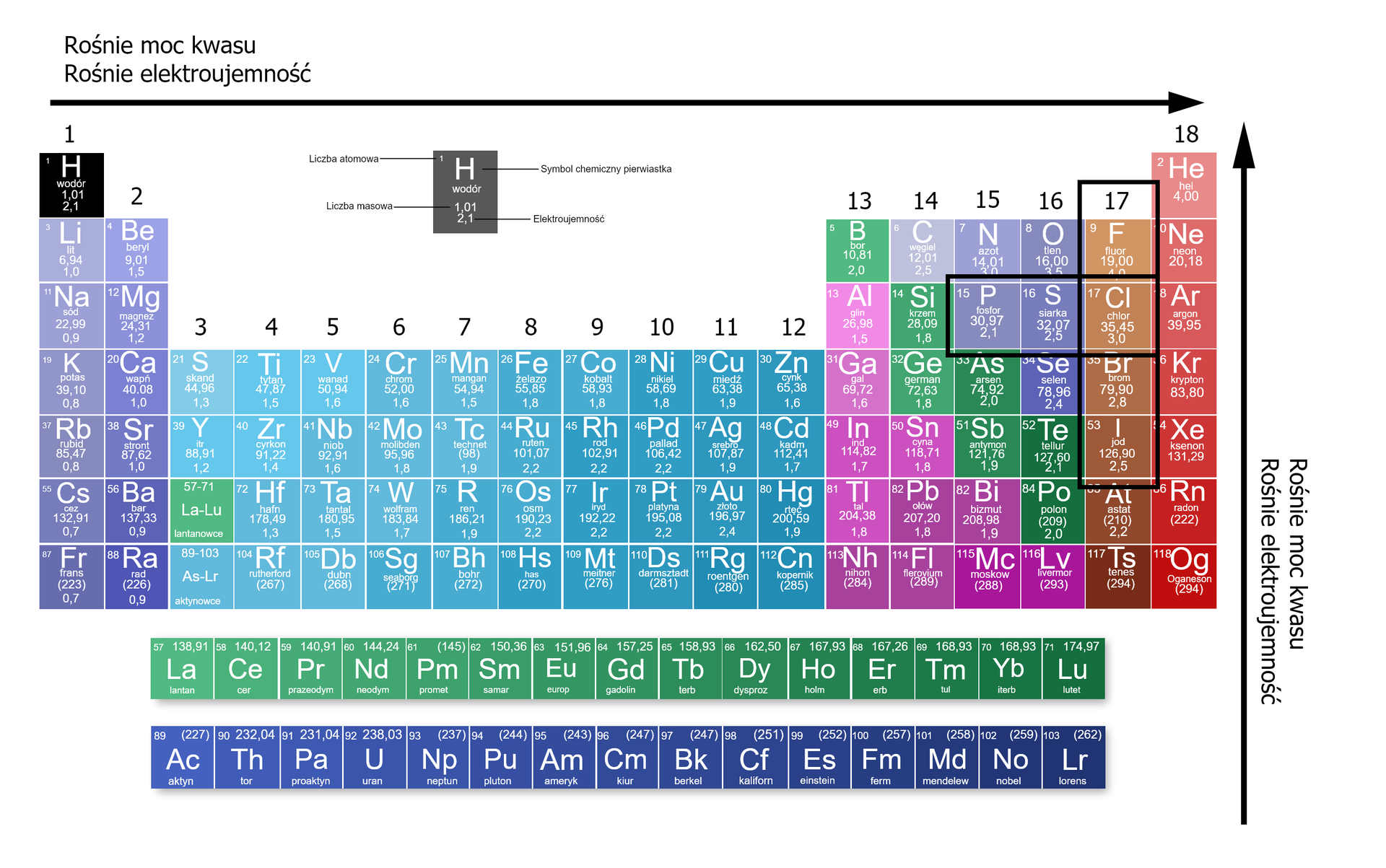
Moc kwasów tlenowych wzrasta wraz ze wzrostem wartości elektroujemności atomów pierwiastka zawartego w reszcie kwasowej – zarówno w grupie, jak i w okresie układu okresowego pierwiastków chemicznych.
Należy jednak pamiętać, że regułę tę możemy stosować tylko w przypadku porównywania kwasów o tej samej budowie, np. , gdzie jest symbolem pierwiastka. Zatem możemy porównywać ze sobą i , nie zaś np. i . Stąd uniwersalnym kluczem, który umożliwia porównanie mocy kwasów, jest analiza zgodna z wartościami stałych dysocjacji.
Porównując moc kwasów tlenowych tego samego pierwiastka, należy pamiętać, że moc kwasu wzrasta wraz ze wzrostem stopnia utlenienia atomu centralnego.
Czy zawsze mocniejszy kwas wypiera słabszy z jego soli? Co ma wpływ na tę reakcję chemiczną?
Gdy do roztworu octanu sodu () doda się kwas solny (np. ), to równanie omawianej reakcji chemicznej wygląda następująco:
Jak widać, w wyniku powyższej reakcji otrzymano chlorek sodu oraz kwas octowy (etanowy). Octan (etanian) sodu jest solą złożoną z kationu metalu oraz anionu reszty kwasu octowego, który jest słabym kwasemsłabym kwasem ( = 1,8 · 10Indeks górny -5-5). Natomiast kwas solny jest kwasem mocnym ( = 1,0 · 10Indeks górny 77; ) , który wyparł kwas słabszy (kwas octowy) z roztworu jego soli.
Im większa różnica w mocy kwasu, tym silniej stan równowagi przesunięty jest w prawo. Jednak dotyczy to tylko przypadku słabych kwasów i bardzo mocnych.
Metody otrzymywania kwasu przez wypieranie go z jego soli
Wypierany kwas jest słabszy niż kwas działający na sól
Kwasy, których tlenki nie reagują z wodą, otrzymuje się zazwyczaj z ich soli. Na taką sól działa się innym mocnym kwasem, w wyniku czego interesujący nas kwas zostaje wyparty z soli.
Problem badawczy: czy po zmieszaniu wodnego roztworu krzemianu sodu i rozcieńczonego kwasu chlorowodorowego otrzymamy kwas krzemowy?
Wybierz jedną z poniższych hipotez.
- W wyniku zmieszania roztworu krzemianu sodu i rozcieńczonego kwasu chlorowodorowego otrzyma się kwas krzemowy.
- W wyniku zmieszania roztworu krzemianu sodu i rozcieńczonego kwasu chlorowodorowego nie otrzyma się kwasu krzemowego.
Wykonanie:
1. Do probówki wlej 2-3 cm3 roztworu krzemianu sodu.
2. Dodaj około 1 cm3 kwasu chlorowodorowego.
3. Obserwuj zachodzące zmiany.
Narysuj schemat doświadczenia.
Schemat wykonaj w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Równanie reakcji chemicznej:
Równanie reakcji zapisz w zeszycie, zrób zdjęcie, a następne umieść je w wyznaczonym polu.
Podsumowanie:
Reakcja wypierania kwasu w wyniku reakcji strąceniowych
W omawianym przypadku sól trudno rozpuszczalna powstaje z kwasu, który jest substratem.
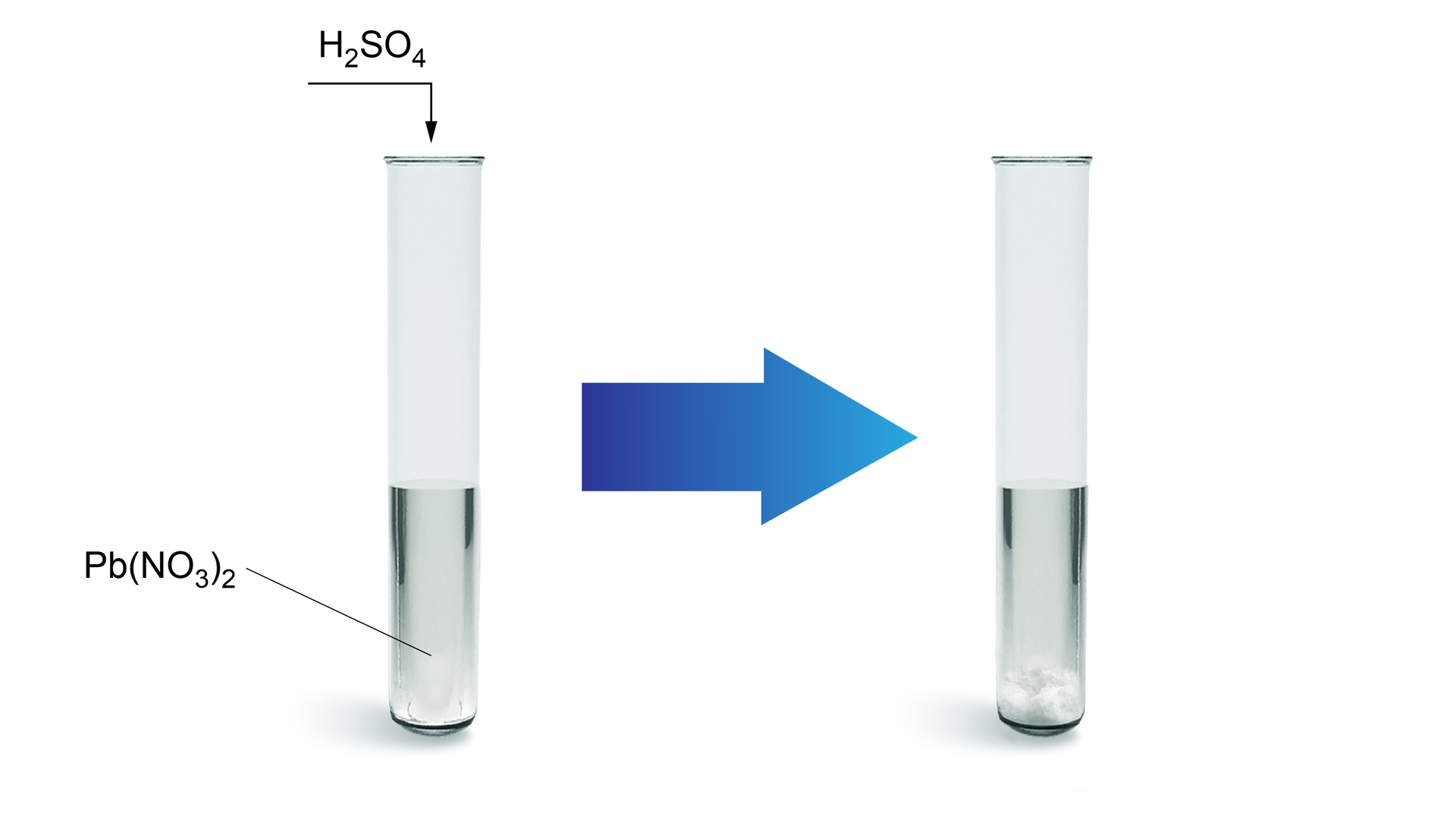
Czy po zmieszaniu roztworów kwasu siarkowego(VI) i azotanu(V) ołowiu(II) otrzymamy kwas azotowy(V)?
Hipoteza:
W wyniku zmieszania dwóch roztworów: kwasu siarkowego(VI) i azotanu(V) ołowiu(II) otrzyma się kwas azotowy(V).
Sprzęt i odczynniki:
Wykonanie:
1. Do probówki wlej 2-3 cm3 roztworu azotanu(V) ołowiu(II).
2. Dodaj około 1 cm3 roztworu kwasu siarkowego(VI).
3. Obserwuj zachodzące zmiany.
Narysuj schemat doświadczenia.
Schemat wykonaj w zeszycie do lekcji chemii, zrób zdjęcie, a następnie umieść je w wyznaczonym polu.
Równanie reakcji chemicznej:
Równanie reakcji zapisz w zeszycie, zrób zdjęcie, a następne umieść je w wyznaczonym polu.
Podsumowanie:
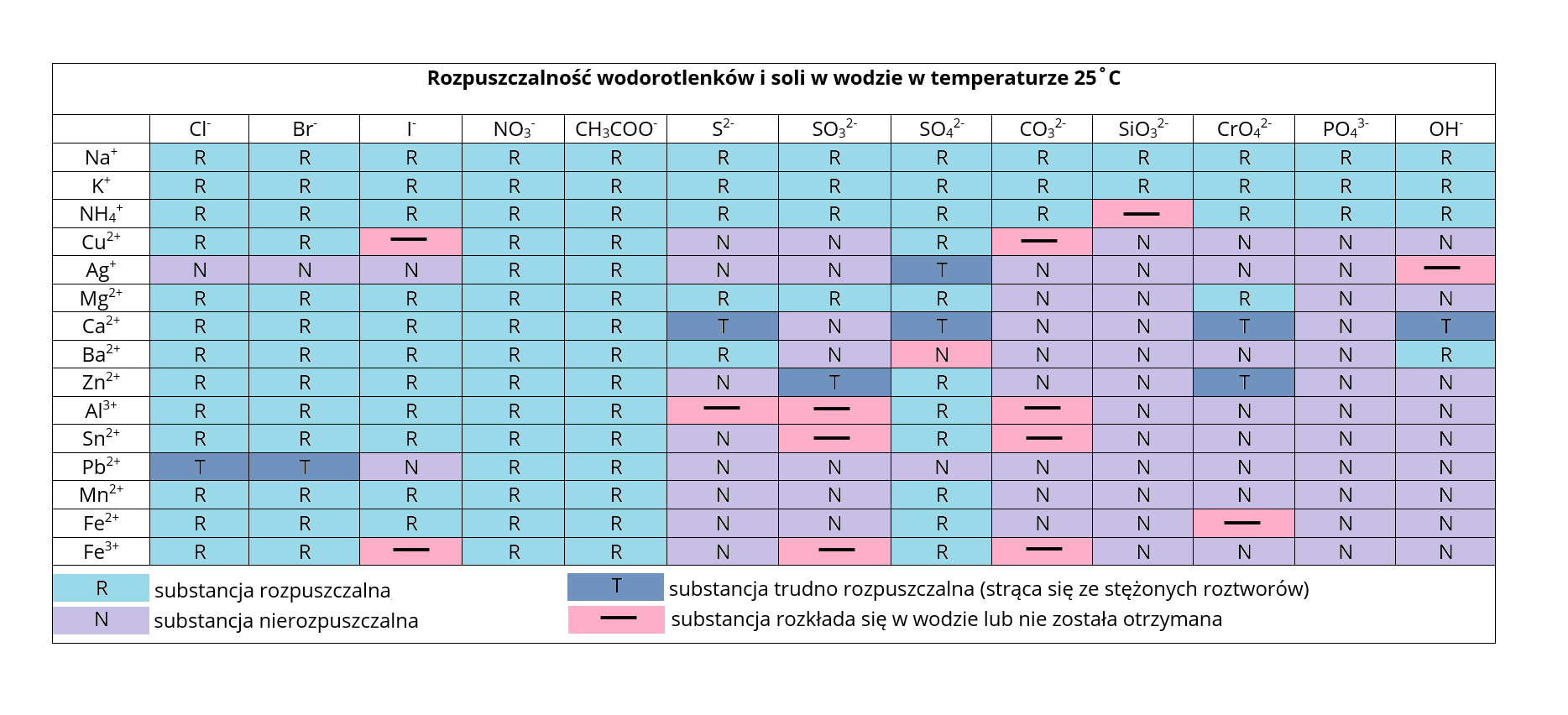
Gdzie sprawdzisz, czy powstająca w hipotetycznej reakcji strąceniowej sól faktycznie się wytrąci? Oczywiście w tabeli rozpuszczalności.
Wypierany kwas jest lotny
Słownik
według teorii Brønsteda jest to donor protonu, a zgodnie z teorią Arrheniusa substancja, która w roztworze wodnym dysocjuje na kation wodoru i anion reszty kwasowej
kwas, który w roztworze wodnym ulega całkowitej dysocjacji
kwas, który w roztworze wodnym ulega dysocjacji w małym stopniu
Bibliografia
Atkins P., Jones L., Chemia ogólna: cząsteczki, materia, reakcje, Warszawa 2009.
Bielański A., Podstawy chemii nieorganicznej, Warszawa 1987.