Przeczytaj
W organizmie ludzkim żelazo występuje tylko w postaci jonowej, lub jest związane z innymi cząsteczkami, ale nie występuje w formie atomowej, mimo że często domyślnie używamy formy „żelazo” w miejsce formy „jony żelaza” w czasie opisywania wpływu tego pierwiastka na funkcjonowanie organizmu. Oglądając zatem reklamę telewizyjną, czytając informacje o składzie leku czy nawet analizując treść tej lekcji, pamiętaj, że w istocie żelazo wprowadzane do organizmu ma formę zjonizowaną, nie atomową.
Dla organizmu niekorzystny jest zarówno niedobór związków żelaza – niedokrwistość, jak i ich nadmiar – hemosyderozahemosyderoza lub hemochromatozahemochromatoza.
Stężenie jonów żelaza w organizmie zależy od:
wieku;
płci (niższe u kobiet o ok. );
wewnątrzosobniczej zmienności;
zmienności okołodobowej (większe wartości w godzinach porannych).
Zależy także od przejściowego zwiększenia po spożyciu łatwo przyswajalnego żelaza (pokarm, suplementacja).
Jednostka stosowana jest dla ułatwienia. Otrzymuje się ją poprzez wymnożenie stężenia molowego żelaza i jego masy molowej.
Przyczyny niedoboru jonów żelaza
Wyróżniamy następujące przyczyny niedoboru jonów żelaza:
złe przyzwyczajenia dietetyczne, niedożywienie lub brak niezbędnych składników, wegetarianizm (wegetarianie mogą zastąpić mięso warzywami zawierającymi dużo żelaza, np. szpinakiem), brak czerwonego mięsa, niedobór białek, niedożywienie starcze;
zwiększone zużycie w okresie wzrostu, ciąży, laktacji czy rekonwalescencji, a z kolei zmniejszenie zapasów w życiu płodowym, u wcześniaków bądź niemowląt niekarmionych mlekiem matki;
zaburzenia wchłaniania spowodowane chorobami przewodu pokarmowego: obniżenie kwasoty soku żołądkowego, ZUWZUW, biegunki, choroba Crohna, resekcja żołądka i jelit, nietolerancja glutenu;
zwiększona utrata krwi przez różne krwawienia: krwawienia ginekologiczne (miesiączki), przewlekłe upusty krwi, zabiegi, krwawienia z przewodu pokarmowego: wrzody, nowotwory, polipowatośćpolipowatość, choroby zapalne;
choroby pasożytnicze;
niedobór funkcjonalny: mutacje, niedobór białek transportowych; hipotransferrynemia, niewydolność nerek, hemodializy, zaburzenia syntezy hemu, choroby przewlekłe.
Przez wiele lat wierzono, że szpinak zawiera razy więcej jonów żelaza niż w rzeczywistości. Teraz już wiadomo, że w szpinaku znajduje się jonów żelaza, a nie .
Objawy niedoboru jonów żelaza
Do objawów niedoboru jonów żelaza zalicza się:
obniżoną sprawność fizyczną i umysłową,
apatię,
drażliwość,
senność,
bóle i zawroty głowy.
Występują także zaburzenia łaknienia (tzw. łaknienie spaczone – jedzenie ziemi, tynku itp.). Osoba cierpiąca na niedobór żelaza może się borykać również ze zmianą śluzówki języka i dziąseł, powstawaniem zajadów, zmian zanikowych śluzówki żołądka.
Ze strony układu krwionośnego może wystąpić kołatanie serca, bóle wieńcowe czy tachykardia, natomiast z układu oddechowego duszność. Niedobór jonów żelaza wpływa także na kondycje włosów i paznokci, które stają się kruche i łamliwe. Powoduje także obniżoną odporność na zakażenia, przez co stajemy się bardziej podatni na infekcje. Następuje spadek liczby erytrocytów i stężenia hemoglobiny we krwi.
Profilaktyka
Zapobieganie niedoborom jonów żelaza ma podstawowe znaczenie w zapobieganiu niedokrwistości. Najprostszym sposobem jest wzbogacenie diety w produkty zawierające żelazo.
W pożywieniu znajdują się zarówno związki zawierające żelazo na , jak i na stopniu utlenienia. W żołądku żelazo jest uwalniane ze związków organicznych, a jego kwasowe środowisko sprzyja redukcji jonów do postaci , której związki są rozpuszczalne w wodzie i wchłaniane w jelicie w optymalnym pH.
Jony przyjmowane z pokarmem często związane są w nierozpuszczalnych kompleksach, ze względu na alkaliczny odczyn przyjmowanego pokarmu. Po wprowadzaniu do żołądka, te alkaliczne kompleksy zostają rozpuszczone przez działanie kwasu żołądkowego, co ułatwia ich redukcję i wchłanianie do organizmu. Zatem zmniejszenie kwasowości soku żołądkowego upośledza wchłanianie żelaza. Istotne jest również spożywanie w diecie i z suplementami żelaza odpowiedniej ilości związków redukujących, np. kwasu askorbinowego (witaminy C), które wspomagają redukcję jonów do jonów .
Związki przyjmowane na nadkwasotę podwyższają pH soku żołądkowego, a tym samym utrudniają wchłanianie żelaza. Osoby, które przyjmują środki przeciw zgadze, powinny więc zwrócić szczególną uwagę na dostarczenie odpowiedniej ilości tego pierwiastka do organizmu.
- Nazwa kategorii: Źródła żelaza w pożywieniu
- Nazwa kategorii: mięso
- Nazwa kategorii: wędliny
- Nazwa kategorii: wątróbka
- Nazwa kategorii: nerki
- Nazwa kategorii: ziarna słonecznika
- Nazwa kategorii: soja
- Nazwa kategorii: kiełki pszenicy
- Nazwa kategorii: otręby
- Nazwa kategorii: czerwone wino
- Nazwa kategorii: ryby
- Nazwa kategorii: żółtko jaj
- Nazwa kategorii: twaróg
- Nazwa kategorii: orzechy
- Nazwa kategorii: mleko
- Nazwa kategorii: warzywa strączkowe
- Nazwa kategorii: brokuły
- Nazwa kategorii: szpinak
- Nazwa kategorii: krewetki Koniec elementów należących do kategorii Źródła żelaza w pożywieniu
- Elementy należące do kategorii Źródła żelaza w pożywieniu
-
Źródła żelaza w pożywieniu
-
mięso
-
wędliny
-
wątróbka
-
nerki
-
ziarna słonecznika
-
soja
-
kiełki pszenicy
-
otręby
-
czerwone wino
-
ryby
-
żółtko jaj
-
twaróg
-
orzechy
-
mleko
-
warzywa strączkowe
-
brokuły
-
szpinak
-
krewetki
-
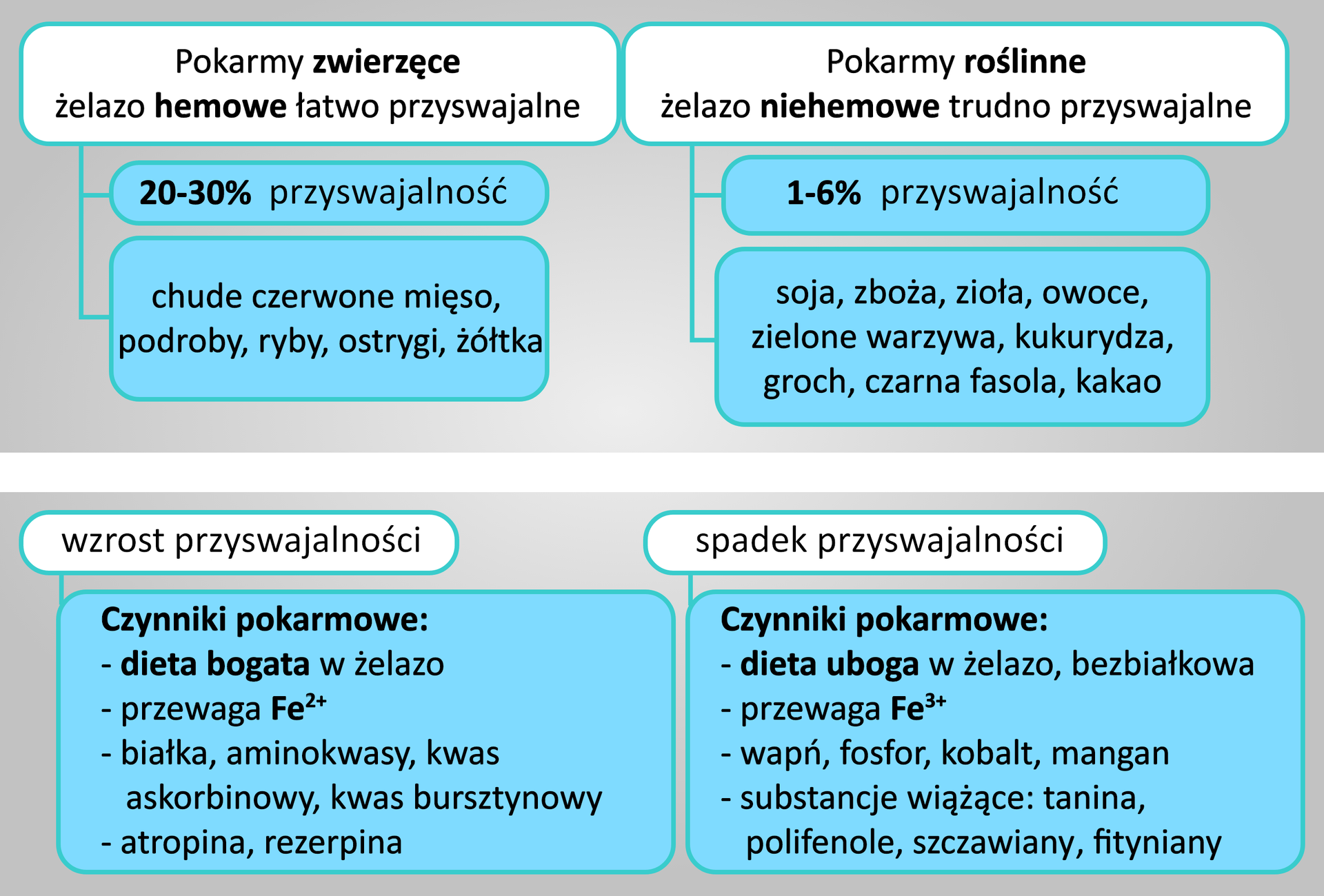
Najlepiej przyswajalne jest żelazo związane z hemem, czyli żelazo dwuwartościowe, znajdujące się w pokarmach pochodzenia zwierzęcego.
Należy jednak pamiętać, że niektóre związki utrudniają wykorzystanie żelaza z pokarmu, są to: fosforany, wapń, fityniany, szczawiany i taniny. Znajdują się m.in. w mleku, jajkach, herbacie, kawie i szpinaku.
Ich niekorzystny wpływ możemy zniwelować poprzez pobieranie wraz z pokarmem związków, które korzystnie działają na wykorzystanie żelaza z diety. I są to: cysteina, glutation, kwas askorbinowy, kwas bursztynowy i fruktoza. Możemy je odnaleźć w sokach owocowych, papryce, kwaszonej kapuście czy czerwonym winie.
- Nazwa kategorii: związki
- Nazwa kategorii: wpływające korzystanie
- Nazwa kategorii: cysteina
- Nazwa kategorii: glutation
- Nazwa kategorii: kwas askorbinowy
- Nazwa kategorii: kwas bursztynowy
- Nazwa kategorii: fruktoza Koniec elementów należących do kategorii wpływające korzystanie
- Nazwa kategorii: wpływające niekorzystnie
- Nazwa kategorii: fosforany
- Nazwa kategorii: wapń
- Nazwa kategorii: fityniany
- Nazwa kategorii: szczawiany
- Nazwa kategorii: taniny Koniec elementów należących do kategorii wpływające niekorzystnie
- Elementy należące do kategorii związki
- Elementy należące do kategorii wpływające korzystanie
- Elementy należące do kategorii wpływające niekorzystnie
-
związki
-
wpływające korzystanie
-
cysteina
-
glutation
-
kwas askorbinowy
-
kwas bursztynowy
-
fruktoza
-
-
wpływające niekorzystnie
-
fosforany
-
wapń
-
fityniany
-
szczawiany
-
taniny
-
-
Doustna suplementacja jonów żelaza
Aby zwiększyć poziom jonów żelaza w organizmie, można stosować dodatkową suplementację:
dawka dobowa powinna wynosić - elementarnego żelazaelementarnego żelaza w dwóch/trzech podzielonych dawkach;
preparat powinien być podawany na pusty żołądek i bez równoczesnego podawania innych leków;
dodatkowo należy stosować sole żelaza() – siarczan, fumaran, glukonian.
Należy pamiętać, że równoczesne przyjmowanie wraz z suplementowanym żelazem pokarmu może zmniejszyć wchłanianie żelaza nawet do .
- Nazwa kategorii: cechy idealnego preparatu żelaza
- Nazwa kategorii: wysoka biodostępność
- Nazwa kategorii: minimalna toksyczność
- Nazwa kategorii: łatwa forma podawania
- Nazwa kategorii: niski koszt lub refundacja Koniec elementów należących do kategorii cechy idealnego preparatu żelaza
- Elementy należące do kategorii cechy idealnego preparatu żelaza
-
cechy idealnego preparatu żelaza
-
wysoka biodostępność
-
minimalna toksyczność
-
łatwa forma podawania
-
niski koszt lub refundacja
-
W poniższej tabeli znajdują się przykładowe nazwy preparatów oraz dodatki, które zawierają.
Preparat | Dodatek |
|---|---|
Sorbifer | witamina C |
Hemofer F | kwas foliowy |
Resoferon | kwas bursztynowy |
Słownik
choroba genetyczna; występowanie licznych polipów gruczolakowatych, najczęściej w jelicie grubym
gromadzenie się hemosyderyny (żelaza zawartego w białkach) w komórkach układu makrofagów różnych narządów, m.in. wątroby; obserwujemy ją głównie u ludzi, którzy mieli wielokrotnie przetaczaną krew
genetyczna choroba metabolizmu żelaza, w której dochodzi do nadmiernego wchłaniania tego pierwiastka z pożywienia i nadmiernego gromadzenia w tkankach, co prowadzi do objawów chorobowych
stan wynikający z nieprawidłowości w trawieniu i wchłanianiu składników odżywczych z przewodu pokarmowego; upośledzenie wchłaniania może dotyczyć jednego lub wielu składników odżywczych w zależności od nieprawidłowości; może to prowadzić do niedożywienia i różnych rodzajów niedokrwistości
tripeptyd złożony z kwasu glutaminowego, cysteiny i glicyny o właściwościach przeciwutleniających; występuje we wszystkich organizmach roślinnych i zwierzęcych (poza organizmem jest nietrwały); jest najbardziej rozpowszechnionym i najobfitszym tiolem (składnikiem zawierającym siarkę) wewnątrzkomórkowym, występującym w komórkach ssaków, oraz drobnocząsteczkowym tripeptydem, budującym żywe komórki
grupa organicznych związków chemicznych; pochodne fenoli, naturalnie wytwarzane przez rośliny; masa cząsteczkowa tanin mieści się w zakresie od kilkuset do kilku tysięcy Da; wyróżniane są taniny łatwo hydrolizujące oraz skondensowane – pierwsza grupa to związki powstałe w wyniku polimeryzacji kwasu galusowego lub innych kwasów fenolowych oraz cukrów, zwykle glukozy (łatwo ulega hydrolizie kwasowej), z kolei druga grupa ulega hydrolizie jedynie przy zastosowaniu silnych kwasów
żelazo na zerowym stopniu utlenienia, które do formy jonów łatwo przyswajalnych przez organizm () utlenia się dopiero w żołądku, pod wpływem działania kwasu solnego
substancja wydzielona z roztworu, praktycznie nierozpuszczalna; osad
Bibliografia
Bańkowski W. E., Biochemia. Podręcznik dla studentów uczelni medycznych, Amsterdam, Holandia, 2009, s. 406.
Beghetti M., Mermillod B., Halperin D. S., Blue sclerae: a sign of iron deficiency anemia in children?, „Pediatrics” 1993, t. 91, nr 6, s. 1195‑6.
Bielański A., Podstawy chemii nieorganicznej, Warszawa 1987.
Biggs M., McVicar J., Flowerdew B., Wielka księga warzyw, ziół i owoców, Warszawa 2007, s. 174–175.
Fazary A. E., Taha M., Yi‑Hsu Ju., Iron Complexation Studies of Gallic, „Acid, J. Chem. Eng.” 2009.
Gassmann B., Requirements of Vitamin A, Iron, Folate, and Vitamin B12, Rzym 1988.
Lange K. W., i in., The Role of Nutritional Supplements in the Treatment of ADHD: What the Evidence Says, „Current Psychiatry Reports” 2017, t. 19, nr 8.
Litwin M., Styka – Wlazło Sz., Szymońska J., Chemia ogólna i nieorganiczna, Warszawa 2002.
Pazdro K. M., Chemia. Podręcznik do kształcenia rozszerzonego w liceach, Warszawa 2009.
Sheftel A. D., Mason A. B., Ponka P., The long history of iron in the Universe and in health and disease, „Biochim Biophys Acta” 2012, nr 3, s. 161‑187.
Szczeklik A., Podręcznik chorób wewnętrznych, Kraków 2012,
Traczyk W. Z., Trzebski A., Fizjologia człowieka z elementami fizjologii stosowanej, Warszawa 2015, wyd. 3.