Przeczytaj
Jak zbudowane są amidy?
Pierwszorzędowe amidy to pochodne kwasów karboksylowychkwasów karboksylowych bądź nieorganicznych, w których grupę hydroksylową w grupie funkcyjnej zastąpiono grupą aminowąaminową .

Ponieważ Międzynarodowa Unia Chemii Czystej i Stosowanej zaleciła niestosowanie określenia rzędowości amidów jako pierwszo-, drugo- oraz trzeciorzędowych ze względu na liczbę podstawionych atomów wodoru w grupie aminowej, to ich podział przedstawia się następująco:
Wzór ogólny | Rzędowość | Grupa funkcyjna |
|---|---|---|
 | Pierwszorzędowe (I‑rzędowe, 1°). Mające jedną grupę acylową przy atomie azotu. 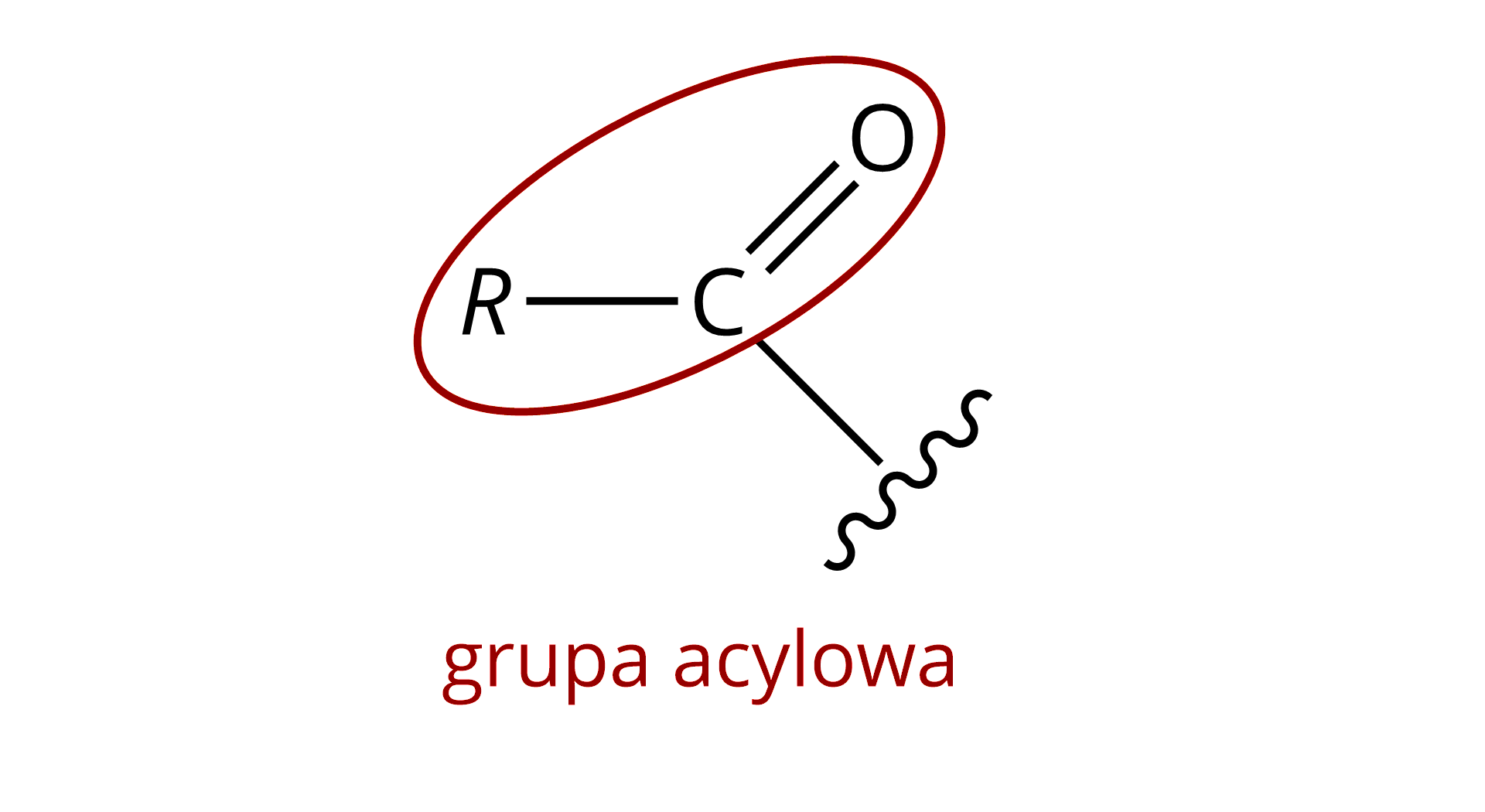 |  |
 | Drugorzędowe (II‑rzędowe, 2°). Mające dwie grupy acylowe przy atomie azotu. Są to inaczej imidy.  |  |
 | Trzeciorzędowe (III‑rzędowe, 3°). Mające trzy grupy acylowe przy atomie azotu. Są to inaczej triacyloiminy.  |  |
Tabela. Rzędowość amidów. Źródło: GroMar Sp. z o.o., licencja: CC BY‑SA 3.0.
Właściwości fizyczne amidów
Stan skupienia w temperaturze pokojowej

W temperaturze pokojowej amidy to krystaliczne ciała stałe. Wyjątek stanowi metanoamid (formamid) oraz N, N‑dimetyloformamid, które w temperaturze pokojowej są cieczami.

Rozpuszczalność amidów
Amidy posiadające do sześciu atomów węgla w swojej strukturze są bardzo dobrze rozpuszczalne w wodzie. Wynika to z faktu, iż tworzą z cząsteczkami wody liczne wiązania wodorowe. Dzieje się tak, ponieważ posiadają w swojej strukturze grupę karbonylową oraz grupę aminową . To właśnie te grupy są odpowiedzialne za tworzenie wiązań wodorowych z cząsteczkami wody.

Wodne roztwory amidów wykazują odczyn obojętny.
Temperatury wrzenia i topnienia amidów
Ze względu na tworzenie wiązań wodorowych pomiędzy atomem azotu grupy a karbonylowym atomem tlenu, amidy posiadają duże temperatury wrzeniawrzenia i topnieniatopnienia.
Wartości temperatur topnienia i wrzenia dla wybranych amidów:
Nazwa związku | Wzór | TIndeks dolny t Indeks dolny koniect [°C] | TIndeks dolny w Indeks dolny koniecw [°C] |
mocznik (diamid kwasu węglowego) | 132,7 | r | |
formamid (metanoamid) | 2,55 | 220 | |
N‑metyloformamid | -3,8 | 199,5 | |
N‑fenylo‑N‑metyloformamid | 14,5 | 243 | |
acetamid (etanoamid) | 81 | 222 | |
benzamid (enzenokarboksyamid) | 129,1 | 290 |
Indeks górny Źródło: opracowano na podstawie www.naukowiec.org/tablice Indeks górny koniecŹródło: opracowano na podstawie www.naukowiec.org/tablice
* r - rozkład przed osiągnięciem temperatury wrzenia
Słownik
związek organiczny, którego cząsteczka zawiera grupę karboksylową () połączoną z grupą alifatyczną, alicykliczną, aromatyczną lub heterocykliczną
związek organiczny; pochodna amoniaku, w którego cząsteczce jeden, dwa lub trzy atomy wodoru są zastąpione grupami alifatycznymi – aminy alifatyczne – lub aromatycznymi – aminy aromatyczne
temperatura, w której substancja przechodzi ze stanu stałego w stan ciekły
temperatura, w której ciśnienie pary nasyconej jest równe ciśnieniu atmosferycznemu
Bibliografia
Jelińska‑Kazimierczuk M., Megiel E., Teraz matura. Chemia. Vademecum, Warszawa 2018.
Litwin M., Styska‑Wlazło S., Szymońska J., To jest chemia 2. Chemia organiczna. Podręcznik dla liceum ogólnokształcącego i technikum. Zakres rozszerzony, Warszawa 2018.