Przeczytaj
Amidy
Amidy to pochodne kwasów karboksylowych i amin. Wyróżniamy amidy pierwszo-, drugo- i trzeciorzędowe.
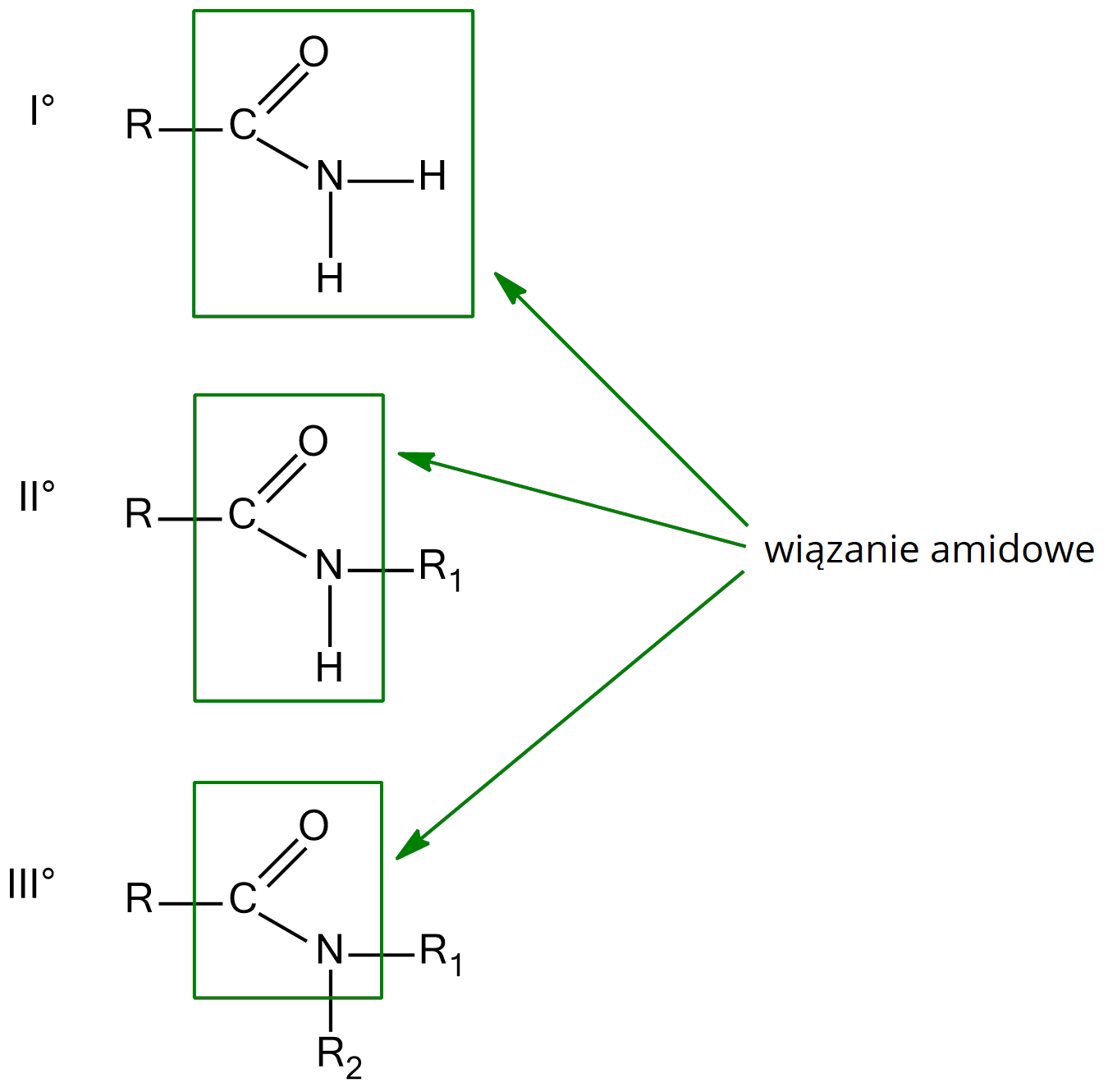
Otrzymywanie amidów z kwasów karboksylowych
Amidy pierwszorzędowe można otrzymać, ogrzewając kwasy karboksylowe z amoniakiem. Produktem pośrednim jest sól amonowa kwasu karboksylowego, z której, w wyniku reakcji pirolizyreakcji pirolizy, powstaje amid i woda.
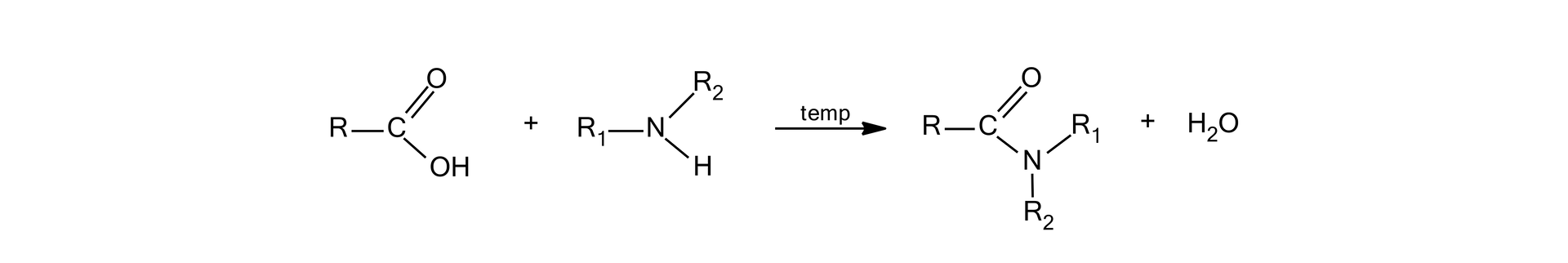
Ogólny schemat otrzymywania amidów pierwszorzędowych z kwasów karboksylowych:
etap :
etap :
Równania reakcji otrzymywania metanoamidu (formamidu):
etap :
etap :
Równania reakcji otrzymywania etanoamidu (acetamidu):
etap :
etap :
Amidy drugorzędowe można otrzymać w wyniku ogrzewania kwasu karboksylowego z aminą pierwszorzędowąaminą pierwszorzędową.

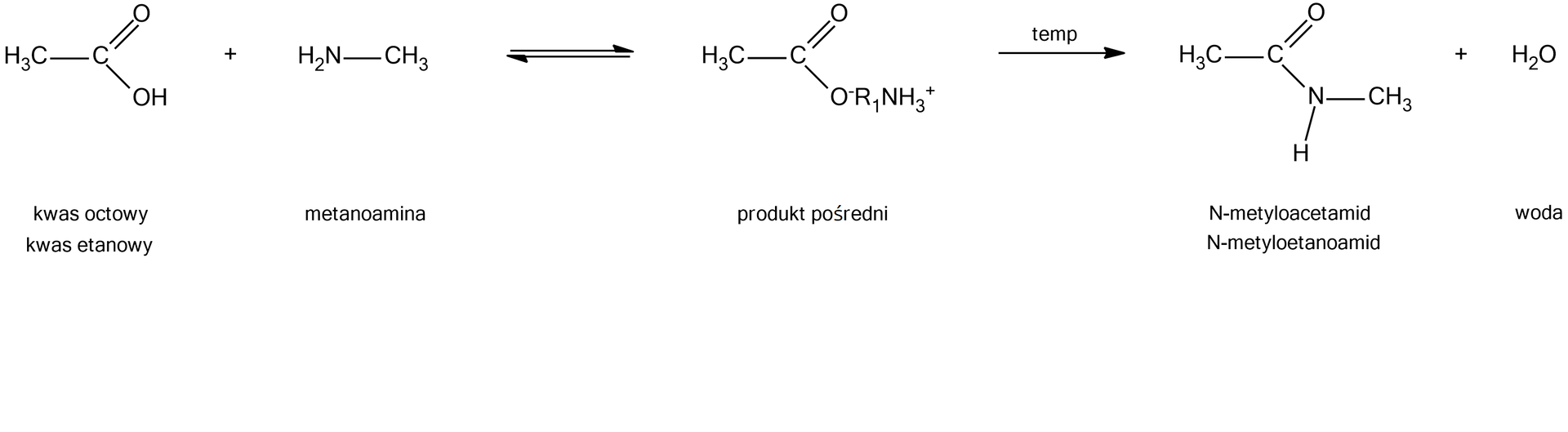
Z kolei amidy trzeciorzędowe można otrzymać w wyniku ogrzewania kwasu karboksylowego z aminą drugorzędowąaminą drugorzędową.

Mocznik jest amidem, naturalną substancją chemiczną, która powstaje w organizmach jako produkt przemiany metabolicznej białek oraz innych związków azotowych.
Mocznik znalazł zastosowanie m.in. w kosmetykach oraz preparatach dermatologicznych. W mniejszych stężeniach (około -) działa nawilżająco na skórę oraz zapobiega przed utratą wody. W większych stężeniach (około -) jest wykorzystywany w preparatach przeznaczonych dla pacjentów z łuszczycą czy przebarwieniami skórnymi. Stosuje się go także w preparatach do pielęgnacji stóp w stężeniu około -.
Podsumowanie
Reakcja kwasów karboksylowych z amoniakiem, prowadzona w wysokiej temperaturze, prowadzi do otrzymywania amidów pierwszorzędowych.
Reakcja kwasów karboksylowych z aminami pierwszorzędowymi, prowadzona w wysokiej temperaturze, prowadzi do otrzymywania amidów drugorzędowych.
Reakcja kwasów karboksylowych z aminami drugorzędowymi, prowadzona w wysokiej temperaturze, prowadzi do otrzymywania amidów trzeciorzędowych.

Słownik
(gr. lytikόs „mogący się rozwiązać”, gr. lỳsis „rozpuszczenie”, „rozluźnienie”) reakcja rozkładu polegająca na rozpadzie związków chemicznych, która zachodzi pod wpływem wysokiej temperatury
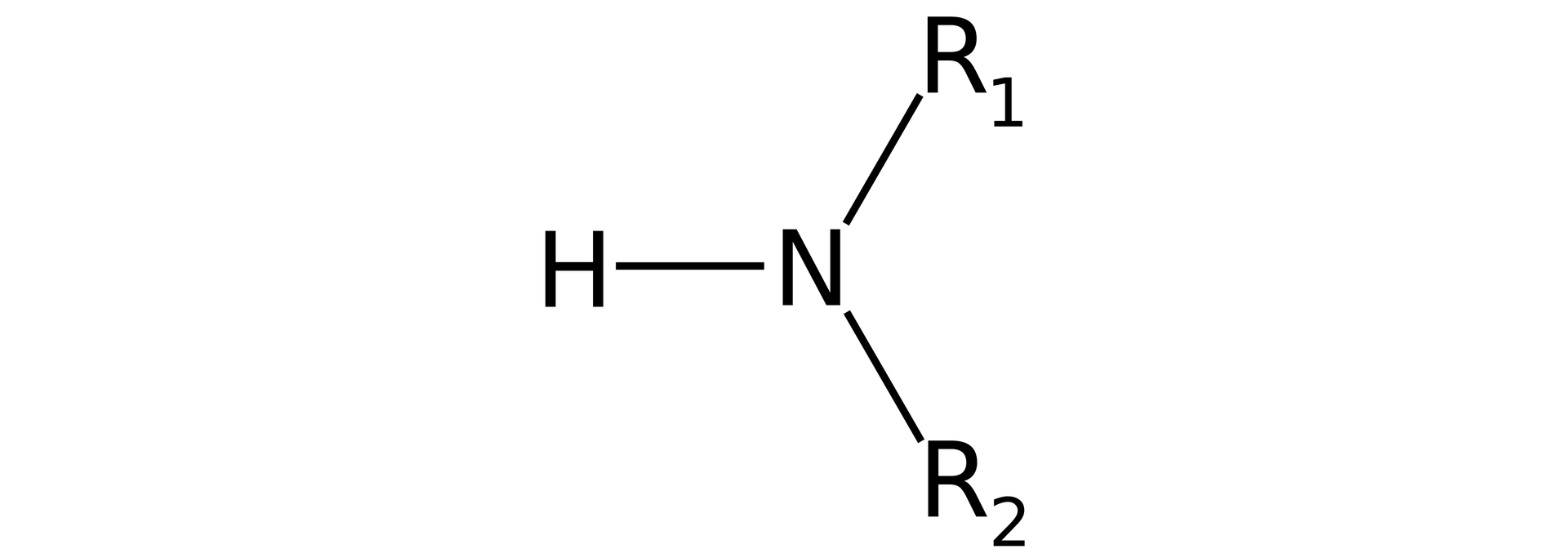
amina, w której cząsteczce jedna grupa alkilowa jest powiązana z atomem azotu. Wzór ogólny aminy alifatycznej -rzędowej: – , gdzie: – oznacza grupę alkilową; – oznacza grupę aminową
amina, w której cząsteczce dwie grupy alkilowe są powiązane z atomem azotu. Wzór ogólny aminy alifatycznej -rzędowej, gdzie: i – oznaczają grupy alkilowe
(łac. psoriasis „łuszczyca”) przewlekła choroba skóry, która objawia się występowaniem czerwonych ognisk pokrytych drobną, białawą, złuszczającą się łuską
Bibliografia
Buczek I., Chrzanowski M., Dymara J., Persona A., Kowalik E., Kuśmierczyk K., Odrowąż E., Sobczak M., Sygniewicz J., Chemia. Rozszerzenie. Repetytorium matura., Warszawa 2014.
Czerwiński A., Czerwińska A., Jelińska‑Kazimierczuk M., Kuśmierczyk K., Chemia 2. Podręcznik dla liceum ogólnokształcącego, liceum profilowanego, technikum., Warszawa 2003.
Danikiewicz W., Chemia. Związki organiczne. Podręcznik do liceów i techników. Zakres rozszerzony, Warszawa 2016.
Kapuścińska A., Nowak I., Wykorzystanie mocznika i jego pochodnych w przemyśle kosmetycznym, „Chemik” 2014, 2, 68, s. 91‑96.
Litwin M., Styka‑Wlazło Sz., Szymońska J., To jest chemia 2. Chemia organiczna. Podręcznik dla liceum ogólnokształcącego i technikum. Zakres rozszerzony, Warszawa 2016.
Majewski W., Mechanizmy reakcji organicznych, Lublin 2012.
McMurry J., Chemia organiczna 4, Warszawa 2004.