Przeczytaj
Tlenek miedzi(II) jako utleniacz
Gdy drut miedziany ogrzewamy w płomieniu palnika, pokrywa się on czarnym nalotem. Czarnym nalotem jest tlenek miedzi(II) powstający w wyniku reakcji miedzi z tlenem z powietrza, zgodnie z równaniem reakcji chemicznej:

Tlenek miedzi(II) to łagodny utleniaczutleniacz, który po ogrzaniu:
Utlenianie alkoholi pierwszorzędowych do aldehydów
Alkohole pierwszorzędowe (alkohole, w których grupa hydroksylowa przyłączona jest do atomu węgla połączonego z jednym atomem węgla i dwoma atomami wodoru) utleniają się za pomocą tlenku miedzi(II) w podwyższonej temperaturze do aldehydów (), zgodnie ze schematem:

gdzie: – grupa alkilowa/pierścień węglowy/pierścień aromatyczny
Przykłady reakcji utleniania alkoholi pierwszorzędowych do aldehydów
utlenianieutlenianie metanolu za pomocą tlenku miedzi(II) do metanalu:

W powyższej reakcji nastąpiło utlenienie atomu węgla w metanolu (stopień utlenienia: -II) do atomu węgla w metanalu (stopień utlenienia: 0) oraz redukcja kationu miedzi(II) w tlenku miedzi(II) (stopień utlenienia: II) do miedzi (stopień utlenienia: 0).
utlenianie etanolu za pomocą tlenku miedzi(II) do etanalu:
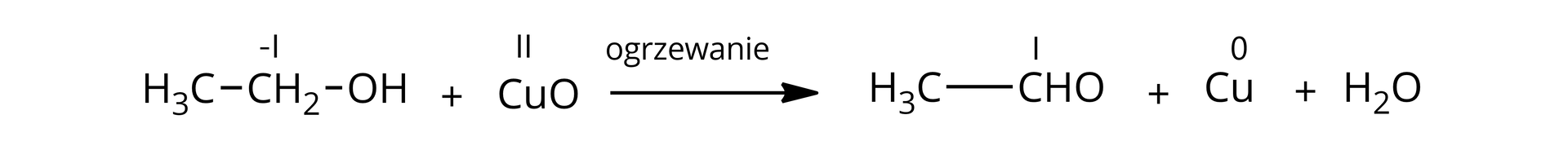
W powyższej reakcji nastąpiło utlenienie atomu węgla w ugrupowaniu (stopień utlenienia: -I) do atomu węgla w grupie aldehydowej (stopień utlenienia: I) oraz redukcja kationu miedzi(II) w tlenku miedzi(II) (stopień utlenienia: II) do miedzi (stopień utlenienia: 0).
Utlenianie alkoholi drugorzędowych do ketonów
Alkohole drugorzędowe (alkohole, w których grupa hydroksylowa przyłączona jest do atomu węgla połączonego z dwoma atomami węgla i jednym atomem wodoru) utleniają się za pomocą tlenku miedzi(II) w podwyższonej temperaturze do ketonów (), zgodnie ze schematem:

gdzie: , – grupa alkilowa/pierścień węglowy/pierścień aromatyczny (mogą być tymi samymi grupami lub różnymi)
Przykłady utleniania alkoholi drugorzędowych do ketonów
utlenianie propan‑2-olu za pomocą tlenku miedzi(II) do propanonu:

W powyższej reakcji nastąpiło utlenienie atomu węgla połączonego z grupą hydroksylową (stopień utlenienia: 0) do atomu węgla w grupie karbonylowej propanonu (stopień utlenienia: II) oraz redukcja kationu miedzi(II) w tlenku miedzi(II) (stopień utlenienia: II) do miedzi (stopień utlenienia: 0).
utlenianie butan‑2-olu za pomocą tlenku miedzi(II) do butanonu:

W powyższej reakcji nastąpiło utlenienie atomu węgla połączonego z grupą hydroksylową (stopień utlenienia: 0) do atomu węgla w grupie karbonylowej butanonu (stopień utlenienia: II) oraz redukcja kationu miedzi(II) w tlenku miedzi(II) (stopień utlenienia: II) do miedzi (stopień utlenienia: 0).
Alkohole trzeciorzędowe
Alkohole trzeciorzędowe nie ulegają utlenianiu za pomocą tlenku miedzi(II) w podwyższonej temperaturze, ponieważ obecność trzech grup węglowych przyłączonych do atomu węgla związanego z grupą hydroksylową, uniemożliwia przekształcenie grupy hydroksylowej w grupę karbonylową bez zrywania wiązań węgiel - węgiel (atom węgla nie może być pięciowiązalny).
Możliwe jest jednak utlenianie takich alkoholi w drastycznych warunkach, biegnące z rozerwaniem łańcucha węglowego. W reakcji tej, zachodzącej w obecności stężonego kwasu siarkowego(VI) następuje wpierw dehydratacja cząsteczki alkoholu, a następnie alken, powstały jako produkt pośredni, ulega w warunkach reakcji utlenieniu z rozerwaniem łańcucha węglowego cząsteczki.

Słownik
substancja powodująca utlenianie innych substancji
reakcja chemiczna polegająca na oddaniu elektronu (elektronów) przez jon, atom bądź grupy atomów, połączone z procesem redukcji
(od początkowych sylab wyrazów łac. alcohol dehydrogenatum „alkohol pozbawiony wodoru”) związek organiczny zawierający grupę aldehydową (), powstający przez utlenianie alkoholu pierwszorzędowego
(łac. reductio „zmniejszenie”) reakcja chemiczna polegająca na przyłączeniu elektronów do jonu, atomu bądź grupy atomów, połączona z procesem utleniania
związek organiczny zawierający grupę karbonylową () połączoną z dwoma takimi samymi lub różnymi grupami, powstający przez utlenianie alkoholu drugorzędowego
Bibliografia
Litwin M., Styka‑Wlazło Sz., Szymońska J., To jest chemia 2, Warszawa 2016.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1, tłum. Wiesław Antkowiak i in., Warszawa 1985.