Przeczytaj
Czynnik elektrofilowy
Czynnik elektrofilowy (elektrofil) to indywiduum chemiczne, które „lubi elektrony”. Zawiera w swojej strukturze atom posiadający deficyt elektronów. To pozwala mu tworzyć wiązanie poprzez przyjęcie (akceptację) pary elektronów pochodzących od donoradonora. Czynnik elektrofilowy to kation lub silnie polarna cząsteczka z niedomiarem elektronów.
Przedstawiciele czynników elektrofilowych
Atomy z cząstkowym ładunkiem dodatnim w cząsteczkach z wiązaniami kowalencyjnymi silnie spolaryzowanymi
Do pierwiastków, posiadających wyższą wartość elektroujemności niż węgiel, należą: fluor, brom, tlen i azot. W związku z tym, atom węgla, połączony wiązaniem chemicznym z jednym z tych elektroujemnych pierwiastków, posiada cząstkowy ładunekcząstkowy ładunek dodatni (), natomiast atom elektroujemny obarczony jest cząstkowym ładunkiem ujemnym (). W związkach metaloorganicznychzwiązkach metaloorganicznych sytuacja wygląda odwrotnie: atom węgla posiada cząstkowy ładunek ujemny, natomiast atom metalu – cząstkowy ładunek dodatni.
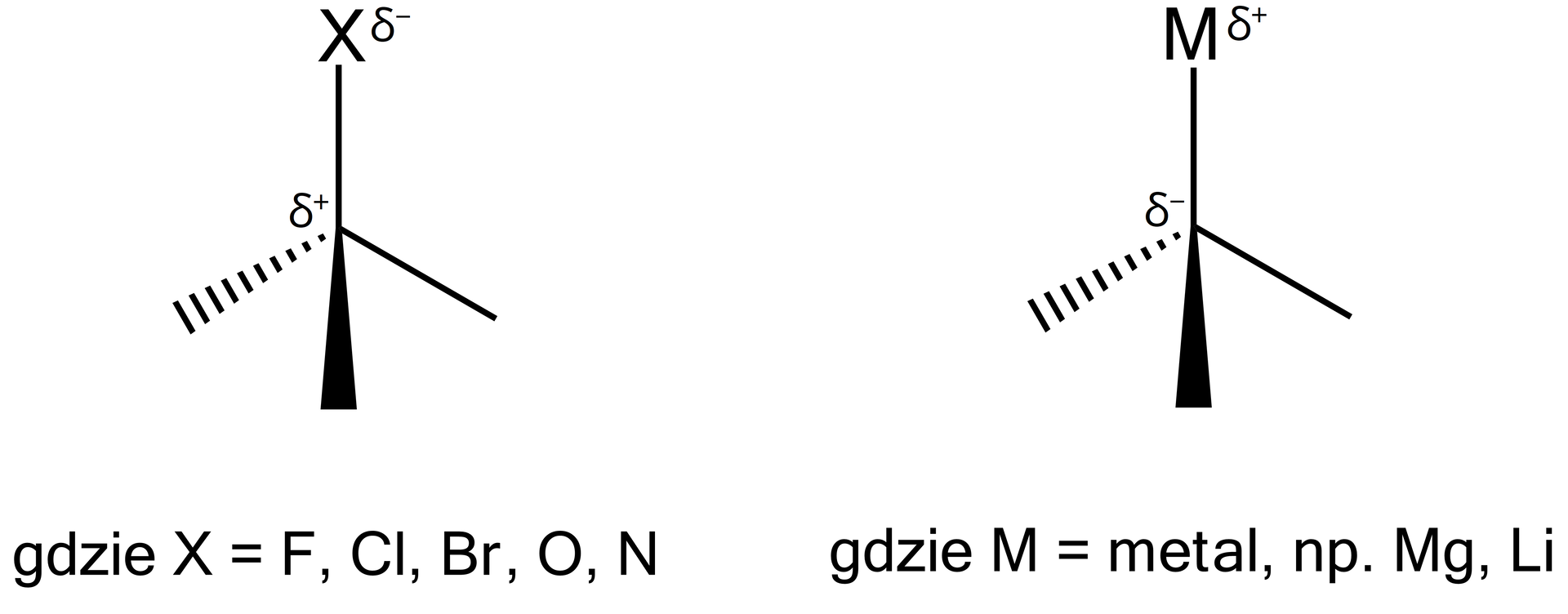
- W związkach organicznych atom węgla posiada cząstkowy ładunek dodatni, gdy jest połączony wiązaniem chemicznym z jednym z elektroujemnych pierwiastków o cząstkowym ładunku ujemnym.
- W związkach metaloorganicznych atom węgla posiada cząstkowy ładunek ujemny, a atom metalu – cząstkowy ładunek dodatni.
Atomy z cząstkowym ładunkiem dodatnim w cząsteczkach, w których doszło do polaryzacji wiązania
Kiedy pole elektryczne wokół cząsteczki zmieni się pod wpływem oddziaływania z rozpuszczalnikiem lub cząsteczkami polarnymi, rozkład chmury elektronowej, występujący wokół atomów tworzących cząsteczkę, także ulegnie zmianie. W wyniku tego dojdzie do polaryzacji wiązania i powstaną cząstkowe ładunki dodatnie i ujemne na atomach tworzących cząsteczkę. Przykładem są cząsteczki fluorowców, w których następuje polaryzacja wiązania pod wpływem np. pary elektronowej z wiązania podwójnego w alkenach.

Cząsteczki, zawierające w swojej budowie atomy z deficytem elektronów, nie posiadają oktetu elektronowego:
;
.
Kationy:
;
;
;
;
;
KarbokationyKarbokationy: , np. ;
Kationy acyliowe;Kationy acyliowe;
Kationy acyliowe występują w dwóch formach rezonansowychformach rezonansowych, np:

, np. .
Reakcja cyklopentenu z bromem – przykład addycji elektrofilowej
Spójrzmy na reakcję cząsteczki bromu z cyklopentenem. Teoretycznie możemy zapisać wzory półstrukturalne dwóch izomerów geometrycznych cis-trans. Jeden z produktów posiada dwa atomu bromu po tej samej stronie pierścienia i jest izomerem cis. Drugi z produktów posiada dwa atomy bromu po przeciwnych stronach pierścienia i stanowi izomer trans. Doświadczenie chemiczne wykazało, że jedynym produktem jest izomer trans-,-dibromocyklopentanu, natomiast izomer cis nie powstaje wcale.

Gdy dwa atomy przyłączają się po przeciwnych stronach podwójnego wiązania, mówimy o stereochemii anti reakcji addycji. W przeciwnym przypadku, czyli kiedy dwa atomy przyłączają się po tej samej stronie wiązania, mówimy o stereochemii syn.

Czy w innych przypadkach addycji cząsteczki bromu do alkenu również powstaje jedynie produkt o stereochemii anti?

Dokładnie tak samo! Atomy bromu przyłączają się po przeciwnych stronach wiązania podwójnego. Dlaczego tak się dzieje? Wyjaśnienie mechanizmu addycji elektrofilowej cząsteczki bromu do alkenu przedstawili w roku George Kimball i Irving Roberts, a zapoznasz się z nim w grafice interaktywnej w Poleceniu 1.
Słownik
atom lub jon mający zdolność przekazywania pary elektronowej innemu indywiduum chemicznemu
ładunek powstający na atomach cząsteczki w wyniku niesymetrycznego rozkładu chmury elektronowej elektronów tworzących wiązanie pomiędzy atomami
związki organiczne o cząsteczkach, w których występuje co najmniej jedno bezpośrednie wiązanie , tj. wiązanie między atomami węgla () i metalu (), z wyjątkiem węglików, cyjanków oraz karbonylków metali, zaliczanych do związków nieorganicznych
(łac. carbo „węgiel”; gr. katiṓn „idący w dół”) jon karboniowy, kation organiczny, w którym dodatni ładunek, wywołany deficytem elektronów, jest zlokalizowany na atomie węgla
kation organiczny, powstały z halogenku kwasu karboksylowego, w którym dodatni ładunek, wywołany deficytem elektronów, jest zlokalizowany na atomie węgla w jednej z dwóch form rezonansowych oraz na atomie tlenu w drugiej formie rezonansowej
sposób przedstawiania wzoru indywiduów chemicznych za pomocą struktur granicznych, gdzie rzeczywisty wzór opisywany jest poprzez kombinację tych struktur
Bibliografia
Litwin M., Styka‑Wlazło Sz., Szymońska J., To jest chemia 2, Warszawa 2016.
McMurry J., Chemia organiczna, tłum. Henryk Koroniak i in., t. 1, Warszawa 2018.