Przeczytaj
Berylowce są srebrzystobiałymi metalamimetalami, które, będąc aktywne chemicznie, występują w przyrodzie wyłącznie w postaci związków chemicznych. Spośród berylowców, to właśnie wapń, bar i stront, ze względu na dużą reaktywność, przechowuje się w nafcienafcie. W związkach chemicznych berylowce przyjmują stopień utlenieniastopień utlenienia.
Konfiguracje elektronowe berylowców
Berylowce posiadają na ostatniej powłoce elektronowejpowłoce elektronowej dwa elektrony. Ich konfigurację elektronową można przedstawić następująco:
Dla porównania, kofigurację sodu, który należy do litowców, zapisujemy następująco:
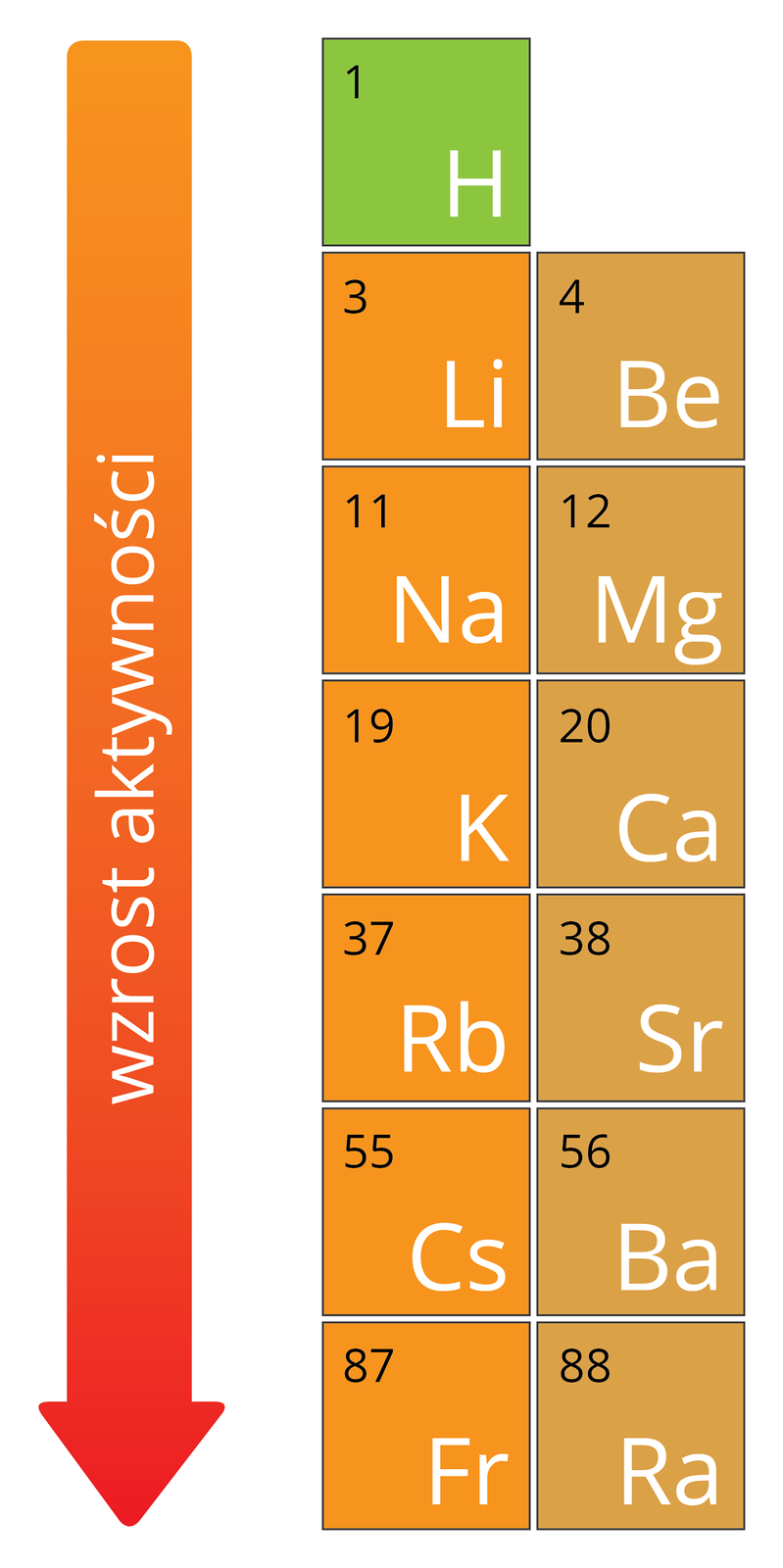
Porównując konfigurację elektronową berylowców i litowców – które posiadają tylko jeden elektron walencyjnyelektron walencyjny – można zauważyć, że do uzyskania konfiguracji gazu szlachetnego, czyli do całkowitego zapełnienia powłok elektronowych, berylowce muszą oddać dwa elektrony. Wymaga to większej energii niż w przypadku oddania tylko jednego elektronu, dlatego wartość energii jonizacji berylowców jest większa niż litowców, a ich reaktywność mniejsza.
Berylowce reagują z wodą, ale nie aż tak gwałtownie jak litowce. Reaktywność berylowców rośnie w dół grupy, wynika to z tego, że elektrony walencyjne znajdują się dalej od jądra atomowego, które słabiej na nie oddziałuje. Są więc bardziej ekranowane od jądra.
Promienie atomowe i jonowe litowców i berylowców
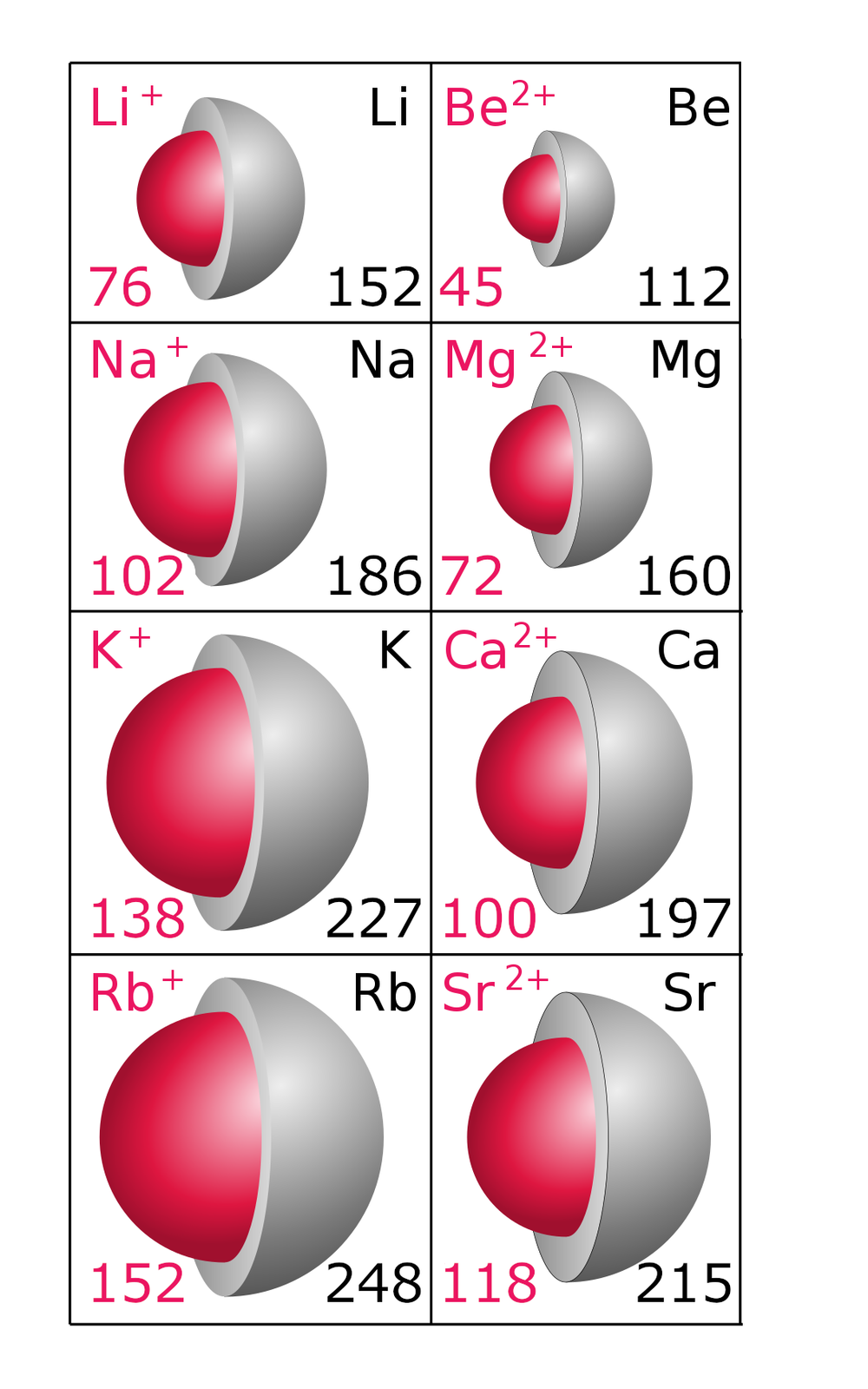
Porównując promienie jonowe litowców i berylowców można zauważyć, że berylowce z tego samego okresu co litowce mają mniejszy promień atomowy. Ponieważ jądra berylowców zawierają o jeden proton więcej niż litowców, to silniej przyciągają elektrony, co powoduje skrócenie promieni atomowych oraz wzrost energii potrzebnej do oderwania elektronów.
Jednym ze znanych minerałów, zawierających w swojej cząsteczce jony berylu, jest szmaragd.

Słownik
(łac. metallum, gr. métallon „kopalnia”, „kruszec”) substancje odznaczające się dobrym przewodnictwem elektrycznym i cieplnym, charakterystycznym połyskiem, dużą wytrzymałością mechaniczną oraz plastycznością
frakcja destylacji ropy naftowej o temperaturze wrzenia ; stosowana gł. jako składnik paliw do silników odrzutowych, paliwo do traktorów, rozpuszczalnik olejów i smarów, jako środek konserwacyjny oraz do celów oświetleniowych
pojęcie umowne, określające liczbę dodatnich lub ujemnych ładunków elementarnych, które można by przypisać atomowi pierwiastka chemicznego wchodzącego w określonego związku, gdyby wszystkie występujące w nim wiązania chemiczne były jonowe
elektronowa powłoka atomu, elektrony atomu, które w stanie podstawowym (poziom energetyczny) i przy założeniu występowania tylko centralnego pola jądra atomu wykazują taką samą energię oznaczoną główną liczbą kwantową (atom)
elektrony walencyjne, elektrony wartościowości, elektrony zapełniające w atomie danego pierwiastka tzw. orbitale walencyjne, czyli orbitale o największej dla tego atomu wartości energii (w stanie podstawowym)
zmniejszanie oddziaływania jądra na dany elektron w atomie przez elektrony, znajdujące się pomiędzy nim i jądrem atomu
Bibliografia
Krzeczkowska M., Loch J., Mizera A., Repetytorium chemia. Liceum – poziom podstawowy i rozszerzony, Warszawa – Bielsko–Biała .