Przeczytaj
Alkohole ‑rzędowe
Tlenek miedzi() w podwyższonej temperaturze utlenia alkohole -rzędowe do aldehydówaldehydów. Etanol utlenia się do acetaldehydu, natomiast tlenek miedzi() redukuje się do miedzi, co przedstawia poniższe równanie reakcji chemicznej.
Obserwując przebieg reakcji chemicznej, widać wyraźnie, że zanika czarny osad (tlenek miedzi()), a pojawia się różowy (miedź).
Alkohole -rzędowe utleniają się do kwasów karboksylowychkwasów karboksylowych pod wpływem dichromianu() potasu w środowisku kwasu siarkowego(). Etanol utlenia się do kwasu octowego, natomiast anion dichromianowy() redukuje się do kationu chromu(), co przedstawia poniższe równanie reakcji chemicznej.
Obserwując przebieg reakcji chemicznej, da się zauważyć, jak pomarańczowy roztwór (dichromian() potasu) zmienia zabarwienie na zielone (siarczan() chromu()).
Alkohole ‑rzędowe
Alkohole -rzędowe utleniają się do ketonówketonów pod wpływem tlenku miedzi() i ogrzewania. Propan--ol utlenia się do propan--onu, natomiast tlenek miedzi() redukuje się do miedzi, co przedstawia poniższe równanie reakcji chemicznej:

Obserwując przebieg reakcji chemicznej, obserwujemy, że zanika czarny osad (tlenek miedzi()), a pojawia się różowy (miedź). Alkohole -rzędowe utleniają się także do ketonów pod wpływem dichromianu() potasu w środowisku kwasu siarkowego(). Propan--ol utlenia się do propan--onu, z kolei anion dichromianowy() redukuje się do kationu chromu(), co przedstawia poniższe równanie reakcji chemicznej:
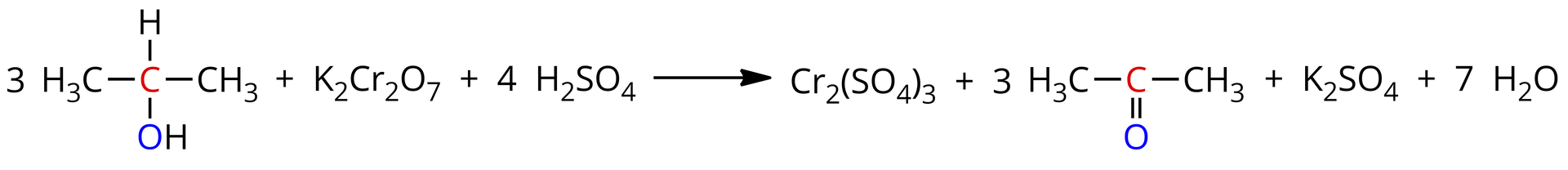
Obserwując przebieg reakcji chemicznej, widać, że pomarańczowy roztwór (dichromian() potasu) zmienia zabarwienie na zielone (siarczan() chromu()).
Alkohole ‑rzędowe
Alkohole trzeciorzędowe nie ulegają utlenieniu. Fakt ten można z powodzeniem wykorzystać do odróżniania ich od alkoholi - czy -rzędowych.
Słownik
powstał od początkowych sylab wyrazów łac. alcohol dehydrogenatum, czyli „alkohol pozbawiony wodoru”; związek organiczny, który zawiera grupę aldehydową (); powstaje przez utlenianie alkoholu pierwszorzędowego
związek organiczny zawierający grupę karboksylową ()
związek organiczny, który zawiera grupę karbonylową () połączoną z dwoma takimi samymi lub różnymi grupami; powstaje przez utlenianie alkoholu drugorzędowego
Bibliografia
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1, tłum. Wiesław Antkowiak i in., Warszawa 1985.
Litwin M., Styka‑Wlazło Sz., Szymońska J., To jest chemia 2, Warszawa 2016.