Przeczytaj
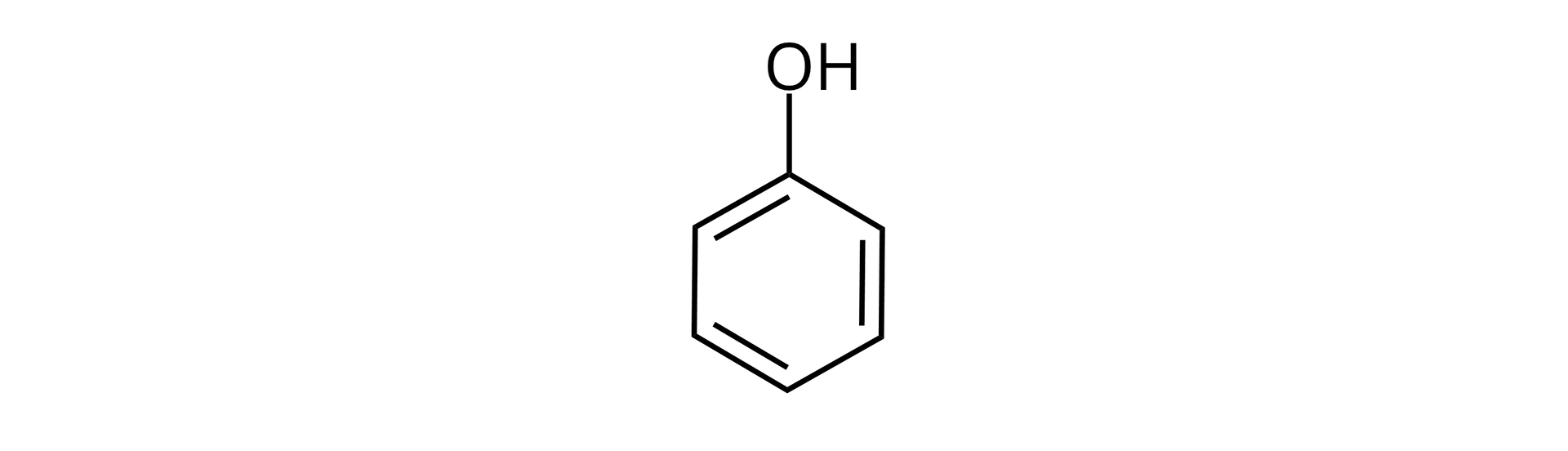
FenoleFenole to związki chemiczne, które posiadają przynajmniej jedną grupę hydroksylową (). Grupy te są przyłączone bezpośrednio do atomów węgla z pierścienia aromatycznego. Najprostszym przedstawicielem tej grupy związków jest fenolfenol o wzorze . To nazwa zalecana przez IUPAC, dla związku o wzorze sumarycznym , zapisywanego jako . Inna nazwa tego związku to benzenol. Fenole należą do pochodnych węglowodorów, w których orbitale walencyjne atomów węgla tworzących pierścień są w stanie hybrydyzacji spIndeks górny 22hybrydyzacji spIndeks górny 22.
Wzór ogólny fenoli
Fenole posiadają następujący wzór ogólny:
gdzie:
stanowi grupę arylową;
to grupa hydroksylowa.
Grupa arylowa to reszta węglowodorowa utworzona przez oderwanie atomu wodoru od pierścienia aromatycznego.

Budowa fenolu
Jaka inna grupa związków chemicznych, należących do pochodnych węglowodorów, posiada jedną grupę ? Wszystkie atomy węgla, budujące takie związki, posiadają hybrydyzację spIndeks górny 33hybrydyzację spIndeks górny 33.
Czy wiesz, do jakiej grupy związków chemicznych należy związek, którego wzór szkieletowy podano poniżej?

Jeżeli porównamy wzory ogólne fenolu i alkoholu monohydroksylowego, to możemy dostrzec pewne ich podobieństwa, ale również różnice. Jakie? Uzupełnij tabelę.
Fenol jest najprostszym przedstawicielem grupy związków o tej samej nazwie, czyli fenoli. Zawiera on w swojej cząsteczce jedno ugrupowanie . W przypadku gdy grup hydroksylowych jest więcej, mówimy o fenolach polihydroksylowych (polifenolach), np.:
Bazą dla nazw fenoli, posiadających tylko jedną grupę przy pierścieniu aromatycznym, jest słowo „fenol”. W przypadku polifenoli, korzystamy z nazwy benzenol.
Teoria rezonansu w cząsteczkach związków
Gdy cząsteczkę możemy przedstawić za pomocą dwóch lub większej liczby struktur Lewisa, to mówimy o zjawisku rezonansurezonansu.
W dalszej części zapoznaj się z filmem samouczkiem, który wyjaśni ci efekt rezonansowy w cząsteczce fenolu.
Słownik
(gr. kýklos „koło”) związki o budowie pierścieniowej
(łac. hybrida „mieszaniec”) zabieg matematyczny z udziałem odpowiednich orbitali walencyjnych atomu centralnego cząsteczki, umożliwiający interpretację kształtu cząsteczki; efektem hybrydyzacji jest utworzenie zestawu orbitali zhybrydyzowanych
zabieg matematyczny polegający na wyznaczeniu liniowej kombinacji orbitalu typu i dwóch orbitali typu ; atom w hybrydyzacji może utworzyć wiązania z trzema sąsiednimi atomami: dwa wiązania pojedyncze typu i jedno wiązanie podwójne, składające się z wiązania i wiązania
zabieg matematyczny polegający na wyznaczeniu liniowej kombinacji orbitalu typu i trzech orbitali typu ; atom w hybrydyzacji może utworzyć pojedyncze wiązania z czterema sąsiednimi atomami; są to wiązania typu
związek organiczny, najprostszy przedstawiciel grupy monohydroksylowych fenoli o wzorze:
teoria stosowana w celu opisania struktury związku chemicznego za pomocą struktur granicznych
związki organiczne, mono-, di- i polihydroksylowe, pochodne benzenu oraz alkilobenzenów, których cząsteczki zawierają grupy hydroksylowe () związane z atomem węgla pierścienia benzenowego
Bibliografia
Atkins P., Jones L., Chemia ogólna. Cząsteczki, materia, reakcje, Warszawa 2004, s. 524‑525.
Dudek‑Różycki K., Płotek M., Wichur T., Węglowodory. Repetytorium i zadania, Kraków 2020.
Dudek‑Różycki K., Płotek M., Wichur T., Kompendium terminologii oraz nazewnictwa związków organicznych. Poradnik dla nauczycieli i uczniów, Kraków 2020.
Encyklopedia PWN
Mastalerz P., Podręcznik chemii organicznej, Warszawa 1998.
McMurry J., Chemia organiczna, t. 1 i 2, Warszawa 2000.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1 i 2, Warszwa 1997.
Wojcieszyńska D., Wilczek A. Związki fenolowe pochodzenia naturalnego, „Chemia w szkole” 2006, nr 6.