Przeczytaj
Hydroksykwasy
HydroksykwasyHydroksykwasy to związki organiczne, które zawierają dwie grupy funkcyjnegrupy funkcyjne: karboksylową i hydroksylową – po jednej lub po kilka. W związku z tym, że grupa karboksylowa jest dominująca, traktujemy te związki jak kwasy. Z kolei grupę hydroksylową traktujemy jako podstawnikpodstawnik.
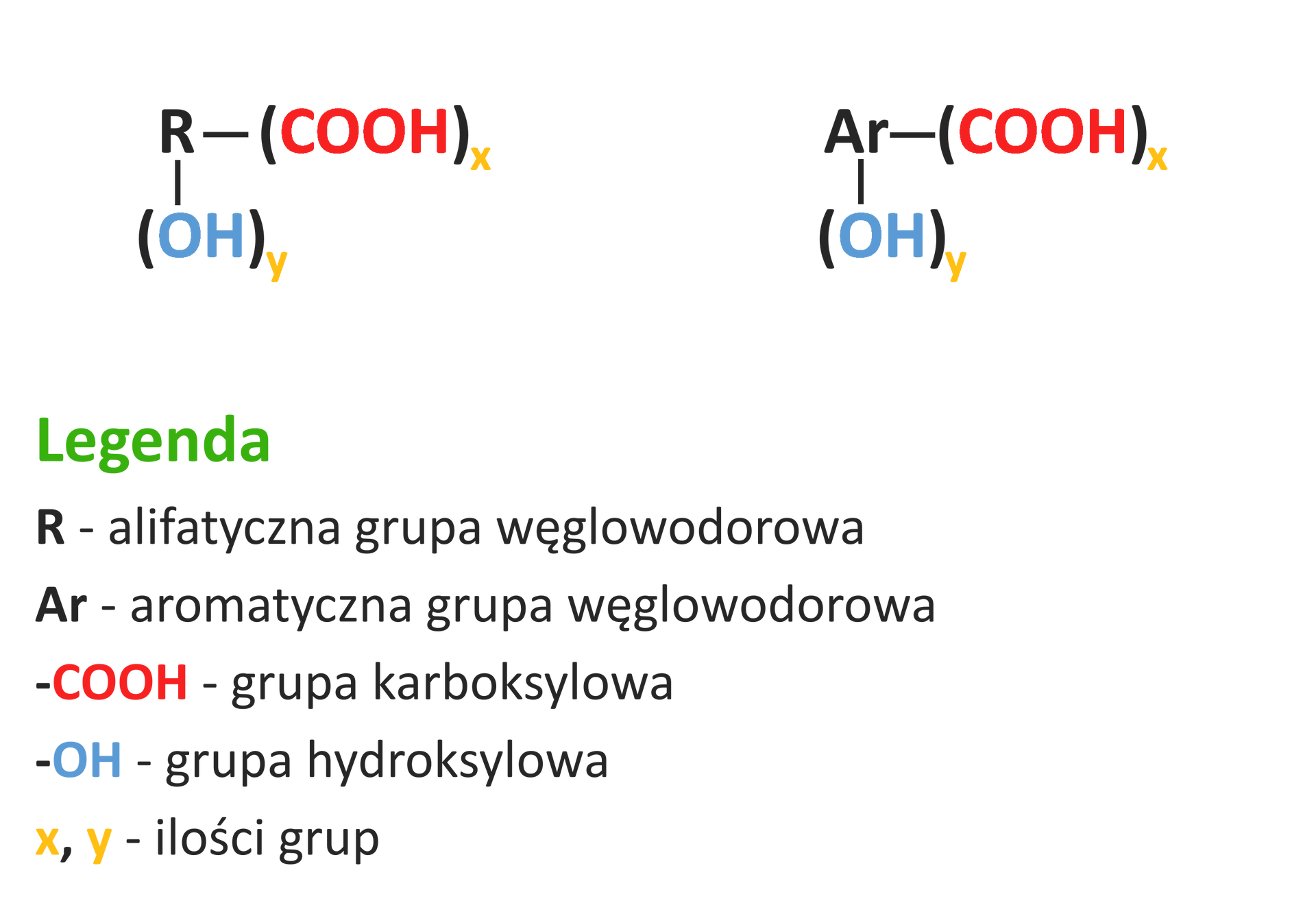
Wyróżniamy trzy sposoby nazewnictwa hydroksykwasów:
nazewnictwo systematyczne;
nazewnictwo zwyczajowe;
nazewnictwo związane z położeniem grupy hydroksylowej, z wykorzystaniem alfabetu greckiego oraz nazw zwyczajowych kwasów karboksylowych.
Skonstruuj model cząsteczki kwasu mlekowego. Model cząsteczki tego kwasu składa się z trzech atomów węgla, trzech atomów tlenu oraz sześciu atomów wodoru.
Model cząsteczki tego kwasu mlekowego składa się z trzech atomów węgla, trzech atomów tlenu oraz sześciu atomów wodoru. Zapisz w zeszycie wzór strukturalny kwasu mlekowego.
Wzory
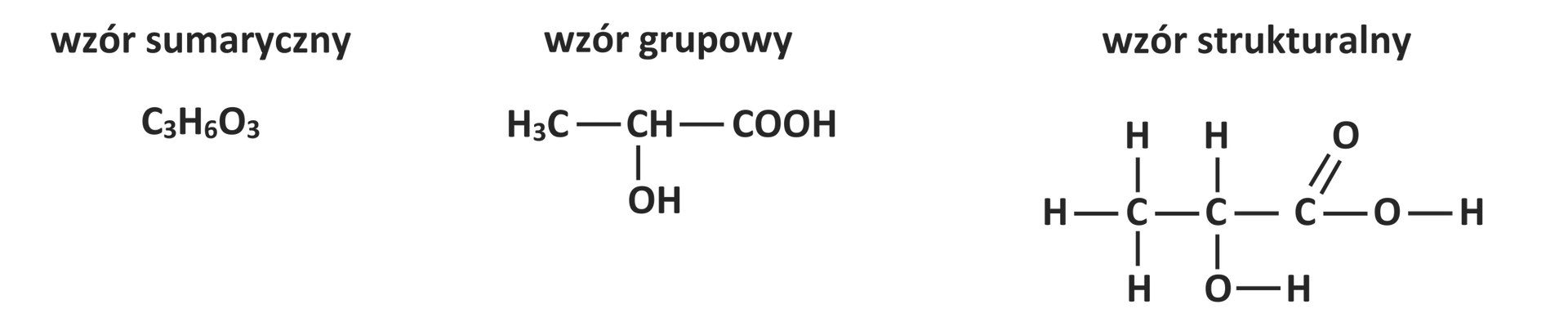
Wzór sumaryczny pokazuje liczbę poszczególnych atomów. Wzór strukturalny z kolei informuje nas o liczbie wiązań pomiędzy poszczególnymi atomami oraz o kątach między wiązaniami. Wzór grupowy (półstrukturalny) to uproszczona forma wzoru strukturalnego, która pokazuje tylko wiązania między atomami węgla oraz wiązania między atomami węgla a podstawnikami lub grupami funkcyjnymi.
Nazewnictwo systematyczne
Nazwy systematyczne tworzymy dodając do nazwy odpowiedniego kwasu karboksylowego przedrostek hydroksy-, oznaczający grupę hydroksylową. Podajemy lokantlokant podstawnika, czyli numer atomu/atomów węgla, przy których się znajduje. Jeśli w związku występuje więcej niż jedna grupa hydroksylowa lub karboksylowa, należy również podać ich krotność, wykorzystując przedrostki z języka greckiego, np.: di – dwa; tri – trzy; tetra – cztery; penta – pięć itd.
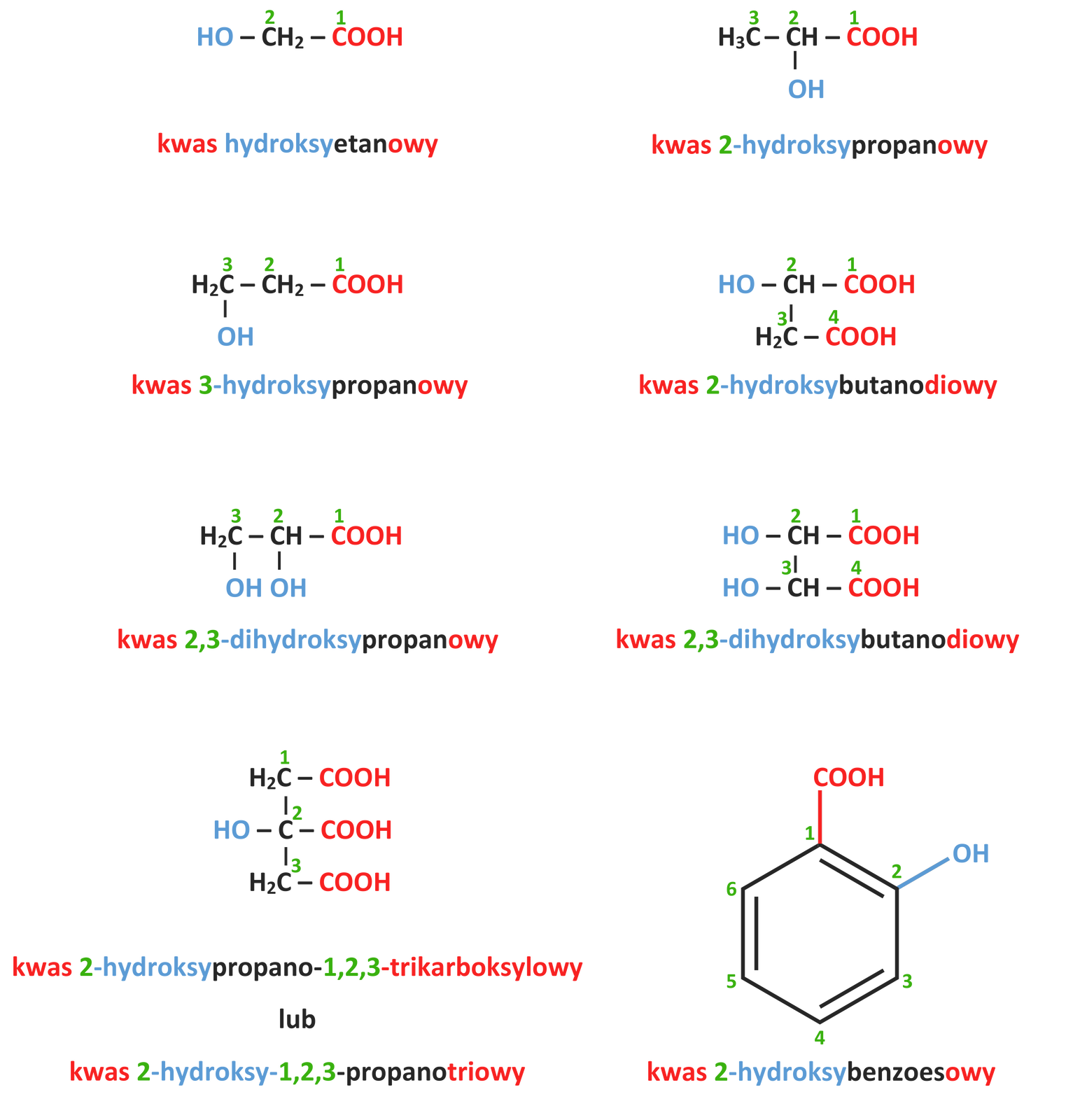
Nazewnictwo zwyczajowe
Zamiast nazw systematycznych bardzo często używa się nazw zwyczajowych dla hydroksykwasów. Wynika to z przyzwyczajenia. Nazwy zwyczajowe mają związek z występowaniem hydroksykwasów. Na przykład kwas mlekowy występuje w kwaśnym mleku, a kwas jabłkowy w wielu owocach, m.in. w jabłkach.
Nazewnictwo związane z położeniem grupy hydroksylowej z użyciem alfabetu greckiego oraz wykorzystaniem nazw zwyczajowych kwasów karboksylowych
Często w literaturze możemy odnaleźć skrót AHA, który oznacza alfa‑hydroksykwasy (czyt. alfa‑hydroksykwasy). Nazewnictwo z wykorzystaniem alfabetu greckiego to również jeden ze sposobów nazewnictwa hydroksykwasów. Opiera się na tych samych zasadach, co nazewnictwo systematyczne. Z tym, że zamiast liczb określających położenie grupy hydroksylowej bądź innego podstawnika, używamy liter z alfabetu greckiego.

Ten rodzaj nazewnictwa stosujemy do hydroksykwasów monokarboksylowychhydroksykwasów monokarboksylowych, gdzie atom węgla w grupie karboksylowej jest zawsze pierwszy. Literą alfa (alfa) określamy drugi atom węgla w łańcuchu głównym (za grupą karboksylową), literą beta (beta) trzeci atom węgla w łańcuchu głównym, a literą gamma (gamma) czwarty atom węgla w łańcuchu głównym. Dodatkowo, w tym sposobie, zamiast nazwy systematycznej kwasu karboksylowego stosujemy jego nazwę zwyczajową.

Naturalnie występuje w cytrusach, winie, a także w ośrodkowym układzie nerwowym człowieka. Należy do hydroksykwasów, a jego nazwy to: kwas 4 -hydroksybutanowy lub kwas gamma‑hydroksymasłowy. Skrótowo określany jako GHB.
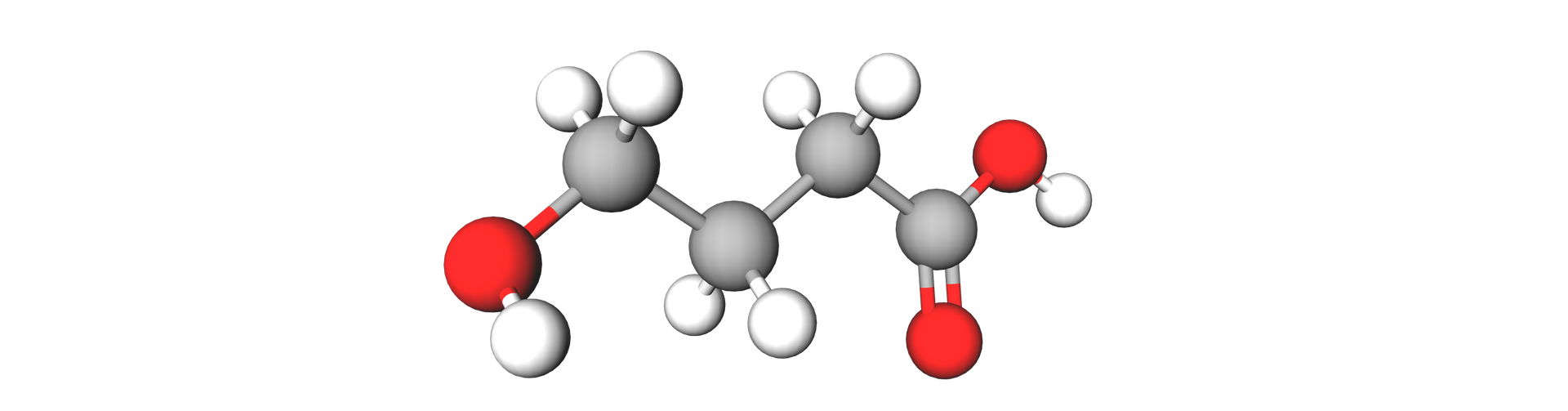
Jest to substancja psychoaktywna. Wykazuje działanie euforyzujące, energetyzujące oraz rozweselające. Przez wiele lat był wykorzystywany w anestezjologii. Został jednak wycofany ze względu na efekty uboczne i działanie uzależniające. Używano go również w walce z bezsennością, a także jako środek dopingujący przez sportowców. Obecnie wykorzystuje się go w leczeniu alkoholizmu, ponieważ łagodzi symptomy odstawienne oraz wspomaga detoksykację organizmu.
Nazwa handlowa leku to Alcover. Natomiast jako lek Xyrem jest stosowany w leczeniu narkolepsji.
Zestawienie nazw oraz wzorów półstrukturalnych wybranych hydroksykwasów
Wzór grupowy | Nazwa systematyczna | Nazwa zwyczajowa | Inna nazwa |
|---|---|---|---|
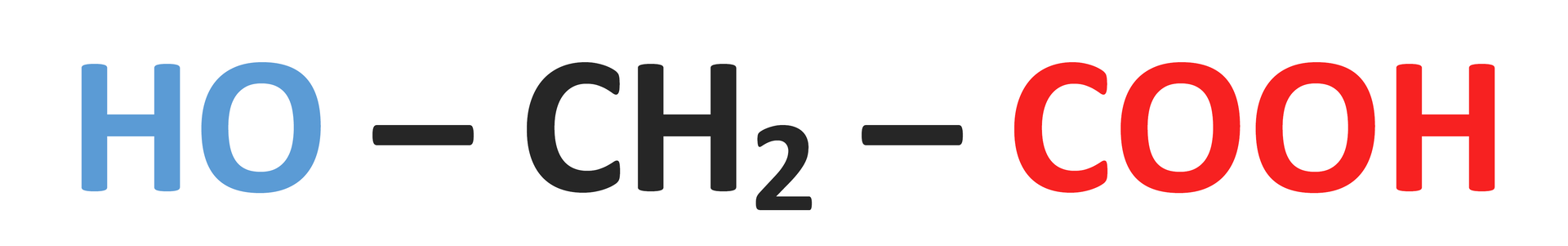 | |||
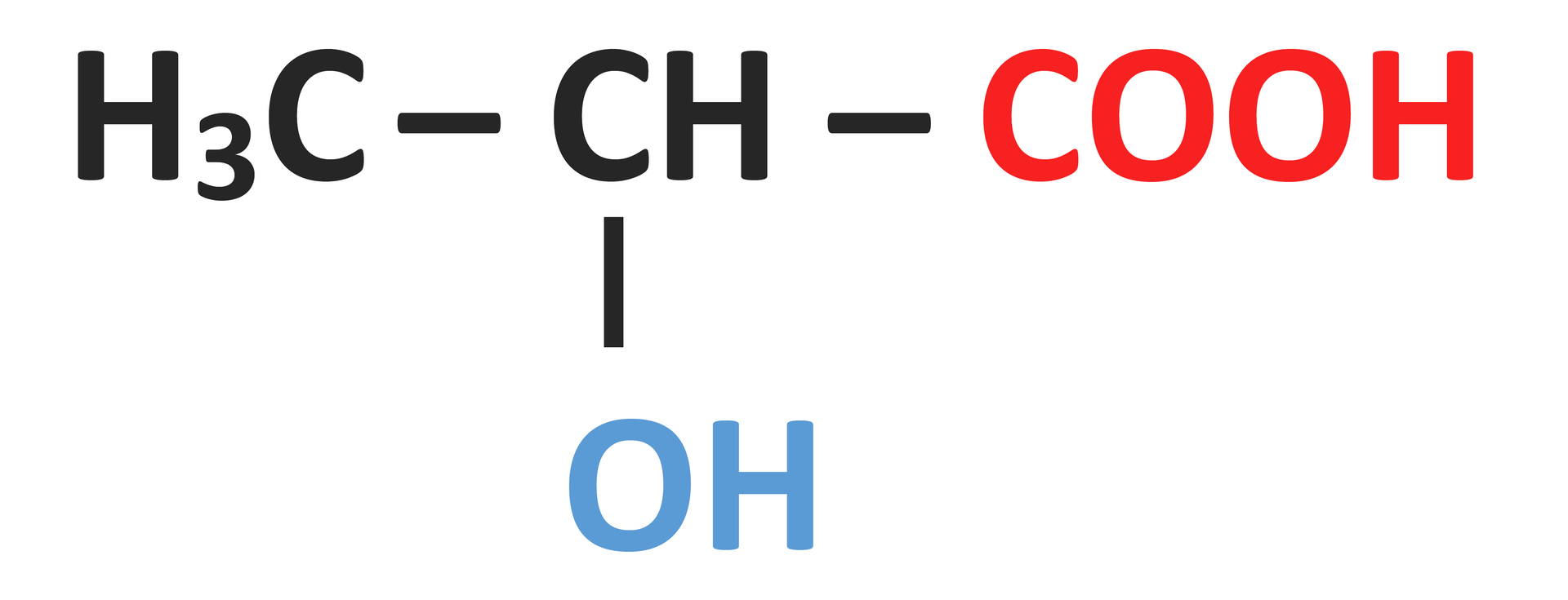 | |||
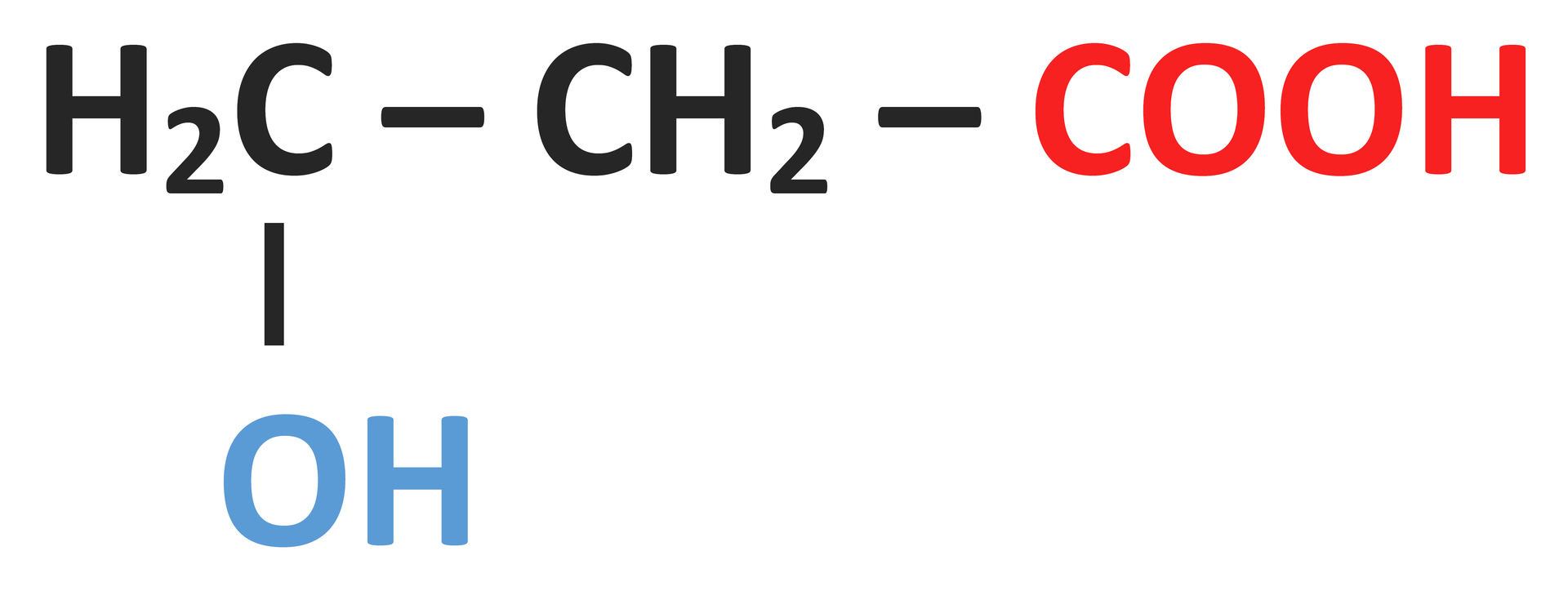 | - | ||
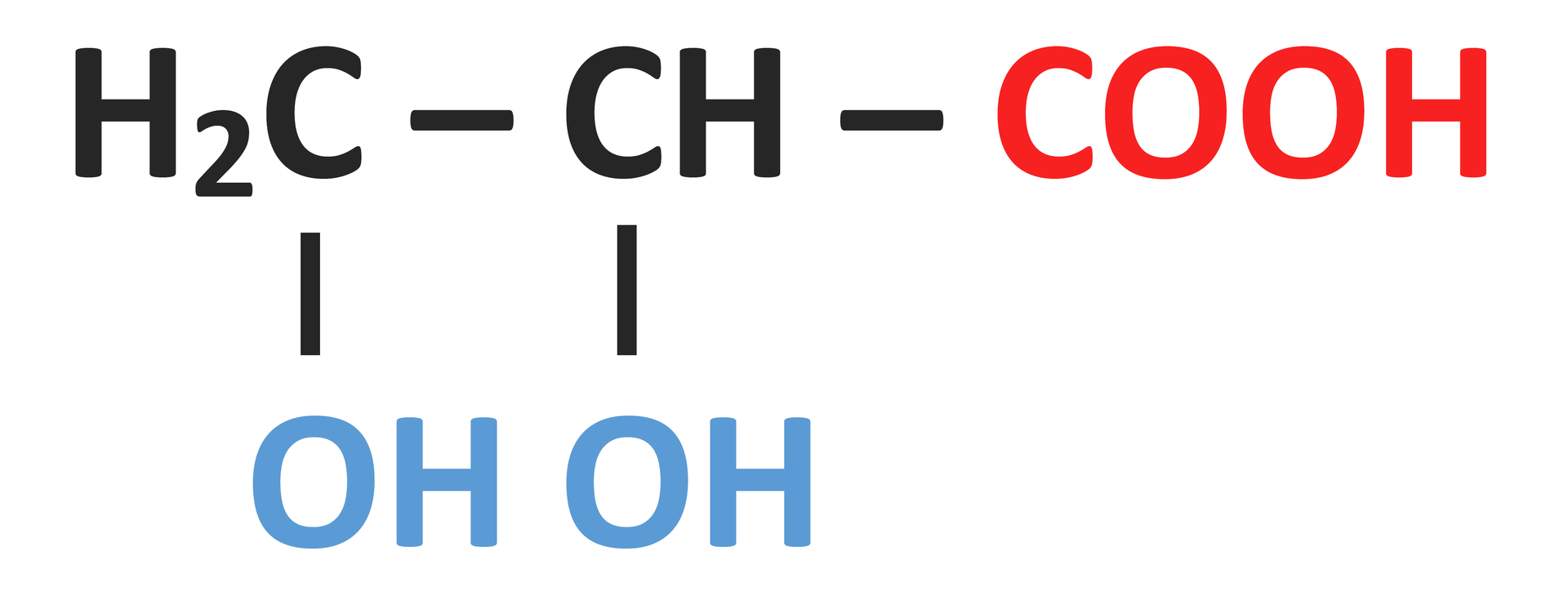 | |||
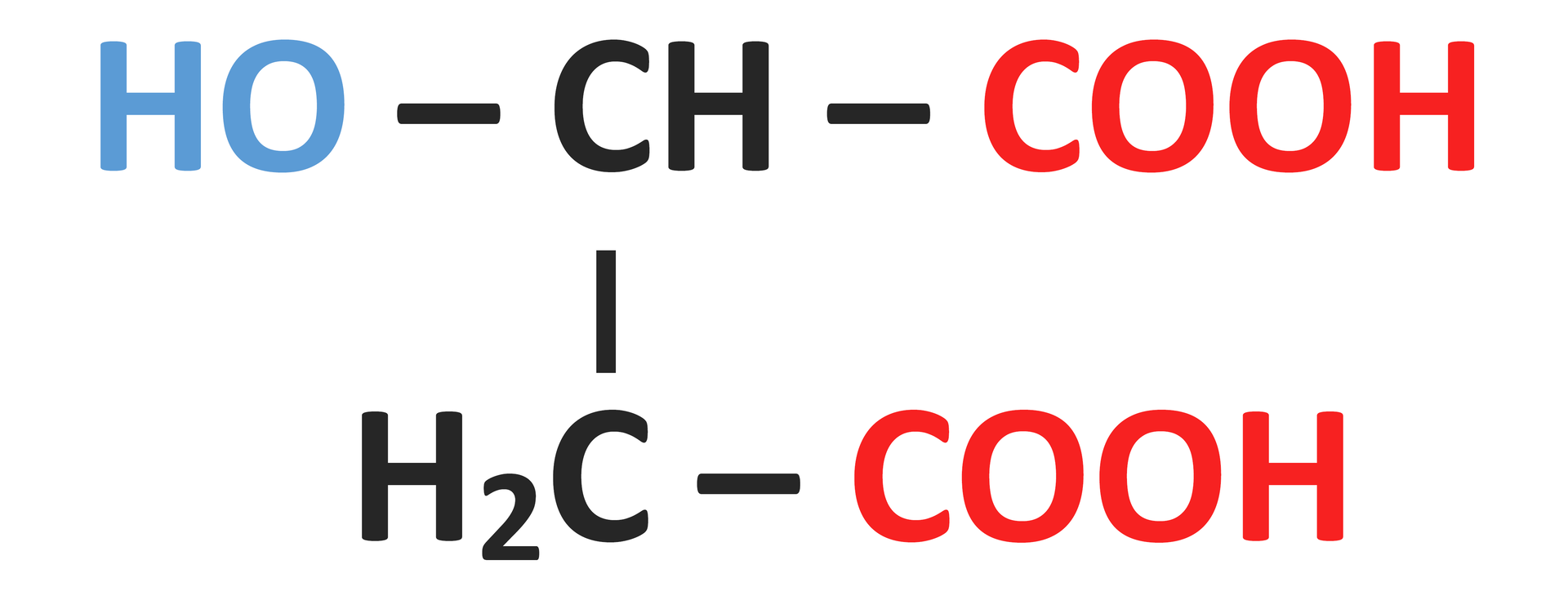 | - | ||
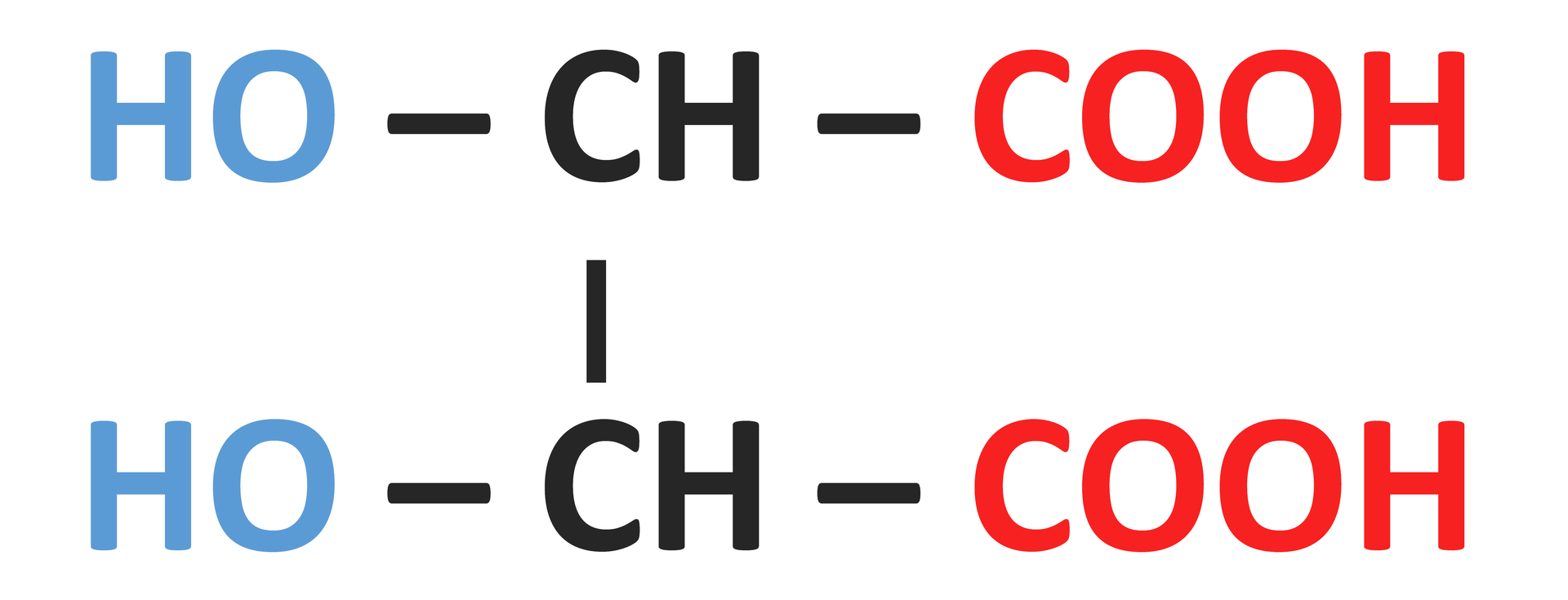 | - | ||
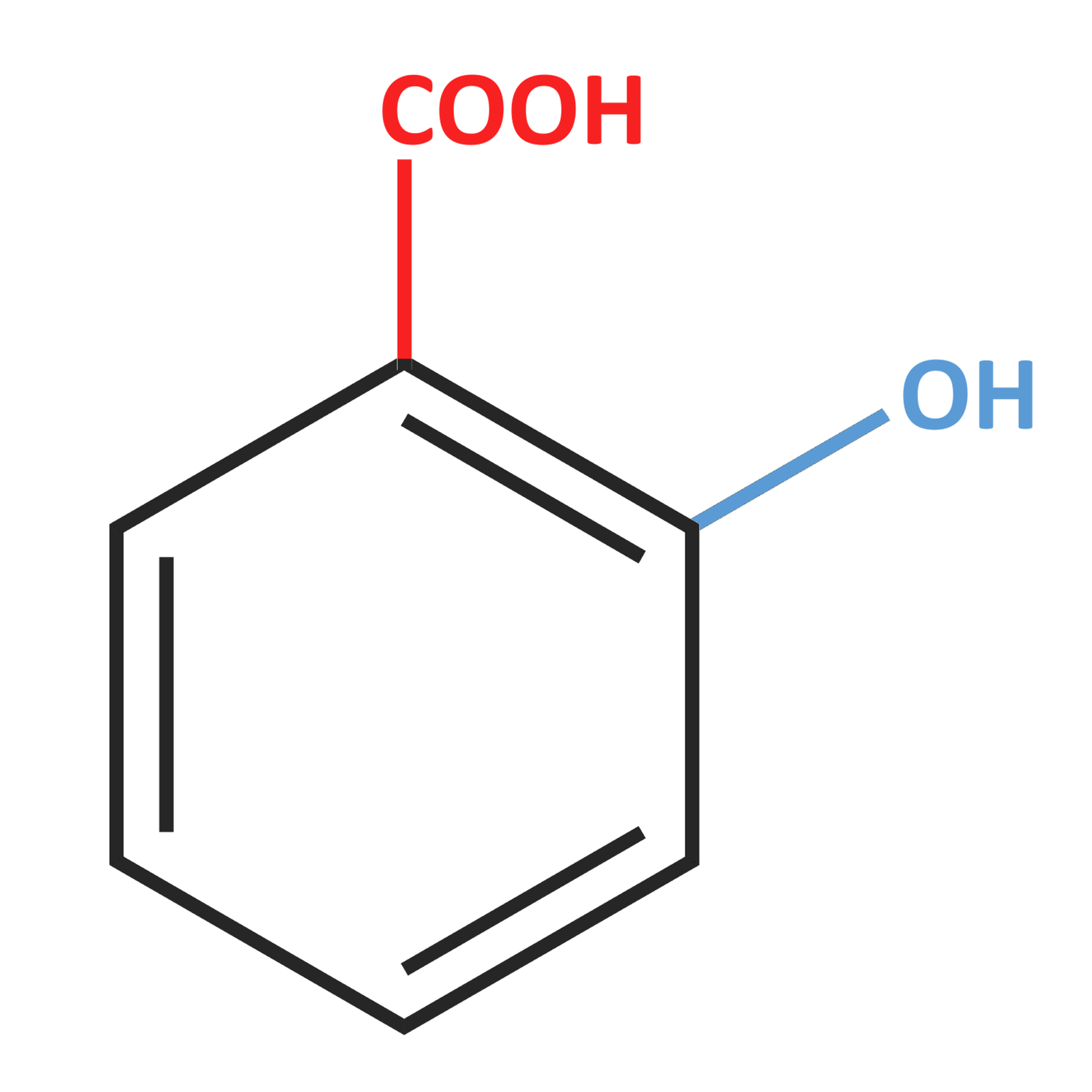 | |||
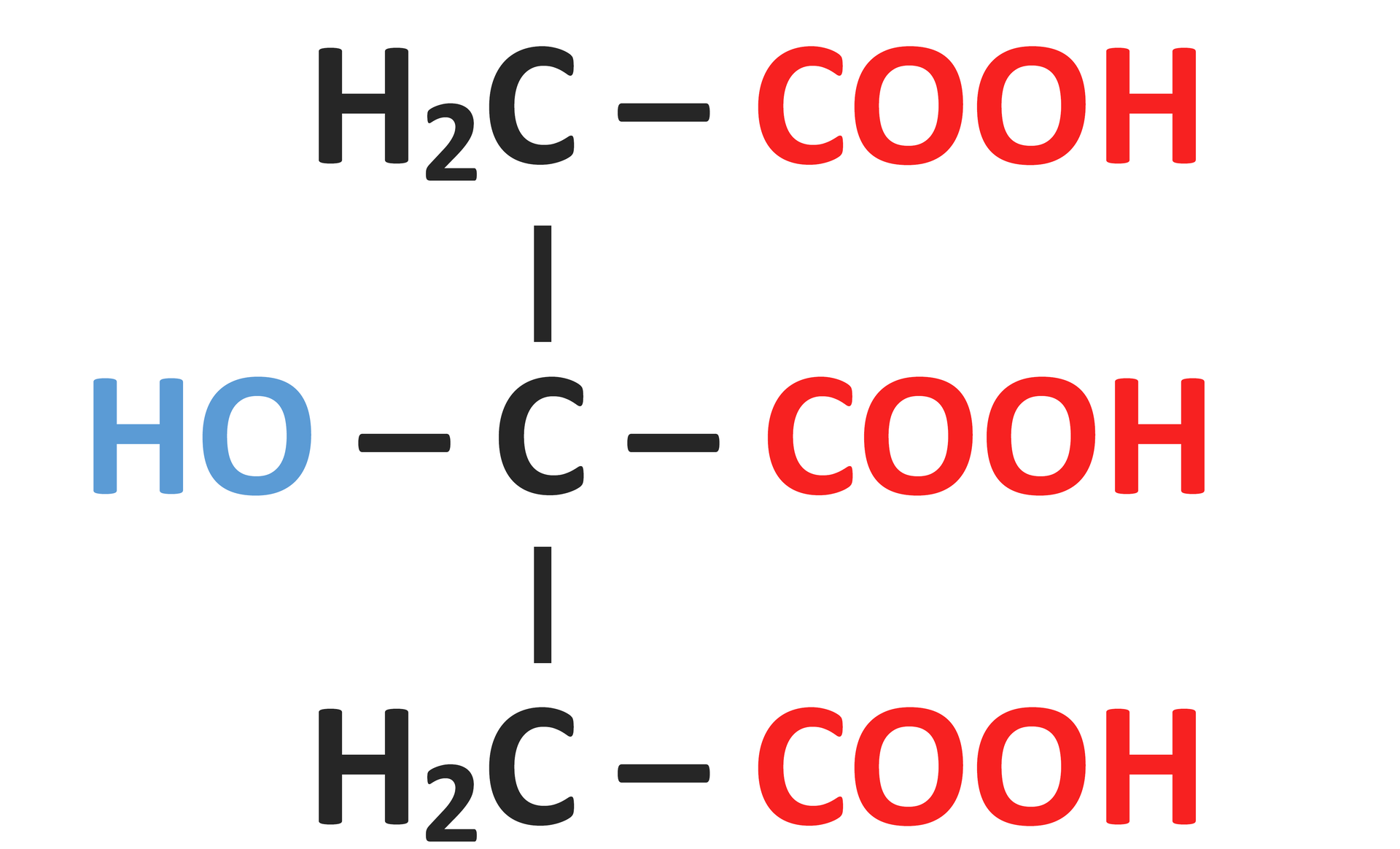 |
Indeks dolny Źródło: Gromar Sp. z o.o.; licencja: CC BY‑SA 3.0 Indeks dolny koniecŹródło: Gromar Sp. z o.o.; licencja: CC BY‑SA 3.0
Podsumowanie
Reasumując, hydroksykwasy to wielofunkcyjne związki organiczne. Posiadają dwie grupy funkcyjne: karboksylową i hydroksylową – po jednej lub po kilka. Dominującą jest grupa karboksylowa. Stąd wynika ogólna nazwa tych związków. Istnieją różne sposoby nazewnictwa hydroksykwasów: nazewnictwo systematyczne, nazewnictwo zwyczajowe i nazewnictwo związane z nazwami zwyczajowymi kwasów karboksylowych. Najczęściej wykorzystuje się nazwy zwyczajowe, które są związane z występowaniem hydroksykwasów. Ich wzory są takie same, jak dla pozostałych grup związków, jednak najpowszechniej używane są wzory grupowe.
Słownik
związek organiczny zawierający dwie grupy funkcyjne: hydroksylową i karboksylową
(łac. functio „czynność”) atom lub grupa atomów w związkach organicznych, która decyduje o właściwościach danego związku oraz jego przynależności do danej klasy związków
(łac. locus „miejsce”) liczba, która określa numer atomu węgla, przy którym znajduje się podstawnik
atom lub grupa atomów, które stanowią odgałęzienie od łańcucha głównego w związku organicznym
(gr. mono „pojedynczy”) hydroksykwas posiadający jedną grupę karboksylową
Bibliografia
Bobrański B., Chemia organiczna, Warszawa 1992.
Buczek I., Chrzanowski M., Dymara J., Persona A., Kowalik E., Kuśmierczyk K., Odrowąż E., Sobczak M., Sygniewicz J., Chemia. Rozszerzenie. Repetytorium matura, Warszawa 2014.
Danikiewicz W., Chemia. Związki organiczne. Podręcznik do liceów i techników. Zakres rozszerzony, Warszawa 2016.
Kalembkiewicz J., Lubczak J., Lubczak R., Nazwy związków chemicznych, Rzeszów 1998.
Lautenschläger K.H., Schröter W., Wanninger A., Nowoczesne kompendium chemii, Warszawa 2007.
Litwin M., Styka – Wlazło S., Szymońska J., To jest chemia 2. Chemia organiczna. Podręcznik dla liceum ogólnokształcącego i technikum. Zakres rozszerzony, Warszawa 2016.
McMurry J., Chemia organiczna 4, Warszawa 2004.
McMurry J., Chemia organiczna 3, Warszawa 2003.
Waszkielewicz A., Bojarski J., Gamma‑hydrobutyric acid (GHB) and its chemical modifications: a review of the GHBergic system, „Pol J Pharmacol”, 56 (1), s. 43–49.